解题方法
1 . 铜、铁、铝是重要的金属材料,铜、铁、铝及其化合物有非常重要的用途。
(1)工业上可用Cu2S和O2反应制取粗铜,该反应中氧化剂为________ .电解粗铜制取精铜,电解时,阳极材料是________ 。
(2)铁元素与氯元素可形成FeCl2和FeCl3两种化合物,下列说法正确的是______ (填序号)。
①保存FeCl2溶液时,需向溶液中加入少量Fe
②FeCl2只能通过置换反应生成,FeCl3只能通过化合反应生成
③铜片、碳棒和FeCl3溶液组成原电池,电子由铜片沿导线流向碳棒
④向淀粉-碘化钾溶液中滴加几滴FeCl2的浓溶液,原无色溶液变为蓝色
⑤纯铁与稀盐酸反应产生氢气的速率较慢;再加入少量CuCl2·2H2O晶体,速率加快
(3)高铁酸钾(K2FeO4)是一种高效多功能水处理剂。K2FeO4可以铁为电极,通过电解浓的KOH溶液来制取,写出电解法制取K2FeO4的阳极反应式:__________________ 。
(4)工业上常用铝土矿(含SiO2等杂质)生产铝。从Na2SiO3和NaAlO2混合溶液中制得Al(OH)3,需要从下列试剂中选择两种,选用的试剂组合最好是________ 。
a.NaOH溶液 b.氨水 c.CO2 d.盐酸
(5)四氢铝锂(LiAlH4)是有机合成中重要的还原剂,溶解于NaOH溶液时产生一种无色气体,请完成并配平该反应的离子方程式。
LiAlH4+_________ =____________ +___________ +__________
(1)工业上可用Cu2S和O2反应制取粗铜,该反应中氧化剂为
(2)铁元素与氯元素可形成FeCl2和FeCl3两种化合物,下列说法正确的是
①保存FeCl2溶液时,需向溶液中加入少量Fe
②FeCl2只能通过置换反应生成,FeCl3只能通过化合反应生成
③铜片、碳棒和FeCl3溶液组成原电池,电子由铜片沿导线流向碳棒
④向淀粉-碘化钾溶液中滴加几滴FeCl2的浓溶液,原无色溶液变为蓝色
⑤纯铁与稀盐酸反应产生氢气的速率较慢;再加入少量CuCl2·2H2O晶体,速率加快
(3)高铁酸钾(K2FeO4)是一种高效多功能水处理剂。K2FeO4可以铁为电极,通过电解浓的KOH溶液来制取,写出电解法制取K2FeO4的阳极反应式:
(4)工业上常用铝土矿(含SiO2等杂质)生产铝。从Na2SiO3和NaAlO2混合溶液中制得Al(OH)3,需要从下列试剂中选择两种,选用的试剂组合最好是
a.NaOH溶液 b.氨水 c.CO2 d.盐酸
(5)四氢铝锂(LiAlH4)是有机合成中重要的还原剂,溶解于NaOH溶液时产生一种无色气体,请完成并配平该反应的离子方程式。
LiAlH4+
您最近一年使用:0次
13-14高三·江西·阶段练习
2 . 实验室采用MgCl2、AlCl3的混合溶液与过量氨水反应制备MgAl2O4二主要流程如下:
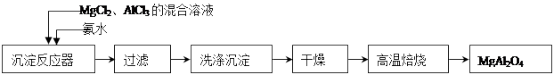

(1)制备MgAl2O4过程中,高温焙烧时发生反应的化学方程式_____________ 。
(2)如图所示,过滤操作中的一处错误是________________ 。
判断流程中沉淀是否洗净所用的试剂是___________ 。高温焙烧时,用于盛放固 体的仪器名称是___________ 。
(3)在25℃下,向浓度均为0.01 mol・L-1的MgCl2和AlCl3混合溶液中逐滴加入氨水,先生成_________________ 沉淀(填化学式),生成该沉淀的离子方程式_____________________ (已知25℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Al(OH)3]="3×10" -34。)
(4)无水AlCl3(183℃升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。
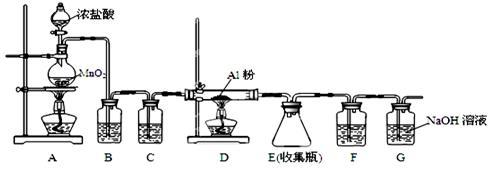
装置B中盛放饱和NaCl溶液,该装置的主要作用是_________ ;F中试剂的作用是________ ;用一件仪器装填适当试剂后也可起到F和G的作用,所装填的试剂为___________________ 。
(5)将Mg、Cu组成的3.92g混合物投入过量稀硝酸中,充分反应后,固体完全溶解时收集到还原产物NO气体1.792L(标准状况),向反应后的溶液中加入4mol/L的NaOH溶液80mL时金属离子恰好完全沉淀。则形成沉淀的质量为_______________________ g。


(1)制备MgAl2O4过程中,高温焙烧时发生反应的化学方程式
(2)如图所示,过滤操作中的一处错误是

判断流程中沉淀是否洗净所用的试剂是
(3)在25℃下,向浓度均为0.01 mol・L-1的MgCl2和AlCl3混合溶液中逐滴加入氨水,先生成
(4)无水AlCl3(183℃升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。

装置B中盛放饱和NaCl溶液,该装置的主要作用是
(5)将Mg、Cu组成的3.92g混合物投入过量稀硝酸中,充分反应后,固体完全溶解时收集到还原产物NO气体1.792L(标准状况),向反应后的溶液中加入4mol/L的NaOH溶液80mL时金属离子恰好完全沉淀。则形成沉淀的质量为
您最近一年使用:0次
名校
3 . 向59.2 g Fe2O3和FeO的混合物中加入某浓度的稀硝酸1.0 L,固体物质完全反应,生成NO和Fe(NO3)3。在所得溶液中加入1.0 mol/L的NaOH溶液2.8 L,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为85.6 g。下列有关说法错误的是
| A.Fe2O3与FeO的物质的量之比为1∶6 |
| B.硝酸的物质的量浓度为3.0 mol/L |
| C.产生的NO在标准状况下的体积为4.48 L |
| D.Fe2O3,FeO与硝酸反应后剩余HNO3为0.2 mol |
您最近一年使用:0次
2016-11-17更新
|
3600次组卷
|
21卷引用:2016届辽宁省沈阳市第二中学高三10月月考化学试卷
2016届辽宁省沈阳市第二中学高三10月月考化学试卷2016届湖南省衡阳市第八中学高三上学期第三次月考化学试卷2017届湖南省衡阳八中高三上学期9月月考化学试卷2017届辽宁省瓦房店市高级中学高三上10月月考化学试卷四川省眉山中学2018届高三10月月考理科综合化学试题甘肃省天水市第一中学2017-2018学年度上学期高三第三阶段考试化学试题甘肃省天水市一中2018届高三上学期第三学段考试化学试题云南省玉溪第一中学2017-2018学年高一下学期4月月考化学试题云南省玉溪市玉溪一中2017-2018学年高一下学期4月月考化学试题(已下线)《2018,我的高考我的教师君》-【临考技能篇】速解高考题——高考化学题型分类技巧指导(已下线)解密03 氧化还原反应——备战2018年高考化学之高频考点解密四川省广安市第二中学2019届高三上学期第一次月考化学试题(已下线)考点05 氧化还原反应——备战2019年浙江新高考化学考点(已下线)2019年1月16日 《每日一题》高考二轮复习-铁及其化合物湖南省长沙市雅礼中学2020-2021学年高一下学期期中考试化学试题浙江省台州市书生中学2021-2022学年高一下学期阶段性测试(3月)化学试题湖南省邵阳市第二中学2021-2022学年高一下学期期中考试化学试题湖南省邵东市第一中学2021-2022学年高一下学期第三次月考化学试题辽宁省实验中学2022-2023学年高三上学期期中考试化学试题江西省宜春市丰城拖船中学2023-2024学年高三上学期11月期中化学试题河南省周口市太康县第一高级中学2023-2024学年高一下学期4月第三次月考化学试题
解题方法
4 . 硼氢化钠(NaBH4)为白色粉末,容易吸水潮解,可溶于异丙胺(熔点:-101℃,沸点:33℃),在干空气中稳定,在湿空气中分解,是无机合成和有机合成中常用的选择性还原剂.某研究小组采用偏硼酸钠(NaBO2)为主要原料制备NaBH4,其流程如下:
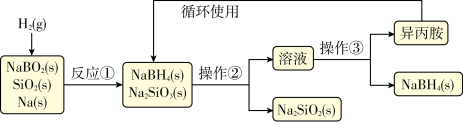
下列说法不正确的是( )

下列说法不正确的是( )
| A.实验室中取用少量钠需要用到的实验用品有镊子、滤纸、玻璃片和小刀 |
| B.操作②、操作③分别是过滤与蒸发结晶 |
| C.反应①加料之前需将反应器加热至100℃以上并通入氩气 |
| D.反应①中氧化剂与还原剂的物质的量之比为1:2 |
您最近一年使用:0次
2016-07-12更新
|
1193次组卷
|
7卷引用:2016届浙江省金丽衢十二校高三第二次联考理综化学试卷
5 . 已知:Fe2+能被稀硝酸氧化,反应方程式:3Fe(NO3)2+ 4HNO3(稀) ="=" 3 Fe(NO3)3+ NO↑+ 2H2O
现将一定量的铁和铜的混合物分为等质量的4份,分别加入等浓度不同体积的稀硝酸(假设反应中稀硝酸的还原产物只有NO),产生气体的体积与剩余固体的质量如下表:
(1)放出4480 mL气体时,消耗金属的质量为_______g
(2)稀硝酸的浓度为_______mol·L-1
(3)计算原混合物中铁和铜的物质的量比为
(4)加入400 mL稀硝酸,反应完全后,溶液中硝酸根离子的物质的量为 。
现将一定量的铁和铜的混合物分为等质量的4份,分别加入等浓度不同体积的稀硝酸(假设反应中稀硝酸的还原产物只有NO),产生气体的体积与剩余固体的质量如下表:
| 硝酸体积(mL) | 100 | 200 | 300 | 400 |
| 剩余固体(g) | 18.0 | 9.6 | 0 | 0 |
| 放出气体的体积(mL) | 2240 | 4480 | 6720 |
(1)放出4480 mL气体时,消耗金属的质量为_______g
(2)稀硝酸的浓度为_______mol·L-1
(3)计算原混合物中铁和铜的物质的量比为
(4)加入400 mL稀硝酸,反应完全后,溶液中硝酸根离子的物质的量为 。
您最近一年使用:0次
解题方法
6 . 常温下钛的化学活性很小,在较高温度下可与多种物质反应。工业上由金红石(含TiO2大于96%)为原料生产钛的流程如下:
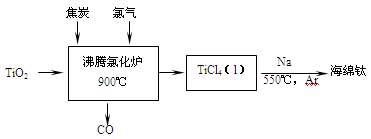
(1)TiCl4遇水强烈水解,写出其水解的化学方程式___________________ 。
(2)①若液氯泄漏后遇到苯,在钢瓶表面氯与苯的反应明显加快,原因是___________ 。
②Cl2含量检测仪工作原理如下图,则Cl2在Pt电极放电的电极反应式为_______ 。

③实验室也可用KClO3和浓盐酸制取Cl2,方程式为:KClO3+ 6HCl(浓) =" KCl" + 3Cl2↑+ 3H2O。
当生成6.72LCl2(标准状况下)时,转移的电子的物质的量为____ mol。
(3)一定条件下CO可以发生如下反应:4H2(g)+2CO(g) CH3OCH3(g)+H2O(g) △H。
CH3OCH3(g)+H2O(g) △H。
①该反应的平衡常数表达式为K=_____________ 。
②将合成气以n(H2)/n(CO)=2通入1 L的反应器中,CO的平衡转化率随温度、压强变化关系如图所示,下列判断正确的是___________ (填序号)。
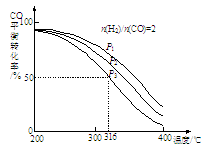
a.△H <0
b.P1<P2<P3
c.若在P3和316℃时,起始时n(H2)/n(CO)=3,则达到平衡时,CO转化率小于50%
③采用一种新型的催化剂(主要成分是Cu-Mn的合金),利用CO和H2制备二甲醚(简称DME)。观察下图回答问题。
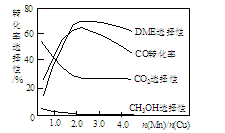
催化剂中n(Mn)/n(Cu)约为___________ 时最有利于二甲醚的合成。

(1)TiCl4遇水强烈水解,写出其水解的化学方程式
(2)①若液氯泄漏后遇到苯,在钢瓶表面氯与苯的反应明显加快,原因是
②Cl2含量检测仪工作原理如下图,则Cl2在Pt电极放电的电极反应式为

③实验室也可用KClO3和浓盐酸制取Cl2,方程式为:KClO3+ 6HCl(浓) =" KCl" + 3Cl2↑+ 3H2O。
当生成6.72LCl2(标准状况下)时,转移的电子的物质的量为
(3)一定条件下CO可以发生如下反应:4H2(g)+2CO(g)
 CH3OCH3(g)+H2O(g) △H。
CH3OCH3(g)+H2O(g) △H。①该反应的平衡常数表达式为K=
②将合成气以n(H2)/n(CO)=2通入1 L的反应器中,CO的平衡转化率随温度、压强变化关系如图所示,下列判断正确的是

a.△H <0
b.P1<P2<P3
c.若在P3和316℃时,起始时n(H2)/n(CO)=3,则达到平衡时,CO转化率小于50%
③采用一种新型的催化剂(主要成分是Cu-Mn的合金),利用CO和H2制备二甲醚(简称DME)。观察下图回答问题。

催化剂中n(Mn)/n(Cu)约为
您最近一年使用:0次
2015-03-20更新
|
1263次组卷
|
2卷引用:2015届江苏省泰州市姜堰区高三下学期期初联考化学试卷
解题方法
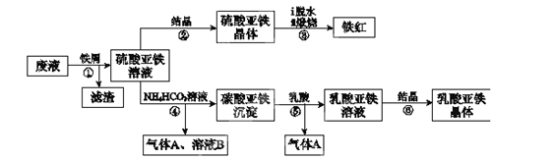
7 . 某工厂对工业生产钛白粉产生的废液进行综合利用,废液中含有大量FeSO4、H2SO4和少量Fe2(SO4)3、TiOSO4,可用于生产颜料铁红和补血剂乳酸亚铁。其生产工艺流程如下:(已知乳酸酸性强于碳酸)
已知:①TiOSO4可溶于水,在水中可以电离为TiO2+和SO42—;
②TiOSO4水解的反应为:TiOSO4+(x+1)H2O →TiO2 • xH2O↓+H2SO4。
请回答:
(1)步骤①所得滤渣的主要成分为____________________ ,分离硫酸亚铁溶液和滤渣的操作中所用的玻璃仪器是____________________ ;步骤②中得到纯净硫酸亚铁晶体的操作为蒸发浓缩、____________________ 。
(2)步骤③硫酸亚铁在空气中煅烧生成铁红和三氧化硫,该反应中氧化剂和还原剂的物质的量之比为____________________ 。
(3)步骤④的离子方程式是____________________ 。
(4)试用平衡移动原理解释步骤⑤生成乳酸亚铁的原因:____________________ 。
(5)实验室中常用KMnO4滴定法测定晶体中FeSO4·7H2O的质量分数,取步骤②中所得FeSO4·7H2O晶体样品a g,配成500.00 mL溶液,取出25.00 mL溶液,用KMnO4溶液滴定(杂质与KMnO4不反应)。若消耗0.1000 mol•L-1KMnO4溶液25.00 mL,所得晶体中FeSO4·7H2O的质量分数为(用a表示)____________________ 。

已知:①TiOSO4可溶于水,在水中可以电离为TiO2+和SO42—;
②TiOSO4水解的反应为:TiOSO4+(x+1)H2O →TiO2 • xH2O↓+H2SO4。
请回答:
(1)步骤①所得滤渣的主要成分为
(2)步骤③硫酸亚铁在空气中煅烧生成铁红和三氧化硫,该反应中氧化剂和还原剂的物质的量之比为
(3)步骤④的离子方程式是
(4)试用平衡移动原理解释步骤⑤生成乳酸亚铁的原因:
(5)实验室中常用KMnO4滴定法测定晶体中FeSO4·7H2O的质量分数,取步骤②中所得FeSO4·7H2O晶体样品a g,配成500.00 mL溶液,取出25.00 mL溶液,用KMnO4溶液滴定(杂质与KMnO4不反应)。若消耗0.1000 mol•L-1KMnO4溶液25.00 mL,所得晶体中FeSO4·7H2O的质量分数为(用a表示)
您最近一年使用:0次
12-13高三上·吉林长春·阶段练习
8 . 卤化物和卤酸盐在工业生产中有着重要的作用。某小组为探究其中一些盐的性质,查阅资料并进行实验。查阅资料如下:
① BrO3- + 6I- + 6H+ = 3I2+ Br-+ 3H2O
② 2BrO3- + I2= 2IO3- + Br2
③ IO3- + 5I- + 6H+ = 3I2+ 3H2O
④ 2IO3- + 10Br-+ 12H+ = I2+ 5Br2+ 6H2O
实验如下:
请回答:
(1)步骤ⅰ开始时发生的反应如资料①所示,溶液中I-完全被氧化时转移 mol e-,该反应中硫酸表现出的化学性质是 。
(2)上述资料中的反应 (填序号)可表示步骤ⅱ中的反应,通过该反应 (填“能”或“不能”)说明碘的非金属性强于溴,原因是 。
(3)根据资料中的反应①~④并结合所学知识,判断IO3-、BrO3-、I2、Br2的氧化性由强到弱的顺序是 ;KBrO3溶液与KBr溶液在酸性条件下反应的离子方程式是 。
(4)若用y表示锥形瓶中含碘物质的物质的量,用x表示所滴入KBrO3的物质的量,在图中画出上述整个实验过程中y随x的变化曲线(要求:在图中标出终点坐标)。
① BrO3- + 6I- + 6H+ = 3I2+ Br-+ 3H2O
② 2BrO3- + I2= 2IO3- + Br2
③ IO3- + 5I- + 6H+ = 3I2+ 3H2O
④ 2IO3- + 10Br-+ 12H+ = I2+ 5Br2+ 6H2O
实验如下:
| 步骤 | 现象 |
| ⅰ. 向盛有30 mL 0.2 mol·L-1 KI溶液的锥形瓶中依次滴入几滴淀粉溶液和足量稀硫酸,再用滴定管逐滴加入KBrO3溶液 | 随着KBrO3溶液的滴入,溶液由无色变为蓝色并逐渐加深,最终保持不变 |
| ⅱ. 继续向上述溶液中滴入KBrO3溶液 | 溶液的蓝色逐渐褪去 |
请回答:
(1)步骤ⅰ开始时发生的反应如资料①所示,溶液中I-完全被氧化时转移 mol e-,该反应中硫酸表现出的化学性质是 。
(2)上述资料中的反应 (填序号)可表示步骤ⅱ中的反应,通过该反应 (填“能”或“不能”)说明碘的非金属性强于溴,原因是 。
(3)根据资料中的反应①~④并结合所学知识,判断IO3-、BrO3-、I2、Br2的氧化性由强到弱的顺序是 ;KBrO3溶液与KBr溶液在酸性条件下反应的离子方程式是 。
(4)若用y表示锥形瓶中含碘物质的物质的量,用x表示所滴入KBrO3的物质的量,在图中画出上述整个实验过程中y随x的变化曲线(要求:在图中标出终点坐标)。

您最近一年使用:0次



