名校
解题方法
1 . CuS、Cu2S用于处理酸性废水中的Cr2O 反应如下:
反应如下:
反应I: CuS+Cr2O +H+ →Cu2++SO
+H+ →Cu2++SO +Cr3++H2O(未配平)
+Cr3++H2O(未配平)
反应II:Cu2S+ Cr2O +H+→Cu2++SO
+H+→Cu2++SO +Cr3++H2O(未配平)
+Cr3++H2O(未配平)
下列说法正确的是
 反应如下:
反应如下:反应I: CuS+Cr2O
 +H+ →Cu2++SO
+H+ →Cu2++SO +Cr3++H2O(未配平)
+Cr3++H2O(未配平) 反应II:Cu2S+ Cr2O
 +H+→Cu2++SO
+H+→Cu2++SO +Cr3++H2O(未配平)
+Cr3++H2O(未配平)下列说法正确的是
| A.反应I和II中各有 2种元素的化合价发生变化 |
| B.反应II中还原剂与氧化剂的物质的量之比为3:5 |
C.处理1molCr2O 时反应I、II中消耗H+的物质的量相等 时反应I、II中消耗H+的物质的量相等 |
D.质量相同时,Cu2S能去除更多的Cr2O |
您最近一年使用:0次
2020-12-05更新
|
224次组卷
|
8卷引用:湖南省株洲市攸县第四中学2022-2023学年高三上学期第四次月考化学试题
湖南省株洲市攸县第四中学2022-2023学年高三上学期第四次月考化学试题(已下线)小题必刷08 氧化还原反应的规律及应用——2021年高考化学一轮复习小题必刷(通用版)(已下线)【南昌新东方】4. 2020 高一上 南大附中 期中 项金辉安徽省六安市城南中学2021届高三上学期第二次月考化学试题四川省内江市威远中学2020-2021学年高一下学期期中考试化学试题河南省信阳市2021-2022学年高三上学期第一次教学质量检测化学试题(已下线)专题04 氧化还原反应及其应用(练)-2023年高考化学二轮复习讲练测(新高考专用)湖北省宜昌英杰学校2021-2022学年高三上学期10月月考化学试题
解题方法
2 . 按要求回答下列各题:
I.已知实验室制取氯气的反应原理为:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,据此回答下列问题:
MnCl2+Cl2↑+2H2O,据此回答下列问题:
(1)氧化剂是__________ (填写化学式),发生__________ 反应;还原剂是__________ (填写化学式),发生__________ 反应;氧化产物是__________ (填写化学式),还原产物是__________ (填写化学式);氧化剂和还原剂个数比是______ 。
(2)该实验室制取氯气反应的离子方程式为_____________________________________ 。
II.用双线桥法表示电子转移的方向和数目:KClO3+6HCl(浓) KCl+3Cl2↑+3H2O
KCl+3Cl2↑+3H2O _____________________________________
III. 医学上常用酸性高锰酸钾溶液与草酸溶液的反应来测定血钙的含量,配平以下离子方程式,并填上合适的微粒:___ H++___ MnO +
+___ H2C2O4 =___ CO2↑+___ Mn2++______
I.已知实验室制取氯气的反应原理为:MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O,据此回答下列问题:
MnCl2+Cl2↑+2H2O,据此回答下列问题:(1)氧化剂是
(2)该实验室制取氯气反应的离子方程式为
II.用双线桥法表示电子转移的方向和数目:KClO3+6HCl(浓)
 KCl+3Cl2↑+3H2O
KCl+3Cl2↑+3H2O III. 医学上常用酸性高锰酸钾溶液与草酸溶液的反应来测定血钙的含量,配平以下离子方程式,并填上合适的微粒:
 +
+
您最近一年使用:0次
名校
解题方法
3 . 铬元素及其化合物在生产、生活中具有广泛的用途。以某铬矿石(主要成分是Cr2O3,含Fe2O3、SiO2等杂质)为原料生产Cr2O3的流程如下:
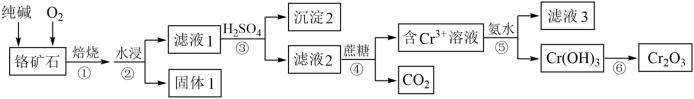
(1)为了提高焙烧速率,可采取的措施有_______ (写出2种方法)。Cr2O3在焙烧时生成Na2CrO4,写出第①步发生的所有方程式_____________ 。
(2)沉淀2的化学式为______ 。
(3)步骤③中CrO 转化成Cr2O
转化成Cr2O ,能否将硫酸换成盐酸,并说明其理由
,能否将硫酸换成盐酸,并说明其理由_______ 。
(4)步骤⑤的分离方法为______ 。滤液3中主要溶质的化学式为________ 。
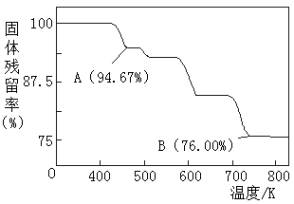
(5)CrO3的热稳定性较差,加热时逐步分解,其固体残留率随温度的变化如图所示,则B点时铬的氧化物化学式为_____________ 。

(1)为了提高焙烧速率,可采取的措施有
(2)沉淀2的化学式为
(3)步骤③中CrO
 转化成Cr2O
转化成Cr2O ,能否将硫酸换成盐酸,并说明其理由
,能否将硫酸换成盐酸,并说明其理由(4)步骤⑤的分离方法为
(5)CrO3的热稳定性较差,加热时逐步分解,其固体残留率随温度的变化如图所示,则B点时铬的氧化物化学式为

您最近一年使用:0次
名校
4 . 已知A、B、C、D、E、W分属于三个短周期的主族元素,且原子序数依次增大。 B的氢化物水溶液呈碱性,C的原子最外层电子数是其电子层数的3倍;A、D同主族,C、E同主族。请回答下列问题:
(1)B、D、E元素的简单离子半径由大到小顺序为(用离子符号表示)__________________ ;
(2)D2E2可以做制革工业中原皮的脱毛剂,写出D2E2(写化学符号)的电子式______________ ;
(3)D2E2C4中E元素的化合价为_______ ;D2E2C4暴露于空气中易吸收氧气和水蒸气而变质,发生反应时,当氧化剂和还原剂的物质的量之比为1:2时,反应的化学方程式为_____________ ;
(4)利用尿素CO(NH2)2制备B2A4·H2O的实验流程如下图所示
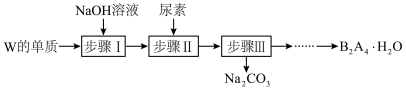
已知:W的单质与烧碱溶液的反应是放热反应;B2A4·H2O有强还原性,能与DWC剧烈反应生成B的单质。
①实验中,为使步骤Ⅰ中反应温度不高于40 ℃,除可采用减慢W单质通入速率之外,还可采取的措施是__________ 。
②写出流程图中生成B2A4·H2O反应的化学方程式:___________ ;
③蒸馏分离得B2A4·H2O粗产品,称取馏分0.350 0 g,加水配成20.0 mL溶液,在一定条件下,用0.650 0 mol·L-1的碘的标准溶液滴定。已知:B2A4·H2O+2I2=B2↑+4AI+H2O。滴定时,选用的指示剂为_____ 。若达到滴定终点时消耗碘的标准溶液20.00 mL,馏分中B2A4·H2O的质量分数为___________ 。(保留4位有效数字)。
(1)B、D、E元素的简单离子半径由大到小顺序为(用离子符号表示)
(2)D2E2可以做制革工业中原皮的脱毛剂,写出D2E2(写化学符号)的电子式
(3)D2E2C4中E元素的化合价为
(4)利用尿素CO(NH2)2制备B2A4·H2O的实验流程如下图所示

已知:W的单质与烧碱溶液的反应是放热反应;B2A4·H2O有强还原性,能与DWC剧烈反应生成B的单质。
①实验中,为使步骤Ⅰ中反应温度不高于40 ℃,除可采用减慢W单质通入速率之外,还可采取的措施是
②写出流程图中生成B2A4·H2O反应的化学方程式:
③蒸馏分离得B2A4·H2O粗产品,称取馏分0.350 0 g,加水配成20.0 mL溶液,在一定条件下,用0.650 0 mol·L-1的碘的标准溶液滴定。已知:B2A4·H2O+2I2=B2↑+4AI+H2O。滴定时,选用的指示剂为
您最近一年使用:0次
名校
解题方法
5 . Cl2在70℃的NaOH水溶液中,能同时发生两个自身氧化还原反应,反应完全后测得溶液中NaClO与NaClO3的物质的量之比为1︰2,若有0.7molCl2参加反应,则该反应中转移的电子的物质的量为
| A.0.7mol | B.1.1mol | C.1.4mol | D.2.2mol |
您最近一年使用:0次
2020-12-01更新
|
166次组卷
|
2卷引用:湖南省常德市临澧县一中2021届高三第四次检测(期中)考试化学试题
名校
解题方法
6 . 分析以下A~D四个涉及H2O2的反应(未配平),填空:
A.
B.
C.
D.
(1)H2O2仅体现氧化性的反应是________ ,H2O2体现还原性的反应是________ ,H2O2既体现氧化性,又体现还原性的反应是________ ,H2O2既不作氧化剂又不作还原剂的反应是________ (填字母)。
(2)用单线桥法表示D反应中电子转移的方向和数目:

_______________________________________________ 。
该反应中氧化剂是________ ,氧化产物是________ 。
(3)已知:在一定条件下H2O2能和酸性高锰酸钾溶液反应生成O2,请完成下列缺项方程式的配平:
____ 
____ 
____ ( ) = ____ 
____ 
____ ( )
在该反应中H2O2作________ 剂。
A.

B.

C.

D.

(1)H2O2仅体现氧化性的反应是
(2)用单线桥法表示D反应中电子转移的方向和数目:

该反应中氧化剂是
(3)已知:在一定条件下H2O2能和酸性高锰酸钾溶液反应生成O2,请完成下列缺项方程式的配平:




在该反应中H2O2作
您最近一年使用:0次
名校
7 . 垃圾分类意义重大,工业上回收光盘金属层中的Ag的流程如图所示,下列说法正确的是
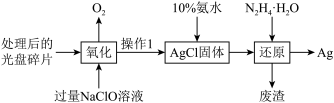

| A.氧化过程中参加反应的Ag和NaClO的物质的量比之为1:1 |
| B.为了提高氧化过程的反应速率和产率,氧化过程应该在酸性、加强热条件下进行 |
| C.氧化过程中,可以用HNO3代替NaClO 氧化Ag |
D.还原过程,若水合肼转化为无害气体 ,则还原过程的离子方程式为4Ag++N2H4 ,则还原过程的离子方程式为4Ag++N2H4 H2O+4OH-=4Ag↓+N2↑+5H2O H2O+4OH-=4Ag↓+N2↑+5H2O |
您最近一年使用:0次
2020-11-25更新
|
868次组卷
|
8卷引用:湖南省临澧县第一中学2021-2022学年高三上学期第四阶段性考试化学试题
湖南省临澧县第一中学2021-2022学年高三上学期第四阶段性考试化学试题山东师范大学附属中学2021届高三上学期期中考试(11月)化学试题辽宁省名校联盟2021届高三3月联合考试化学试题福建省莆田二中、泉州一中、南安一中三校2020-2021学年高三下学期联考化学试题(已下线)卷05 工艺流程型选择题-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)河北省石家庄市2023届高中毕业年级教学质量检测(一模)变式题(选择题11-14)(已下线)第5讲 氧化还原反应方程式的配平与计算广东省广州市执信中学2021届高三第五次月考化学试题
名校
8 . (1)维生素C又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有___ (填“氧化性”或“还原性”)。
(2)我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为:S+2KNO3+3C=K2S+N2↑+3CO2↑
在该反应中,还原剂是____ (填化学式,下同),氧化剂是___ 。
(3)把碎纸片b补充到a中,可得到一个完整的离子方程式(未配平)。
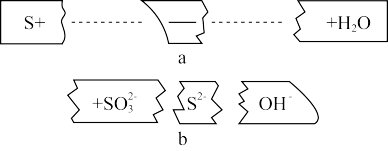
①写出并配平该反应的离子方程式:___ 。
②在上述反应中,用双线桥标出电子转移的方向和数目___ 。
(2)我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为:S+2KNO3+3C=K2S+N2↑+3CO2↑
在该反应中,还原剂是
(3)把碎纸片b补充到a中,可得到一个完整的离子方程式(未配平)。
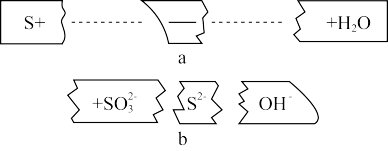
①写出并配平该反应的离子方程式:
②在上述反应中,用双线桥标出电子转移的方向和数目
您最近一年使用:0次
名校
9 .  储氢材料、燃料电池等方面具有重要应用。
储氢材料、燃料电池等方面具有重要应用。
(1) 中H元素的化合价为
中H元素的化合价为 ,具有强还原性,一定条件下,向
,具有强还原性,一定条件下,向 溶液中滴加碱性
溶液中滴加碱性 溶液,溶液中
溶液,溶液中 与
与 反应生成纳米铁粉、
反应生成纳米铁粉、 和
和 ,参加反应的
,参加反应的 与生成的纳米铁粉的物质的量之比为
与生成的纳米铁粉的物质的量之比为________ 。
(2) 燃料电池中,
燃料电池中, 转化为
转化为 ,电解
,电解 溶液又可制得
溶液又可制得 ,实现物质的循环利用,电解装置示意图如图所示。
,实现物质的循环利用,电解装置示意图如图所示。

①电解池阴极的电极反应式为_______ 。
②两电极区间使用阳离子交换膜,不允许阴离子通过的原因是_______ 。
(3) 催化释氢。在催化剂作用下,
催化释氢。在催化剂作用下, 与水反应生成
与水反应生成 ,可能的反应机理如图所示。
,可能的反应机理如图所示。

①其他条件不变时,以 代替
代替 催化释氢,所得气体的分子式为
催化释氢,所得气体的分子式为________ 。
②已知: 为一元弱酸,
为一元弱酸, 水溶液呈酸性的原因是
水溶液呈酸性的原因是_______ (用离子方式表示)。
(4)在催化剂的作用下, 与水反应,释氢体积及温度随反应时间的变化如图所示。
与水反应,释氢体积及温度随反应时间的变化如图所示。

①0~20min内,温度随时间快速升高的原因是______ 。
②20min后,氢气体积在增加,而温度却下降的原因是________ 。
 储氢材料、燃料电池等方面具有重要应用。
储氢材料、燃料电池等方面具有重要应用。(1)
 中H元素的化合价为
中H元素的化合价为 ,具有强还原性,一定条件下,向
,具有强还原性,一定条件下,向 溶液中滴加碱性
溶液中滴加碱性 溶液,溶液中
溶液,溶液中 与
与 反应生成纳米铁粉、
反应生成纳米铁粉、 和
和 ,参加反应的
,参加反应的 与生成的纳米铁粉的物质的量之比为
与生成的纳米铁粉的物质的量之比为(2)
 燃料电池中,
燃料电池中, 转化为
转化为 ,电解
,电解 溶液又可制得
溶液又可制得 ,实现物质的循环利用,电解装置示意图如图所示。
,实现物质的循环利用,电解装置示意图如图所示。
①电解池阴极的电极反应式为
②两电极区间使用阳离子交换膜,不允许阴离子通过的原因是
(3)
 催化释氢。在催化剂作用下,
催化释氢。在催化剂作用下, 与水反应生成
与水反应生成 ,可能的反应机理如图所示。
,可能的反应机理如图所示。
①其他条件不变时,以
 代替
代替 催化释氢,所得气体的分子式为
催化释氢,所得气体的分子式为②已知:
 为一元弱酸,
为一元弱酸, 水溶液呈酸性的原因是
水溶液呈酸性的原因是(4)在催化剂的作用下,
 与水反应,释氢体积及温度随反应时间的变化如图所示。
与水反应,释氢体积及温度随反应时间的变化如图所示。
①0~20min内,温度随时间快速升高的原因是
②20min后,氢气体积在增加,而温度却下降的原因是
您最近一年使用:0次
2020-11-25更新
|
558次组卷
|
6卷引用:湖南省常德市第一中学2023-2024学年高三上学期第六次月考化学试题
10 . 氮元素在海洋中的循环,是整个海洋生态系统的基础和关键。海洋中无机氮的循环过程可用下图表示。

(1)海洋中的氮循环起始于氮的固定,其中属于固氮作用的一步是_____ (填图中数字序号)。
(2)下列关于海洋氮循环的说法正确的是_____ (填字母序号)。
a.海洋中存在游离态的氮
b.海洋中的氮循环起始于氮的氧化
c.海洋中的反硝化作用一定有氧气的参与
d.向海洋排放含NO 的废水会影响海洋中NH
的废水会影响海洋中NH 的含量
的含量
(3)有氧时,在硝化细菌作用下,NH 可实现过程④的转化,将过程④的离子方程式补充完整:4NH
可实现过程④的转化,将过程④的离子方程式补充完整:4NH +5O2 =2NO
+5O2 =2NO +_____H++_____+
+_____H++_____+
____________________________________________________________
(4)为避免含氮废水对海洋氮循环系统的影响,需经处理后排放。右图是间接氧化工业废水中氨氮(NH )示意图。
)示意图。

①结合电极反应式简述间接氧化法去除氨氮的原理:_____ 。
② 若生成H2和N2的物质的量之比为3:1,则处理后废水的pH将______ 填“增大”“不变”或“减小”)。

(1)海洋中的氮循环起始于氮的固定,其中属于固氮作用的一步是
(2)下列关于海洋氮循环的说法正确的是
a.海洋中存在游离态的氮
b.海洋中的氮循环起始于氮的氧化
c.海洋中的反硝化作用一定有氧气的参与
d.向海洋排放含NO
 的废水会影响海洋中NH
的废水会影响海洋中NH 的含量
的含量(3)有氧时,在硝化细菌作用下,NH
 可实现过程④的转化,将过程④的离子方程式补充完整:4NH
可实现过程④的转化,将过程④的离子方程式补充完整:4NH +5O2 =2NO
+5O2 =2NO +_____H++_____+
+_____H++_____+ (4)为避免含氮废水对海洋氮循环系统的影响,需经处理后排放。右图是间接氧化工业废水中氨氮(NH
 )示意图。
)示意图。
①结合电极反应式简述间接氧化法去除氨氮的原理:
② 若生成H2和N2的物质的量之比为3:1,则处理后废水的pH将
您最近一年使用:0次



