名校
解题方法
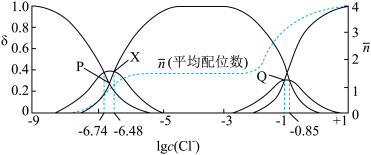
1 . 常温下,用Hg(NO3)2测定NaCl溶液中的c(Cl-)时,含Hg微粒的分布系数与lgc(Cl-)的关系如图所示。Hg2+与Cl-的配合物存在如下平衡: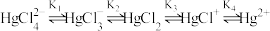 。下列说法正确的是
。下列说法正确的是
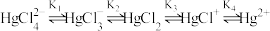 。下列说法正确的是
。下列说法正确的是
| A.当lgc(Cl-)=+1时主要以Hg2+形式存在 |
| B.当lgc(Cl-)﹤-3时Hg2+几乎没有与Cl-发生配合反应 |
C.在Q点:反应HgCl +Cl- +Cl- HgCl HgCl 的平衡常数K=10 的平衡常数K=10 |
D.反应HgCl++Cl- HgCl2的平衡常数大于反应HgCl2+Cl- HgCl2的平衡常数大于反应HgCl2+Cl- HgCl HgCl 的平衡常数 的平衡常数 |
您最近半年使用:0次
2024-01-22更新
|
372次组卷
|
2卷引用:山东省高中名校2023-2024学年高三上学期12月统一调研考试化学试题
名校
解题方法
2 . 向 溶液中滴加
溶液中滴加 溶液,发生反应
溶液,发生反应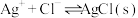 和
和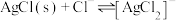 。
。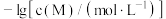 与
与 的关系如下图所示(其中
的关系如下图所示(其中 代表
代表 或
或 )。下列说法错误的是
)。下列说法错误的是
 溶液中滴加
溶液中滴加 溶液,发生反应
溶液,发生反应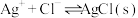 和
和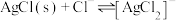 。
。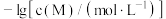 与
与 的关系如下图所示(其中
的关系如下图所示(其中 代表
代表 或
或 )。下列说法错误的是
)。下列说法错误的是
A.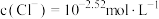 时,溶液中 时,溶液中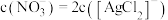 |
B.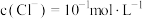 时,溶液中 时,溶液中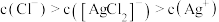 |
C. 的平衡常数 的平衡常数 的值为 的值为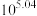 |
D.用 沉淀 沉淀 ,溶液中 ,溶液中 浓度过大时,沉淀效果不好 浓度过大时,沉淀效果不好 |
您最近半年使用:0次
2024-01-22更新
|
1037次组卷
|
5卷引用:2024年1月安徽普通高等学校招生考试适应性测试化学试题
2024年1月安徽普通高等学校招生考试适应性测试化学试题(已下线)选择题11-14(已下线)2024年1月“九省联考”安徽真题完全解读与考后提升(已下线)热点18 电解质溶液图像分析重庆市第八中学2023-2024学年高二下学期第一次月考化学试卷
名校
解题方法
3 . 绿色能源是未来能源发展的方向,积极发展氢能,是实现“碳达峰、碳中和”的重要举措,可以用以下方法制备氢气。
Ⅰ.甲烷和水蒸气催化制氢气。主要反应如下:
i.CH4(g)+H2O(g)⇌CO(g)+3H2(g) ΔH=+206.2kJ•mol-1
ii.CO(g)+H2O(g)⇌CO2(g)+H2(g) ΔH=-41.2kJ•mol-1
(1)反应CH4(g)+CO2(g)⇌2CO(g)+2H2(g)的 ΔH=___________ kJ•mol-1。
(2)在容积不变的绝热密闭容器中发生反应i,下列能说明反应达到平衡状态的是___________ (填标号)。
A.气体混合物的密度不再变化
B.CH4消耗速率和H2的生成速率相等
C.CO的浓度保持不变
D.气体平均相对分子质量不再变化
E.体系的温度不再发生变化
(3)恒定压强为P0MPa时,将n(CH4):n(H2O)=1:3的混合气体投入反应器中发生反应i和ii,平衡时,各组分的物质的量分数与温度的关系如图所示。
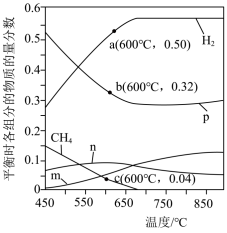
①图中表示CO2的物质的量分数与温度的变化曲线是___________ (填字母)。
②结合图中数据,其他条件不变,若要H2的产量最大,最适宜的反应温度是___________ (填标号)。
A.550~600℃ B.650~700℃ C.750~800℃
在其他条件不变的情况下,向体系中加入CaO可明显提高平衡体系中H2的含量,原因是________ 。
③600℃时,反应ii的平衡常数的计算式为Kp=___________ (Kp是以分压表示的平衡常数,分压=总压×物质的量分数)。
Ⅱ.“氰化提金”产生的废水中含有一定量的 ,为处理含氰废水科研人员进行了大量研究。回答下列问题:
,为处理含氰废水科研人员进行了大量研究。回答下列问题:
(4)25℃,氢氰酸(HCN)、碳酸在水中的电离常数如下表:
①将少量 通入NaCN溶液中,反应的离子方程式是
通入NaCN溶液中,反应的离子方程式是___________ 。
②常温下,在 溶液中加入
溶液中加入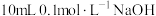 溶液。所得混合溶液中离子浓度由大到小的顺序是
溶液。所得混合溶液中离子浓度由大到小的顺序是___________ 。
Ⅰ.甲烷和水蒸气催化制氢气。主要反应如下:
i.CH4(g)+H2O(g)⇌CO(g)+3H2(g) ΔH=+206.2kJ•mol-1
ii.CO(g)+H2O(g)⇌CO2(g)+H2(g) ΔH=-41.2kJ•mol-1
(1)反应CH4(g)+CO2(g)⇌2CO(g)+2H2(g)的 ΔH=
(2)在容积不变的绝热密闭容器中发生反应i,下列能说明反应达到平衡状态的是
A.气体混合物的密度不再变化
B.CH4消耗速率和H2的生成速率相等
C.CO的浓度保持不变
D.气体平均相对分子质量不再变化
E.体系的温度不再发生变化
(3)恒定压强为P0MPa时,将n(CH4):n(H2O)=1:3的混合气体投入反应器中发生反应i和ii,平衡时,各组分的物质的量分数与温度的关系如图所示。

①图中表示CO2的物质的量分数与温度的变化曲线是
②结合图中数据,其他条件不变,若要H2的产量最大,最适宜的反应温度是
A.550~600℃ B.650~700℃ C.750~800℃
在其他条件不变的情况下,向体系中加入CaO可明显提高平衡体系中H2的含量,原因是
③600℃时,反应ii的平衡常数的计算式为Kp=
Ⅱ.“氰化提金”产生的废水中含有一定量的
 ,为处理含氰废水科研人员进行了大量研究。回答下列问题:
,为处理含氰废水科研人员进行了大量研究。回答下列问题:(4)25℃,氢氰酸(HCN)、碳酸在水中的电离常数如下表:
| 酸 | HCN |  |
 | 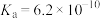 |   |
 通入NaCN溶液中,反应的离子方程式是
通入NaCN溶液中,反应的离子方程式是②常温下,在
 溶液中加入
溶液中加入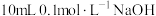 溶液。所得混合溶液中离子浓度由大到小的顺序是
溶液。所得混合溶液中离子浓度由大到小的顺序是
您最近半年使用:0次
名校
4 . 下列有关化学平衡图像描述正确的是
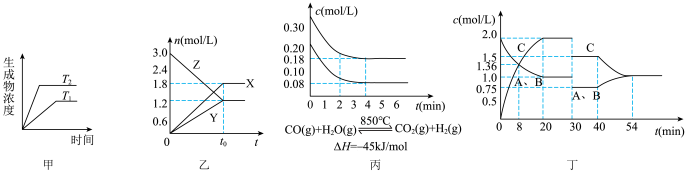

| A.图像甲T2>T1,代表任何可逆反应中生成物浓度随温度的变化关系图 |
| B.图像乙表示反应的化学方程式为:2Z(s)⇌3X(g)+2Y(g) |
| C.图像丙代表在10L容器、850℃时反应,到4min时,反应放出51.6kJ的热量 |
| D.图像丁代表在一定温度下发生反应A(g)+B(g)⇌2C(g),达到平衡后,只改变反应的一个条件,其在20∼40min之间的平衡常数不相等 |
您最近半年使用:0次
5 .  是存在于燃气中的一种有害气体,脱除
是存在于燃气中的一种有害气体,脱除 的方法有多种。回答下列问题:
的方法有多种。回答下列问题:
(1)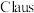 氧化回收硫的反应原理为:
氧化回收硫的反应原理为:
i: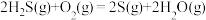
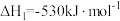 ;
;
ii: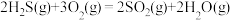
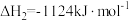
iii: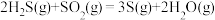

①根据盖斯定律,反应iii中的
______  。
。
②化学反应的焓变与反应物和生成物的键能(气态分子中 化学键解离成气态原子所吸收的能量)有关。已知某些化学键的键能如下表所示:
化学键解离成气态原子所吸收的能量)有关。已知某些化学键的键能如下表所示:
结合(1)中反应原理a=___________ 。
(2)电解法治理 是先用
是先用 溶液吸收含
溶液吸收含 的工业废气,所得溶液用惰性电极电解,阳极区所得溶液循环利用。
的工业废气,所得溶液用惰性电极电解,阳极区所得溶液循环利用。
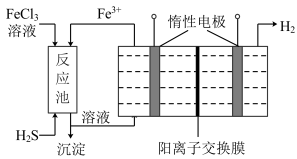
①进入电解池的溶液中,溶质是______ (填化学式)。
②阳极的电极反应式为_________ 。
(3)天然气中含有 杂质,某科研小组用氨水吸收得到
杂质,某科研小组用氨水吸收得到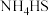 溶液,已知
溶液,已知 时,
时,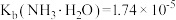 ,
,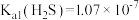 ,
,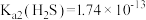 ,
,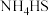 溶液中所含粒子浓度大小关系正确的是_______(填字母)。
溶液中所含粒子浓度大小关系正确的是_______(填字母)。
(4)工业上采用高温热分解 的方法制取
的方法制取 ,在膜反应器中分离出
,在膜反应器中分离出 。
。 下,
下, 分解:
分解: 。保持压强不变,反应达到平衡时,气体的体积分数
。保持压强不变,反应达到平衡时,气体的体积分数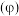 随温度的变化曲线如图:
随温度的变化曲线如图:
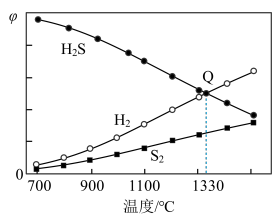
①在密闭容器中,关于上述反应的说法正确的是______ (填字母)。
A. 随温度的升高而增大
随温度的升高而增大
B.低压有利于提高 的平衡分解率
的平衡分解率
C.维持温度、气体总压强不变时,向平衡体系中通入氩气,则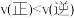
D.在恒容密闭容器中进行反应,当气体密度不再变化时,反应达到平衡状态
②图中Q点: 的平衡转化率为
的平衡转化率为______ ;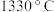 时,反应
时,反应 的
的
______  (
( 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。
 是存在于燃气中的一种有害气体,脱除
是存在于燃气中的一种有害气体,脱除 的方法有多种。回答下列问题:
的方法有多种。回答下列问题:(1)
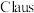 氧化回收硫的反应原理为:
氧化回收硫的反应原理为:i:
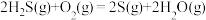
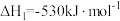 ;
;ii:
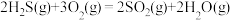
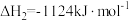
iii:
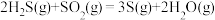

①根据盖斯定律,反应iii中的

 。
。②化学反应的焓变与反应物和生成物的键能(气态分子中
 化学键解离成气态原子所吸收的能量)有关。已知某些化学键的键能如下表所示:
化学键解离成气态原子所吸收的能量)有关。已知某些化学键的键能如下表所示:| 共价键 | 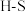 |  | 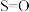 |  |
键能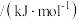 | 339 | 246 | a | 120 |
(2)电解法治理
 是先用
是先用 溶液吸收含
溶液吸收含 的工业废气,所得溶液用惰性电极电解,阳极区所得溶液循环利用。
的工业废气,所得溶液用惰性电极电解,阳极区所得溶液循环利用。
①进入电解池的溶液中,溶质是
②阳极的电极反应式为
(3)天然气中含有
 杂质,某科研小组用氨水吸收得到
杂质,某科研小组用氨水吸收得到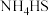 溶液,已知
溶液,已知 时,
时,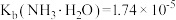 ,
,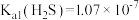 ,
,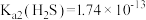 ,
,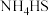 溶液中所含粒子浓度大小关系正确的是_______(填字母)。
溶液中所含粒子浓度大小关系正确的是_______(填字母)。A.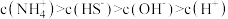 | B. |
C.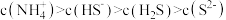 | D.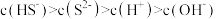 |
(4)工业上采用高温热分解
 的方法制取
的方法制取 ,在膜反应器中分离出
,在膜反应器中分离出 。
。 下,
下, 分解:
分解: 。保持压强不变,反应达到平衡时,气体的体积分数
。保持压强不变,反应达到平衡时,气体的体积分数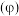 随温度的变化曲线如图:
随温度的变化曲线如图:
①在密闭容器中,关于上述反应的说法正确的是
A.
 随温度的升高而增大
随温度的升高而增大B.低压有利于提高
 的平衡分解率
的平衡分解率C.维持温度、气体总压强不变时,向平衡体系中通入氩气,则
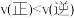
D.在恒容密闭容器中进行反应,当气体密度不再变化时,反应达到平衡状态
②图中Q点:
 的平衡转化率为
的平衡转化率为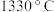 时,反应
时,反应 的
的
 (
( 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。
您最近半年使用:0次
名校
解题方法
6 . 习近平主席在第75届联合国大会提出:“我国要实现“2030年碳达峰、2060年碳中和的目标”。因此 的捕获利用与封存成为科学家研究的重要课题。
的捕获利用与封存成为科学家研究的重要课题。 和
和 的干法重整(DRM)反应可同时转化两种温室气体,并制备
的干法重整(DRM)反应可同时转化两种温室气体,并制备 和
和 。主要反应如下:
。主要反应如下:
反应Ⅰ: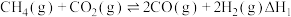 ;
;
反应Ⅱ: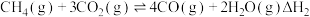 ;
;
反应Ⅲ: ;
;
已知:反应Ⅰ、Ⅱ的自发均需高温条件。
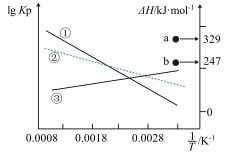
(1)上述三个反应的平衡常数 与温度T关系如图所示。图中a点代表的是
与温度T关系如图所示。图中a点代表的是___________ (填“Ⅰ”“Ⅱ”或“Ⅲ”)反应的 ,
,
___________  。
。
(2)将原料按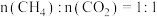 充入密闭容器中发生反应Ⅰ,保持体系压强为
充入密闭容器中发生反应Ⅰ,保持体系压强为 发生反应,达到平衡时
发生反应,达到平衡时 体积分数与温度的关系(图中黑线)如图所示:
体积分数与温度的关系(图中黑线)如图所示:
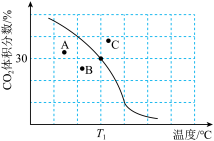
①T1℃,100kPa下,平衡时容器体积与初始容器体积之比为___________ ;该温度下,此反应的平衡常数
___________  (用平衡分压代替平衡浓度计算,分压=总压
(用平衡分压代替平衡浓度计算,分压=总压 物质的量分数)。
物质的量分数)。
②若A、B、C三点表示不同温度和压强下已达平衡时 的体积分数,
的体积分数,___________ 点对应的平衡常数最小,___________ 点对应的压强最大。
(3)在其他条件相同,不同催化剂(A、B)作用下,使原料 和
和 发生反应Ⅰ反应相同的时间,
发生反应Ⅰ反应相同的时间, 的产率随反应温度的变化如图:
的产率随反应温度的变化如图:
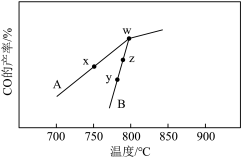
①在催化剂A、B作用下,它们正、逆反应活化能差值分别用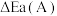 和
和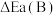 表示,则
表示,则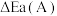
___________ 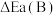 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
②y点对应的逆反应速率v(逆)___________ z点对应的正反应速率v()正)(填“>”“<”或“=”)
 的捕获利用与封存成为科学家研究的重要课题。
的捕获利用与封存成为科学家研究的重要课题。 和
和 的干法重整(DRM)反应可同时转化两种温室气体,并制备
的干法重整(DRM)反应可同时转化两种温室气体,并制备 和
和 。主要反应如下:
。主要反应如下:反应Ⅰ:
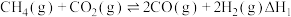 ;
;反应Ⅱ:
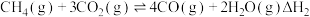 ;
;反应Ⅲ:
 ;
;已知:反应Ⅰ、Ⅱ的自发均需高温条件。
(1)上述三个反应的平衡常数
 与温度T关系如图所示。图中a点代表的是
与温度T关系如图所示。图中a点代表的是 ,
,
 。
。
(2)将原料按
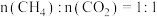 充入密闭容器中发生反应Ⅰ,保持体系压强为
充入密闭容器中发生反应Ⅰ,保持体系压强为 发生反应,达到平衡时
发生反应,达到平衡时 体积分数与温度的关系(图中黑线)如图所示:
体积分数与温度的关系(图中黑线)如图所示:
①T1℃,100kPa下,平衡时容器体积与初始容器体积之比为

 (用平衡分压代替平衡浓度计算,分压=总压
(用平衡分压代替平衡浓度计算,分压=总压 物质的量分数)。
物质的量分数)。②若A、B、C三点表示不同温度和压强下已达平衡时
 的体积分数,
的体积分数,(3)在其他条件相同,不同催化剂(A、B)作用下,使原料
 和
和 发生反应Ⅰ反应相同的时间,
发生反应Ⅰ反应相同的时间, 的产率随反应温度的变化如图:
的产率随反应温度的变化如图:
①在催化剂A、B作用下,它们正、逆反应活化能差值分别用
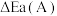 和
和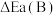 表示,则
表示,则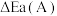
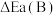 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。②y点对应的逆反应速率v(逆)
您最近半年使用:0次
名校
解题方法
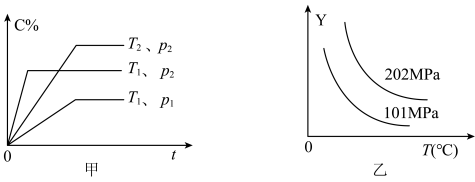
7 . 在一密闭容器中发生如下反应:aA(g)+bB(g) xC(g) ΔH=Q kJ/mol,某化学小组根据不同条件下的实验数据作出如图所示曲线( C%表示平衡混合气中产物C的百分含量,T表示温度,p表示压强,t表示反应时间)。其他条件不变时,下列分析正确的是
xC(g) ΔH=Q kJ/mol,某化学小组根据不同条件下的实验数据作出如图所示曲线( C%表示平衡混合气中产物C的百分含量,T表示温度,p表示压强,t表示反应时间)。其他条件不变时,下列分析正确的是
 xC(g) ΔH=Q kJ/mol,某化学小组根据不同条件下的实验数据作出如图所示曲线( C%表示平衡混合气中产物C的百分含量,T表示温度,p表示压强,t表示反应时间)。其他条件不变时,下列分析正确的是
xC(g) ΔH=Q kJ/mol,某化学小组根据不同条件下的实验数据作出如图所示曲线( C%表示平衡混合气中产物C的百分含量,T表示温度,p表示压强,t表示反应时间)。其他条件不变时,下列分析正确的是
| A.p2>p1,a+b<x |
| B.T2>T1,Q<0 |
| C.Y可能表示平衡混合气的平均相对分子质量 |
| D.升高温度,A的转化率增大 |
您最近半年使用:0次
名校
解题方法
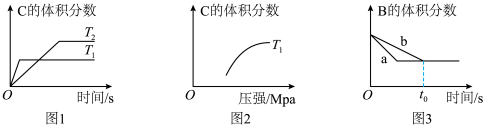
8 . 某化学研究小组探究外界条件对化学反应 的影响,如图所示,下列判断正确的是
的影响,如图所示,下列判断正确的是
 的影响,如图所示,下列判断正确的是
的影响,如图所示,下列判断正确的是
A.由图1可知, ,化学平衡常数 ,化学平衡常数 |
B.由图2可知,该反应的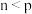 |
C.由图3可知,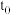 时刻两曲线中B的转化率相同 时刻两曲线中B的转化率相同 |
D.由图3可知,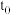 时刻后,a曲线和b曲线开始重合,故 时刻后,a曲线和b曲线开始重合,故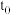 时刻二者同时到达平衡 时刻二者同时到达平衡 |
您最近半年使用:0次
9 . 以 为原料炼铁,主要发生如下反应:
为原料炼铁,主要发生如下反应:
反应I: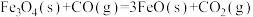
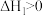
反应Ⅱ:

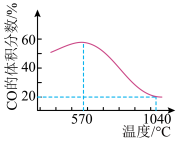
将一定体积CO 通入装有 粉末的反应器,其它条件不变,反应达平衡,测得 CO的体积分数随温度的变化关系如图所示。下列说法错误的是
粉末的反应器,其它条件不变,反应达平衡,测得 CO的体积分数随温度的变化关系如图所示。下列说法错误的是
 为原料炼铁,主要发生如下反应:
为原料炼铁,主要发生如下反应:反应I:
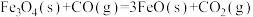
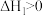
反应Ⅱ:


将一定体积CO 通入装有
 粉末的反应器,其它条件不变,反应达平衡,测得 CO的体积分数随温度的变化关系如图所示。下列说法错误的是
粉末的反应器,其它条件不变,反应达平衡,测得 CO的体积分数随温度的变化关系如图所示。下列说法错误的是
A. <0 <0 |
| B.在恒温、恒容条件下, 当容器压强保持不变,反应Ⅰ、 Ⅱ均达到平衡状态 |
| C.1040℃时, 反应Ⅰ的化学平衡常数K=4 |
D.反应温度较高时,  主要还原产物为 FeO 主要还原产物为 FeO |
您最近半年使用:0次
名校
10 . 反应
 ,在温度为
,在温度为 、
、 时,平衡体系中
时,平衡体系中 的体积分数随压强变化的曲线如图所示。下列说法正确的是
的体积分数随压强变化的曲线如图所示。下列说法正确的是


 ,在温度为
,在温度为 、
、 时,平衡体系中
时,平衡体系中 的体积分数随压强变化的曲线如图所示。下列说法正确的是
的体积分数随压强变化的曲线如图所示。下列说法正确的是
| A.X、Z两点气体的颜色:X比Z浅 |
| B.X、Y两点的反应速率:X<Y |
C. |
| D.X、Z两点气体的平均相对分子质量:X>Z |
您最近半年使用:0次



