1 . 亚硝酰氯(NOCl,熔点:-64.5℃,沸点:-5.5℃)为红褐色液体或黄色气体,具有刺鼻恶臭味,遇水剧烈发生反应:2NOCl+H2O=NO+NO2+2HCl,常可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。某研究性学习小组在实验室中按照下图所示装置制备NOCl,并测定其纯度。请按照要求回答下列问题:
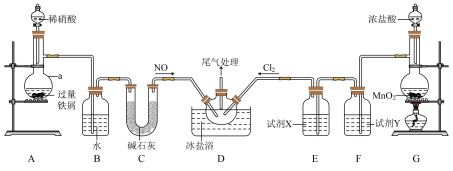
(1)a中反应的离子方程式为_______ 。亚硝酰氯的结构式为_______ 。
(2)装置D中,将三颈烧瓶浸在-10℃冰盐水中的目的是_______ 。
(3)装置C、E中碱石灰和试剂X的作用是_______ 。
(4)反应结束后用NaOH溶液吸收尾气,写出NOCl和NaOH的化学反应方程式:_______ 。(已知:NO+NO2+2NaOH=2NaNO2+H2O)。
(5)氢氧化钠溶液只能吸收氯气和NOCl,不能吸收NO,经过查阅资料发现用高锰酸钾溶液可以吸收NO气体,反应产生黑色沉淀,写出该反应的离子反应方程式:_______ 。
(6)测量产物NOCl的纯度:取三颈烧瓶中所得产物mg溶于水,配成250mL溶液,取出25.00mL,与VmLcmol·L-1的AgNO3溶液恰好完全反应,则产物中NOCl纯度的计算式为_______ 。

(1)a中反应的离子方程式为
(2)装置D中,将三颈烧瓶浸在-10℃冰盐水中的目的是
(3)装置C、E中碱石灰和试剂X的作用是
(4)反应结束后用NaOH溶液吸收尾气,写出NOCl和NaOH的化学反应方程式:
(5)氢氧化钠溶液只能吸收氯气和NOCl,不能吸收NO,经过查阅资料发现用高锰酸钾溶液可以吸收NO气体,反应产生黑色沉淀,写出该反应的离子反应方程式:
(6)测量产物NOCl的纯度:取三颈烧瓶中所得产物mg溶于水,配成250mL溶液,取出25.00mL,与VmLcmol·L-1的AgNO3溶液恰好完全反应,则产物中NOCl纯度的计算式为
您最近一年使用:0次
名校
2 . 载人航天器中的物质和能量资源都十分宝贵,我国科学家进行了如图所示的氧循环研究,实现了空间站中氧气的再生。下列说法不正确的是


| A.用于循环的氢原子利用率为100% |
| B.太阳能可作为反应①和②的能量来源 |
C.反应①为 |
D.等物质的量的 和 和 含有的电子数相同 含有的电子数相同 |
您最近一年使用:0次
2023-03-16更新
|
2058次组卷
|
8卷引用:广东省深圳市高级中学2022-2023学年高一下学期3月月考化学试题
22-23高三上·云南保山·期末
3 . 三氧化二砷(As2O3)可用于治疗急性早幼粒白血病。利用某酸性含砷废水(含 、H+、
、H+、 )可提取三氧化二砷,提取工艺流程如图所示:
)可提取三氧化二砷,提取工艺流程如图所示:

已知:①As2O3+6NaOH=2Na3AsO3+3H2O;
②As2S3易溶于过量的Na2S溶液中,加入FeSO4的目的是除去过量的S2-。
请回答下列问题:
(1)基态As原子的价层电子排布式为___________ 。
(2)操作M的名称是___________ ,滤液N中含有的阳离子有Fe2+、H+、___________ 。
(3)“焙烧”操作中,As2S3参与反应的化学方程式为___________ 。
(4)“碱浸”的目的是___________ 。
(5)“氧化”中发生反应的离子方程式为___________ 。
(6)砷化镓(GaAs)可由(CH3)3Ga和AsH3在700°C制得。已知GaAs的熔点为1238°C,其晶胞结构如图所示,该晶体的类型为___________ 。若阿伏加德罗常数的值为NA,GaAs的密度为ρg·cm-3,摩尔质量为Mg·mol-1,则GaAs的晶胞边长为___________ pm。

 、H+、
、H+、 )可提取三氧化二砷,提取工艺流程如图所示:
)可提取三氧化二砷,提取工艺流程如图所示:
已知:①As2O3+6NaOH=2Na3AsO3+3H2O;
②As2S3易溶于过量的Na2S溶液中,加入FeSO4的目的是除去过量的S2-。
请回答下列问题:
(1)基态As原子的价层电子排布式为
(2)操作M的名称是
(3)“焙烧”操作中,As2S3参与反应的化学方程式为
(4)“碱浸”的目的是
(5)“氧化”中发生反应的离子方程式为
(6)砷化镓(GaAs)可由(CH3)3Ga和AsH3在700°C制得。已知GaAs的熔点为1238°C,其晶胞结构如图所示,该晶体的类型为

您最近一年使用:0次
名校
解题方法
4 . 工业上以赤泥[主要成分是Sc2O3,另含有少量Fe2O3、SiO2(不溶于酸)、Al2O3等]为主要原料提取氧化钪,其工艺流程如图所示(P2O4是一种磷酸酯萃取剂,草酸化学式为H2C2O4)。
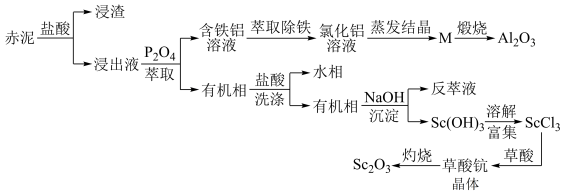
回答下列问题:
(1)赤泥经盐酸处理后所得“浸渣”主要成分为____ (化学式)。
(2)赤泥“盐酸酸浸”时不宜温度过高,原因是____ 。
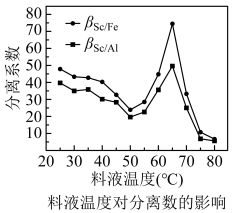
(3)P2O4萃取浸出液,其浓度、料液温度对萃取率的影响如表所示,萃取时P2O4最佳浓度及料液温度分别为____ 、____ ;
P2O4浓度对萃取率的影响如表:
料液温度对分离系数的影响如图:
(4)M经煅烧后可得到Al2O3,则M成分为____ 。
(5)为探究所得草酸钪晶体Sc2(C2O4)3·xH2O中结晶水的含量,取2.96g样品(纯度为75%),灼烧得到0.69gSc2O3固体,则x=____ 。
(6)草酸钪晶体在空气中灼烧分解反应方程式为____ 。

回答下列问题:
(1)赤泥经盐酸处理后所得“浸渣”主要成分为
(2)赤泥“盐酸酸浸”时不宜温度过高,原因是
(3)P2O4萃取浸出液,其浓度、料液温度对萃取率的影响如表所示,萃取时P2O4最佳浓度及料液温度分别为
P2O4浓度对萃取率的影响如表:
试验编号 | P2O4浓度/% | 分相情况 | 钪萃取率/% | 铁萃取率/% |
1-1 | 1 | 分相快 | 90.76 | 15.82 |
1-2 | 2 | 分相容易 | 91.53 | 19.23 |
1-3 | 3 | 分相容易 | 92.98 | 13.56 |
1-4 | 4 | 有第三相 | 90.69 | 30.12 |
1-5 | 5 | 轻微乳化 | 91.74 | 39.79 |
料液温度对分离系数的影响如图:

(4)M经煅烧后可得到Al2O3,则M成分为
(5)为探究所得草酸钪晶体Sc2(C2O4)3·xH2O中结晶水的含量,取2.96g样品(纯度为75%),灼烧得到0.69gSc2O3固体,则x=
(6)草酸钪晶体在空气中灼烧分解反应方程式为
您最近一年使用:0次
2023·黑龙江大庆·一模
名校
5 . 工业上采用电化学法对煤进行脱硫处理(煤中含硫物质主要是 ),以减少硫排放。模拟装置如图所示。下列说法错误的是
),以减少硫排放。模拟装置如图所示。下列说法错误的是
 ),以减少硫排放。模拟装置如图所示。下列说法错误的是
),以减少硫排放。模拟装置如图所示。下列说法错误的是
| A.电子流向:b极→石墨2→电解质溶液→石墨1→a极 |
B.石墨1为阳极,发生氧化反应, 被氧化 被氧化 |
C.脱硫反应为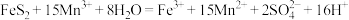 |
D.电路中转移 电子,理论上处理 电子,理论上处理  |
您最近一年使用:0次
2023-02-17更新
|
697次组卷
|
6卷引用:广东省深圳市2022-2023学年高三第一次调研考试变式题(选择题6-10)
(已下线)广东省深圳市2022-2023学年高三第一次调研考试变式题(选择题6-10)黑龙江省大庆市2023届高三下学期第一次教学质量检测化学试题广东省佛山市南海区狮山石门高级中学2022-2023学年高二下学期3月月考化学试题(已下线)专题10 电化学的综合应用湖南省衡阳市第一中学2023届高三下学期5月月考化学试题浙江省杭州市富阳区场口中学2023-2024学年高二下学期3月月考化学试题
解题方法
6 . 金属钯的一种离子[PdCl4]2-可催化合成H2O2,反应过程如图所示。下列叙述错误的是
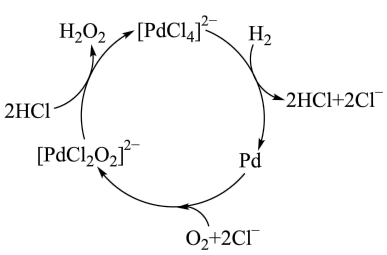

| A.[PdCl2O2]2-是反应中间体 |
B.催化合成H2O2总反应为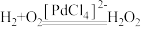 |
| C.过程中所发生的反应均为氧化还原反应 |
| D.过程中存在反应:Pd+O2+2Cl-=[PdCl2O2]2- |
您最近一年使用:0次
22-23高三上·广东茂名·期末
7 . 氧化亚铜主要用于制造船底防污漆(用来杀死低级海生动物)、杀虫剂,以及各种铜盐、分析试剂、红色玻璃,还用于镀铜及镀铜合金溶液的配制。用某铜矿(主要含CuS、FeO)制备 的一种工艺流程如下图:
的一种工艺流程如下图:

已知:常温下,相关金属离子生成氢氧化物沉淀的pH见表:
请回答下列问题:
(1)基态Cu原子价层电子的排布图为_______ 。
(2)滤渣的主要成分是_______ (填化学式)。
(3)“酸浸”中加入 的作用是
的作用是_______ ;写出其中生成单质S的化学方程式_______ 。
(4)“调pH”的范围是_______ 。
(5)“还原”前Cu元素以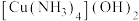 的形式存在,水合肼被氧化的化学方程式为
的形式存在,水合肼被氧化的化学方程式为_______ ;一定体积下,保持其它条件不变,水合肼浓度对 的产率的影响如图所示。当水合肼浓度大于
的产率的影响如图所示。当水合肼浓度大于 时,
时, 的转化率仍增大,但
的转化率仍增大,但 的产率下降,其可能的原因是
的产率下降,其可能的原因是_______ 。

(6)氧化亚铜立方晶胞结构如图所示,若规定A原子坐标是 ,C原子的坐标是
,C原子的坐标是 ,则B原子的坐标是
,则B原子的坐标是_______ ;该氧化物的密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶胞中
,则该晶胞中 和
和 之间的最近距离为
之间的最近距离为_______ nm。(用含 、
、 的代数式表示)
的代数式表示)

 的一种工艺流程如下图:
的一种工艺流程如下图:
已知:常温下,相关金属离子生成氢氧化物沉淀的pH见表:
| 氢氧化物 |  |  |  |  |
| 开始沉淀的pH | 4.8 | 1.9 | 7.5 | 8.8 |
| 沉淀完全的pH | 6.4 | 3.2 | 9.7 | 10.4 |
(1)基态Cu原子价层电子的排布图为
(2)滤渣的主要成分是
(3)“酸浸”中加入
 的作用是
的作用是(4)“调pH”的范围是
(5)“还原”前Cu元素以
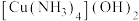 的形式存在,水合肼被氧化的化学方程式为
的形式存在,水合肼被氧化的化学方程式为 的产率的影响如图所示。当水合肼浓度大于
的产率的影响如图所示。当水合肼浓度大于 时,
时, 的转化率仍增大,但
的转化率仍增大,但 的产率下降,其可能的原因是
的产率下降,其可能的原因是
(6)氧化亚铜立方晶胞结构如图所示,若规定A原子坐标是
 ,C原子的坐标是
,C原子的坐标是 ,则B原子的坐标是
,则B原子的坐标是 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶胞中
,则该晶胞中 和
和 之间的最近距离为
之间的最近距离为 、
、 的代数式表示)
的代数式表示)
您最近一年使用:0次
2023-02-03更新
|
674次组卷
|
3卷引用:广东省深圳市2022-2023学年高三第一次调研考试变式题(工业流程题)
(已下线)广东省深圳市2022-2023学年高三第一次调研考试变式题(工业流程题)广东省茂名市第一中学2022-2023学年高三上学期期末化学诊断检测题重庆市2023届高三第一次联合诊断检测(一模)(康德卷)化学试题
名校
解题方法
8 . “绿水青山就是金山银山”,现在人们越来越注重对环境的保护,污水的处理和废旧电池的回收成为环境保护的重要课题。
Ⅰ.工业上常用还原沉淀法处理含铬废水(Cr2O 和CrO
和CrO ),其流程为
),其流程为
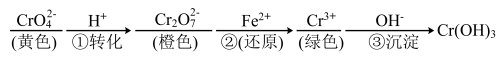
已知步骤③生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s) Cr3+(aq)+3OH-(aq) Ksp=c(Cr3+)·c3(OH-)=10-32。
Cr3+(aq)+3OH-(aq) Ksp=c(Cr3+)·c3(OH-)=10-32。
(1)步骤①中存在反应2CrO +2H+
+2H+ Cr2O
Cr2O +H2O,若向K2Cr2O7溶液中加NaOH浓溶液,能出现的现象是
+H2O,若向K2Cr2O7溶液中加NaOH浓溶液,能出现的现象是_______ ,原因是 _______ 。
(2)步骤③中,当将溶液的pH调节至_______ 时,可认为废水中的铬元素已基本除尽。(当溶液中c(Cr3+)≤10-5mol·L-1时,可视作该离子沉淀完全)
Ⅱ.镍电池广泛应用于混合动力汽车系统,电极材料由Ni(OH)2、碳粉、氧化铁等涂覆在铝箔上制成。由于电池使用后电极材料对环境有危害,某兴趣小组对该电池电极材料进行资源回收研究,设计实验流程如下:
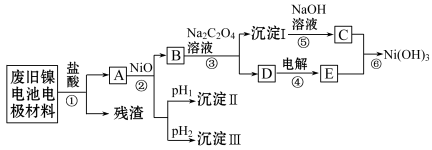
已知:①NiCl2易溶于水,Fe3+不能氧化Ni2+;
②某温度下一些金属氢氧化物的Ksp及沉淀析出的理论pH如表所示:
回答下列问题:
(3)根据上表数据判断步骤②依次析出沉淀Ⅱ_______ 和沉淀Ⅲ_______ (填化学式),则pH1_______ pH2(填“>”“=”或“<”)。
(4)已知溶解度:NiC2O4>NiC2O4·H2O>NiC2O4·2H2O,则③的化学方程式是_______ 。第③步反应后的操作名称是 _______ 。
(5)试写出⑥的离子方程式_______ 。
Ⅰ.工业上常用还原沉淀法处理含铬废水(Cr2O
 和CrO
和CrO ),其流程为
),其流程为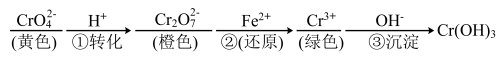
已知步骤③生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)
 Cr3+(aq)+3OH-(aq) Ksp=c(Cr3+)·c3(OH-)=10-32。
Cr3+(aq)+3OH-(aq) Ksp=c(Cr3+)·c3(OH-)=10-32。(1)步骤①中存在反应2CrO
 +2H+
+2H+ Cr2O
Cr2O +H2O,若向K2Cr2O7溶液中加NaOH浓溶液,能出现的现象是
+H2O,若向K2Cr2O7溶液中加NaOH浓溶液,能出现的现象是(2)步骤③中,当将溶液的pH调节至
Ⅱ.镍电池广泛应用于混合动力汽车系统,电极材料由Ni(OH)2、碳粉、氧化铁等涂覆在铝箔上制成。由于电池使用后电极材料对环境有危害,某兴趣小组对该电池电极材料进行资源回收研究,设计实验流程如下:

已知:①NiCl2易溶于水,Fe3+不能氧化Ni2+;
②某温度下一些金属氢氧化物的Ksp及沉淀析出的理论pH如表所示:
| M(OH)n | Ksp | pH | |
| 开始沉淀 | 沉淀完全 | ||
| Al(OH)3 | 1.9×10-23 | 3.43 | 4.19 |
| Fe(OH)3 | 3.8×10-38 | 2.53 | 2.94 |
| Ni(OH)2 | 1.6×10-14 | 7.60 | 9.75 |
(3)根据上表数据判断步骤②依次析出沉淀Ⅱ
(4)已知溶解度:NiC2O4>NiC2O4·H2O>NiC2O4·2H2O,则③的化学方程式是
(5)试写出⑥的离子方程式
您最近一年使用:0次
名校
解题方法
9 . 向重铬酸盐酸性溶液中加入乙醚和H2O2,水层发生反应:Cr2O +4H2O2+2H+=2CrO5+5H2O(已知CrO5中Cr的化合价为+6价),乙醚层发生反应:CrO5+(C2H5)2O=CrO5•O(C2H5)2(蓝色)。反应现象为上层出现蓝色,一段时间后溶液蓝色褪去,且水相变为绿色(Cr3+),下列说法正确的是
+4H2O2+2H+=2CrO5+5H2O(已知CrO5中Cr的化合价为+6价),乙醚层发生反应:CrO5+(C2H5)2O=CrO5•O(C2H5)2(蓝色)。反应现象为上层出现蓝色,一段时间后溶液蓝色褪去,且水相变为绿色(Cr3+),下列说法正确的是
 +4H2O2+2H+=2CrO5+5H2O(已知CrO5中Cr的化合价为+6价),乙醚层发生反应:CrO5+(C2H5)2O=CrO5•O(C2H5)2(蓝色)。反应现象为上层出现蓝色,一段时间后溶液蓝色褪去,且水相变为绿色(Cr3+),下列说法正确的是
+4H2O2+2H+=2CrO5+5H2O(已知CrO5中Cr的化合价为+6价),乙醚层发生反应:CrO5+(C2H5)2O=CrO5•O(C2H5)2(蓝色)。反应现象为上层出现蓝色,一段时间后溶液蓝色褪去,且水相变为绿色(Cr3+),下列说法正确的是| A.CrO5•O(C2H5)2中存在非极性键 |
B.由水层反应可知,氧化性:H2O2>Cr2O |
| C.乙醚在检验过程中作稳定剂和萃取剂,不可用乙醇代替 |
| D.水相变为绿色的离子反应为4CrO5+12H+=4Cr3++6H2O+7O2↑ |
您最近一年使用:0次
10 . 双碱法脱硫过程如图所示。下列说法不正确的是
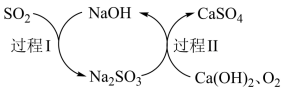

| A.过程I中,SO2表现还原性 |
| B.过程II中,1个O2可氧化2个Na2SO3 |
| C.双碱法脱硫过程中,NaOH可以循环利用 |
| D.总反应为2Ca(OH)2+2SO2+O2=2CaSO4+2H2O |
您最近一年使用:0次
2022-11-29更新
|
487次组卷
|
15卷引用:广东省深圳市福田区福田中学2022-2023学年高三上学期第三次考试化学试题
广东省深圳市福田区福田中学2022-2023学年高三上学期第三次考试化学试题北京市朝阳区2021届高三上学期期末考试化学试题广东省广州市2021-2022学年高三上学期12月调研考试化学试题(已下线)押新高考卷11题 反应机理分析-备战2022年高考化学临考题号押题(新高考通版)广东省惠州市2022届高三第二次调研考试化学试题北京市海淀实验中学2022-2023学年高三上学期10月学科展示化学试题广东省华南师范大学附属中学2023届高三上学期第一次月考化学试题湖南省永州市第一中学2022-2023学年高三上学期第三次月考化学试题广东实验中学2022-2023学年高一上学期期中考试化学试题(已下线)3.3.1 硫循环-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)湖北省宜昌英杰学校2021-2022学年高三上学期10月月考化学试题(已下线)专题13 反应微观机理分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)广东省台山市第一中学2022-2023学年高二上学期期末考试化学试题(已下线)化学-2023年高考押题预测卷01(广东卷)(含考试版、全解全析、参考答案、答题卡)广东省广州市第一一三中学2023-2024学年高一上学期10月月考化学试题



