名校
解题方法
1 . 碱式氧化镍是镍电池的正极活性材料。利用镍渣(主要含NiO,及少量 、CuO、CaO、
、CuO、CaO、 等杂质)制备碱式氧化镍的流程如下:
等杂质)制备碱式氧化镍的流程如下:
(2)浸渣的主要成分是_______ 。
(3)“沉铜”过程中生成单质S的离子方程式为______ 。
(4)“氧化”中的目的是将 氧化为
氧化为 ,试剂R可选用
,试剂R可选用_____ (填标号)。写出“氧化”时反应的离子方程式:_____ 。
A.氯水 B. 酸性溶液 C.
酸性溶液 C.
(5)碱式氧化镍(NiOOH)可用作镍氢电池的正极材料,电池的总反应为
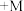 ,其工作时的正极电极反应式为
,其工作时的正极电极反应式为_______ 。
(6)若用2.0t废料(含NiO75%)制得NiOOH 0.92 t,则NiOOH的产率为_____ %。
 、CuO、CaO、
、CuO、CaO、 等杂质)制备碱式氧化镍的流程如下:
等杂质)制备碱式氧化镍的流程如下: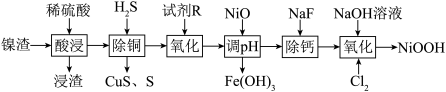
| A.研磨废料 | B.加入大量水 | C.搅拌 | D.适当升高温度 |
(2)浸渣的主要成分是
(3)“沉铜”过程中生成单质S的离子方程式为
(4)“氧化”中的目的是将
 氧化为
氧化为 ,试剂R可选用
,试剂R可选用A.氯水 B.
 酸性溶液 C.
酸性溶液 C.
(5)碱式氧化镍(NiOOH)可用作镍氢电池的正极材料,电池的总反应为

 ,其工作时的正极电极反应式为
,其工作时的正极电极反应式为(6)若用2.0t废料(含NiO75%)制得NiOOH 0.92 t,则NiOOH的产率为
您最近半年使用:0次
2024-05-03更新
|
201次组卷
|
2卷引用:广东省茂名市高州中学2023-2024学年高二下学期期中考试化学试题
解题方法
2 . 某制酸工厂产生的废酸液主要成分为HF、 、
、 、
、 、
、 ,一种处理工艺如下:
,一种处理工艺如下: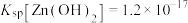
回答下列问题:
(1)基态As原子的价层电子排布图为__________________ ,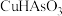 中As的化合价为
中As的化合价为_________ 。
(2)原废水中含有的 浓度为52.0
浓度为52.0 ,则
,则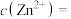
_____  ,常温下,有B离子的去除量、“调pH”为6.0后,
,常温下,有B离子的去除量、“调pH”为6.0后, 的去除率为
的去除率为_______ 。(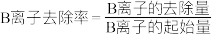 )
)
(3)强碱(AOH)的化学式为_____________ 。
(4)写出“还原”过程中 发生反应的化学方程式
发生反应的化学方程式_______________ 。
(5)产品结构分析。晶体W的晶胞结构如图所示:__________ 。
②W的化学式为_____________ 。
(6)产品纯度分析。称取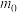 g
g  样品,用碱溶解,加入淀粉作指示剂,用浓度为
样品,用碱溶解,加入淀粉作指示剂,用浓度为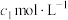 的碘标准溶液滴定As(Ⅲ)至As(Ⅴ),消耗体积为
的碘标准溶液滴定As(Ⅲ)至As(Ⅴ),消耗体积为 mL,则制得的产品纯度为
mL,则制得的产品纯度为___________ 。(用含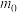 、
、 、
、 的代数式表示)
的代数式表示)
 、
、 、
、 、
、 ,一种处理工艺如下:
,一种处理工艺如下: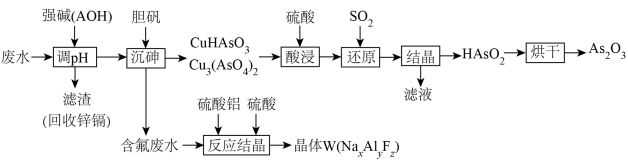
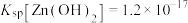
回答下列问题:
(1)基态As原子的价层电子排布图为
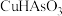 中As的化合价为
中As的化合价为(2)原废水中含有的
 浓度为52.0
浓度为52.0 ,则
,则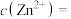
 ,常温下,有B离子的去除量、“调pH”为6.0后,
,常温下,有B离子的去除量、“调pH”为6.0后, 的去除率为
的去除率为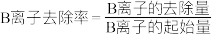 )
)(3)强碱(AOH)的化学式为
(4)写出“还原”过程中
 发生反应的化学方程式
发生反应的化学方程式(5)产品结构分析。晶体W的晶胞结构如图所示:

②W的化学式为
(6)产品纯度分析。称取
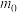 g
g  样品,用碱溶解,加入淀粉作指示剂,用浓度为
样品,用碱溶解,加入淀粉作指示剂,用浓度为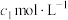 的碘标准溶液滴定As(Ⅲ)至As(Ⅴ),消耗体积为
的碘标准溶液滴定As(Ⅲ)至As(Ⅴ),消耗体积为 mL,则制得的产品纯度为
mL,则制得的产品纯度为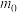 、
、 、
、 的代数式表示)
的代数式表示)
您最近半年使用:0次
3 . 铁的单质及其化合物用途广泛,下列相关的离子方程式书写正确的是
A.用KSCN溶液检验 : : |
B.硫酸亚铁溶液中滴加双氧水: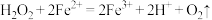 |
C.NaClO碱性条件下制备绿色消毒剂 : : |
D.用 溶液刻蚀Cu电路板: 溶液刻蚀Cu电路板: |
您最近半年使用:0次
4 . 化学离不开实验,请结合实验回答相应问题。
I.实验室需配制250mL浓度为 的
的 标准溶液进行有关实验。
标准溶液进行有关实验。
(1)配制时,先用托盘天平称取 固体
固体___________ g,然后进行下列操作,其中错误的是___________ (填标号)。
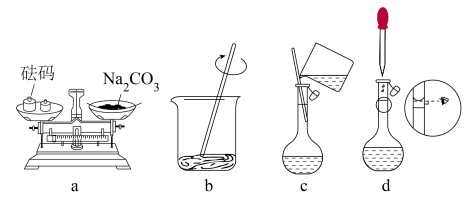
(2)下列有关容量瓶使用方法的操作中,正确的是___________(填标号)。
(3)___________ 
 的
的 溶液与
溶液与
 的盐酸恰好完全反应生成
的盐酸恰好完全反应生成 。
。
II.某研究性学习小组为了制取、收集纯净干燥的氯气并探究氯气的性质,他们设计如下图所示的实验装置。
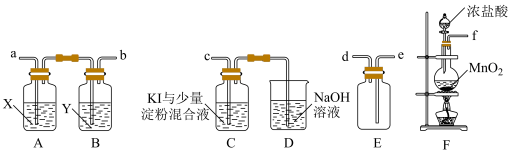
(4)整套装置的连接顺序是:f→___________ →c(按气体流动方向填各接口的小写字母,不重复)。
(5)B装置的作用是___________ 。
(6)某反应体系有反应物和生成物共7种: ,
, 、
、 、
、 、
、 、
、 、
、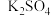 ,已知该反应过程中产生气泡,则该反应中的还原剂是
,已知该反应过程中产生气泡,则该反应中的还原剂是___________ (填化学式),请正确书写该反应的化学方程式___________ 。
I.实验室需配制250mL浓度为
 的
的 标准溶液进行有关实验。
标准溶液进行有关实验。(1)配制时,先用托盘天平称取
 固体
固体
(2)下列有关容量瓶使用方法的操作中,正确的是___________(填标号)。
| A.容量瓶只能用于配制溶液,不能储存溶液。 |
| B.进行容量瓶检漏时,容量瓶倒置一次即可。 |
| C.容量瓶用蒸馏水洗涤干净后,可以自然晾干或者烘箱烘干。 |
D. 固体在烧杯里完全溶解后,立即将溶液转移到容量瓶中。 固体在烧杯里完全溶解后,立即将溶液转移到容量瓶中。 |
(3)

 的
的 溶液与
溶液与
 的盐酸恰好完全反应生成
的盐酸恰好完全反应生成 。
。II.某研究性学习小组为了制取、收集纯净干燥的氯气并探究氯气的性质,他们设计如下图所示的实验装置。

(4)整套装置的连接顺序是:f→
(5)B装置的作用是
(6)某反应体系有反应物和生成物共7种:
 ,
, 、
、 、
、 、
、 、
、 、
、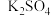 ,已知该反应过程中产生气泡,则该反应中的还原剂是
,已知该反应过程中产生气泡,则该反应中的还原剂是
您最近半年使用:0次
5 . 电子工业用 溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,运用所学知识,回答下列问题。
溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,运用所学知识,回答下列问题。
(1)请写出 溶液与铜反应的离子方程式
溶液与铜反应的离子方程式___________ 。
(2)某研究性学习小组为测定 溶液腐蚀铜后所得溶液的组成,进行了研究,其中部分实验如下:
溶液腐蚀铜后所得溶液的组成,进行了研究,其中部分实验如下:
①取少量待测液,滴入KSCN溶液呈红色,则待测液中含有的金属阳离子是___________ 。
②溶液组成的测定:取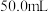 待测液,加入足量的
待测液,加入足量的 溶液,得到
溶液,得到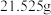 白色沉淀,则溶液中
白色沉淀,则溶液中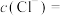
___________  。
。
(3)从腐蚀废液(主要含 、
、 、
、 )中回收铜,并重新获得
)中回收铜,并重新获得 溶液,废液处理流程如下:
溶液,废液处理流程如下:
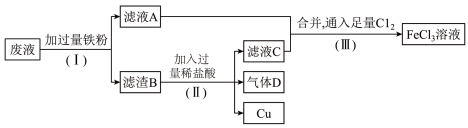
①滤渣B中主要含有___________ ,气体D是___________ 。
②写出步骤(Ⅲ)中生成 的化学方程式
的化学方程式___________ 。
③步骤(Ⅲ)中,将 换成
换成___________ 也能达到同样的目的,写出所换成的物质将 氧化为
氧化为 的离子方程式
的离子方程式___________ 。
 溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,运用所学知识,回答下列问题。
溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,运用所学知识,回答下列问题。(1)请写出
 溶液与铜反应的离子方程式
溶液与铜反应的离子方程式(2)某研究性学习小组为测定
 溶液腐蚀铜后所得溶液的组成,进行了研究,其中部分实验如下:
溶液腐蚀铜后所得溶液的组成,进行了研究,其中部分实验如下:①取少量待测液,滴入KSCN溶液呈红色,则待测液中含有的金属阳离子是
②溶液组成的测定:取
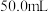 待测液,加入足量的
待测液,加入足量的 溶液,得到
溶液,得到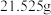 白色沉淀,则溶液中
白色沉淀,则溶液中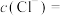
 。
。(3)从腐蚀废液(主要含
 、
、 、
、 )中回收铜,并重新获得
)中回收铜,并重新获得 溶液,废液处理流程如下:
溶液,废液处理流程如下:
①滤渣B中主要含有
②写出步骤(Ⅲ)中生成
 的化学方程式
的化学方程式③步骤(Ⅲ)中,将
 换成
换成 氧化为
氧化为 的离子方程式
的离子方程式
您最近半年使用:0次
名校
解题方法
6 . 运动会上的发令枪所用“火药”的主要成分是氯酸钾和红磷,经撞击发出响声,同时产生白烟。撞击时发生反应的化学方程式(未配平): ,则下列有关叙述错误的是
,则下列有关叙述错误的是
 ,则下列有关叙述错误的是
,则下列有关叙述错误的是A.该反应属于氧化还原反应, 为氧化反应的产物 为氧化反应的产物 |
| B.该反应中n(氧化剂):n(还原剂)=6:5 |
| C.该反应中消耗2molP时,转移10mol电子 |
D.白烟是由于剧烈反应生成的白色固体小颗粒 和KCl化合价 和KCl化合价 |
您最近半年使用:0次
名校
7 . 工业上用赤铁矿(主要成分为 ,含
,含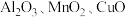 等杂质)制备绿矾
等杂质)制备绿矾 的流程如下:
的流程如下: 能与
能与 溶液反应生成可溶性盐
溶液反应生成可溶性盐 。
。
回答下列问题:
(1)试剂a为___________ 。
(2)试剂b需过量,其目的是___________ ;“滤渣”的成分是___________ 。
(3)“结晶”需隔绝空气,原因是___________ 。
(4)绿矾隔绝空气加强热可用于制备红色颜料铁红。取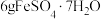 样品隔绝空气加热(杂质不反应),受热过程中样品质量随温度变化的曲线如图所示(已知固体
样品隔绝空气加热(杂质不反应),受热过程中样品质量随温度变化的曲线如图所示(已知固体 不含结晶水)。
不含结晶水)。 主要成分的化学式为
主要成分的化学式为___________ 。
②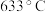 时,除生成铁红外,同时生成能使
时,除生成铁红外,同时生成能使 溶液变浑浊的气体和使品红溶液裉色的气体。该温度下反应的化学方程式为
溶液变浑浊的气体和使品红溶液裉色的气体。该温度下反应的化学方程式为___________ ;该样品中 的质量分数为
的质量分数为___________  (保留一位小数)。
(保留一位小数)。
 ,含
,含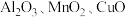 等杂质)制备绿矾
等杂质)制备绿矾 的流程如下:
的流程如下: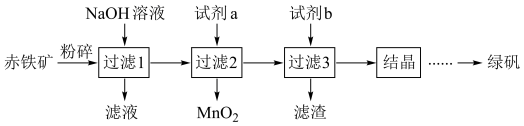
 能与
能与 溶液反应生成可溶性盐
溶液反应生成可溶性盐 。
。回答下列问题:
(1)试剂a为
(2)试剂b需过量,其目的是
(3)“结晶”需隔绝空气,原因是
(4)绿矾隔绝空气加强热可用于制备红色颜料铁红。取
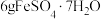 样品隔绝空气加热(杂质不反应),受热过程中样品质量随温度变化的曲线如图所示(已知固体
样品隔绝空气加热(杂质不反应),受热过程中样品质量随温度变化的曲线如图所示(已知固体 不含结晶水)。
不含结晶水)。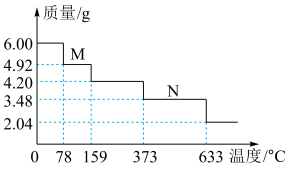
 主要成分的化学式为
主要成分的化学式为②
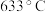 时,除生成铁红外,同时生成能使
时,除生成铁红外,同时生成能使 溶液变浑浊的气体和使品红溶液裉色的气体。该温度下反应的化学方程式为
溶液变浑浊的气体和使品红溶液裉色的气体。该温度下反应的化学方程式为 的质量分数为
的质量分数为 (保留一位小数)。
(保留一位小数)。
您最近半年使用:0次
2024-02-02更新
|
236次组卷
|
3卷引用:广东省化州市第一中学2023-2024学年高一下学期月考(一)化学试题
名校
解题方法
8 . (一)工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如下:
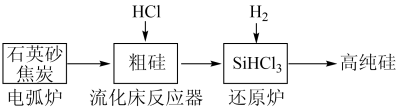
(1)工业上用石英砂和焦炭在电弧炉中高温加热到1600℃-1800℃生成粗硅的化学方程式为:___________ 。
(2)在流化床反应的产物中,SiHCl3大约占85%,还有SiCl4、SiH2Cl2、SiH3Cl等,粗硅生成SiHCl3的化学反应为:Si+3HCl SiHCl3+H2,生成物SiHCl3的结构式为:
SiHCl3+H2,生成物SiHCl3的结构式为:___________ 。
(二)某化学兴趣小组利用下列图示装置探究氨气的性质。
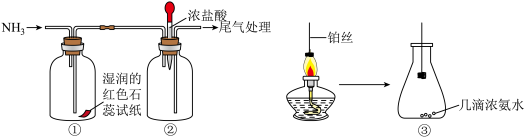
(3)①中湿润的红色石蕊试纸变蓝的原因:___________ (用化学方程式表示)。
(4)向②中滴入浓盐酸,现象为:___________ 。
(5)将灼热的铂丝伸入③中锥形瓶,可观察到铂丝保持红热,有红棕色气体及少量白烟生成。该过程会同时发生多个反应,写出NH3和O2催化氧化的化学方程式:___________ ,瓶中红棕色气体为___________ (填化学式)。
(三)某氨氮废水( 、
、 )的生物法处理流程如图所示:
)的生物法处理流程如图所示:

(6)检验氨氮废水中含有 的方法是:
的方法是:___________ 。
(7)过程Ⅱ在硝化细菌作用下实现 的转化,称为硝化过程。在碱性条件下实现上述硝化过程的总反应的离子方程式为:
的转化,称为硝化过程。在碱性条件下实现上述硝化过程的总反应的离子方程式为:___________ 。

(1)工业上用石英砂和焦炭在电弧炉中高温加热到1600℃-1800℃生成粗硅的化学方程式为:
(2)在流化床反应的产物中,SiHCl3大约占85%,还有SiCl4、SiH2Cl2、SiH3Cl等,粗硅生成SiHCl3的化学反应为:Si+3HCl
 SiHCl3+H2,生成物SiHCl3的结构式为:
SiHCl3+H2,生成物SiHCl3的结构式为:(二)某化学兴趣小组利用下列图示装置探究氨气的性质。

(3)①中湿润的红色石蕊试纸变蓝的原因:
(4)向②中滴入浓盐酸,现象为:
(5)将灼热的铂丝伸入③中锥形瓶,可观察到铂丝保持红热,有红棕色气体及少量白烟生成。该过程会同时发生多个反应,写出NH3和O2催化氧化的化学方程式:
(三)某氨氮废水(
 、
、 )的生物法处理流程如图所示:
)的生物法处理流程如图所示:
(6)检验氨氮废水中含有
 的方法是:
的方法是:(7)过程Ⅱ在硝化细菌作用下实现
 的转化,称为硝化过程。在碱性条件下实现上述硝化过程的总反应的离子方程式为:
的转化,称为硝化过程。在碱性条件下实现上述硝化过程的总反应的离子方程式为:
您最近半年使用:0次
名校
9 . 锂电池是目前应用广泛的新型电池,一种回收钴酸锂废旧电池(主要成分为LiCoO2,同时含有少量Fe、Al、C单质)的流程如下图所示。
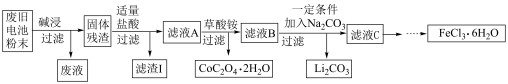
已知:Fe3+能与C2O 结合成[Fe(C2O4)3]3-,[Fe(C2O4)3]3-在强酸性环境下重新转化为Fe3+
结合成[Fe(C2O4)3]3-,[Fe(C2O4)3]3-在强酸性环境下重新转化为Fe3+
请回答下列问题:
(1)由滤液A制取CoC2O4·2H2O的过程发生的___________ (填“是”或“不是”)氧化还原反应,CoC2O4·2H2O中C的化合价为___________ ,滤渣I的主要成份为___________ 。
(2)用过量的NaOH溶液进行“碱浸”,“碱浸”的目的是___________ 。
写出该过程发生的化学反应方程式___________ 。
(3)加入适量盐酸,LiCoO2溶解后生成的Co3+能将Fe2+氧化为Fe3+,请写出该反应的离子方程式___________ 。
(4)请设计实验方案检验滤液C中的Cl-。___________
(5)高铁酸钠(Na2FeO4 ,其中铁为+6价)是一种高效多功能水处理剂。工业上用次氯酸钠和氯化铁为原料来制取高铁酸钠,该反应的离子方程式为:_________
___________ClO- +___________Fe3++___________=___________FeO +___________Cl- +___________H2O,请配平该方程式。
+___________Cl- +___________H2O,请配平该方程式。

已知:Fe3+能与C2O
 结合成[Fe(C2O4)3]3-,[Fe(C2O4)3]3-在强酸性环境下重新转化为Fe3+
结合成[Fe(C2O4)3]3-,[Fe(C2O4)3]3-在强酸性环境下重新转化为Fe3+请回答下列问题:
(1)由滤液A制取CoC2O4·2H2O的过程发生的
(2)用过量的NaOH溶液进行“碱浸”,“碱浸”的目的是
写出该过程发生的化学反应方程式
(3)加入适量盐酸,LiCoO2溶解后生成的Co3+能将Fe2+氧化为Fe3+,请写出该反应的离子方程式
(4)请设计实验方案检验滤液C中的Cl-。
(5)高铁酸钠(Na2FeO4 ,其中铁为+6价)是一种高效多功能水处理剂。工业上用次氯酸钠和氯化铁为原料来制取高铁酸钠,该反应的离子方程式为:
___________ClO- +___________Fe3++___________=___________FeO
 +___________Cl- +___________H2O,请配平该方程式。
+___________Cl- +___________H2O,请配平该方程式。
您最近半年使用:0次
2024-01-16更新
|
221次组卷
|
3卷引用:广东省茂名市七校2023-2024学年高一上学期12月联考化学试题
名校
10 . 高铁酸钾(K2FeO4)是一种环保、高效、多功能饮用水处理剂,在水处理过程中,高铁酸钾转化为Fe(OH)3胶体,制备高铁酸钾流程如图所示。

下列叙述不正确的是

下列叙述不正确的是
A.反应I的化学方程式是2Fe+3Cl2 2FeCl3 2FeCl3 |
| B.反应Ⅱ中氧化剂与还原剂的物质的量之比为2∶3 |
| C.用FeCl2溶液吸收反应Ⅰ中尾气所得产物可再利用 |
| D.用K2FeO4对饮用水杀菌消毒的同时,Fe(OH)3胶体吸附杂质净化水 |
您最近半年使用:0次



