名校
解题方法
1 . 氯元素可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用如图装置(部分装置省略)制备KClO3和NaClO,并比较其氧化性。
已知:氯气与碱溶液反应,在低温和稀碱溶液中主要产物是ClO-和Cl-,在75℃以上和浓碱溶液中主要产物是ClO 和Cl-
和Cl-

回答下列问题:
(1)甲中盛放浓盐酸的仪器名称是___________ ,甲中发生的反应的化学方程式是___________ ;
(2)乙中的试剂为___________ ;
(3)丙中发生反应的化学方程式是___________ ;
(4)丁采用冰水浴冷却的目的是___________ ;
(5)戊的作用是尾气吸收,可选用试剂 ___________(填字母)。
(6)反应结束后,取出丙中试管,经冷却结晶、___________ 、洗涤、干燥,得到KClO3晶体。
(7)取少量KClO3和NaClO溶液分别置于1号和2号试管中,滴加KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入CCl4振荡,静置后CCl4层显紫色。可知该条件下KClO3的氧化能力___________ NaClO(填“大于”或“小于”)。
已知:氯气与碱溶液反应,在低温和稀碱溶液中主要产物是ClO-和Cl-,在75℃以上和浓碱溶液中主要产物是ClO
 和Cl-
和Cl-
回答下列问题:
(1)甲中盛放浓盐酸的仪器名称是
(2)乙中的试剂为
(3)丙中发生反应的化学方程式是
(4)丁采用冰水浴冷却的目的是
(5)戊的作用是尾气吸收,可选用试剂 ___________(填字母)。
| A.H2SO4 | B.NaOH | C.NaCl | D.Ca(OH)2 |
(6)反应结束后,取出丙中试管,经冷却结晶、
(7)取少量KClO3和NaClO溶液分别置于1号和2号试管中,滴加KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入CCl4振荡,静置后CCl4层显紫色。可知该条件下KClO3的氧化能力
您最近半年使用:0次
名校
解题方法
2 . 钠是一种非常活泼、具有广泛应用的金属。
(1)钠的原子结构示意图为___________ ,钠在反应中容易___________ 电子(填“得到”或“失去”)。
(2)汽车安全气囊的气体发生剂 可由金属钠生产。某汽车安全气囊内含
可由金属钠生产。某汽车安全气囊内含 、
、 和
和 等物质。
等物质。
ⅰ.当汽车发生较严重的碰撞时,引发 分解
分解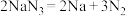 ,从而为气囊充气。产生的Na立即与
,从而为气囊充气。产生的Na立即与 发生置换反应生成
发生置换反应生成 ,化学方程式是
,化学方程式是___________ 。
ⅱ. 是冷却剂,吸收产气过程释放的热量。
是冷却剂,吸收产气过程释放的热量。 起冷却作用时发生反应的化学方程式为
起冷却作用时发生反应的化学方程式为___________ 。
ⅲ.一个安全气囊通常装有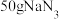 ,其完全分解所释放的
,其完全分解所释放的 为
为___________ mol。(保留两位小数)
(3)工业通过电解NaCl生产金属钠: ,过程如下:
,过程如下:
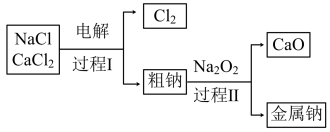
已知:电解时需要将NaCl加热至熔融状态。NaCl的熔点为801℃,为降低能耗,通常加入 从而把熔点降至约580℃。
从而把熔点降至约580℃。
①把NaCl固体加热至熔融状态,目的是___________ 。
②粗钠中含有少量杂质Ca,过程Ⅱ除去Ca的化学方程式是___________ 。
(1)钠的原子结构示意图为
(2)汽车安全气囊的气体发生剂
 可由金属钠生产。某汽车安全气囊内含
可由金属钠生产。某汽车安全气囊内含 、
、 和
和 等物质。
等物质。ⅰ.当汽车发生较严重的碰撞时,引发
 分解
分解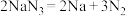 ,从而为气囊充气。产生的Na立即与
,从而为气囊充气。产生的Na立即与 发生置换反应生成
发生置换反应生成 ,化学方程式是
,化学方程式是ⅱ.
 是冷却剂,吸收产气过程释放的热量。
是冷却剂,吸收产气过程释放的热量。 起冷却作用时发生反应的化学方程式为
起冷却作用时发生反应的化学方程式为ⅲ.一个安全气囊通常装有
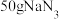 ,其完全分解所释放的
,其完全分解所释放的 为
为(3)工业通过电解NaCl生产金属钠:
 ,过程如下:
,过程如下:
已知:电解时需要将NaCl加热至熔融状态。NaCl的熔点为801℃,为降低能耗,通常加入
 从而把熔点降至约580℃。
从而把熔点降至约580℃。①把NaCl固体加热至熔融状态,目的是
②粗钠中含有少量杂质Ca,过程Ⅱ除去Ca的化学方程式是
您最近半年使用:0次
名校
3 . 硫化氢(H2S)是一种无色、有臭鸡蛋气味的有毒气体。处理某废气中的 H2S,是将废气与空气混合通入 FeCl2,CuCl2、FeCl3的混合液中,其转化的流程如图所示。下列说法正确的是
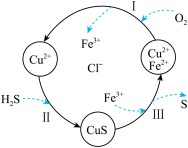

| A.转化过程中参与循环的离子只有 Cu2+、Fe2+ |
| B.转化过程有两种元素的化合价发生了变化 |
| C.氧化性由强到弱的顺序:S>Fe3+>O2 |
| D.过程Ⅲ中发生反应的离子方程式为 CuS+2Fe3+=S+2Fe2++Cu2+ |
您最近半年使用:0次
2023-11-01更新
|
451次组卷
|
12卷引用:广东省清远市名校2023-2024学年高一上学期期中调研联考化学试题
广东省清远市名校2023-2024学年高一上学期期中调研联考化学试题重庆市2021-2022学年高一上学期期末联合检测化学试题广东省广州市第五中学2022-2023学年高一上学期段考试化学试题陕西省西安市铁一中2022-2023学年高一上学期第一次月考化学试题广东省广州市第五中学2022-2023学年高一上学期期中考试化学试题湖北省麻城市实验高级中学2021-2022学年高一下学期2月迎春考化学试题四川省达州天立学校2022-2023学年高一上学期第一次月考选科摸底测试学试题【2022】【高一上】【长河高级中学】【期中考】【高中化学】吉林省长春市第二实验中学2023-2024学年高一上学期期中考试化学试题安徽省阜阳市临泉第一中学2023-2024学年高一上学期10月月考化学试题云南会泽县实验高级中学校2023-2024学年高一上学期10月月考化学试题安徽省合肥市第三中学2023-2024学年高一上学期12月份学情调研化学试题
名校
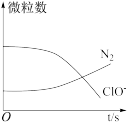
4 . 某离子反应涉及 H2O、ClO-、 NH 、OH-、N2、Cl- 等微粒,其中 N2、ClO- 的数目随时间变化的曲线如图所示,下列说法错误的是
、OH-、N2、Cl- 等微粒,其中 N2、ClO- 的数目随时间变化的曲线如图所示,下列说法错误的是
 、OH-、N2、Cl- 等微粒,其中 N2、ClO- 的数目随时间变化的曲线如图所示,下列说法错误的是
、OH-、N2、Cl- 等微粒,其中 N2、ClO- 的数目随时间变化的曲线如图所示,下列说法错误的是
| A.该反应中Cl-为还原产物 | B.消耗1个还原剂微粒,转移6 个电子 |
C.NH 被ClO- 氧化成N2 被ClO- 氧化成N2 | D.反应后溶液的碱性减弱 |
您最近半年使用:0次
2023-11-01更新
|
153次组卷
|
3卷引用:广东省清远市名校2023-2024学年高一上学期期中调研联考化学试题
名校
5 . 废旧锌锰干电池内部的黑色物质A主要含有MnO2、MnOOH、NH4C1、ZnCl2、碳单质,用黑色物质A制备高纯MnCO3的流程如图:
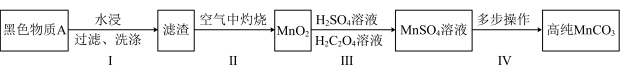
已知: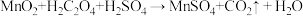 (未配平)。
(未配平)。
(1)第I步操作是为了除去可溶性的_____ (填化学式)。
(2)第I步后在空气中灼烧的目的有两个,一个是将MnOOH转化为MnO2,另一个是_____ 。灼烧时,MnOOH与空气中的氧气反应的化学方程式为_____ 。
(3)第Ⅲ步中为提高反应速率,可以采取的措施有_____ (任写一条),第Ⅲ步过程中加入H2SO4溶液的作用是_____ 。
(4)已知:MnCO3难溶于水和乙醇,潮湿时易被空气氧化,100℃时开始分解;Mn2+在pH大于7.7时,开始转化为Mn(OH)2沉淀。第Ⅳ步中的多步操作可按如图步骤进行:
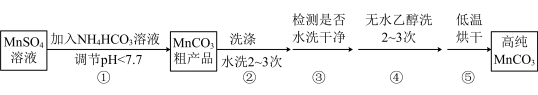
操作①加入NH4HCO3溶液调节溶液pH的过程中有CO2产生,则MnSO4溶液与NH4HCO3溶液反应的离子方程式为_____ ;操作②中需要的玻璃仪器有_____ ;你认为操作③中检测的方法及现象是_____ 时可继续进行操作④;操作④中用无水乙醇洗涤的目的是_____ (答一条即可)。

已知:
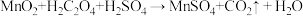 (未配平)。
(未配平)。(1)第I步操作是为了除去可溶性的
(2)第I步后在空气中灼烧的目的有两个,一个是将MnOOH转化为MnO2,另一个是
(3)第Ⅲ步中为提高反应速率,可以采取的措施有
(4)已知:MnCO3难溶于水和乙醇,潮湿时易被空气氧化,100℃时开始分解;Mn2+在pH大于7.7时,开始转化为Mn(OH)2沉淀。第Ⅳ步中的多步操作可按如图步骤进行:

操作①加入NH4HCO3溶液调节溶液pH的过程中有CO2产生,则MnSO4溶液与NH4HCO3溶液反应的离子方程式为
您最近半年使用:0次
2023-07-05更新
|
160次组卷
|
3卷引用:广东省清远市2022-2023学年高一下学期期末质量检测化学试题
名校
解题方法
6 . 钠是一种非常活泼,具有广泛应用的金属。
(1)钠的原子结构示意图为_______ 。
(2)金属钠非常活泼,通常保存在_______ 里,以隔绝空气。
(3) 、
、 、
、 、
、 久置于空气中最终都变为
久置于空气中最终都变为_______ (填化学式)。
(4)将 投入
投入 溶液中发生反应的现象有
溶液中发生反应的现象有_______ 。
(5)汽车安全气囊的气体发生剂NaN3可由金属钠生产。某汽车安全气囊内含NaN3、Fe2O3和NaHCO3等物质。
i.当汽车发生较严重的碰撞时,受热分解为Na和N2,其化学方程式为_______ ;
ii.产生的Na立即与Fe2O3发生置换反应生成Na2O,化学方程式是_______ ;
(1)钠的原子结构示意图为
(2)金属钠非常活泼,通常保存在
(3)
 、
、 、
、 、
、 久置于空气中最终都变为
久置于空气中最终都变为(4)将
 投入
投入 溶液中发生反应的现象有
溶液中发生反应的现象有(5)汽车安全气囊的气体发生剂NaN3可由金属钠生产。某汽车安全气囊内含NaN3、Fe2O3和NaHCO3等物质。
i.当汽车发生较严重的碰撞时,受热分解为Na和N2,其化学方程式为
ii.产生的Na立即与Fe2O3发生置换反应生成Na2O,化学方程式是
您最近半年使用:0次
名校
解题方法
7 . 某研究性学习小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略)。已知:Cl2易溶于CCl4而HCl不溶于CCl4

按要求回答问题:
(1)装置A中仪器H的名称是_______ ,写出装置A制取Cl2的化学方程式_______ 。
(2)装置B中的试剂是_______ ,现象是_______ 。装置D和E中出现的不同现象说明氯气没有漂白性,氯水有漂白性。
(3)装置F的作用是_______ 。
(4)有一种“地康法”制取氯气的反应原理如图所示:
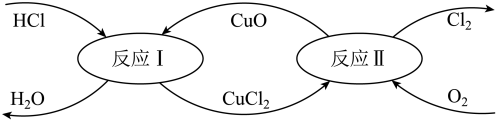
①反应I属于_______ 反应。(填四种基本反应类型之一)
②在450℃条件下,反应II的化学方程式为_______ 。
③工业生产中常用氨气检查输送氯气的管道是否有Cl2泄漏。若Cl2有泄漏,可以观察到有大量的白烟生成(为NH4Cl固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式:_______ 。

按要求回答问题:
(1)装置A中仪器H的名称是
(2)装置B中的试剂是
(3)装置F的作用是
(4)有一种“地康法”制取氯气的反应原理如图所示:

①反应I属于
②在450℃条件下,反应II的化学方程式为
③工业生产中常用氨气检查输送氯气的管道是否有Cl2泄漏。若Cl2有泄漏,可以观察到有大量的白烟生成(为NH4Cl固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式:
您最近半年使用:0次
8 . 如图所示是蒽(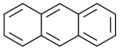 )氧化为蒽醌(
)氧化为蒽醌(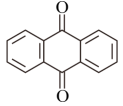 )的间接合成示意图。下列说法错误的是
)的间接合成示意图。下列说法错误的是

 )氧化为蒽醌(
)氧化为蒽醌( )的间接合成示意图。下列说法错误的是
)的间接合成示意图。下列说法错误的是
A.电解槽中,阳极附近溶液的 浓度升高 浓度升高 |
B.1 mol蒽被完全氧化成蒽醌转移电子数目为 |
| C.活性炭的作用是吸收有机物 |
D.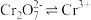 化学再生过程,对环境是友好的 化学再生过程,对环境是友好的 |
您最近半年使用:0次
9 . 市政污泥含大量金属(Cu、Zn、Ni、Fe、Ag等),不经处理直接填埋会对环境造成严重的污染。市政污泥的综合利用能够使其得到科学、妥善的处置,并可以作为资源再次被我们利用,同时可以带来一定的经济价值。某科研团队利用市政污泥回收皓矾(ZnSO4·7H2O)的工艺流程如下:
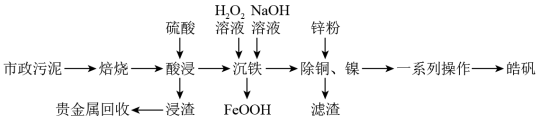
已知:“沉铁”时若pH过高,会产生具有较强吸附性的氢氧化铁胶状沉淀。回答下列问题:
(1)为提高“酸浸”效率,可采取的措施有___________ (任写一条)。
(2)“一系列操作”主要包括___________ 、___________ 、过滤、洗涤,干燥。
(3)用锌粉除铜、镍时,先除去铜,然后分离再置换除镍,用锌粉直接置换速率极慢,目前采用“锑盐净化法”,即置换时在酸性含Ni2+溶液中同时加入锌粉和Sb2O3,得到金属Ni和Sb的混合物,该混合物可表示为NiSb,形成NiSb的离子方程式为___________ 。
(4)“浸渣”中含有Ag2S,经一系列处理得Ag(NH3)2Cl(可溶于水,电离成[Ag(NH3)2]+和Cl-},用肼(N2H4)还原Ag(NH3)2Cl得到单质银,N2H4的氧化产物为N2,写出该反应的离子方程式:_______ ,则反应中氧化剂与还原剂的物质的量之比为_______ 。
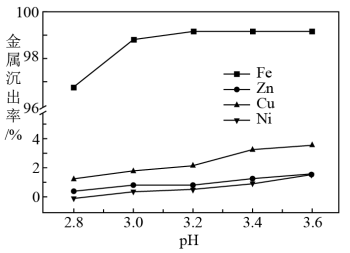
(5)浸出液中含有Fe2+,“沉铁”步骤中发生反应的离子方程式为_______ 。pH对不同金属沉出率的影响如图所示,则“沉铁’时最合理的pH约为_______ 。在pH<6时,Zn2+、Cu2+、Ni2+在溶液中以离子形式存在,但是有铁离子存在时,pH升高,Zn、Cu、Ni损失率均升高,原因可能是_______ 。

已知:“沉铁”时若pH过高,会产生具有较强吸附性的氢氧化铁胶状沉淀。回答下列问题:
(1)为提高“酸浸”效率,可采取的措施有
(2)“一系列操作”主要包括
(3)用锌粉除铜、镍时,先除去铜,然后分离再置换除镍,用锌粉直接置换速率极慢,目前采用“锑盐净化法”,即置换时在酸性含Ni2+溶液中同时加入锌粉和Sb2O3,得到金属Ni和Sb的混合物,该混合物可表示为NiSb,形成NiSb的离子方程式为
(4)“浸渣”中含有Ag2S,经一系列处理得Ag(NH3)2Cl(可溶于水,电离成[Ag(NH3)2]+和Cl-},用肼(N2H4)还原Ag(NH3)2Cl得到单质银,N2H4的氧化产物为N2,写出该反应的离子方程式:
(5)浸出液中含有Fe2+,“沉铁”步骤中发生反应的离子方程式为

您最近半年使用:0次
2022-01-11更新
|
1496次组卷
|
5卷引用:广东省清远市2021-2022学年高三上学期期末教学质量检测化学试题
10 . 宏观辨识与微观探析是化学学科核心素养之一。下列物质性质实验对应的离子方程式书写错误的是
A.将KI溶液滴入稀硫酸酸化的KIO3溶液中:5I-+ +6H+=3I2+3H2O +6H+=3I2+3H2O |
B.过量铁粉与稀硝酸反应:Fe+4H++ =Fe3++NO↑+2H2O =Fe3++NO↑+2H2O |
C.用酸性KMnO4溶液吸收含SO2尾气:5SO2+2 +2H2O=2Mn2++4H++5 +2H2O=2Mn2++4H++5 |
D.用碳酸钠溶液浸泡处理锅炉水垢(主要成分为CaSO4):CaSO4(s)+ (aq)⇌CaCO3(s)+ (aq)⇌CaCO3(s)+ (aq) (aq) |
您最近半年使用:0次
2022-01-11更新
|
411次组卷
|
4卷引用:广东省清远市2021-2022学年高三上学期期末教学质量检测化学试题
广东省清远市2021-2022学年高三上学期期末教学质量检测化学试题河北省邢台市名校联盟2021-2022学年高三上学期期末测试化学试题 (已下线)一轮巩固卷1-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(广东专用)(已下线)2022年浙江1月高考真题变式题(11-20)



