1 . 肼( ,无色液体)是一种用途广泛的化工原料。实验室中先制备次氯酸钠,再用次氯酸钠溶液和氨反应制备肼并验证肼的性质。实验装置如图所示。
,无色液体)是一种用途广泛的化工原料。实验室中先制备次氯酸钠,再用次氯酸钠溶液和氨反应制备肼并验证肼的性质。实验装置如图所示。

已知: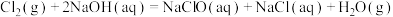
 。当温度超过40℃时,
。当温度超过40℃时, 与
与 溶液反应生成
溶液反应生成 。
。
回答下列问题:
(1)装置B的作用是______________ 。
(2)为控制D装置中的反应温度,除用冷水浴外,还需采取的实验操作是_________ 。
(3)当三颈烧瓶中出现黄绿色气体时立即关闭分液漏斗活塞、移去酒精灯、关闭 。此时装置C的作用是
。此时装置C的作用是_______________ 。
(4)将D装置水槽中的冷水换为热水,把三颈烧瓶中黄绿色气体赶走后,打开 ,通入
,通入 ,使其与
,使其与 溶液反应制取肼。理论上通入三颈烧瓶的
溶液反应制取肼。理论上通入三颈烧瓶的 和
和 的最佳物质的量之比为
的最佳物质的量之比为______ 。
(5)请从提供的下列试剂中选择合适试剂,设计合理的实验方案验证肼的还原性(说明操作、现象和结论)。____________ 。
①淀粉- 溶液 ②稀硫酸(酚酞) ③
溶液 ②稀硫酸(酚酞) ③ ④
④
 ,无色液体)是一种用途广泛的化工原料。实验室中先制备次氯酸钠,再用次氯酸钠溶液和氨反应制备肼并验证肼的性质。实验装置如图所示。
,无色液体)是一种用途广泛的化工原料。实验室中先制备次氯酸钠,再用次氯酸钠溶液和氨反应制备肼并验证肼的性质。实验装置如图所示。
已知:
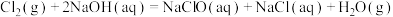
 。当温度超过40℃时,
。当温度超过40℃时, 与
与 溶液反应生成
溶液反应生成 。
。回答下列问题:
(1)装置B的作用是
(2)为控制D装置中的反应温度,除用冷水浴外,还需采取的实验操作是
(3)当三颈烧瓶中出现黄绿色气体时立即关闭分液漏斗活塞、移去酒精灯、关闭
 。此时装置C的作用是
。此时装置C的作用是(4)将D装置水槽中的冷水换为热水,把三颈烧瓶中黄绿色气体赶走后,打开
 ,通入
,通入 ,使其与
,使其与 溶液反应制取肼。理论上通入三颈烧瓶的
溶液反应制取肼。理论上通入三颈烧瓶的 和
和 的最佳物质的量之比为
的最佳物质的量之比为(5)请从提供的下列试剂中选择合适试剂,设计合理的实验方案验证肼的还原性(说明操作、现象和结论)。
①淀粉-
 溶液 ②稀硫酸(酚酞) ③
溶液 ②稀硫酸(酚酞) ③ ④
④
您最近一年使用:0次
2 . (1)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,反应的化学方程式_____________ 漂白粉的有效成分是__________ (填化学式)。
(2)实验室制取氨气的化学方程式:__________________________________
(3)1.2gRSO4中含0.01molR2+,则RSO4的摩尔质量是______________ ;
(4)实验室制Fe(OH)2一般看不到白色的Fe(OH)2沉淀,原因___________________ 现象是:_________________________ 。反应的化学方程式:__________________________________
(5)碳酸钠水解反应的离子方程式(第一步):_________________________ 。
(6)铅蓄电池的负极反应式:_________________________ 。
(7)硫酸钡的沉淀溶解平衡:__________________________________ 。
(2)实验室制取氨气的化学方程式:
(3)1.2gRSO4中含0.01molR2+,则RSO4的摩尔质量是
(4)实验室制Fe(OH)2一般看不到白色的Fe(OH)2沉淀,原因
(5)碳酸钠水解反应的离子方程式(第一步):
(6)铅蓄电池的负极反应式:
(7)硫酸钡的沉淀溶解平衡:
您最近一年使用:0次
名校
3 . 消毒剂在生产生活中有极其重要的作用。
(1)Cl2、H2O2、ClO2(还原产物为Cl-)、O3(1 mol O3转化为1 mol O2和1 mol H2O)等物质常被用作消毒剂。等物质的量上述物质消毒效率最高的是________ (填序号)。
A.Cl2 B.H2O2 C.ClO2 D.O3
(2)H2O2可作为废液消毒剂,有“绿色氧化剂”的美称。如消除采矿业胶液中的氰化物(如KCN),经以下反应实现:KCN+H2O2+H2O=A+NH3↑,则生成物A的化学式为_______________________ ,H2O2被称为“绿色氧化剂”的理由是____________________________ 。
(3)漂白剂亚氯酸钠(NaClO2)在常温、黑暗处可保存一年。亚氯酸不稳定,可分解,反应的离子方程式为HClO2→ClO2↑+H++Cl-+H2O(未配平)。在该反应中,当有1 mol ClO2生成时转移的电子个数约为________ 。
(4)“84”消毒液(主要成分是NaClO)和洁厕剂(主要成分是浓盐酸)不能混用,原因是_______ (用离子方程式表示)。
(1)Cl2、H2O2、ClO2(还原产物为Cl-)、O3(1 mol O3转化为1 mol O2和1 mol H2O)等物质常被用作消毒剂。等物质的量上述物质消毒效率最高的是
A.Cl2 B.H2O2 C.ClO2 D.O3
(2)H2O2可作为废液消毒剂,有“绿色氧化剂”的美称。如消除采矿业胶液中的氰化物(如KCN),经以下反应实现:KCN+H2O2+H2O=A+NH3↑,则生成物A的化学式为
(3)漂白剂亚氯酸钠(NaClO2)在常温、黑暗处可保存一年。亚氯酸不稳定,可分解,反应的离子方程式为HClO2→ClO2↑+H++Cl-+H2O(未配平)。在该反应中,当有1 mol ClO2生成时转移的电子个数约为
(4)“84”消毒液(主要成分是NaClO)和洁厕剂(主要成分是浓盐酸)不能混用,原因是
您最近一年使用:0次
名校
4 . 氯酸钾是一种强氧化剂,在不同条件下KClO3将KI氧化为I2或KIO3。某实验小组在实验室中对KClO3和KI的反应进行了探究。回答下列问题:
实验一 制取氯酸钾

(1)A中反应的化学方程式为_______ 。实验开始时,首先进行的实验步骤是________ 。
(2)A和B装置之间缺少除去氯气中氯化氢的装置,是否会对实验结果产生不利影响,其理由是__ (填“是”或“否”,若选择“是”请说明理由,若选择“否”则不需说明理由)
实验二 氯酸钾与碘化钾反应的研究
(3)该小组研究条件对反应产物的影响,系列a实验的记录表如下(实验在室温下进行):
①系列a实验的实验目的是__ .②设计1号试管实验的作用是__ .
③若2号试管实验现象是溶液变为黄色,取少量该溶液加入淀粉溶液显蓝色;假设氧化产物唯一,还原产物为KCl,则此反应的离子方程式为______ .
实验一 制取氯酸钾

(1)A中反应的化学方程式为
(2)A和B装置之间缺少除去氯气中氯化氢的装置,是否会对实验结果产生不利影响,其理由是
实验二 氯酸钾与碘化钾反应的研究
(3)该小组研究条件对反应产物的影响,系列a实验的记录表如下(实验在室温下进行):
| 试管编号 | 1 | 2 | 3 | 4 |
| 0.20mol•L﹣1KI/mL | 1.0 | 1.0 | 1.0 | 1.0 |
| KClO3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
| 6.0mol•L﹣1H2SO4/mL | 0 | 3.0 | 6.0 | 9.0 |
| 蒸馏水/mL | 9.0 | 6.0 | 3.0 | 0 |
| 实验现象 |
①系列a实验的实验目的是
③若2号试管实验现象是溶液变为黄色,取少量该溶液加入淀粉溶液显蓝色;假设氧化产物唯一,还原产物为KCl,则此反应的离子方程式为
您最近一年使用:0次
解题方法
5 . 已知 Ca(OH)2 与 Cl2 反应的氧化产物与温度有关,在一定量的石灰乳中通入足量的氯气,二者恰好完全反应。生成 Cl-、ClO-、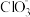 三种含氯元素的离子,其中 ClO- 、
三种含氯元素的离子,其中 ClO- 、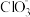 两种离子的物质的量(n)与反应时间
两种离子的物质的量(n)与反应时间
(t)的曲线如图所示。
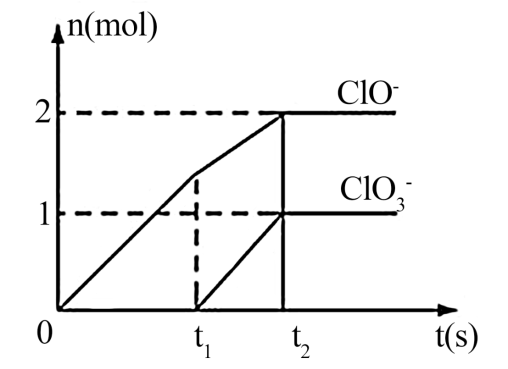
(1)t1 时,开始有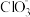 生成的原因是
生成的原因是_____ 。
(2)t2 时,Ca(OH)2 与 Cl2 发生反应的总的化学方程式为___________ 。
(3)该石灰乳中含有 Ca(OH)2 的物质的量是________ mol。
(4)若反应物的量不变,在某温度下恰好完全反应时,氧化产物比值为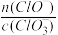 a ,则 n(Cl-)=
a ,则 n(Cl-)=_____ mol
(用含 a 的代数式来表示)。
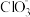 三种含氯元素的离子,其中 ClO- 、
三种含氯元素的离子,其中 ClO- 、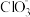 两种离子的物质的量(n)与反应时间
两种离子的物质的量(n)与反应时间(t)的曲线如图所示。

(1)t1 时,开始有
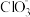 生成的原因是
生成的原因是(2)t2 时,Ca(OH)2 与 Cl2 发生反应的总的化学方程式为
(3)该石灰乳中含有 Ca(OH)2 的物质的量是
(4)若反应物的量不变,在某温度下恰好完全反应时,氧化产物比值为
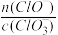 a ,则 n(Cl-)=
a ,则 n(Cl-)=(用含 a 的代数式来表示)。
您最近一年使用:0次
名校
解题方法
6 . 短周期主族元素A、B、C、D的原子序数依次增大,其中A、C同主族,B、C、D同周期,A原子的最外层电子数是次外层电子数的3倍,B是短周期元素中原子半径最大的主族元素,D的原子半径在同周期元素中最小。
(1)A的元素符号____________ 。
(2)A、B、C三种元素形成的简单离子的半径由大到小的顺序是_____________ 。
(3)A、B形成的某化合物能与CO2发生氧化还原反应。每消耗1 mol CO2,转移的电子数为_________________________ 。
(4)B的最高价氧化物对应的水化物与D元素的单质在水溶液中反应的化学方程式是________________________________________ 。
(1)A的元素符号
(2)A、B、C三种元素形成的简单离子的半径由大到小的顺序是
(3)A、B形成的某化合物能与CO2发生氧化还原反应。每消耗1 mol CO2,转移的电子数为
(4)B的最高价氧化物对应的水化物与D元素的单质在水溶液中反应的化学方程式是
您最近一年使用:0次
2018-04-13更新
|
165次组卷
|
2卷引用:黑龙江省双鸭山市第一中学2017-2018学年高一4月月考化学试题1
7 . 在周期表中找到第3横行17纵行的元素,回答下列问题:
(1)该元素的符号是________ ,其原子结构示意图为________
(2)该元素位于第________ 周期,第________ 族。
(3)写出下列反应的化学方程式:
①该元素的单质+水:_______________________________________ ;
②该元素的单质+氢氧化钠:_________________________________ 。
(1)该元素的符号是
(2)该元素位于第
(3)写出下列反应的化学方程式:
①该元素的单质+水:
②该元素的单质+氢氧化钠:
您最近一年使用:0次
名校
8 . 月球含有H、He、N、Na、Mg、Si等元素,是人类未来的资源宝库。
(1)3He是高效核能原料,其原子核内中子数为_____________ 。
(2)Na的原子结构示意图为______ 。
(3)MgCl2在工业上应用广泛,可由MgO制备。
①月球上某矿石经处理得到的MgO中含有少量SiO2,用NaOH溶液除去SiO2的化学方程式为______ 。
②MgO与炭粉和氯气在一定条件下反应可制备MgCl2,尾气中的氯气可用足量冷的NaOH溶液完全吸收,则生成的盐为_________ 、_________ (写化学式)。
(1)3He是高效核能原料,其原子核内中子数为
(2)Na的原子结构示意图为
(3)MgCl2在工业上应用广泛,可由MgO制备。
①月球上某矿石经处理得到的MgO中含有少量SiO2,用NaOH溶液除去SiO2的化学方程式为
②MgO与炭粉和氯气在一定条件下反应可制备MgCl2,尾气中的氯气可用足量冷的NaOH溶液完全吸收,则生成的盐为
您最近一年使用:0次
2018-03-13更新
|
634次组卷
|
4卷引用:辽宁省普通高中2017-2018学年高二学业水平考试模拟化学试题
9 . 某些化学反应可用下式表示:A+B→C+D+H2O
请回答下列问题:
(1)若A、C、D均含有氯元素,且A的化合价介于C与D之间,写出该反应的离子方程式:________________________________________________________________________ 。
(2)若C、D均为气体且都能使澄清石灰水变浑浊,则A与B的组合是____________________ 。
(3)若A为Na2O2,B为硫酸,则C和D的化学式是________________ 。
(4)若A、C均含有铝元素。
①当B是盐酸时,C是__________________ 。
②当B是NaOH时,C是________________ 。
(5)若A为单质,B为第2周期某种元素的最高价氧化物的水化物,请写出符合上式的化学方程式:________________________________________________ (写出两个反应)。
请回答下列问题:
(1)若A、C、D均含有氯元素,且A的化合价介于C与D之间,写出该反应的离子方程式:
(2)若C、D均为气体且都能使澄清石灰水变浑浊,则A与B的组合是
(3)若A为Na2O2,B为硫酸,则C和D的化学式是
(4)若A、C均含有铝元素。
①当B是盐酸时,C是
②当B是NaOH时,C是
(5)若A为单质,B为第2周期某种元素的最高价氧化物的水化物,请写出符合上式的化学方程式:
您最近一年使用:0次
10 . Ⅰ、实 验室可以用KMnO4固体和浓盐酸反应制取少量Cl2,反应的化学方程式为:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O回答下列问题:
验室可以用KMnO4固体和浓盐酸反应制取少量Cl2,反应的化学方程式为:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O回答下列问题:
(1)该反应中被氧化的元素是__________ .
(2)氧化性:KMnO4__________ Cl2(填“>”、“<”或“= ”)
”)
(3)该反应中氧化 剂和氧化产物的物质的量之比为
剂和氧化产物的物质的量之比为__________ .
(4)用双线桥法表示该反应中电子转移的方向和数目:_________
2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O
(5)每生成标准状况下2.24L Cl2,反应中转移电子的物质的量为__________ .
Ⅱ、实验室常用以下方法制取氯气:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O请你根据所学知识回答下列问题:
MnCl2+Cl2↑+2H2O请你根据所学知识回答下列问题:
(1)把氯气通入紫色石蕊试液中,可以观察到的现象是:________________ ,请你解释其中的原因 __________________________________________________
(2)为保证实验安全,常用NaOH溶液吸收多余的氯气。写出反应的化学方程式__________________________________ ;
 验室可以用KMnO4固体和浓盐酸反应制取少量Cl2,反应的化学方程式为:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O回答下列问题:
验室可以用KMnO4固体和浓盐酸反应制取少量Cl2,反应的化学方程式为:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O回答下列问题:(1)该反应中被氧化的元素是
(2)氧化性:KMnO4
 ”)
”)(3)该反应中氧化
 剂和氧化产物的物质的量之比为
剂和氧化产物的物质的量之比为(4)用双线桥法表示该反应中电子转移的方向和数目:
2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O
(5)每生成标准状况下2.24L Cl2,反应中转移电子的物质的量为
Ⅱ、实验室常用以下方法制取氯气:MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O请你根据所学知识回答下列问题:
MnCl2+Cl2↑+2H2O请你根据所学知识回答下列问题:(1)把氯气通入紫色石蕊试液中,可以观察到的现象是:
(2)为保证实验安全,常用NaOH溶液吸收多余的氯气。写出反应的化学方程式
您最近一年使用:0次
2018-01-25更新
|
221次组卷
|
5卷引用:山东省桓台县2017-2018学年高一上学期期末考试化学试题
山东省桓台县2017-2018学年高一上学期期末考试化学试题山东省桓台第二中学2017-2018学年高一上学期期末考试化学试题辽宁省抚顺中学2017-2018学年高一上学期期末考试化学试题黑龙江省牡丹江中学2017-2018学年高一上学期期末考试化学试题(已下线)【艺体生百日捷进提升系列-技能方法】专题3.12 卤族方面试题的解题方法与技巧



