1 . 工业上,我们用电解饱和食盐水制取氯气,请写出其中的化学方程式:_______ ,阳极产物是_______ 。实验室制备氯气时,为防止氯气污染空气,通常将氯气通入氢氧化钠溶液中,写出化学方程式:_______ ;对应的离子方程式_______ 。
您最近一年使用:0次
解题方法
2 . 工业上是将氯气通入到 的
的 溶液中来制备
溶液中来制备 溶液,若
溶液,若 溶液中
溶液中 的质量分数为
的质量分数为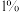 ,则生产
,则生产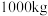 该溶液需消耗氯气的质量为
该溶液需消耗氯气的质量为_______  (保留整数)。
(保留整数)。
 的
的 溶液中来制备
溶液中来制备 溶液,若
溶液,若 溶液中
溶液中 的质量分数为
的质量分数为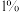 ,则生产
,则生产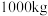 该溶液需消耗氯气的质量为
该溶液需消耗氯气的质量为 (保留整数)。
(保留整数)。
您最近一年使用:0次
名校
3 . 回答下列问题
(1)1mol/L的CaCl2溶液0.5L,Cl-离子的物质的量浓度___________ mol/L。
(2)标准状况下,33.6L的NH3所具有的物质的量为___________ mol,将其溶解于水配成1L的溶液,则溶液的物质的量浓度为___________ mol/L,在Cl2+2NaOH=NaCl+NaClO+H2O的反应中,写出反应的离子方程式___________ 。氧化产物是___________ ,还原产物是___________ ;氧化剂与还原剂的物质的量的比是___________ 。
(3)用双线桥表示出电子转移的方向和数目___________ 。
Cl2+2NaOH=NaCl+NaClO+H2O
(1)1mol/L的CaCl2溶液0.5L,Cl-离子的物质的量浓度
(2)标准状况下,33.6L的NH3所具有的物质的量为
(3)用双线桥表示出电子转移的方向和数目
Cl2+2NaOH=NaCl+NaClO+H2O
您最近一年使用:0次
解题方法
4 . 现有以下物质:①Cl2②SO2③Na2O④NaHSO4⑤漂白粉⑥NaOH溶液⑦Ba(OH)2。回答下列问题:
(1)上述物质中,属于酸性氧化物的有_______ (填标号,下同),属于电解质的有_______ ,⑤的有效成分为_______ (填化学式)。
(2)将②通入足量⑥中,发生反应的离子方程式为_______ 。
(3)④在熔融状态下的电离方程式_______ 。
(4)向⑥中通入适量①可制取84消毒液,反应的化学方程式_______ 。
(1)上述物质中,属于酸性氧化物的有
(2)将②通入足量⑥中,发生反应的离子方程式为
(3)④在熔融状态下的电离方程式
(4)向⑥中通入适量①可制取84消毒液,反应的化学方程式
您最近一年使用:0次
5 . 根据下列实验过程,请回答:
(1)在常温下,将氯气通入氢氧化钠溶液中,所发生反应的离子方程式为:_______ ;
(2)将上述呈碱性的溶液与FeCl3溶液混合,可制得一种新型绿色消毒剂——高铁酸钠(Na2FeO4),反应如下:3ClO-+2Fe3++10OH-=2FeO +3Cl-+5H2O,则该反应中的氧化产物是
+3Cl-+5H2O,则该反应中的氧化产物是_______ (填离子符号),当反应中转移电子的数目是0.3NA时,所消耗的氧化剂的物质的量为_______ 。
(1)在常温下,将氯气通入氢氧化钠溶液中,所发生反应的离子方程式为:
(2)将上述呈碱性的溶液与FeCl3溶液混合,可制得一种新型绿色消毒剂——高铁酸钠(Na2FeO4),反应如下:3ClO-+2Fe3++10OH-=2FeO
 +3Cl-+5H2O,则该反应中的氧化产物是
+3Cl-+5H2O,则该反应中的氧化产物是
您最近一年使用:0次
名校
6 . 医疗机构常用质量分数为7.45% 的次氯酸钠消毒液(密度为1.00 g·cm−3)进行消毒,回答下列问题:
(1)该消毒液的物质的量浓度为_______ mol·L−1(保留到小数点后2位)。
(2)次氯酸钠消毒液使用时需要稀释。某化学实验小组用上述消毒液配制95mL 0.7mol·L−1的溶液。
①需用量筒量取该次氯酸钠消毒液_______ mL;量取时若仰视,所配溶液的浓度将_______ (填“偏高”、“偏低”或“无影响”)。
②定容时加蒸馏水,若不慎超过刻度线,应采取的处理方法是_______ 。
(3)资料显示,次氯酸钠消毒液不能与洁厕灵(含盐酸)混合使用,对此某小组开展如下研究。

能观察到两表面皿之间出现黄绿色气体,写出该反应的离子方程式_______ ;蘸有NaOH溶液的脱脂棉吸收黄绿色气体的离子方程式是_______ 。
(1)该消毒液的物质的量浓度为
(2)次氯酸钠消毒液使用时需要稀释。某化学实验小组用上述消毒液配制95mL 0.7mol·L−1的溶液。
①需用量筒量取该次氯酸钠消毒液
②定容时加蒸馏水,若不慎超过刻度线,应采取的处理方法是
(3)资料显示,次氯酸钠消毒液不能与洁厕灵(含盐酸)混合使用,对此某小组开展如下研究。

能观察到两表面皿之间出现黄绿色气体,写出该反应的离子方程式
您最近一年使用:0次
22-23高二上·全国·课时练习
7 . 电解饱和食盐水的装置如图所示,若收集的H2为2L,则同样条件下收集的Cl2_____ (填“>”“=”或“<”)2L,原因是_____ 。装置改进后,可用于制备NaOH溶液,若测定NaOH溶液的浓度,常用的方法为_____ 。


您最近一年使用:0次
解题方法
8 . 新冠疫情的发生,消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一,而氯气是制取消毒液的重要原料之一。
请回答下列问题:
(1)请写出舍勒发现氯气的化学反应方程式___________________________________ ,若收集到标准状况下3.36LCl2,则被氧化的HCl的物质的量为_____________ mol。
(2)84消毒液(主要成分是NaClO)是常用的消毒剂,工业上将氯气通入烧碱溶液中制取84消毒液,写出此反应的离子方程式_______________________________________ ,若要制取1.5L 2 mol/L的84消毒液,则需要标准状况下___________ L 氯气。
(3)新冠疫情下,人们对杀菌消毒特别重视,曾有报道某居民将84消毒液与洁厕灵(主要成分是浓盐酸)混合使用而中毒,请解释原因__________________________________ (用化学方程式表示), 该反应中氧化剂是______________ 。
请回答下列问题:
(1)请写出舍勒发现氯气的化学反应方程式
(2)84消毒液(主要成分是NaClO)是常用的消毒剂,工业上将氯气通入烧碱溶液中制取84消毒液,写出此反应的离子方程式
(3)新冠疫情下,人们对杀菌消毒特别重视,曾有报道某居民将84消毒液与洁厕灵(主要成分是浓盐酸)混合使用而中毒,请解释原因
您最近一年使用:0次
9 . 回答下列问题
(1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象:
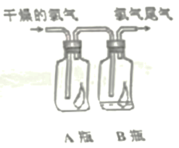
A瓶中有色布条_______ ;B瓶中有色布条_______ 。
(2)为防止氯气尾气污染空气,根据氯水显酸性的性质,可用_______ 溶液吸收多余的氯气,原理是_______ (用化学方程式表示)
(3)根据以上原理,工业上常用廉价的 吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是
吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是_______ (填化学式),长期露置于空气中的漂白粉,加稀盐酸后产生的气体是_______ (用字母代号填)。
A. B.
B. C.
C. D.
D.
(1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象:

A瓶中有色布条
(2)为防止氯气尾气污染空气,根据氯水显酸性的性质,可用
(3)根据以上原理,工业上常用廉价的
 吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是
吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是A.
 B.
B. C.
C. D.
D.
您最近一年使用:0次
名校
解题方法
10 . 某学习小组的同学用MnO2和浓盐酸反应来制备纯净的氯气并验证其有无漂白性,设计装置如图:

(1)A装置中反应的化学方程式:____________________________ ;D装置中现象:___________________ ;该套装置存在的缺陷:_________________________________ 。
(2)取少量E装置中溶液与洁厕灵(含盐酸)混合产生有毒气体,原因是_______________________ (用离子方程式表示)。
(3)若将Cl2通入热的烧碱溶液中,可以发生如下两个反应:
Cl2+2NaOH=NaCl+NaClO+H2O和3Cl2+6NaOH=5NaCl+NaClO3+3H2O。
从氧化还原角度分析Cl2表现了_______________ 。当混合液中Cl-和ClO 的个数比为15∶2时,混合液中ClO-和ClO
的个数比为15∶2时,混合液中ClO-和ClO 的个数比为
的个数比为__________________ 。
(4)近年来,随着化学工业的快速发展,氯气的需求迅速增加。下图是制备氯气的原理示意图,其反应物是___________ ,CuO的作用是_____________ ,写出总反应的化学方程式,并用单线桥法标出该反应的电子转移情况______________________________ 。


(1)A装置中反应的化学方程式:
(2)取少量E装置中溶液与洁厕灵(含盐酸)混合产生有毒气体,原因是
(3)若将Cl2通入热的烧碱溶液中,可以发生如下两个反应:
Cl2+2NaOH=NaCl+NaClO+H2O和3Cl2+6NaOH=5NaCl+NaClO3+3H2O。
从氧化还原角度分析Cl2表现了
 的个数比为15∶2时,混合液中ClO-和ClO
的个数比为15∶2时,混合液中ClO-和ClO 的个数比为
的个数比为(4)近年来,随着化学工业的快速发展,氯气的需求迅速增加。下图是制备氯气的原理示意图,其反应物是

您最近一年使用:0次
2022-12-14更新
|
395次组卷
|
3卷引用:上海市松江二中2021-2022学年高一上学期期末考试化学试题



