解题方法
1 . 化学与人类生活密切相关。请按要求,回答下列问题:
(1)氯气是重要的化工原科,实验室常用 反应制备氯气,该反应的氧化剂是
反应制备氯气,该反应的氧化剂是_______ ;当生成的气体在标准状况下的体积为5.6L时转移的电子数为_______ 个,此时被氧化的物质的物质的量为_______ mol。
(2)“84”消毒液在生活中使用广泛,其有效成分是次氯酸钠。可在常温下将氯气通入NaOH溶液制得,该反应的离子方程式为_______ 。
(3)小苏打可用于治疗胃酸过多,其反应的离子方程式为_______ 。
(1)氯气是重要的化工原科,实验室常用
 反应制备氯气,该反应的氧化剂是
反应制备氯气,该反应的氧化剂是(2)“84”消毒液在生活中使用广泛,其有效成分是次氯酸钠。可在常温下将氯气通入NaOH溶液制得,该反应的离子方程式为
(3)小苏打可用于治疗胃酸过多,其反应的离子方程式为
您最近一年使用:0次
2 . 一种生产高铁酸钾的流程如图所示,写出下列反应的离子方程式
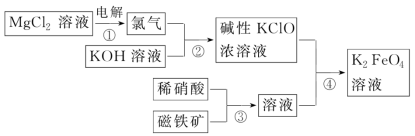
(1)反应①:_______
(2)反应②:_______
(3)反应③:_______
(4)反应④:_______

(1)反应①:
(2)反应②:
(3)反应③:
(4)反应④:
您最近一年使用:0次
名校
3 . 根据题目信息,完成有关方程式的书写。
(1)制备氢氧化铁胶体的离子方程式为_______ 。
(2) 与石灰乳反应的化学方程式:
与石灰乳反应的化学方程式:_______ 。
(3)用单线桥分析 与水反应中电子转移的方向和数目:
与水反应中电子转移的方向和数目:_______ 。
(4)将 固体(黄色,微溶)加入
固体(黄色,微溶)加入 和
和 的混合溶液里,加热,溶液显紫色(
的混合溶液里,加热,溶液显紫色( 无色)。写出该反应的离子方程式:
无色)。写出该反应的离子方程式:_______ 。
(1)制备氢氧化铁胶体的离子方程式为
(2)
 与石灰乳反应的化学方程式:
与石灰乳反应的化学方程式:(3)用单线桥分析
 与水反应中电子转移的方向和数目:
与水反应中电子转移的方向和数目:(4)将
 固体(黄色,微溶)加入
固体(黄色,微溶)加入 和
和 的混合溶液里,加热,溶液显紫色(
的混合溶液里,加热,溶液显紫色( 无色)。写出该反应的离子方程式:
无色)。写出该反应的离子方程式:
您最近一年使用:0次
名校
解题方法
4 . 2004年4月15日,重庆某化工厂氯气泄露并发生爆炸,爆炸现场弥漫着黄色烟雾,这起事故共造成7人丧生,并致使近15万群众紧急疏散。问题:
(1)爆炸现场弥漫的黄色烟雾,除氯气外,形成雾的主要原因是Cl2与水反应,反应的化学方程式为____ ;形成烟的成分包含Cl2与Fe反应的产物____ ,Cl2是一种有毒气体,为消除毒气,消防部门用消防用水与碱液在外围50米处形成两道水幕进行稀释,写出Cl2与强碱溶液反应的离子方程式____ 。
(2)Cl2及其无机产品常用做消毒剂,如“84消毒液”(NaClO)、“漂白粉”等,它们的消毒原理都是在潮湿的空气中与CO2和水蒸气反应生成了次氯酸,请写出“84消毒液”(NaClO)在空气中发生作用的化学方程式:____ 。
(3)用氯气对饮用水消毒已经有百年的历史,这种消毒的方法中氯气会与水中的有机物发生氯代生成对人体有害的的氯代物,于是世界环保联盟建议推广广谱高效消毒剂二氧化氯(ClO2),制取二氧化氯的其中一种方法是:Na2SO3+2NaClO3+H2SO4=2Na2SO4+2ClO2↑+H2O,若生成1 mol ClO2则转移电子数为____ (NA表示阿伏加德罗常数)。
(1)爆炸现场弥漫的黄色烟雾,除氯气外,形成雾的主要原因是Cl2与水反应,反应的化学方程式为
(2)Cl2及其无机产品常用做消毒剂,如“84消毒液”(NaClO)、“漂白粉”等,它们的消毒原理都是在潮湿的空气中与CO2和水蒸气反应生成了次氯酸,请写出“84消毒液”(NaClO)在空气中发生作用的化学方程式:
(3)用氯气对饮用水消毒已经有百年的历史,这种消毒的方法中氯气会与水中的有机物发生氯代生成对人体有害的的氯代物,于是世界环保联盟建议推广广谱高效消毒剂二氧化氯(ClO2),制取二氧化氯的其中一种方法是:Na2SO3+2NaClO3+H2SO4=2Na2SO4+2ClO2↑+H2O,若生成1 mol ClO2则转移电子数为
您最近一年使用:0次
5 . 氯是一种生产生活中常见的元素,下图是几种含氯产品。

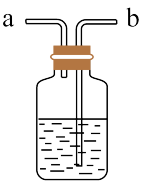
(1) 是有毒气体,为了防止多余
是有毒气体,为了防止多余 污染空气、需要如图装置进行尾气处理,用离子方程式表示该原理
污染空气、需要如图装置进行尾气处理,用离子方程式表示该原理_______ 气体应该由_______ (填a或b)管通入。若要吸收标准状况下 ,至少需要
,至少需要 上述溶液
上述溶液_______ mL。
(2)工业上制取漂白粉的化学方程式是_______ 。
(3)同学们探究“84”消毒液在不同pH不使红纸褪色的情况,做了如下实验:
步骤1:将5mL市售“84”消毒液100倍,测得稀释后溶液的pH=12;
步骤2:将稀释后溶液各20mL分别加入3个洁净的小烧杯中;
步骤3:用 溶液将3个烧杯内溶液的pH分别调至10、7和4.(溶液体积变化忽略不计)
溶液将3个烧杯内溶液的pH分别调至10、7和4.(溶液体积变化忽略不计)
步骤4:在3个烧杯中分别放入大小相同的红纸,观察现象,记录如下:
已知溶液中 、
、 和
和 的物质的量分数(a)随溶液pH变化的关系如图所示:
的物质的量分数(a)随溶液pH变化的关系如图所示:
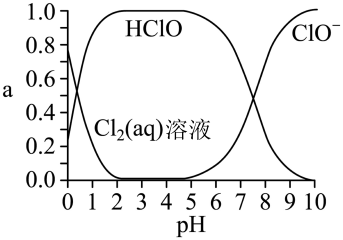
①由实验现象可获得结论:溶液的pH在4~10范围内,pH越大,红纸褪色_______ (填“越快”或“越慢”)。
②结合图像进行分析,b、c两烧杯中实验现象出现差异的原因是_______ 。
③预测pH=1、10min后,红纸的颜色(与a、b、c颜色相比)_______ 。

(1)
 是有毒气体,为了防止多余
是有毒气体,为了防止多余 污染空气、需要如图装置进行尾气处理,用离子方程式表示该原理
污染空气、需要如图装置进行尾气处理,用离子方程式表示该原理 ,至少需要
,至少需要 上述溶液
上述溶液
(2)工业上制取漂白粉的化学方程式是
(3)同学们探究“84”消毒液在不同pH不使红纸褪色的情况,做了如下实验:
步骤1:将5mL市售“84”消毒液100倍,测得稀释后溶液的pH=12;
步骤2:将稀释后溶液各20mL分别加入3个洁净的小烧杯中;
步骤3:用
 溶液将3个烧杯内溶液的pH分别调至10、7和4.(溶液体积变化忽略不计)
溶液将3个烧杯内溶液的pH分别调至10、7和4.(溶液体积变化忽略不计)步骤4:在3个烧杯中分别放入大小相同的红纸,观察现象,记录如下:
| 烧杯 | 溶液的pH | 现象 |
| a | 10 | 10min后,红纸基本不褪色;4h后红纸褪色 |
| b | 7 | 10min后,红纸颜色变浅;4h后红纸褪色 |
| c | 4 | 10min后,红纸颜色变得更浅;4h后红纸褪色 |
 、
、 和
和 的物质的量分数(a)随溶液pH变化的关系如图所示:
的物质的量分数(a)随溶液pH变化的关系如图所示:
①由实验现象可获得结论:溶液的pH在4~10范围内,pH越大,红纸褪色
②结合图像进行分析,b、c两烧杯中实验现象出现差异的原因是
③预测pH=1、10min后,红纸的颜色(与a、b、c颜色相比)
您最近一年使用:0次
2022-11-05更新
|
188次组卷
|
2卷引用:福建省厦门双十中学2022-2023学年高一上学期期中考试化学试题
6 . 按要求完成下列化学用语
(1)碳酸氢钠的电离方程式_______ 。
(2)氢氧化铜的电离方程式_______ 。
(3)Na与水反应离子方程式_______ 。
(4)Na2O2与二氧化碳反应的化学方程式_______ 。
(5)工业制备漂白粉的化学方程式_______ 。
(6)过量碳酸氢钠溶液与澄清石灰水反应的离子方程式_______ 。
(7)Na2CO3溶液与少量盐酸反应离子方程式_______ 。
(1)碳酸氢钠的电离方程式
(2)氢氧化铜的电离方程式
(3)Na与水反应离子方程式
(4)Na2O2与二氧化碳反应的化学方程式
(5)工业制备漂白粉的化学方程式
(6)过量碳酸氢钠溶液与澄清石灰水反应的离子方程式
(7)Na2CO3溶液与少量盐酸反应离子方程式
您最近一年使用:0次
解题方法
7 . 回答下列问题
(1)H2在单质B中燃烧产生苍白色的火焰,产物溶于水得到常见的强酸,其反应的化学方程式为_______ 。
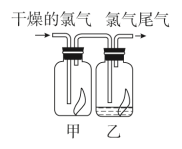
(2)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶甲和盛有潮湿有色布条的广口瓶乙,可观察到的现象是_______ ,这是因为氯气通入水中发生化学反应,生成了具有漂白性的物质:_______ (填化学式),化学方程式为_______ 。
(3)实验室制备氯气时要在通风橱内完成,并且为了防止氯气污染空气,要有尾气处理装置,一般用_______ 溶液吸收多余的氯气,原理是_______ (用化学方程式表示)。
(4)根据这一原理,工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是_______ (填化学式),长期露置于空气中的漂白粉,加稀盐酸后产生的气体主要是_______ (用字母代号填)。
A.O2 B.Cl2 C.CO2 D.HClO
(1)H2在单质B中燃烧产生苍白色的火焰,产物溶于水得到常见的强酸,其反应的化学方程式为
(2)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶甲和盛有潮湿有色布条的广口瓶乙,可观察到的现象是

(3)实验室制备氯气时要在通风橱内完成,并且为了防止氯气污染空气,要有尾气处理装置,一般用
(4)根据这一原理,工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是
A.O2 B.Cl2 C.CO2 D.HClO
您最近一年使用:0次
8 . 某漂粉精说明书如下:
(1)从主要成分看,可知生产漂粉精的原料是氯气和石灰乳,请写出制漂粉精的化学方程式:_______ ,漂粉精中有效成分为_______ 。
(2)生活中常有的漂白剂还有“84消毒液”,制备“84消毒液”的反应物是通过氯碱工业制得,请写出电解饱和食盐水的化学方程式:_______ ,并进一步写出制备“84消毒液”的化学方程式_______ 。
(3)为什么家庭中的漂白剂使用漂粉精,而不使用氯水?_______ 。
| 使用说明书 主要成分:次氯酸钙、氯化钙 用途用量:取漂粉精2-3克,水100克,配成溶液,将禽流感病人用具浸泡其中5-10分钟,如需要可延长时间,提高浓度。 注意事项:密封保存于阴凉处,随配随用,有腐蚀性,少与手接触。 |
(2)生活中常有的漂白剂还有“84消毒液”,制备“84消毒液”的反应物是通过氯碱工业制得,请写出电解饱和食盐水的化学方程式:
(3)为什么家庭中的漂白剂使用漂粉精,而不使用氯水?
您最近一年使用:0次
9 . Ⅰ.NaClO是“84”消毒液的有效成分。请回答下列问题:
(1)NaClO中Cl元素的化合价是_______ 。
(2)浸泡衣物时加入“84”消毒液,在空气中放置一段时间后漂白效果更好,结合离子方程式解释原因:_______ 。(已知酸性: )
)
(3)若将“84”消毒液与洁厕灵(主要成分是HCl)混合使用,会产生黄绿色的有毒气体,其反应的离子方程式是_______ 。
Ⅱ. 是一种有毒气体,如果泄漏会造成严重的危害。
是一种有毒气体,如果泄漏会造成严重的危害。
(4)已知 ,化工厂可用浓氨水来检验
,化工厂可用浓氨水来检验 是否泄漏。该反应中被氧化和未被氧化的
是否泄漏。该反应中被氧化和未被氧化的 分子的个数比为
分子的个数比为_______ 。
(5)喷射石灰乳等碱性物质可以减轻少量 泄漏造成的危害。
泄漏造成的危害。 和石灰乳反应的化学方程式是
和石灰乳反应的化学方程式是_______ 。
(1)NaClO中Cl元素的化合价是
(2)浸泡衣物时加入“84”消毒液,在空气中放置一段时间后漂白效果更好,结合离子方程式解释原因:
 )
)(3)若将“84”消毒液与洁厕灵(主要成分是HCl)混合使用,会产生黄绿色的有毒气体,其反应的离子方程式是
Ⅱ.
 是一种有毒气体,如果泄漏会造成严重的危害。
是一种有毒气体,如果泄漏会造成严重的危害。(4)已知
 ,化工厂可用浓氨水来检验
,化工厂可用浓氨水来检验 是否泄漏。该反应中被氧化和未被氧化的
是否泄漏。该反应中被氧化和未被氧化的 分子的个数比为
分子的个数比为(5)喷射石灰乳等碱性物质可以减轻少量
 泄漏造成的危害。
泄漏造成的危害。 和石灰乳反应的化学方程式是
和石灰乳反应的化学方程式是
您最近一年使用:0次
解题方法
10 . 氯气是一种非常重要的化工原料,可用于制造盐酸、漂白剂、农药等,但氯气有毒,使用或接触到有关物质时应注意安全。请回答下列问题:
(1)新制氯水中,含有氯元素的微粒有___________ (填微粒符号,下同,不考虑水中杂质与氯气的反应),其中使新制氯水显淡黄绿色的微粒是___________ 。
(2) 和
和 可用于生产农药、催化剂等。31g红磷在一定量的氯气中燃烧,红磷和氯气均完全反应,生成白色烟雾,其中
可用于生产农药、催化剂等。31g红磷在一定量的氯气中燃烧,红磷和氯气均完全反应,生成白色烟雾,其中 和
和 的物质的量之比为3:2,则消耗的氯气在标准状况下的体积为
的物质的量之比为3:2,则消耗的氯气在标准状况下的体积为___________ L。
(3)标准状况下,氯气的密度为___________ 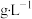 (结果保留两位小数),比空气的密度大。某地施工时挖破了废弃自来水厂的储氯罐,导致氯气泄漏。当地居民逃生和自救的正确做法是
(结果保留两位小数),比空气的密度大。某地施工时挖破了废弃自来水厂的储氯罐,导致氯气泄漏。当地居民逃生和自救的正确做法是___________ (填序号)。
a.逆风往高处跑 b.顺风往低处跑
c.用蘸有肥皂水的毛巾捂住口鼻 d.戴上用浓NaOH溶液处理过的口罩
(4)实验室制氯气时,要用NaOH溶液吸收尾气,反应的化学方程式为___________ ;通常不用澄清石灰水吸收氯气的原因是___________ 。
(1)新制氯水中,含有氯元素的微粒有
(2)
 和
和 可用于生产农药、催化剂等。31g红磷在一定量的氯气中燃烧,红磷和氯气均完全反应,生成白色烟雾,其中
可用于生产农药、催化剂等。31g红磷在一定量的氯气中燃烧,红磷和氯气均完全反应,生成白色烟雾,其中 和
和 的物质的量之比为3:2,则消耗的氯气在标准状况下的体积为
的物质的量之比为3:2,则消耗的氯气在标准状况下的体积为(3)标准状况下,氯气的密度为
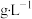 (结果保留两位小数),比空气的密度大。某地施工时挖破了废弃自来水厂的储氯罐,导致氯气泄漏。当地居民逃生和自救的正确做法是
(结果保留两位小数),比空气的密度大。某地施工时挖破了废弃自来水厂的储氯罐,导致氯气泄漏。当地居民逃生和自救的正确做法是a.逆风往高处跑 b.顺风往低处跑
c.用蘸有肥皂水的毛巾捂住口鼻 d.戴上用浓NaOH溶液处理过的口罩
(4)实验室制氯气时,要用NaOH溶液吸收尾气,反应的化学方程式为
您最近一年使用:0次



