名校
1 . 现有下列物质:①熔融NaCl ② 溶液 ③氯气 ④
溶液 ③氯气 ④ ⑤NaOH溶液 ⑥氢氧化铁胶体 ⑦
⑤NaOH溶液 ⑥氢氧化铁胶体 ⑦ ⑧铜 ⑨ 过氧化钠 ⑩
⑧铜 ⑨ 过氧化钠 ⑩
(1)上述物质中属于电解质的是_______ (填标号)。
(2)将②逐滴加入⑥中的现象是_______ 。
(3)④加入过量的氢氧化钡溶液中,发生反应的离子方程式为_______ 。
(4)③通入石灰乳中,发生反应的离子方程式为_______ 。
(5)⑦与⑨反应的方程式为:_______ ,标准状况下,生成22.4L氧气转移的电子数目为_______ 。
 溶液 ③氯气 ④
溶液 ③氯气 ④ ⑤NaOH溶液 ⑥氢氧化铁胶体 ⑦
⑤NaOH溶液 ⑥氢氧化铁胶体 ⑦ ⑧铜 ⑨ 过氧化钠 ⑩
⑧铜 ⑨ 过氧化钠 ⑩
(1)上述物质中属于电解质的是
(2)将②逐滴加入⑥中的现象是
(3)④加入过量的氢氧化钡溶液中,发生反应的离子方程式为
(4)③通入石灰乳中,发生反应的离子方程式为
(5)⑦与⑨反应的方程式为:
您最近一年使用:0次
解题方法
2 . Ⅰ.氯气是一种重要的化工原料,氯气及其化合物在自来水的消毒、农药的生产、药物的合成等领域都有着重要的应用。
(1)Ca(ClO)2中Cl的化合价为___________ ,Ca(ClO)2具有较强的_________ (填“氧化”或“还原”)性,是常用的漂白粉的有效成分。
(2)黄色气体ClO2可用于污水杀菌和饮用水净化。
①KClO3与SO2在强酸性溶液中反应可制得ClO2,SO2被氧化为 ,该反应的离子方程式为:
,该反应的离子方程式为:___________ 。
②NaClO可将酸性废水中的Fe2+氧化为Fe3+,本身被还原为NaCl,该反应过程中氧化剂与还原剂的物质的量之比为___________ 。
Ⅱ.某学生设计如图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(该反应为放热反应),回答下列问题(消石灰为氢氧化钙):
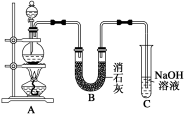
(3)在A装置中用固体二氧化锰与浓盐酸在加热条件下反应制取氯气,写出该反应的化学方程式:___ 。
(4)C装置的作用是(用离子方程式表示)_____________ 。
(5)此实验所得漂白粉的有效成分偏低,该学生经分析并查阅资料发现,主要原因是在U形管中还存在两个副反应。
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是将U型管置于________ 中(填“冰水浴还是热水浴”)。
②另一个副反应是2HCl+Ca(OH)2=CaCl2+2H2O,为避免此副反应的发生,装置的改进措施为______ 。
(1)Ca(ClO)2中Cl的化合价为
(2)黄色气体ClO2可用于污水杀菌和饮用水净化。
①KClO3与SO2在强酸性溶液中反应可制得ClO2,SO2被氧化为
 ,该反应的离子方程式为:
,该反应的离子方程式为:②NaClO可将酸性废水中的Fe2+氧化为Fe3+,本身被还原为NaCl,该反应过程中氧化剂与还原剂的物质的量之比为
Ⅱ.某学生设计如图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(该反应为放热反应),回答下列问题(消石灰为氢氧化钙):

(3)在A装置中用固体二氧化锰与浓盐酸在加热条件下反应制取氯气,写出该反应的化学方程式:
(4)C装置的作用是(用离子方程式表示)
(5)此实验所得漂白粉的有效成分偏低,该学生经分析并查阅资料发现,主要原因是在U形管中还存在两个副反应。
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是将U型管置于
②另一个副反应是2HCl+Ca(OH)2=CaCl2+2H2O,为避免此副反应的发生,装置的改进措施为
您最近一年使用:0次
3 . FeCl3具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3高效,且腐蚀性小。常见水处理剂还有高铁酸盐及ClO2,请回答下列问题:
(1)FeCl3可以用来刻蚀铜箔制造电路板,写出对应离子方程式________________ ;高铁酸盐是一种绿色净水剂,其有效成分是高铁酸根FeO 。能消毒,且能净水。工业上常在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠,该反应的化学方程式为:
。能消毒,且能净水。工业上常在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠,该反应的化学方程式为:_______________
(2)ClO2是一种高效、低毒的消毒剂,工业上可用KC1O3与Na2SO3在H2SO4存在下制得ClO2,该反应氧化剂与还原剂物质的量之比为___________
(3)漂白粉在工业中常用氯气通入石灰乳来制备,写出对应化学方程式_________________
(4)描述实验室制备氢氧化铁胶体的方法______________ ;写出对应的化学方程式_______________
(5)为节约成本,工业上用NaClO3氧化酸性FeCl2废液得到FeCl3,配平下列反应:_____ 。
___________ClO + _____Fe2+ + _____ ( ) = ____Fe3+ + ___ Cl-+ _______ ( )
+ _____Fe2+ + _____ ( ) = ____Fe3+ + ___ Cl-+ _______ ( )
(1)FeCl3可以用来刻蚀铜箔制造电路板,写出对应离子方程式
 。能消毒,且能净水。工业上常在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠,该反应的化学方程式为:
。能消毒,且能净水。工业上常在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠,该反应的化学方程式为:(2)ClO2是一种高效、低毒的消毒剂,工业上可用KC1O3与Na2SO3在H2SO4存在下制得ClO2,该反应氧化剂与还原剂物质的量之比为
(3)漂白粉在工业中常用氯气通入石灰乳来制备,写出对应化学方程式
(4)描述实验室制备氢氧化铁胶体的方法
(5)为节约成本,工业上用NaClO3氧化酸性FeCl2废液得到FeCl3,配平下列反应:
___________ClO
 + _____Fe2+ + _____ ( ) = ____Fe3+ + ___ Cl-+ _______ ( )
+ _____Fe2+ + _____ ( ) = ____Fe3+ + ___ Cl-+ _______ ( )
您最近一年使用:0次
名校
4 . “7•20”特大洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效措施之一。“84”消毒液、漂白粉和ClO2等都是有效的消杀试剂。
(1)用化学方程式表示氯气与烧碱溶液制备“84”消毒液的原理____ ,标况下56L氯气完全被吸收,需要____ L1mol/L的NaOH溶液。
(2)使用漂白粉漂白,只需取适量漂白粉溶于水即可,漂白原理用化学方程式表示为_____ 。
(3)漂白粉的保存要注意密封,为了判断一份儿久置的漂白粉是①没有失效②部分失效③完全失效。某化学兴趣小组设计实验进行验证。
已知:Ca(ClO)2溶液呈碱性;Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O;Ca(ClO)2+2HCl(稀)=CaCl2+2HClO
a.甲同学取适量漂白粉样品,滴加浓盐酸,将产生的气体直接通入澄清石灰水中,没有发现石灰水变浑浊。由此,判断结论为①,你是否同意他的结论____ (填“同意”或“不同意”),若不同意,你认为的结论是____ (若同意,此空不用填)
A.② B.③ C.①或② D.①②③均有可能
b.乙同学改用滴加稀盐酸,发现产生大量气泡,将气体通入澄清石灰水中,石灰水变浑浊;他又取少量漂白粉样品配成溶液,滴在pH试纸上,最终试纸变白。据此你得出的结论是_____ (从①②③中选填)。
(4)目前普遍使用ClO2代替Cl2及次氯酸盐作为广谱抗菌消毒剂,因为它安全、低毒,高效。其摩尔质量为_____ 。ClO2还可以将剧毒的NaCN转化为无毒物质除去,产物是氯化钠和两种常见气体。试写出该反应的化学方程式_____ 。
(1)用化学方程式表示氯气与烧碱溶液制备“84”消毒液的原理
(2)使用漂白粉漂白,只需取适量漂白粉溶于水即可,漂白原理用化学方程式表示为
(3)漂白粉的保存要注意密封,为了判断一份儿久置的漂白粉是①没有失效②部分失效③完全失效。某化学兴趣小组设计实验进行验证。
已知:Ca(ClO)2溶液呈碱性;Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O;Ca(ClO)2+2HCl(稀)=CaCl2+2HClO
a.甲同学取适量漂白粉样品,滴加浓盐酸,将产生的气体直接通入澄清石灰水中,没有发现石灰水变浑浊。由此,判断结论为①,你是否同意他的结论
A.② B.③ C.①或② D.①②③均有可能
b.乙同学改用滴加稀盐酸,发现产生大量气泡,将气体通入澄清石灰水中,石灰水变浑浊;他又取少量漂白粉样品配成溶液,滴在pH试纸上,最终试纸变白。据此你得出的结论是
(4)目前普遍使用ClO2代替Cl2及次氯酸盐作为广谱抗菌消毒剂,因为它安全、低毒,高效。其摩尔质量为
您最近一年使用:0次
解题方法
5 . 氯及其化合物在生产生活中有重要的作用。已知某品牌的84消毒液和洁厕灵的部分标签如图所示:
回答下列问题:
(1)工业上通常将氯气通入氢氧化钠溶液中制备84消毒液,请写出该反应的离子方程式___________ 。
(2)各类杀菌消毒剂使用时,必须严格按照使用说明。
①巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是 与
与 反应产生
反应产生 促进藻类快速生长。该反应说明氧化性:
促进藻类快速生长。该反应说明氧化性:
___________  (填“>”或“<”)。当有0.1
(填“>”或“<”)。当有0.1
 生成时,反应中转移电子为
生成时,反应中转移电子为___________  。
。
②王女士在清洁马桶时,在倒入上述洁厕灵后将上述84消毒液也倒入其中,随后突然晕倒,原因是该过程产生了有毒的氯气,该过程发生反应的离子方程式为___________ 。
| ××牌洁厕灵 规格:1L 有效成分:盐酸,表面活性剂,香精 | ××牌84消毒液 规格:500  有效成分:  (“有效氯”含量:5.5%~6.5%) |
回答下列问题:
(1)工业上通常将氯气通入氢氧化钠溶液中制备84消毒液,请写出该反应的离子方程式
(2)各类杀菌消毒剂使用时,必须严格按照使用说明。
①巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是
 与
与 反应产生
反应产生 促进藻类快速生长。该反应说明氧化性:
促进藻类快速生长。该反应说明氧化性:
 (填“>”或“<”)。当有0.1
(填“>”或“<”)。当有0.1
 生成时,反应中转移电子为
生成时,反应中转移电子为 。
。②王女士在清洁马桶时,在倒入上述洁厕灵后将上述84消毒液也倒入其中,随后突然晕倒,原因是该过程产生了有毒的氯气,该过程发生反应的离子方程式为
您最近一年使用:0次
解题方法
6 . 填空
(1)金属钠与水反应的化学方程式:_______
(2)写出次氯酸见光分解的化学方程式:_______
(3)写出氯气和氢氧化钠溶液反应的离子方程式 :_______
(1)金属钠与水反应的化学方程式:
(2)写出次氯酸见光分解的化学方程式:
(3)写出氯气和氢氧化钠溶液反应的
您最近一年使用:0次
解题方法
7 . 写出下列反应的化学方程式,标出电子转移的方向和数目,并指出氯气在反应中表现出什么性质。
(1)氢气在氯气中燃烧_______ 。
(2)氯气与氢氧化钠反应_______ 。
(3)铁在氯气中燃烧_______ 。
(1)氢气在氯气中燃烧
(2)氯气与氢氧化钠反应
(3)铁在氯气中燃烧
您最近一年使用:0次
名校
8 . 氯是海水中含量最丰富的元素,氯的单质及其化合物在生成、生活领域应用广泛。
(1)自来水厂常用液氯进行杀菌消毒。氯气溶于水发生的可逆反应为_____________ (用离子方程式表示)。
(2)用液氯消毒会产生微量有机氯代物,危害人体健康,可以使用二氧化氯(ClO2)代替液氯。工业上以二硫化亚铁(FeS2)、氯酸钠(NaClO3)和硫酸溶液混合制备二氧化氯气体。已知黄铁矿中的硫元素最终氧化成 ,写出制备二氧化氯的离子方程式
,写出制备二氧化氯的离子方程式_______ 。
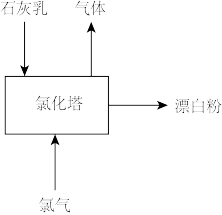
(3)生产漂白粉工厂的主要设备是氯化塔,塔从上到下分为四层,如图为生产流程示意图。生产漂白粉反应的化学方程式为_______ 。实际生产中,将石灰乳(含有3%~6%水分的熟石灰)从塔顶喷洒而下,氯气从塔的最底层通入。这样加料的目的是_______ 。
(1)自来水厂常用液氯进行杀菌消毒。氯气溶于水发生的可逆反应为
(2)用液氯消毒会产生微量有机氯代物,危害人体健康,可以使用二氧化氯(ClO2)代替液氯。工业上以二硫化亚铁(FeS2)、氯酸钠(NaClO3)和硫酸溶液混合制备二氧化氯气体。已知黄铁矿中的硫元素最终氧化成
 ,写出制备二氧化氯的离子方程式
,写出制备二氧化氯的离子方程式(3)生产漂白粉工厂的主要设备是氯化塔,塔从上到下分为四层,如图为生产流程示意图。生产漂白粉反应的化学方程式为

您最近一年使用:0次
解题方法
9 . 化学工业为疫情防控提供了强有力的物质支撑。次氯酸钠和二氧化氯(分子式为ClO2,其中Cl元素的化合价为+4价)在水处理等方面有广泛应用,是一种高效安全的灭菌消毒剂。
(1)NaClO溶液可由低温下将Cl2缓慢通入NaOH溶液中而制得。制备NaClO的化学方程式为_______ ;用于环境杀菌消毒的NaClO溶液须稀释并及时使用,若在空气中暴露时间过长且见光,将会导致消毒作用减弱,其原因是_______ 。
(2)ClO2的制备方法,有下列两种:
方法Ⅰ:2NaClO3 + 4HCl =2ClO2↑ + Cl2↑+ 2NaCl + 2H2O
方法Ⅱ:2NaClO3 + H2O2 +H2SO4 = 2ClO2↑ + O2↑+ Na2SO4 +2H2O
方法Ⅰ反应中,氧化产物为_______ (填化学式);方法Ⅱ反应中,产生1mol ClO2气体,电子转移_______ mol。
(3)将ClO2溶于水得到溶液,为测定其浓度,进行以下实验操作:
步骤1 取待测ClO2溶液20.00mL于锥形瓶中;
步骤2 用稀硫酸调节溶液至酸性,加入足量的KI晶体充分反应,使ClO2转化为Cl-;发生的反应为:4ClO2 + 20 KI +8H2SO4=4KCl +10I2 + 8 X + 8H2O
步骤3 逐滴加入0.1500mol·L-1的Na2S2O3溶液,发生的反应为:I2 + 2Na2S2O3= Na2S4O6 +2NaI,当将步骤2中反应生成的I2恰好完全反应时,消耗Na2S2O3溶液的体积为24.00mL。
①写出步骤2反应方程式中的X的化学式为_______ ;
②计算:ClO2溶液的物质的量浓度为_______ mol·L-1(写出计算过程)。
(1)NaClO溶液可由低温下将Cl2缓慢通入NaOH溶液中而制得。制备NaClO的化学方程式为
(2)ClO2的制备方法,有下列两种:
方法Ⅰ:2NaClO3 + 4HCl =2ClO2↑ + Cl2↑+ 2NaCl + 2H2O
方法Ⅱ:2NaClO3 + H2O2 +H2SO4 = 2ClO2↑ + O2↑+ Na2SO4 +2H2O
方法Ⅰ反应中,氧化产物为
(3)将ClO2溶于水得到溶液,为测定其浓度,进行以下实验操作:
步骤1 取待测ClO2溶液20.00mL于锥形瓶中;
步骤2 用稀硫酸调节溶液至酸性,加入足量的KI晶体充分反应,使ClO2转化为Cl-;发生的反应为:4ClO2 + 20 KI +8H2SO4=4KCl +10I2 + 8 X + 8H2O
步骤3 逐滴加入0.1500mol·L-1的Na2S2O3溶液,发生的反应为:I2 + 2Na2S2O3= Na2S4O6 +2NaI,当将步骤2中反应生成的I2恰好完全反应时,消耗Na2S2O3溶液的体积为24.00mL。
①写出步骤2反应方程式中的X的化学式为
②计算:ClO2溶液的物质的量浓度为
您最近一年使用:0次
解题方法
10 . 生产、生活中处处有化学,利用所学化学知识回答下列问题。
(1)在潜水艇和消防员的呼吸面具中, 与二氧化碳反应的化学方程式为
与二氧化碳反应的化学方程式为_______ ;从氧化剂和还原剂的角度分析,在这个反应中 的作用是
的作用是_______
(2)铝盐,铁盐可以作净水剂, 的电离方程式是
的电离方程式是_______ ;将饱和 溶液滴入沸水制得的
溶液滴入沸水制得的 胶体中,分散剂是
胶体中,分散剂是_______ 。该分散系区别于其他分散系的本质特征是_______ 。
(3)金属钠着火时不能用水灭火,原因是_______ 。
(4)阅读下列科普短文并填空。
84消毒液①和医用酒精②是人们生活中常用的消毒剂,84消毒液的名称源于北京某医院在1984年研制成功的一种高效含氯消毒液。它可用 ③与
③与 溶液④反应制得,其主要成分为
溶液④反应制得,其主要成分为 ⑤、
⑤、 ⑥,是无色或淡黄色液体,人们主要利用84消毒液中
⑥,是无色或淡黄色液体,人们主要利用84消毒液中 的氧化性进行消毒。医用酒精中,乙醇的体积分数通常为75%。过高浓度的乙醇⑦溶液会使病毒表面的蛋白质⑧迅速凝结,形成一层保护膜,减弱消毒效果。过低浓度的乙醇溶液不能使蛋白质变性,同样不能获得很好的消毒效果。
的氧化性进行消毒。医用酒精中,乙醇的体积分数通常为75%。过高浓度的乙醇⑦溶液会使病毒表面的蛋白质⑧迅速凝结,形成一层保护膜,减弱消毒效果。过低浓度的乙醇溶液不能使蛋白质变性,同样不能获得很好的消毒效果。
在上述短文标有序号的物质中,属于混合物的是_______ (填序号,下同);属于电解质的是_______ 。用上述方法制备84消毒液时,发生反应的离子方程式为_______
(1)在潜水艇和消防员的呼吸面具中,
 与二氧化碳反应的化学方程式为
与二氧化碳反应的化学方程式为 的作用是
的作用是(2)铝盐,铁盐可以作净水剂,
 的电离方程式是
的电离方程式是 溶液滴入沸水制得的
溶液滴入沸水制得的 胶体中,分散剂是
胶体中,分散剂是(3)金属钠着火时不能用水灭火,原因是
(4)阅读下列科普短文并填空。
84消毒液①和医用酒精②是人们生活中常用的消毒剂,84消毒液的名称源于北京某医院在1984年研制成功的一种高效含氯消毒液。它可用
 ③与
③与 溶液④反应制得,其主要成分为
溶液④反应制得,其主要成分为 ⑤、
⑤、 ⑥,是无色或淡黄色液体,人们主要利用84消毒液中
⑥,是无色或淡黄色液体,人们主要利用84消毒液中 的氧化性进行消毒。医用酒精中,乙醇的体积分数通常为75%。过高浓度的乙醇⑦溶液会使病毒表面的蛋白质⑧迅速凝结,形成一层保护膜,减弱消毒效果。过低浓度的乙醇溶液不能使蛋白质变性,同样不能获得很好的消毒效果。
的氧化性进行消毒。医用酒精中,乙醇的体积分数通常为75%。过高浓度的乙醇⑦溶液会使病毒表面的蛋白质⑧迅速凝结,形成一层保护膜,减弱消毒效果。过低浓度的乙醇溶液不能使蛋白质变性,同样不能获得很好的消毒效果。在上述短文标有序号的物质中,属于混合物的是
您最近一年使用:0次



