1 . 下表是元素周期表的部分,表中所列的数字分别代表某一种元素。针对表中①-⑩号元素回答下列问题。
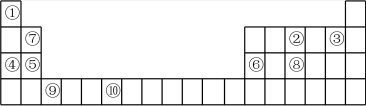
(1)⑩元素的名称是___________ ,⑨元素的原子结构示意图为___________ 。
(2)②、③、④、⑤、⑥五种元素中,原子半径由小到大的顺序是___________ (填元素符号);这五种元素分别形成的简单离子中离子半径最小的是___________ 。(填离子符号)
(3)某些不同族元素的性质也有一定的相似性,如表中元素⑦与元素⑥的氢氧化物有相似的性质,请写出元素⑦的氢氧化物与NaOH溶液反应的化学方程式:___________ 。
(4)元素①和④的单质化合形成的化合物能与水反应生成氢气,向反应后的溶液中滴入酚酞,溶液变红,反应的化学方程式为_________ 。
(5)元素④和⑥相比,金属性较强的是_________ (填元素符号),下列能证明这一事实的有_________ (填序号)。
A.在化合物中④的化合价比⑥的低 B.④的单质能与冷水剧烈反应而⑥的单质不能
C.④的最高价氧化物对应水化物的碱性比⑥强 D.④单质的熔点比⑥单质的低
(6)⑧号元素有多种化合物,次磷酸(H3PO2)和次磷酸钠(NaH2PO2)常为化工生产的还原剂。
I.已知H3PO2是一种一元弱酸,向Ba(H2PO2)2溶液中加入H2SO4制备H3PO2,写出该反应的离子方程式___________ 。
Ⅱ.NaH2PO2可在酸性条件下与Ni2+作用进行“化学镀镍”(如在木材表面生成一层Ni-P合金),反应中磷元素化合价发生的变化是___________ (选填编号)。
a.升高 b.降低 c.既升高又降低

(1)⑩元素的名称是
(2)②、③、④、⑤、⑥五种元素中,原子半径由小到大的顺序是
(3)某些不同族元素的性质也有一定的相似性,如表中元素⑦与元素⑥的氢氧化物有相似的性质,请写出元素⑦的氢氧化物与NaOH溶液反应的化学方程式:
(4)元素①和④的单质化合形成的化合物能与水反应生成氢气,向反应后的溶液中滴入酚酞,溶液变红,反应的化学方程式为
(5)元素④和⑥相比,金属性较强的是
A.在化合物中④的化合价比⑥的低 B.④的单质能与冷水剧烈反应而⑥的单质不能
C.④的最高价氧化物对应水化物的碱性比⑥强 D.④单质的熔点比⑥单质的低
(6)⑧号元素有多种化合物,次磷酸(H3PO2)和次磷酸钠(NaH2PO2)常为化工生产的还原剂。
I.已知H3PO2是一种一元弱酸,向Ba(H2PO2)2溶液中加入H2SO4制备H3PO2,写出该反应的离子方程式
Ⅱ.NaH2PO2可在酸性条件下与Ni2+作用进行“化学镀镍”(如在木材表面生成一层Ni-P合金),反应中磷元素化合价发生的变化是
a.升高 b.降低 c.既升高又降低
您最近一年使用:0次
解题方法
2 . 锂是最轻的活泼金属,其单质及其化合物有广泛的用途。回答下列问题:
(1)在元素周期表中,与
 的化学性质最相似的邻族元素是
的化学性质最相似的邻族元素是___________ ,该元素基态原子中,占据最高能级电子的电子云轮廓图形状为___________ 。
(2)LiH是一种储氢材料。
(i)Li与H中第一电离能较小的元素是___________ 。
(ii)离子半径:Li+___________ H-(填“>”“=”或“<”)。
(3)已知金属锂晶体为FCC(面心立方晶格),面心立方紧密堆积结构示意图如下:
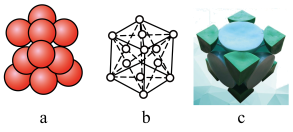
(i)晶胞中锂的配位数为___________ 。
(ii)若锂原子的半径为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则锂晶体密度为
,则锂晶体密度为___________  (列出含有
(列出含有 、
、 的计算式即可)。
的计算式即可)。
(1)在元素周期表中,与
 的化学性质最相似的邻族元素是
的化学性质最相似的邻族元素是(2)LiH是一种储氢材料。
(i)Li与H中第一电离能较小的元素是
(ii)离子半径:Li+
(3)已知金属锂晶体为FCC(面心立方晶格),面心立方紧密堆积结构示意图如下:

(i)晶胞中锂的配位数为
(ii)若锂原子的半径为
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则锂晶体密度为
,则锂晶体密度为 (列出含有
(列出含有 、
、 的计算式即可)。
的计算式即可)。
您最近一年使用:0次
2023-10-28更新
|
93次组卷
|
2卷引用:山西省大同市2023-2024学年高三上学期10月月考化学试题
名校
3 . 下表为元素周期表的一部分,请根据所学知识回答下列问题:

(1)写出J在周期表中的位置___________ 。
(2)B、D、E的简单离子半径由大到小的顺序是___________ (填离子符号)。
(3)上述元素的原子中,写出未成对电子数最多的元素基态原子的核外电子排布式:___________ 。
(4)上述7种元素中金属性最强的元素与B可形成原子个数比为1:1的化合物甲,则甲的电子式为___________ 。
(5)判断B和D的非金属性强弱,并从结构角度说明原因:___________ 。

(1)写出J在周期表中的位置
(2)B、D、E的简单离子半径由大到小的顺序是
(3)上述元素的原子中,写出未成对电子数最多的元素基态原子的核外电子排布式:
(4)上述7种元素中金属性最强的元素与B可形成原子个数比为1:1的化合物甲,则甲的电子式为
(5)判断B和D的非金属性强弱,并从结构角度说明原因:
您最近一年使用:0次
4 . Ⅰ.中国学者姜雪峰、雷晓光入选国际纯粹与应用化学联合会(IUPAC)发起的“化学家元素周期表”的征集提名,分别成为“S”、“N”元素的代言人。硒与硫最外层电子数相同,已知硒的原子结构示意图如图所示 ,试回答下列问题:
,试回答下列问题:
(1)硒在元素周期表中的位置为___________ 。
(2)结合元素周期律,比较并解释硒与硫元素的非金属性强弱:___________ 。
(3)下列说法正确的是___________ (填字母字号)。
a.热稳定性: b.
b.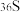 与
与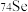 的中子数之和为60
的中子数之和为60
c.酸性: d.还原性:
d.还原性: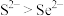
(4)试比较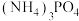 中各元素的原子半径大小
中各元素的原子半径大小___________ (用元素符号由大到小表示)。
Ⅱ.以金红石(主要成分为 )为原料,,制取Ti的工艺流程如图所示:
)为原料,,制取Ti的工艺流程如图所示:

(5)①Ⅰ在高温条件下进行,产物中有一种可燃性无色气体。Ⅰ中反应的化学方程式为___________ 。
②Ⅱ中钛的提取率在不同温度下随时间变化的曲线如图所示,则反应适宜的温度为___________ ℃。

③Ⅱ中氩气的作用是___________ 。
④海绵钛除杂时得到的 可以循环使用,在上述工艺流程中可循环使用的物质还有
可以循环使用,在上述工艺流程中可循环使用的物质还有___________ (填化学式)。
 ,试回答下列问题:
,试回答下列问题:(1)硒在元素周期表中的位置为
(2)结合元素周期律,比较并解释硒与硫元素的非金属性强弱:
(3)下列说法正确的是
a.热稳定性:
 b.
b.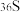 与
与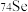 的中子数之和为60
的中子数之和为60c.酸性:
 d.还原性:
d.还原性: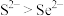
(4)试比较
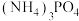 中各元素的原子半径大小
中各元素的原子半径大小Ⅱ.以金红石(主要成分为
 )为原料,,制取Ti的工艺流程如图所示:
)为原料,,制取Ti的工艺流程如图所示:
(5)①Ⅰ在高温条件下进行,产物中有一种可燃性无色气体。Ⅰ中反应的化学方程式为
②Ⅱ中钛的提取率在不同温度下随时间变化的曲线如图所示,则反应适宜的温度为

③Ⅱ中氩气的作用是
④海绵钛除杂时得到的
 可以循环使用,在上述工艺流程中可循环使用的物质还有
可以循环使用,在上述工艺流程中可循环使用的物质还有
您最近一年使用:0次
名校
5 . 某种化合物是工业洗涤剂的中间体,其结构如图所示。其中X、Y、Z、Q、W为原子序数依次增大的五种短周期元素,Q最外层电子数与Y核外电子总数相同,X的原子半径是元素周期表中最小的。回答下列问题:

(1)写出Q元素在周期表中的位置:
________ ,Z单质的电子式:
________ 。
(2)Y、Z、Q三种元素所形成的最简单气态氢化物中,稳定性最强的是
________ (填化学式);X、Y、Z、Q四种元素组成的化合物中,既含离子键又含共价键的是
________ (填化学式)。
(3)利用如图装置可比较Y、Z两元素得电子能力,b中发生反应的化学方程式为
________ 。

(4)碲(52Te)的某化合物是常用的VCR光盘记录材料之一,可在激光照射下记录、储存信号。已知碲与Q同主族,则下列关于碲及其化合物的说法正确的是
________ (填字母)。

(1)写出Q元素在周期表中的位置:
(2)Y、Z、Q三种元素所形成的最简单气态氢化物中,稳定性最强的是
(3)利用如图装置可比较Y、Z两元素得电子能力,b中发生反应的化学方程式为

(4)碲(52Te)的某化合物是常用的VCR光盘记录材料之一,可在激光照射下记录、储存信号。已知碲与Q同主族,则下列关于碲及其化合物的说法正确的是
| A.单质碲在常温下是固体 |
| B.H2Te比H2O稳定 |
| C.H2TeO4的酸性比HIO4弱 |
| D.Cl2通入H2Te溶液中不发生反应 |
您最近一年使用:0次
解题方法
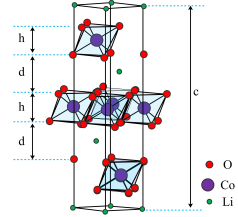
6 . 钴酸锂(LiCoO2)是常见的锂离子电池正极材料,其晶胞结构示意图如图。晶体中O围绕Co形成八面体,八面体共棱形成带负电的层状空间结构,与Li+层交替排列。在充放电过程中,Li+在层间脱出或嵌入。
(1)下列Li原子电子排布图表示的状态中,能量最低的是______ 。
(2)Li+与H-具有相同的电子构型,离子半径r(Li+)小于r(H-)的主要原因是______ 。
(3)观察该晶胞图示,其中Li处于晶胞顶点或晶胞内部,Co处于晶胞内部或晶胞侧棱上,而O的位置不易观察。结合钴酸锂(LiCoO2)化学式,可推断该晶胞中O的个数为______ 。
(4)晶胞底面为菱形,晶胞高度为cnm,Co和O组成八面体层高度为hnm,计算两层间的距离d=______ nm。(列出计算式)
(5)Li+在______ (填“充电”或“放电”)过程中会从八面体层间脱出。该过程会导致晶胞高度c变大,解释原因:______ 。

(1)下列Li原子电子排布图表示的状态中,能量最低的是
A.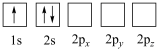 | B.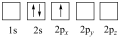 |
C.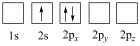 | D. |
(2)Li+与H-具有相同的电子构型,离子半径r(Li+)小于r(H-)的主要原因是
(3)观察该晶胞图示,其中Li处于晶胞顶点或晶胞内部,Co处于晶胞内部或晶胞侧棱上,而O的位置不易观察。结合钴酸锂(LiCoO2)化学式,可推断该晶胞中O的个数为
(4)晶胞底面为菱形,晶胞高度为cnm,Co和O组成八面体层高度为hnm,计算两层间的距离d=
(5)Li+在
您最近一年使用:0次
名校
解题方法
7 . 一种新型硫酸盐功能电解液由 和
和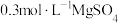 混合组成,电化学测试表明该电解液构建的
混合组成,电化学测试表明该电解液构建的 、
、 电池可以稳定循环500次以上。
电池可以稳定循环500次以上。
(1) 中三种原子的半径由小到大的顺序是
中三种原子的半径由小到大的顺序是_____ (用元素符号表示),其中电负性最大的元素是_____ (填名称)。
(2)第一电离能 的原因是
的原因是_____ 。
(3) 中,基态
中,基态 核外电子的空间运动状态有
核外电子的空间运动状态有_____ 种, 中
中 键和
键和 键的数目之比为
键的数目之比为_____ 。
(4) 中磷原子的杂化类型是
中磷原子的杂化类型是_____ 。
(5)N、O两种元素形成的简单氢化物的键角:
_____  (填“>”“<”或“=”),其原因是
(填“>”“<”或“=”),其原因是_____ 。
(6) 的立方晶胞结构如图所示。已知晶胞的边长为npm,设
的立方晶胞结构如图所示。已知晶胞的边长为npm,设 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。
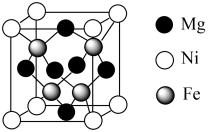
①
_____ 。
②该晶体密度是_____  (用含n、
(用含n、 的代数式表示)。
的代数式表示)。
 和
和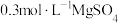 混合组成,电化学测试表明该电解液构建的
混合组成,电化学测试表明该电解液构建的 、
、 电池可以稳定循环500次以上。
电池可以稳定循环500次以上。(1)
 中三种原子的半径由小到大的顺序是
中三种原子的半径由小到大的顺序是(2)第一电离能
 的原因是
的原因是(3)
 中,基态
中,基态 核外电子的空间运动状态有
核外电子的空间运动状态有 中
中 键和
键和 键的数目之比为
键的数目之比为(4)
 中磷原子的杂化类型是
中磷原子的杂化类型是(5)N、O两种元素形成的简单氢化物的键角:

 (填“>”“<”或“=”),其原因是
(填“>”“<”或“=”),其原因是(6)
 的立方晶胞结构如图所示。已知晶胞的边长为npm,设
的立方晶胞结构如图所示。已知晶胞的边长为npm,设 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。
①

②该晶体密度是
 (用含n、
(用含n、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
2023-09-21更新
|
111次组卷
|
2卷引用:四川省绵阳南山中学2023-2024学年高三上学期第二次综合演练理综化学试题
8 . X、Y,Z、W、M是原子序数依次增大的前四周期主族元素,已知X元素是农作物三大营养元素之一,Y、Z简单离子的核外电子运动状态数量相同,且二者之间能形成两种常见离子化合物;基态W、M原子中能量最高的电子位于N能层上,且二者可形成 的化合物,该化合物在气态时以
的化合物,该化合物在气态时以 的形式存在。
的形式存在。
(1)X、Y、Z简单离子的半径由大到小的顺序为___________ (用离子符号表示),Y、Z两元素形成的含有 键的化合物的电子式为
键的化合物的电子式为___________ 。
(2)已知W的单质既能与强酸反应,又能与强碱反应,写出其单质与NaOH溶液反应的离子方程式:___________ ; 中存在配位键,写出其结构式并用“→”标出配位键:
中存在配位键,写出其结构式并用“→”标出配位键:___________ 。
(3)X的一种氢化物 因能结合水电离出的
因能结合水电离出的 而表现出碱性,常温下,其电离常数分别为
而表现出碱性,常温下,其电离常数分别为 ,
, ,则
,则 发生一级电离的方程式为
发生一级电离的方程式为___________ ,当 4溶液中
4溶液中 时,该溶液的
时,该溶液的
___________ 。
 的化合物,该化合物在气态时以
的化合物,该化合物在气态时以 的形式存在。
的形式存在。(1)X、Y、Z简单离子的半径由大到小的顺序为
 键的化合物的电子式为
键的化合物的电子式为(2)已知W的单质既能与强酸反应,又能与强碱反应,写出其单质与NaOH溶液反应的离子方程式:
 中存在配位键,写出其结构式并用“→”标出配位键:
中存在配位键,写出其结构式并用“→”标出配位键:(3)X的一种氢化物
 因能结合水电离出的
因能结合水电离出的 而表现出碱性,常温下,其电离常数分别为
而表现出碱性,常温下,其电离常数分别为 ,
, ,则
,则 发生一级电离的方程式为
发生一级电离的方程式为 4溶液中
4溶液中 时,该溶液的
时,该溶液的
您最近一年使用:0次
名校
解题方法
9 . 元素周期表是学习物质结构和性质的重要工具,下图是元素周期表的一部分,表中所列字母A、D、F、G、Q、M、R分别代表一种元素。请依据这7种元素回答下列问题:

(1)以上7种元素中原子半径最大的元素是___________ 。(填元素符号)
(2)Q的原子结构示意图为___________ 。
(3)A和F能组成原子个数比为1:1的化合物,该化合物的电子式为___________ ;D和F能组成原子个数比为1:2的化合物,该化合物的结构式为___________ 。
(4)A、G、F三种元素组成的化合物中有哪些化学键___________ 。
(5)为了验证D和M二种元素非金属性的强弱,设计下图装置进行实验

请回答:
①仪器A的名称是___________ 。
②现有试剂:稀硫酸、碳酸钠溶液、碳酸钙、硫酸钠溶液、澄清石灰水。从所给试剂中选择合适的试剂,用如图装置证明D和M两种元素非金属性:M>D,A中装试剂___________ ,C中的实验现象___________ 。
(6)F、M的简单氢化物的沸点由高到低的顺序为___________ (用化学式表示),原因是___________ 。

(1)以上7种元素中原子半径最大的元素是
(2)Q的原子结构示意图为
(3)A和F能组成原子个数比为1:1的化合物,该化合物的电子式为
(4)A、G、F三种元素组成的化合物中有哪些化学键
(5)为了验证D和M二种元素非金属性的强弱,设计下图装置进行实验

请回答:
①仪器A的名称是
②现有试剂:稀硫酸、碳酸钠溶液、碳酸钙、硫酸钠溶液、澄清石灰水。从所给试剂中选择合适的试剂,用如图装置证明D和M两种元素非金属性:M>D,A中装试剂
(6)F、M的简单氢化物的沸点由高到低的顺序为
您最近一年使用:0次
2023高三·全国·专题练习
10 . 氨硼烷(NH3BH3)含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答下列问题:
(1)H、B、N中,原子半径最大的是_______ 。根据对角线规则,B的一些化学性质与元素_______ 的相似。
(2)NH3BH3分子中,N—B化学键称为_______ 键,其电子对由_______ 提供。氨硼烷在催化剂作用下水解释放氢气:3NH3BH3+6H2O=3NH +B3O
+B3O +9H2。B3O
+9H2。B3O 的结构为
的结构为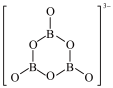 。在该反应中,B原子的杂化轨道类型由
。在该反应中,B原子的杂化轨道类型由_______ 变为_______ 。
(3)NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),电负性大小顺序是_______ 。
(4)研究发现,氨硼烷在低温高压条件下为正交晶系结构,晶胞参数分别为a pm、b pm、c pm,α=β=γ=90°。氨硼烷的2×2×2超晶胞结构如图所示。
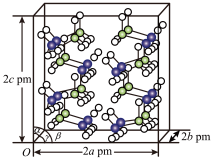
氨硼烷晶体的密度ρ=_______ g·cm-3(列出计算式,设NA为阿伏加德罗常数的值)。
(1)H、B、N中,原子半径最大的是
(2)NH3BH3分子中,N—B化学键称为
 +B3O
+B3O +9H2。B3O
+9H2。B3O 的结构为
的结构为 。在该反应中,B原子的杂化轨道类型由
。在该反应中,B原子的杂化轨道类型由(3)NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),电负性大小顺序是
(4)研究发现,氨硼烷在低温高压条件下为正交晶系结构,晶胞参数分别为a pm、b pm、c pm,α=β=γ=90°。氨硼烷的2×2×2超晶胞结构如图所示。

氨硼烷晶体的密度ρ=
您最近一年使用:0次



