名校
1 . 实验室模拟“镁法工业烟气脱硫”并制备MgSO4∙H2O,其实验过程可表示如下:

(1)在搅拌下向氧化镁浆料[主要成分为Mg(OH)2]中匀速缓慢通入SO2气体,生成 。
。
①“吸收”过程中,发生的主要反应的化学方程式为___________ ;
②64gSO2在标准状况下的体积约为___________ L;
③NaOH溶液也可以用于捕集SO2,配制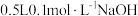 溶液,需NaOH
溶液,需NaOH___________ g;
(2)在催化剂作用下MgSO3被O2氧化为MgSO4。“氧化”过程若转移1mole⁻,则消耗标准状况下O2的体积约为___________ L;
(3)制取MgSO4∙H2O晶体。将氧化后溶液蒸发浓缩、降温至室温结晶,___________ (填写操作步骤),洗涤,干燥,制得MgSO4∙H2O晶体;
(4)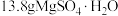 中所含Mg2+的物质的量为
中所含Mg2+的物质的量为___________ mol。

(1)在搅拌下向氧化镁浆料[主要成分为Mg(OH)2]中匀速缓慢通入SO2气体,生成
 。
。①“吸收”过程中,发生的主要反应的化学方程式为
②64gSO2在标准状况下的体积约为
③NaOH溶液也可以用于捕集SO2,配制
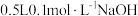 溶液,需NaOH
溶液,需NaOH(2)在催化剂作用下MgSO3被O2氧化为MgSO4。“氧化”过程若转移1mole⁻,则消耗标准状况下O2的体积约为
(3)制取MgSO4∙H2O晶体。将氧化后溶液蒸发浓缩、降温至室温结晶,
(4)
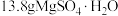 中所含Mg2+的物质的量为
中所含Mg2+的物质的量为
您最近半年使用:0次
2023-11-09更新
|
167次组卷
|
2卷引用:江苏省扬州市江都区2023-2024学年高一上学期期中考试化学试题
名校
解题方法
2 .  是一种广谱型的消毒剂,根据世界环保联盟的要求,
是一种广谱型的消毒剂,根据世界环保联盟的要求, 将逐渐取代
将逐渐取代 成为生产自来水的消毒剂。工业上
成为生产自来水的消毒剂。工业上 常用
常用 和
和 溶液混合并加
溶液混合并加 酸化后反应制得,在以上反应中氧化剂与还原剂的个数之比为
酸化后反应制得,在以上反应中氧化剂与还原剂的个数之比为
 是一种广谱型的消毒剂,根据世界环保联盟的要求,
是一种广谱型的消毒剂,根据世界环保联盟的要求, 将逐渐取代
将逐渐取代 成为生产自来水的消毒剂。工业上
成为生产自来水的消毒剂。工业上 常用
常用 和
和 溶液混合并加
溶液混合并加 酸化后反应制得,在以上反应中氧化剂与还原剂的个数之比为
酸化后反应制得,在以上反应中氧化剂与还原剂的个数之比为A. | B. | C. | D. |
您最近半年使用:0次
2023-11-05更新
|
83次组卷
|
2卷引用:黑龙江省克东县“五校联谊”2023-2024学年高一上学期期中考试化学试题
名校
解题方法
3 . 设计实验探究NO的氧化性。
实验Ⅰ:用排水法收集一瓶NO,将其倒扣在盛有碱性 溶液的水槽中,振荡,观察到集气瓶中液面上升。
溶液的水槽中,振荡,观察到集气瓶中液面上升。
资料:ⅰ.NO与碱性 溶液会发生氧化还原反应,
溶液会发生氧化还原反应, 被还原为
被还原为 。
。
ⅱ. 与
与 反应生成黄色沉淀。
反应生成黄色沉淀。
某同学认为,需通过进一步实验验证NO的氧化性,补充以下实验:
实验Ⅱ:取饱和 溶液,加入少量冰醋酸,再滴加5滴
溶液,加入少量冰醋酸,再滴加5滴 的
的 溶液,无明显变化。
溶液,无明显变化。
实验Ⅲ:
(1)取少量实验Ⅰ反应后集气瓶中的溶液,加入少量冰醋酸,再滴加5滴 的
的 溶液,
溶液,___________ (填实验现象)。
上述实验证明NO有氧化性。
(2)实验Ⅱ的目的是___________
(3)写出NO与碱性 溶液反应的离子方程式
溶液反应的离子方程式___________
(4)一个氧化还原反应可以看成“氧化”和“还原”两个半反应,试用此角度分析NO与碱性 溶液的反应。若还原反应为:
溶液的反应。若还原反应为: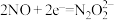 ,则氧化反应为:
,则氧化反应为:___________ 。
(5)某同学结合所学知识设计处理工业废气中 和NO的实验方案,达到消除污染,保护环境的目的。
和NO的实验方案,达到消除污染,保护环境的目的。
①先用饱和纯碱溶液吸收废气中的 ,生成
,生成 ,写出该反应的离子方程式
,写出该反应的离子方程式___________
②再向生成的溶液中加入一定量___________ ,以此溶液来吸收NO气体。
实验Ⅰ:用排水法收集一瓶NO,将其倒扣在盛有碱性
 溶液的水槽中,振荡,观察到集气瓶中液面上升。
溶液的水槽中,振荡,观察到集气瓶中液面上升。资料:ⅰ.NO与碱性
 溶液会发生氧化还原反应,
溶液会发生氧化还原反应, 被还原为
被还原为 。
。ⅱ.
 与
与 反应生成黄色沉淀。
反应生成黄色沉淀。某同学认为,需通过进一步实验验证NO的氧化性,补充以下实验:
实验Ⅱ:取饱和
 溶液,加入少量冰醋酸,再滴加5滴
溶液,加入少量冰醋酸,再滴加5滴 的
的 溶液,无明显变化。
溶液,无明显变化。实验Ⅲ:
(1)取少量实验Ⅰ反应后集气瓶中的溶液,加入少量冰醋酸,再滴加5滴
 的
的 溶液,
溶液,上述实验证明NO有氧化性。
(2)实验Ⅱ的目的是
(3)写出NO与碱性
 溶液反应的离子方程式
溶液反应的离子方程式(4)一个氧化还原反应可以看成“氧化”和“还原”两个半反应,试用此角度分析NO与碱性
 溶液的反应。若还原反应为:
溶液的反应。若还原反应为: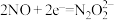 ,则氧化反应为:
,则氧化反应为:(5)某同学结合所学知识设计处理工业废气中
 和NO的实验方案,达到消除污染,保护环境的目的。
和NO的实验方案,达到消除污染,保护环境的目的。①先用饱和纯碱溶液吸收废气中的
 ,生成
,生成 ,写出该反应的离子方程式
,写出该反应的离子方程式②再向生成的溶液中加入一定量
您最近半年使用:0次
名校
解题方法
4 . 元素周期表反映元素之间的内在联系,是研究物质性质的重要工具。如表是元素周期表的一部分,请回答下列问题:
(1)元素④、⑤、⑧的简单离子半径由大到小的排序为___________ (填离子符号)。
(2)①和③两种元素组成一种盐X为六核化合物,X含有___________ 键,X的电子式___________ 。
(3)⑥的氧化物和⑧的最高价氧化物对应的水化物反应的离子方程式为___________ 。
(4)由①④⑤⑦四种元素共同组成两种酸式盐,写出两种酸式盐在溶液中发生反应的离子方程式___________ 。
| 周期 | IA | 0 | |||||||
| 1 | ① | IIA | … | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | ||||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | |||||
(2)①和③两种元素组成一种盐X为六核化合物,X含有
(3)⑥的氧化物和⑧的最高价氧化物对应的水化物反应的离子方程式为
(4)由①④⑤⑦四种元素共同组成两种酸式盐,写出两种酸式盐在溶液中发生反应的离子方程式
您最近半年使用:0次
解题方法
5 . 钠及其化合物在生产、生活中有着重要的用途,根据所学知识,回答下列问题。
Ⅰ.某汽车安全气囊的产气药剂主要含有 、
、 、
、 、
、 等物质。当汽车发生碰撞时,
等物质。当汽车发生碰撞时, 迅速分解产生
迅速分解产生 和Na,同时放出大量的热,
和Na,同时放出大量的热, 使气囊迅速膨胀,从而起到保护作用。
使气囊迅速膨胀,从而起到保护作用。
(1) 是冷却剂,吸收产气过程中释放的热量而分解,其分解的化学方程式为
是冷却剂,吸收产气过程中释放的热量而分解,其分解的化学方程式为___________ 。
Ⅱ.某实验小组设计如下实验方案测定 与
与 混合物中各组分的含量。
混合物中各组分的含量。
(2)方案一:称取30g样品,置于坩埚中加热至恒重,冷却、称量,剩余固体质量为31.6g,计算。
①实验中加热至恒重的目的是___________ 。
②样品中 的质量分数为
的质量分数为___________ 。
(3)方案二:用如图所示装置(铁架台、铁夹等仪器未在图中画出)进行实验。
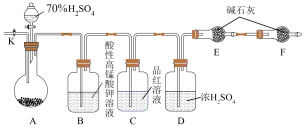
①装置C的作用是___________ ;装置F的作用是___________ 。
②实验过程中,当装置A内的固体反应完全后,需打开活塞K,向A中通入大量的氮气。这样做的目的是___________ 。
(4)方案三:称取一定量样品,置于小烧杯中,加适量水溶解,向小烧杯中加入足量 溶液。过滤、洗涤、干燥沉淀,称量固体质量。实验中判断沉淀洗涤干净的方法是
溶液。过滤、洗涤、干燥沉淀,称量固体质量。实验中判断沉淀洗涤干净的方法是___________ 。
Ⅰ.某汽车安全气囊的产气药剂主要含有
 、
、 、
、 、
、 等物质。当汽车发生碰撞时,
等物质。当汽车发生碰撞时, 迅速分解产生
迅速分解产生 和Na,同时放出大量的热,
和Na,同时放出大量的热, 使气囊迅速膨胀,从而起到保护作用。
使气囊迅速膨胀,从而起到保护作用。(1)
 是冷却剂,吸收产气过程中释放的热量而分解,其分解的化学方程式为
是冷却剂,吸收产气过程中释放的热量而分解,其分解的化学方程式为Ⅱ.某实验小组设计如下实验方案测定
 与
与 混合物中各组分的含量。
混合物中各组分的含量。(2)方案一:称取30g样品,置于坩埚中加热至恒重,冷却、称量,剩余固体质量为31.6g,计算。
①实验中加热至恒重的目的是
②样品中
 的质量分数为
的质量分数为(3)方案二:用如图所示装置(铁架台、铁夹等仪器未在图中画出)进行实验。

①装置C的作用是
②实验过程中,当装置A内的固体反应完全后,需打开活塞K,向A中通入大量的氮气。这样做的目的是
(4)方案三:称取一定量样品,置于小烧杯中,加适量水溶解,向小烧杯中加入足量
 溶液。过滤、洗涤、干燥沉淀,称量固体质量。实验中判断沉淀洗涤干净的方法是
溶液。过滤、洗涤、干燥沉淀,称量固体质量。实验中判断沉淀洗涤干净的方法是
您最近半年使用:0次
6 . 化学实验小组在实验室中利用某化工厂排出的废渣[主要成分为BaCO3、Ba(FeO2)2、BaSO3]制备Ba(NO3)2晶体的流程如图所示。
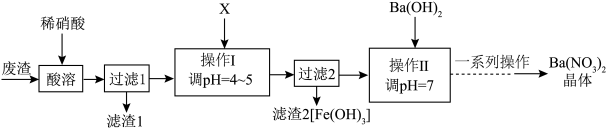
已知:Ba(NO3)2的溶解度受温度影响较大。下列说法错误的是

已知:Ba(NO3)2的溶解度受温度影响较大。下列说法错误的是
| A.酸溶时,Ba(FeO2)2、BaSO3都能与稀硝酸发生氧化还原反应 |
| B.滤渣1的主要成分是BaSO4 |
| C.试剂X可选择BaCO3 |
| D.流程中“一系列操作”有蒸发浓缩、冷却结晶、过滤、洗涤、干燥 |
您最近半年使用:0次
7 . 工业上以 和纯碱为原料制备无水
和纯碱为原料制备无水 的主要流程如图,下列说法错误的是
的主要流程如图,下列说法错误的是

已知:①电离出 的能力:
的能力: ,②
,② 和
和 受热均易分解
受热均易分解
 和纯碱为原料制备无水
和纯碱为原料制备无水 的主要流程如图,下列说法错误的是
的主要流程如图,下列说法错误的是
已知:①电离出
 的能力:
的能力: ,②
,② 和
和 受热均易分解
受热均易分解| A.“吸收”过程中有气体生成 | B.结晶后母液中含有 |
| C.气流干燥湿料时温度不宜过高 | D.“中和”后溶液中含 和 和 |
您最近半年使用:0次
解题方法
8 . 下列离子方程式的书写正确的是
A.向Na2SO3溶液中加入稀HNO3: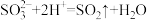 |
B.向水垢中滴加足量醋酸: |
C.用Na2SO3溶液吸收少量Cl2: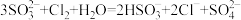 |
D.少量Fe与足量稀HNO3: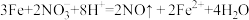 |
您最近半年使用:0次
名校
9 . W、X、Y、Z为原子序数依次增大的短周期主族元素,其中W的核电荷数等于Y的最外层电子数,Z的电子总数是X的2倍,四种元素可形成离子化合物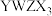 。下列说法错误的是
。下列说法错误的是
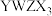 。下列说法错误的是
。下列说法错误的是A.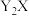 和 和 中阴阳离子个数比相同 中阴阳离子个数比相同 |
B.水溶液中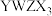 与 与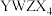 之间能发生反应 之间能发生反应 |
C. 与 与 可以发生氧化还原反应生成 可以发生氧化还原反应生成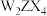 |
| D.X和Z的最简单氢化物的稳定性X<Z |
您最近半年使用:0次
2023-10-31更新
|
129次组卷
|
2卷引用:河北省保定市2023-2024学年高三上学期10月期中考试化学试题
10 . 由实验操作和现象,可得出相应正确结论的是
| 实验操作 | 现象 | 结论 | |
| A | 向某钠盐粉末上滴加浓盐酸,将产生的气体通入品红溶液 | 品红溶液褪色 | 该钠盐只能为 、 、 或 或 |
| B | 向蔗糖溶液中滴加稀硫酸,水浴加热,加入新制的 悬浊液 悬浊液 | 无砖红色沉淀 | 蔗糖未发生水解 |
| C | 铝粉与氧化铁发生铝热反应,冷却后将固体溶于盐酸,向所得溶液滴加 溶液 溶液 | 溶液颜色无明显变化 | 氧化铁已经完全被铝粉还原 |
| D | 石蜡油加强热,将产生的气体通入 的 的 溶液 溶液 | 溶液由橙红色变为无色 | 气体中含不饱和烃 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次



