名校
1 . 石墨烯是从石墨材料中剥离出来,由碳原子组成的只有一层原子厚度的二维晶体,其部分性能优于传统的硅材料,具有广泛的应用前景。
(1)石墨烯加氢完全制得的石墨烷可用 表示。它的结构相当于在不破坏石墨烯独特的六边形晶格结构和单原子厚度的情况下,给每个碳原子上都增加了一个氢原子。下列有关石墨烷的叙述正确的是
表示。它的结构相当于在不破坏石墨烯独特的六边形晶格结构和单原子厚度的情况下,给每个碳原子上都增加了一个氢原子。下列有关石墨烷的叙述正确的是_______ (填字母)。
a.石墨烷属于烷烃 b.石墨烷难溶于水
c.石墨烷中所有碳原子共平面 d.石墨烷可以发生加成反应
(2)石墨晶体由层状石墨“分子”按ABAB…方式堆积而成,如图所示,层与层之间靠_______ 维系。图中用虚线标出了石墨的一个六方晶胞。1个六方石墨晶胞中碳原子的个数为_______ ,D处碳原子的分数坐标为 ,则E处碳原子的分数坐标为
,则E处碳原子的分数坐标为_______ (以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,各原子的位置称作原子的分数坐标)。_______ ,晶体中Si原子与 键的数目之比为
键的数目之比为_______ 。
(4) 与
与 结构相似,分子的空间结构为
结构相似,分子的空间结构为________ ,但性质不同:前者不易与水反应,但后者与水剧烈反应,生成两种酸和一种气体单质,写出该反应的化学方程式:_______ 。
(1)石墨烯加氢完全制得的石墨烷可用
 表示。它的结构相当于在不破坏石墨烯独特的六边形晶格结构和单原子厚度的情况下,给每个碳原子上都增加了一个氢原子。下列有关石墨烷的叙述正确的是
表示。它的结构相当于在不破坏石墨烯独特的六边形晶格结构和单原子厚度的情况下,给每个碳原子上都增加了一个氢原子。下列有关石墨烷的叙述正确的是a.石墨烷属于烷烃 b.石墨烷难溶于水
c.石墨烷中所有碳原子共平面 d.石墨烷可以发生加成反应
(2)石墨晶体由层状石墨“分子”按ABAB…方式堆积而成,如图所示,层与层之间靠
 ,则E处碳原子的分数坐标为
,则E处碳原子的分数坐标为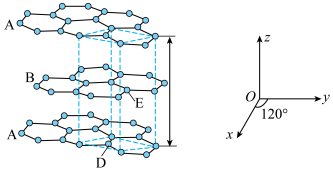
 键的数目之比为
键的数目之比为(4)
 与
与 结构相似,分子的空间结构为
结构相似,分子的空间结构为
您最近一年使用:0次
名校
解题方法
2 . 前四周期元素A、B、C、D、E的原子序数依次增大,A元素原子的核外电子只有一种运动状态;基态B原子s能级的电子总数比p能级的多1;基态C原子和基态E原子中成对电子数均是未成对电子数的3倍;D形成简单离子的半径在同周期元素形成的简单离子中最小。回答下列问题:
(1)E的元素名称为___________ 。
(2)元素A、B、C中,电负性最大的是___________ (填元素符号 ) 。
(3)BC 中B原子轨道的杂化类型为
中B原子轨道的杂化类型为___________ ,BC 的空间结构为
的空间结构为___________ 。
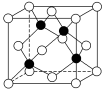
(4)化合物DB是人工合成的半导体材料,它的晶胞结构与金刚石(晶胞结构如图所示)相似。若DB的晶胞参数为a pm,则晶体的密度为___________ g·cm-3(用NA表示阿伏加德罗常数的值)。
(1)E的元素名称为
(2)元素A、B、C中,电负性最大的是
(3)BC
 中B原子轨道的杂化类型为
中B原子轨道的杂化类型为 的空间结构为
的空间结构为(4)化合物DB是人工合成的半导体材料,它的晶胞结构与金刚石(晶胞结构如图所示)相似。若DB的晶胞参数为a pm,则晶体的密度为
您最近一年使用:0次
名校
解题方法
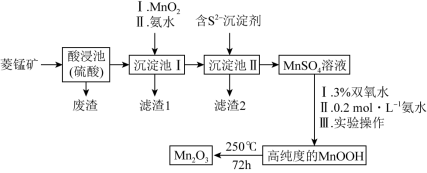
3 . Mn2O3是一种重要的化工产品。以菱锰矿(主要成分为MnCO3,还含有少量Fe3O4、FeO、CoO、Al2O3)为原料制备Mn2O3的工艺流程如图:
已知:氢氧化氧锰(MnOOH)难溶于水和碱性溶液。
(1)MnOOH中Mn的化合价为_______ 价。
(2)向“沉淀池I”中加入MnO2,MnO2的作用是_______ ,在“沉淀池I”中,滴加氨水调节溶液的pH,使溶液中铝、铁元素完全沉淀,则理论上pH的最小值为_______ (当溶液中某离子浓度c≤1.0×10-5mol•L-1时,可认为该离子沉淀完全)。
(3)MnSO4转化为MnOOH的离子方程式为_______ 。
(4)MnSO4转化为MnOOH中“III实验操作”包含过滤、洗涤、干燥,检验MnOOH是否洗涤干净,具体操作为_______ 。
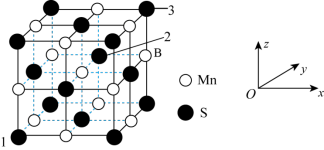
(5)MnS晶胞与NaCl晶胞属于同种类型,MnS晶胞结构如图所示。_______ 。
②已知:MnS晶体的边长为bnm,NA为阿伏加德罗常数的值,则MnS晶胞密度为_______ g•cm-3(列出计算式即可)。
| 物质 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Mn(OH)2 | Co(OH)2 |
| Ksp | 1×10-16.3 | 1×10-38.6 | 1×10-32.3 | 1×10-12.7 | 1.09×10-15 |
(1)MnOOH中Mn的化合价为
(2)向“沉淀池I”中加入MnO2,MnO2的作用是
(3)MnSO4转化为MnOOH的离子方程式为
(4)MnSO4转化为MnOOH中“III实验操作”包含过滤、洗涤、干燥,检验MnOOH是否洗涤干净,具体操作为
(5)MnS晶胞与NaCl晶胞属于同种类型,MnS晶胞结构如图所示。
②已知:MnS晶体的边长为bnm,NA为阿伏加德罗常数的值,则MnS晶胞密度为
您最近一年使用:0次
名校
4 . I.已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
(1)CO 的空间结构是
的空间结构是_______ 。
(2) 溶液呈
溶液呈_______ (填“酸性”“碱性”或“中性”)。
(3)物质的量浓度均为0.1mol·L−1的下列四种溶液:pH由小到大 排列的顺序是_______ 。(填序号)
①CH3COONa②Na2CO3③NaClO④NaHCO3
(4)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:_______ 。
II.为实现“双碳”目标,用二氧化碳制备甲醇可实现二氧化碳资源化利用、降低碳排放。回答下列问题:
已知:反应1:

反应2:
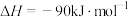
(5)则反应3: 催化加氢制取
催化加氢制取 的热化学方程式为
的热化学方程式为_______ 。
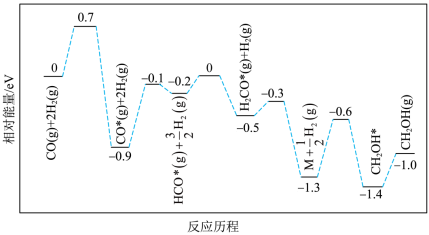
(6)反应2的反应历程如下图所示,其中吸附在催化剂表面的物种用*标注。_______ 。
III.为了探究电解池的工作原理,某研究性学习小组用下图所示的装置进行实验。实验时该小组同学发现两极均有气体产生,且Y极处溶液逐渐变成紫红色;停止实验观察到铁电极明显变细,电解液仍然澄清。查阅资料知,高铁酸根( )在溶液中呈紫红色。
)在溶液中呈紫红色。
(7)电解过程中,Y极发生的电极反应为_______ 、_______ 。
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | Ka=1.810−5 | Kal=4.310−7、Ka2=5.610−11 | Ka=3.010−8 |
 的空间结构是
的空间结构是(2)
 溶液呈
溶液呈(3)物质的量浓度均为0.1mol·L−1的下列四种溶液:pH
①CH3COONa②Na2CO3③NaClO④NaHCO3
(4)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:
II.为实现“双碳”目标,用二氧化碳制备甲醇可实现二氧化碳资源化利用、降低碳排放。回答下列问题:
已知:反应1:


反应2:

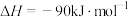
(5)则反应3:
 催化加氢制取
催化加氢制取 的热化学方程式为
的热化学方程式为(6)反应2的反应历程如下图所示,其中吸附在催化剂表面的物种用*标注。
III.为了探究电解池的工作原理,某研究性学习小组用下图所示的装置进行实验。实验时该小组同学发现两极均有气体产生,且Y极处溶液逐渐变成紫红色;停止实验观察到铁电极明显变细,电解液仍然澄清。查阅资料知,高铁酸根(
 )在溶液中呈紫红色。
)在溶液中呈紫红色。
(7)电解过程中,Y极发生的电极反应为
您最近一年使用:0次
名校
5 . 钛被称为继铁、铝之后的“第三金属”。一种制备金属钛的工艺流程如下所示:___________ 。
(2)已知TiCl4在通常情况下是无色液体,熔点为-37℃,沸点为136℃,结构与CCl4相似。试预测CCl4的沸点___________ 136℃(填“>”“<”或“=”)并阐述推测理由___________ 。
(3)纳米TiO2是一种应用广泛的催化剂,其催化作用的一个实例如下所示:___________ 。
(4)硫酸氧钛晶体中阳离子为链状聚合形式的离子,该阳离子的结构片段如图所示。该阳离子中Ti与O的原子数之比为___________ 。___________ g·cm-3(设阿伏加德罗常数的值为NA,用含a、b、NA的代数式表示)。

(2)已知TiCl4在通常情况下是无色液体,熔点为-37℃,沸点为136℃,结构与CCl4相似。试预测CCl4的沸点
(3)纳米TiO2是一种应用广泛的催化剂,其催化作用的一个实例如下所示:

(4)硫酸氧钛晶体中阳离子为链状聚合形式的离子,该阳离子的结构片段如图所示。该阳离子中Ti与O的原子数之比为


您最近一年使用:0次
2024-05-05更新
|
125次组卷
|
2卷引用:福建省福州市闽侯县第一中学2023-2024学年高二下学期3月月考化学试题
6 . 实验室用少量的溴和足量的乙醇制备1,2—二溴乙烷的装置如下图所示:有关数据列表如下:
(1)写出该实验过程中发生的主要反应的化学方程式A处___________ ,D处___________ 。
(2)在装置C中应加入___________ 。
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)判断D处反应已经结束的最简单方法是___________ (填实验现象)。装置B的作用是___________ 。
(4)若产物中有少量未反应的Br2,最好用___________ 洗涤除去。
a.水 b.亚硫酸钠溶液 c.碘化钠溶液 d.乙醇
(5)若产物中有少量副产物乙醚。可用___________ 的方法除去。
(6)反应过程中应用冷水冷却装置D,其主要目的是___________ ;但又不能过度冷却(如用冰水),其原因是___________ 。
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
密度/ | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ |  130 130 | 9 |  116 116 |

(1)写出该实验过程中发生的主要反应的化学方程式A处
(2)在装置C中应加入
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)判断D处反应已经结束的最简单方法是
(4)若产物中有少量未反应的Br2,最好用
a.水 b.亚硫酸钠溶液 c.碘化钠溶液 d.乙醇
(5)若产物中有少量副产物乙醚。可用
(6)反应过程中应用冷水冷却装置D,其主要目的是
您最近一年使用:0次
7 . 已知: 。
。
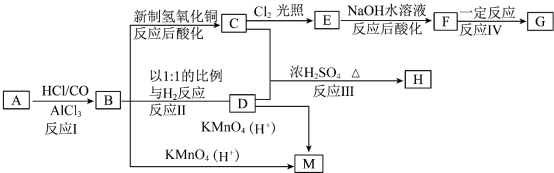
(1)结构简式:A
(2)写出反应III的化学方程式:
(3)写出D生成B的化学方程式:
您最近一年使用:0次
名校
8 . 中国第一辆火星车“祝融号”成功登陆火星。探测发现火星上存在大量橄榄石矿物(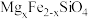 )。回答下列问题:
)。回答下列问题:
(1)橄榄石中,根据各元素电负性大小可判断铁的化合价为___________ 。
(2)已知一些物质的熔点数据如下表:
Na与Si均为第三周期元素,NaCl熔点明显高于 ,原因是
,原因是___________ 。分析同族元素的氯化物 、
、 、
、 熔点变化趋势及其原因
熔点变化趋势及其原因___________ 。 的空间结构为
的空间结构为___________ ,其中Si的轨道杂化形式为___________ 。
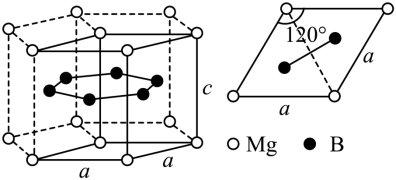
(3)一种硼镁化合物具有超导性能,晶体结构属于六方晶系,其晶体结构、晶胞沿c轴的投影图如下所示,晶胞中含有___________ 个Mg。该物质化学式为___________ ,B-B最近距离为___________ 。
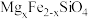 )。回答下列问题:
)。回答下列问题:(1)橄榄石中,根据各元素电负性大小可判断铁的化合价为
(2)已知一些物质的熔点数据如下表:
| 物质 | 熔点/℃ |
| NaCl | 800.7 |
 |  |
 | 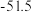 |
 |  |
 ,原因是
,原因是 、
、 、
、 熔点变化趋势及其原因
熔点变化趋势及其原因 的空间结构为
的空间结构为(3)一种硼镁化合物具有超导性能,晶体结构属于六方晶系,其晶体结构、晶胞沿c轴的投影图如下所示,晶胞中含有
您最近一年使用:0次
名校
9 . 结合物质结构与性质相关知识,回答下列问题。
(1)基态Se原子的核外电子排布式为___________ 。
(2) 分子易作为配体与
分子易作为配体与 形成[Cu(NH3)4]2+,在[Cu(NH3)4]2+结构中若用两个H2O分子代替两个
形成[Cu(NH3)4]2+,在[Cu(NH3)4]2+结构中若用两个H2O分子代替两个 分子可以得到两种不同结构的化合物,由此推测[Cu(NH3)4]2+的空间构型为
分子可以得到两种不同结构的化合物,由此推测[Cu(NH3)4]2+的空间构型为___________ 。
(3)吡啶( )在水中的溶解度远大于苯,可能原因是①吡啶和H2O均为极性分子相似相溶而苯为非极性分子;②
)在水中的溶解度远大于苯,可能原因是①吡啶和H2O均为极性分子相似相溶而苯为非极性分子;②___________ 。
(4)氮化钛晶体的晶胞结构如图所示,该晶体结构中所含N、Ti原子个数比为___________ ;N原子周围与其原子距离相等且最近的N原子个数是___________ 个。
(1)基态Se原子的核外电子排布式为
(2)
 分子易作为配体与
分子易作为配体与 形成[Cu(NH3)4]2+,在[Cu(NH3)4]2+结构中若用两个H2O分子代替两个
形成[Cu(NH3)4]2+,在[Cu(NH3)4]2+结构中若用两个H2O分子代替两个 分子可以得到两种不同结构的化合物,由此推测[Cu(NH3)4]2+的空间构型为
分子可以得到两种不同结构的化合物,由此推测[Cu(NH3)4]2+的空间构型为(3)吡啶(
 )在水中的溶解度远大于苯,可能原因是①吡啶和H2O均为极性分子相似相溶而苯为非极性分子;②
)在水中的溶解度远大于苯,可能原因是①吡啶和H2O均为极性分子相似相溶而苯为非极性分子;②(4)氮化钛晶体的晶胞结构如图所示,该晶体结构中所含N、Ti原子个数比为

您最近一年使用:0次
名校
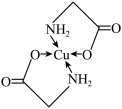
10 . 太阳能的开发利用在新能源研究中占据重要地位,单品硅太阳能电池片在加工时,一般掺杂微量的铜、铁、钴、硼、镓、硒等。其中某种重要的含铜的化合物的结构如图所示。请回答下列问题:_______ 区,最外层原子轨道呈_______ 形。
(2)基态二价铜离子的电子排布式为_______ ,已知高温下 比CuO更稳定,试从核外电子排布角度解释
比CuO更稳定,试从核外电子排布角度解释_______ 。
(3)在基态硼原子中,核外存在_______ 个运动状态不同的电子。
(4) 的价层电子排布图为
的价层电子排布图为_______ 。
(5)根据元素周期律,电负性O_______ Se(填“大于”“小于”或“等于”),N、O、Se三种元素中的第一电离能最大的为_______ 。
(2)基态二价铜离子的电子排布式为
 比CuO更稳定,试从核外电子排布角度解释
比CuO更稳定,试从核外电子排布角度解释(3)在基态硼原子中,核外存在
(4)
 的价层电子排布图为
的价层电子排布图为(5)根据元素周期律,电负性O
您最近一年使用:0次



