名校
解题方法
1 . 反应C(s)+H2O(g)=CO(g)+H2(g)在一个容积可变的密闭容器中进行,下列条件的改变能加快反应速率的是
①增加C(s)的量 ②将容器的体积缩小一半 ③保持体积不变,充入N2使体系压强增大
④保持压强不变,充入N2使容器体积变大 ⑤使用合适的催化剂
①增加C(s)的量 ②将容器的体积缩小一半 ③保持体积不变,充入N2使体系压强增大
④保持压强不变,充入N2使容器体积变大 ⑤使用合适的催化剂
| A.①③ | B.②⑤ | C.①④ | D.②④ |
您最近半年使用:0次
名校
解题方法
2 . 工业合成氨是最重要的人工固氮途径,发生反应: 。请回答:
。请回答:
(1)已知断开1mol的某化学键所需能量如表所示。若固氮反应中有2mol 生成时,
生成时,______ (填 “吸收”或“放出”)热量______ kJ。
(2)恒温恒压条件下,向密闭容器中投入等物质的量的 和
和 发生反应,下列描述能说明反应已达到化学平衡状态的是______。
发生反应,下列描述能说明反应已达到化学平衡状态的是______。
(3)利用 可消除大气污染物NO,可将反应设计为原电池提供电能,如图所示。该电池中M为原电池的
可消除大气污染物NO,可将反应设计为原电池提供电能,如图所示。该电池中M为原电池的______ 极(填“正”或“负”),其电极方程式为______ 。______ (填“a”、“b”或“c”)______
 。请回答:
。请回答:(1)已知断开1mol的某化学键所需能量如表所示。若固氮反应中有2mol
 生成时,
生成时,化学键 |
|
|
|
能量(kJ) | 436 | 391 | 946 |
(2)恒温恒压条件下,向密闭容器中投入等物质的量的
 和
和 发生反应,下列描述能说明反应已达到化学平衡状态的是______。
发生反应,下列描述能说明反应已达到化学平衡状态的是______。A.反应速率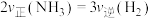 | B.混合气体的密度不再变化 |
| C.混合气体的平均摩尔质量不再变化 | D. 的体积分数不再变化 的体积分数不再变化 |
(3)利用
 可消除大气污染物NO,可将反应设计为原电池提供电能,如图所示。该电池中M为原电池的
可消除大气污染物NO,可将反应设计为原电池提供电能,如图所示。该电池中M为原电池的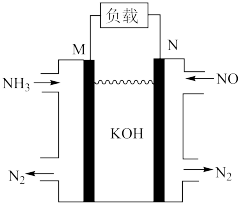


您最近半年使用:0次
3 . Ⅰ.工业上用CO生产燃料甲醇,一定条件下发生反应: 。图1表示反应中能量变化;图2表示一定温度下,在容积为2L的密闭容器中加入4molH2和一定量的CO后,CO和
。图1表示反应中能量变化;图2表示一定温度下,在容积为2L的密闭容器中加入4molH2和一定量的CO后,CO和 的浓度随时间变化。
的浓度随时间变化。
(1)在图1中,曲线________ (填“a”或“b”)表示使用了催化剂。
(2)该反应属于________ (填“吸热”或“放热”)反应。
(3)增大反应体系压强,则该反应化学平衡常数________ (填“增大”“减小”或“不变”)。根据图2计算该反应的化学平衡常数数值为K=________
Ⅱ.CuSO4溶液是一种重要的铜盐试剂,在电镀、印染、颜料、农药等方面有广泛应用。某同学利用CuSO4溶液进行以下实验探究:
(4)以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是________ (填字母)。
a.溶液中Cu2+向阳极移动
b.粗铜接电源正极,发生还原反应
c.电解后CuSO4溶液的浓度减小
d.利用阳极泥可回收Ag、Pt、Au等金属
(5)图中,A是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,该同学想在B中实现铁上镀铜:________ (填“CH4”或“O2),a处的电极反应式为________ 。
②当铜电极的质量减轻3.2g,则消耗的CH4在标准状况下的体积为________ 。
 。图1表示反应中能量变化;图2表示一定温度下,在容积为2L的密闭容器中加入4molH2和一定量的CO后,CO和
。图1表示反应中能量变化;图2表示一定温度下,在容积为2L的密闭容器中加入4molH2和一定量的CO后,CO和 的浓度随时间变化。
的浓度随时间变化。 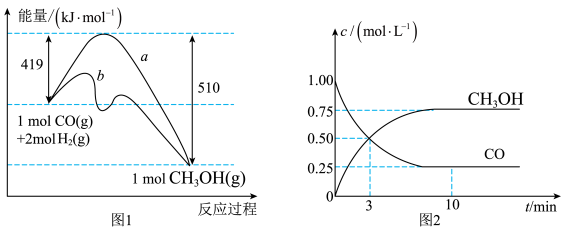
(1)在图1中,曲线
(2)该反应属于
(3)增大反应体系压强,则该反应化学平衡常数
Ⅱ.CuSO4溶液是一种重要的铜盐试剂,在电镀、印染、颜料、农药等方面有广泛应用。某同学利用CuSO4溶液进行以下实验探究:
(4)以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是
a.溶液中Cu2+向阳极移动
b.粗铜接电源正极,发生还原反应
c.电解后CuSO4溶液的浓度减小
d.利用阳极泥可回收Ag、Pt、Au等金属
(5)图中,A是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,该同学想在B中实现铁上镀铜:

②当铜电极的质量减轻3.2g,则消耗的CH4在标准状况下的体积为
您最近半年使用:0次
解题方法
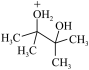
4 . 邻二醇在酸的作用下能转化为酮(或醛),反应的分步机理和协同机理如下:
①当碳原子上连有推电子基团时,有利于碳正离子(通常指的是价层只有6个电子的碳阳离子,是活性中间体)的稳定。
②2,3-二甲基-2,3-丁二醇与酸反应,对应的中间体和生成物相对能量(kJ/mol)如下:
③当碳正离子的相邻碳上有两个不同芳基时,迁移的相对速率与芳基的关系如下表:
下列说法不正确 的是

①当碳原子上连有推电子基团时,有利于碳正离子(通常指的是价层只有6个电子的碳阳离子,是活性中间体)的稳定。
②2,3-二甲基-2,3-丁二醇与酸反应,对应的中间体和生成物相对能量(kJ/mol)如下:
| 过渡态1 | 过渡态2 | 生成物 | |
| 分步机理 | 0.00 | 30.1 | 38.3 | -82.3 |
| 协同机理 | 0.00 | 44.0 | - | -82.3 |
| 芳基 |
|
|
|
| 相对速率 | 0.7 | 1 | 500 |
A.酸性条件下,2,3-二甲基-2,3-丁二醇转化为 主要以分步机理进行 主要以分步机理进行 |
| B.上述转化过程中酸可提高反应速率,但不影响平衡产率 |
| C.乙二醇在酸性条件下只能通过协同机理生成醛,原因是碳正离子中间体不稳定 |
D.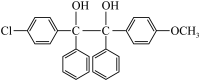 在酸的作用下,产物主要形式为 在酸的作用下,产物主要形式为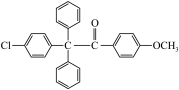 |
您最近半年使用:0次
解题方法
5 . 25℃条件下研究溶液的酸碱性对反应X(aq)→2Y(aq)的影响,各物质浓度c随反应时间t的变化曲线如图,下列说法正确的是
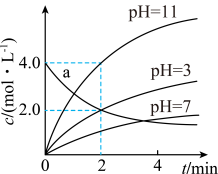
A. 时,反应不能发生 时,反应不能发生 |
| B.H+与OH-相比,H+使反应活化能更低 |
C.a曲线表示 时X的浓度随t的变化 时X的浓度随t的变化 |
D.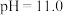 时, 时, 内, 内, |
您最近半年使用:0次
解题方法
6 . 半导体光催化是指半导体材料吸收光子,产生光生电子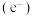 和空穴
和空穴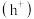 ,从而引发一系列反应的过程。一种光催化选择性氧化甲烷制备甲醇的机理如图所示,下列说法错误的是
,从而引发一系列反应的过程。一种光催化选择性氧化甲烷制备甲醇的机理如图所示,下列说法错误的是
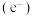 和空穴
和空穴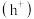 ,从而引发一系列反应的过程。一种光催化选择性氧化甲烷制备甲醇的机理如图所示,下列说法错误的是
,从而引发一系列反应的过程。一种光催化选择性氧化甲烷制备甲醇的机理如图所示,下列说法错误的是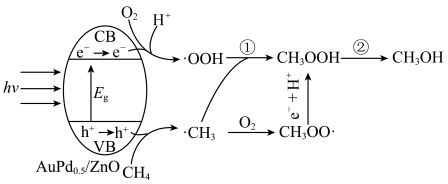
| A.转化①是吸热过程 |
B. 的电子式为 的电子式为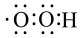 |
C.转化②发生的反应可表示为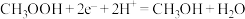 |
D.光照下 可以加快该反应的速率,且不改变反应的焓变 可以加快该反应的速率,且不改变反应的焓变 |
您最近半年使用:0次
7 . 为实现碳达峰,可以将 进行碳捕集、利用与封存。科学研究发现,羟基季铵盐离子液体可以高效催化
进行碳捕集、利用与封存。科学研究发现,羟基季铵盐离子液体可以高效催化 与环氧化合物合成环状碳酸酯的反应,某课题组经研究提出用离子液体三乙基羟乙基溴化铵催化此反应的机理如图所示。下列说法错误的是
与环氧化合物合成环状碳酸酯的反应,某课题组经研究提出用离子液体三乙基羟乙基溴化铵催化此反应的机理如图所示。下列说法错误的是
 进行碳捕集、利用与封存。科学研究发现,羟基季铵盐离子液体可以高效催化
进行碳捕集、利用与封存。科学研究发现,羟基季铵盐离子液体可以高效催化 与环氧化合物合成环状碳酸酯的反应,某课题组经研究提出用离子液体三乙基羟乙基溴化铵催化此反应的机理如图所示。下列说法错误的是
与环氧化合物合成环状碳酸酯的反应,某课题组经研究提出用离子液体三乙基羟乙基溴化铵催化此反应的机理如图所示。下列说法错误的是
| A.三乙基羟乙基溴化铵的催化活性可能优于无羟基结构的四乙基溴化铵 |
| B.该过程有极性键的断裂与形成 |
C.若-R为 ,则 ,则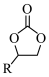 分子中有2个手性碳原子 分子中有2个手性碳原子 |
D.该过程的总反应式可表示为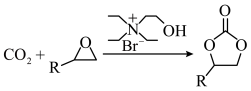 |
您最近半年使用:0次
8 . 为研究反应 (aq)+2I-(aq)=2
(aq)+2I-(aq)=2 (aq)+I2(aq)的反应进程中的能量变化,在
(aq)+I2(aq)的反应进程中的能量变化,在 和I-的混合溶液中加入Fe3+,过程变化如下:
和I-的混合溶液中加入Fe3+,过程变化如下:
第一步:2Fe3+(aq)+2I-(aq)= I2(aq) + 2Fe2+(aq)
第二步:2Fe2+(aq)+ (aq)=2Fe3+(aq)+2
(aq)=2Fe3+(aq)+2 (aq)
(aq)
下列有关该反应的说法正确的是
 (aq)+2I-(aq)=2
(aq)+2I-(aq)=2 (aq)+I2(aq)的反应进程中的能量变化,在
(aq)+I2(aq)的反应进程中的能量变化,在 和I-的混合溶液中加入Fe3+,过程变化如下:
和I-的混合溶液中加入Fe3+,过程变化如下: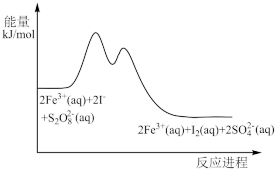
第一步:2Fe3+(aq)+2I-(aq)= I2(aq) + 2Fe2+(aq)
第二步:2Fe2+(aq)+
 (aq)=2Fe3+(aq)+2
(aq)=2Fe3+(aq)+2 (aq)
(aq) 下列有关该反应的说法正确的是
A. (已知其中有1个-O-O-结构)中S元素化合价为+7 (已知其中有1个-O-O-结构)中S元素化合价为+7 |
| B.总反应是吸热反应 |
| C.第一步基元反应是该反应的决速步骤 |
| D.Fe3+改变了总反应的反应历程和焓变 |
您最近半年使用:0次
名校
解题方法
9 . 已知反应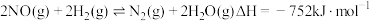 的反应机理如下:
的反应机理如下:
①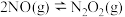 (快)
(快)
② (慢)
(慢)
③ 快)
快)
下列有关说法错误的是
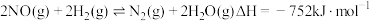 的反应机理如下:
的反应机理如下:①
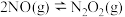 (快)
(快)②
 (慢)
(慢)③
 快)
快)下列有关说法错误的是
| A.①的逆反应速率大于②的正反应速率 | B.②中N2O2与H2的碰撞仅部分有效 |
| C.N2O2和N2O是该反应的催化剂 | D.总反应中逆反应的活化能比正反应的活化能大 |
您最近半年使用:0次
名校
10 . 有机物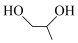 脱氧脱水反应的催化循环机理如下图所示.下列说法正确的是
脱氧脱水反应的催化循环机理如下图所示.下列说法正确的是

A.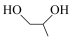 的系统名称为丙二醇 的系统名称为丙二醇 |
B. 为该反应的中间产物 为该反应的中间产物 |
C.过程④中有 键发生断裂 键发生断裂 |
D.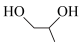 分解的产物有 分解的产物有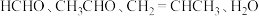 |
您最近半年使用:0次