1 . 下列实验操作或做法正确且能达到目的的是
| 选项 | 实验操作或做法 | 目的 |
| A | 向2 mL0.1 mol/LNa2S溶液中滴加0.1 mol/LZnSO4溶液至不再有沉淀产生,再滴加几滴0.1 mol/LCuSO4溶液,出现黑色沉淀 | 验证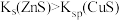 |
| B | 向各盛有5 mLH2O2溶液的两支试管中分别滴入2滴0.1 mol/L的FeCl3溶液和0.1 mol/L的CuSO4溶液 | 比较Fe3+与Cu2+对H2O2分解的催化效果 |
| C | 向盛有淀粉溶液的试管中加入少量稀硫酸,加热,再滴加几滴银氨溶液,水浴加热 | 证明淀粉已发生水解 |
| D | 先用稀硝酸酸化待测液,再滴加BaCl2溶液,生成白色沉淀 | 检验溶液中是否含有 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2 . 甲醛释氢对氢能源和含甲醛污水处理有重要意义。
(1)HCHO电催化释氢
催化电解含较低浓度的HCHO、NaOH混合溶液,可获得 与HCOONa(如图所示),其中电极b表面覆盖一种Mo与P形成的化合物(晶胞结构如图所示)作催化剂。
与HCOONa(如图所示),其中电极b表面覆盖一种Mo与P形成的化合物(晶胞结构如图所示)作催化剂。 与
与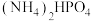 混合物与
混合物与 高温灼烧制得(反应中N元素化合价不变),该反应的化学方程式为
高温灼烧制得(反应中N元素化合价不变),该反应的化学方程式为_________________ 。
②电解时,电极b上同时产生 与
与 的物质的量之比为1∶2,则电极b上的电极反应式为
的物质的量之比为1∶2,则电极b上的电极反应式为_____________ 。
③电解过程中每产生1 mol ,通过阴离子交换膜的
,通过阴离子交换膜的 为
为______ mol。
(2)HCHO水化释氢
45℃时,碱性条件下Ag作催化剂可将甲醛转化为 ,反应的机理如图所示。
,反应的机理如图所示。 表面以防止纳米Ag团聚。其他条件不变,反应相同时间,NaOH浓度对氢气产生快慢的影响如图所示。
表面以防止纳米Ag团聚。其他条件不变,反应相同时间,NaOH浓度对氢气产生快慢的影响如图所示。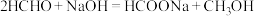 。
。
①若将甲醛中的氢用D原子标记为DCDO,得到的氢气产物为_______ (填化学式)。
②NaOH浓度低于1 mol⋅L 时,NaOH浓度增大产生氢气会加快的原因是
时,NaOH浓度增大产生氢气会加快的原因是__________ 。
③若NaOH浓度过大, 的产生迅速减慢的原因可能是
的产生迅速减慢的原因可能是__________________ 。
(3)甲烷与水在催化剂作用下可产生氢气与碳氧化物,与甲烷水化法制氢气相比,甲醛制氢的优点有______________ 。
(1)HCHO电催化释氢
催化电解含较低浓度的HCHO、NaOH混合溶液,可获得
 与HCOONa(如图所示),其中电极b表面覆盖一种Mo与P形成的化合物(晶胞结构如图所示)作催化剂。
与HCOONa(如图所示),其中电极b表面覆盖一种Mo与P形成的化合物(晶胞结构如图所示)作催化剂。
 与
与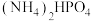 混合物与
混合物与 高温灼烧制得(反应中N元素化合价不变),该反应的化学方程式为
高温灼烧制得(反应中N元素化合价不变),该反应的化学方程式为②电解时,电极b上同时产生
 与
与 的物质的量之比为1∶2,则电极b上的电极反应式为
的物质的量之比为1∶2,则电极b上的电极反应式为③电解过程中每产生1 mol
 ,通过阴离子交换膜的
,通过阴离子交换膜的 为
为(2)HCHO水化释氢
45℃时,碱性条件下Ag作催化剂可将甲醛转化为
 ,反应的机理如图所示。
,反应的机理如图所示。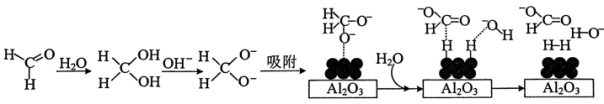
 表面以防止纳米Ag团聚。其他条件不变,反应相同时间,NaOH浓度对氢气产生快慢的影响如图所示。
表面以防止纳米Ag团聚。其他条件不变,反应相同时间,NaOH浓度对氢气产生快慢的影响如图所示。
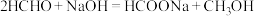 。
。①若将甲醛中的氢用D原子标记为DCDO,得到的氢气产物为
②NaOH浓度低于1 mol⋅L
 时,NaOH浓度增大产生氢气会加快的原因是
时,NaOH浓度增大产生氢气会加快的原因是③若NaOH浓度过大,
 的产生迅速减慢的原因可能是
的产生迅速减慢的原因可能是(3)甲烷与水在催化剂作用下可产生氢气与碳氧化物,与甲烷水化法制氢气相比,甲醛制氢的优点有
您最近半年使用:0次
7日内更新
|
457次组卷
|
2卷引用:江苏省苏锡常镇四市2024届高三一模考试化学试题
解题方法
3 . 中国科学院理化所发现利用Pd-CdS可使PLA(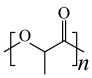 )转化为丙酮酸(
)转化为丙酮酸(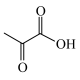 )的速率显著提高,并且优异的稳定性确保了Pd—CdS可以维持100h的反应性能,其反应机理如图所示,Pd-CdS在光照条件下产生带正电空穴(用h+表示,可捕获电子)和电子。下列说法错误的是
)的速率显著提高,并且优异的稳定性确保了Pd—CdS可以维持100h的反应性能,其反应机理如图所示,Pd-CdS在光照条件下产生带正电空穴(用h+表示,可捕获电子)和电子。下列说法错误的是
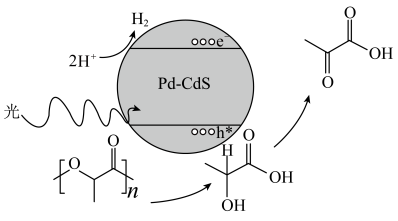
| A.Pd-CdS可作乳酸制备丙酮酸的催化剂 |
| B.在相同条件下,适当增加光的强度有利于加快反应速率 |
| C.整个过程中,氧化产物与还原产物的物质的量之比为1:1 |
| D.当180gPLA完全转化成丙酮酸时,理论上Pd-CdS中至少产生4molh+ |
您最近半年使用:0次
4 . 用 还原
还原 可合成
可合成 。回答下列问题:
。回答下列问题:
(1)利用 光解水制
光解水制 具有重要的经济价值,原理如图所示。
具有重要的经济价值,原理如图所示。 表面发生的电极反应式为
表面发生的电极反应式为_____ 。
写出 还原
还原 生成
生成 和
和 的热化学方程式:
的热化学方程式:_____ 。
(3)一定条件下,向某恒容密闭容器中充入2
 和3
和3
 反应生成
反应生成 和
和 ,起始时压强为
,起始时压强为 ,测得在相同时间内不同温度下
,测得在相同时间内不同温度下 的转化率如图所示。
的转化率如图所示。_____ 。
② K时,该反应的平衡常数
K时,该反应的平衡常数
_____ (列出计算式即可,不必化简。以分压代替浓度,分压=总压×物质的量分数)。
(4)为了探究浓度对反应速率的影响,473K时,向某恒容密闭容器中充入 和
和 进行实验,实验数据如下表所示:
进行实验,实验数据如下表所示:
该反应速率的通式为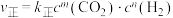 ,
,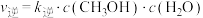 (
( 、
、 是只与温度有关的速率常数)。由表中数据可确定反应速率通式中
是只与温度有关的速率常数)。由表中数据可确定反应速率通式中
_____ 、
_____ 。实验发现,当实验1中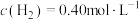 时达到平衡,请计算该温度下此反应的
时达到平衡,请计算该温度下此反应的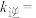
_____ 。
 还原
还原 可合成
可合成 。回答下列问题:
。回答下列问题:(1)利用
 光解水制
光解水制 具有重要的经济价值,原理如图所示。
具有重要的经济价值,原理如图所示。 表面发生的电极反应式为
表面发生的电极反应式为
| 共价键 |  |  |  |  |  |
键能/( ) ) | 464 | 358 | 799 | 432 | 411 |
 还原
还原 生成
生成 和
和 的热化学方程式:
的热化学方程式:(3)一定条件下,向某恒容密闭容器中充入2

 和3
和3
 反应生成
反应生成 和
和 ,起始时压强为
,起始时压强为 ,测得在相同时间内不同温度下
,测得在相同时间内不同温度下 的转化率如图所示。
的转化率如图所示。
②
 K时,该反应的平衡常数
K时,该反应的平衡常数
(4)为了探究浓度对反应速率的影响,473K时,向某恒容密闭容器中充入
 和
和 进行实验,实验数据如下表所示:
进行实验,实验数据如下表所示:| 实验 | 起始浓度/( ) ) | 初始速率/( ) ) | |
 |  | ||
| 1 | 0.25 | 1.00 | 0.45 |
| 2 | 0.25 | 2.00 | 3.60 |
| 3 | 2.00 | 1.00 | 3.6 |
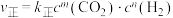 ,
,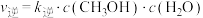 (
( 、
、 是只与温度有关的速率常数)。由表中数据可确定反应速率通式中
是只与温度有关的速率常数)。由表中数据可确定反应速率通式中

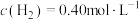 时达到平衡,请计算该温度下此反应的
时达到平衡,请计算该温度下此反应的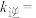
您最近半年使用:0次
解题方法
5 . 下图为 分子在催化剂作用下发生一系列转化的示意图,下列叙述正确的是
分子在催化剂作用下发生一系列转化的示意图,下列叙述正确的是
 分子在催化剂作用下发生一系列转化的示意图,下列叙述正确的是
分子在催化剂作用下发生一系列转化的示意图,下列叙述正确的是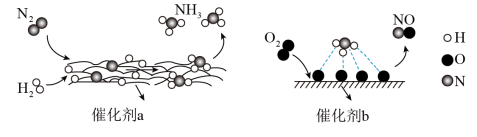
| A.催化剂a、b表面均发生了极性共价键的断裂 |
B. 分子和 分子和 分子的中心原子杂化类型不同 分子的中心原子杂化类型不同 |
C.若 键能是a kJ·mol 键能是a kJ·mol  键能是b kJ·mol 键能是b kJ·mol , , 键能是c kJ·mol 键能是c kJ·mol ,则每生成2 mol ,则每生成2 mol ,放出 ,放出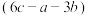 kJ热量 kJ热量 |
| D.在催化剂b作用下发生转化得到的两种生成物,均为直线形分子 |
您最近半年使用:0次
名校
6 . 氮氧化物( )会对生态系统和人体健康造成危害。一种以沸石笼作为载体对
)会对生态系统和人体健康造成危害。一种以沸石笼作为载体对 进行催化还原的原理如图所示。下列说法错误的是
进行催化还原的原理如图所示。下列说法错误的是
 )会对生态系统和人体健康造成危害。一种以沸石笼作为载体对
)会对生态系统和人体健康造成危害。一种以沸石笼作为载体对 进行催化还原的原理如图所示。下列说法错误的是
进行催化还原的原理如图所示。下列说法错误的是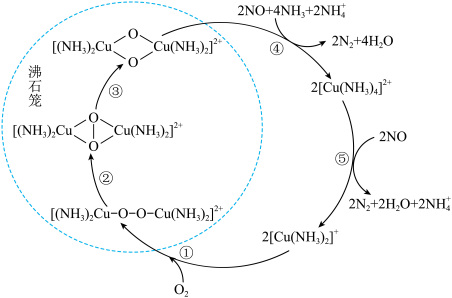
A.反应①每消耗1mol ,转移2mol电子 ,转移2mol电子 |
B.脱除NO的总反应可表示为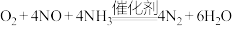 |
C.反应④有 键和 键和 键的形成 键的形成 |
D.反应⑤中 作还原剂 作还原剂 |
您最近半年使用:0次
名校
7 . 在新型催化剂 作用下,
作用下, 氧化
氧化 可获得Cl2:
可获得Cl2: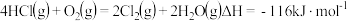 。关于反应
。关于反应 ,下列说法正确的是
,下列说法正确的是
 作用下,
作用下, 氧化
氧化 可获得Cl2:
可获得Cl2: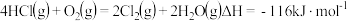 。关于反应
。关于反应 ,下列说法正确的是
,下列说法正确的是A.反应活化能: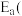 正 正 逆 逆 |
B.每生成标准状况下22.4L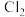 ,放出 ,放出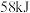 的热量 的热量 |
C.使用高效催化剂,可使平衡时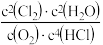 的值增大 的值增大 |
D.断裂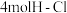 键的同时,有 键的同时,有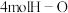 键生成,说明该反应达到平衡状态 键生成,说明该反应达到平衡状态 |
您最近半年使用:0次
8 . 二氧化碳和甲烷是两种温室效应气体,将二者进行转化,可得到具有高附加值的化学品或清洁燃料。
(1) 和
和 催化重整制取
催化重整制取 和
和
主反应:①
副反应:②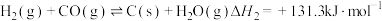
③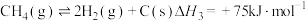
④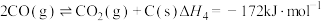
主反应的
___________ ,该反应在___________ (填“较高温度”或“较低温度”)下可自发进行。
(2) 和
和 反应可制取乙烯,反应的化学方程式为
反应可制取乙烯,反应的化学方程式为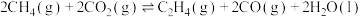 。一定温度下,向某恒容密闭容器中充入
。一定温度下,向某恒容密闭容器中充入 和
和 ,体系的初始压强为
,体系的初始压强为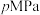 ,若平衡时
,若平衡时 的转化率为
的转化率为 ,不考虑副反应的发生,
,不考虑副反应的发生, 的平衡分压为
的平衡分压为___________ (用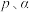 表示,下同),该反应的压强平衡常数
表示,下同),该反应的压强平衡常数
___________ 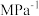 。
。
(3) 过光电化学转化
过光电化学转化 可制得乙二醇,在某催化剂作用下该反应的机理如图所示。图中
可制得乙二醇,在某催化剂作用下该反应的机理如图所示。图中 表示催化剂被光激发出电子之后产生的空穴。
表示催化剂被光激发出电子之后产生的空穴。___________ (填标号)。
A.该反应为自由基型反应
B.生成 的反应为
的反应为
C. 该反应的副产物
该反应的副产物
D.该机理中存在极性键和非极性键的断裂和形成
②以乙二醇为燃料的燃料电池工作时,乙二醇在电池___________ (填“负极”或“正极”)发生反应,若以 溶液为电解液,则该电极的反应式为
溶液为电解液,则该电极的反应式为___________ 。
(4)铜基催化剂电催化还原 制乙醇的两种途径(分别以
制乙醇的两种途径(分别以 和
和 作催化剂)的相对能量变化如图所示,标“
作催化剂)的相对能量变化如图所示,标“ ”的为吸附在催化剂上的物质。分析可知,以
”的为吸附在催化剂上的物质。分析可知,以___________ 作催化剂的催化效率更高。
(1)
 和
和 催化重整制取
催化重整制取 和
和
主反应:①

副反应:②
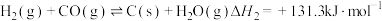
③
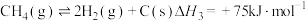
④
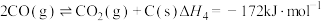
主反应的

(2)
 和
和 反应可制取乙烯,反应的化学方程式为
反应可制取乙烯,反应的化学方程式为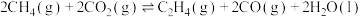 。一定温度下,向某恒容密闭容器中充入
。一定温度下,向某恒容密闭容器中充入 和
和 ,体系的初始压强为
,体系的初始压强为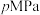 ,若平衡时
,若平衡时 的转化率为
的转化率为 ,不考虑副反应的发生,
,不考虑副反应的发生, 的平衡分压为
的平衡分压为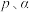 表示,下同),该反应的压强平衡常数
表示,下同),该反应的压强平衡常数
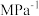 。
。(3)
 过光电化学转化
过光电化学转化 可制得乙二醇,在某催化剂作用下该反应的机理如图所示。图中
可制得乙二醇,在某催化剂作用下该反应的机理如图所示。图中 表示催化剂被光激发出电子之后产生的空穴。
表示催化剂被光激发出电子之后产生的空穴。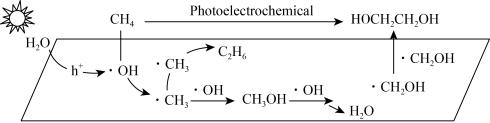
A.该反应为自由基型反应
B.生成
 的反应为
的反应为
C.
 该反应的副产物
该反应的副产物D.该机理中存在极性键和非极性键的断裂和形成
②以乙二醇为燃料的燃料电池工作时,乙二醇在电池
 溶液为电解液,则该电极的反应式为
溶液为电解液,则该电极的反应式为(4)铜基催化剂电催化还原
 制乙醇的两种途径(分别以
制乙醇的两种途径(分别以 和
和 作催化剂)的相对能量变化如图所示,标“
作催化剂)的相对能量变化如图所示,标“ ”的为吸附在催化剂上的物质。分析可知,以
”的为吸附在催化剂上的物质。分析可知,以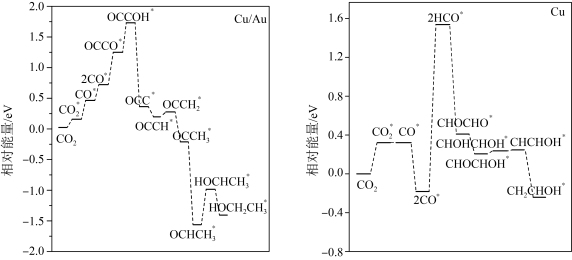
您最近半年使用:0次
9 . CO2和CH4合成CH3COOH对实现“碳中和”目标具有重要意义。回答下列问题:
(1)25℃时,CH4和CH3COOH的燃烧热分别为890.3kJ·mol-1和873.7kJ·mol-1,写出CO2和CH4合成CH3COOH(l)的热化学方程式___________ 。
(2)在硫酸酸化的ZrO2催化剂表面发生反应时,涉及多个基元反应,反应经历pathA,pathB两个路径,其能量变化如下图所示。吸附在催化剂表面的物种用*标注,TS1、TS2、TS3表示过渡态。___________ (填“放出热量”或“吸收热量”)。
②上述基元反应pathA路径中,速率最慢的一步的反应方程式为___________ 。
③pathA和pathB路径相比,___________ 更容易进行。
(3)已知 能自发进行,
能自发进行,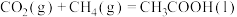
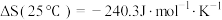 ,下列说法正确的是___________。
,下列说法正确的是___________。
(4)以CuO-ZrO2作催化剂,CO2、CH4投料比为1:1,300℃反应,平衡时CH4转化率为12%,CH3COOH选择性为95%,则CH3COOH的平衡产率为___________ 。(选择性指转化为目标产物的某反应物的质量与发生反应的该反应物的质量之比)
(5)立方ZrO2的晶胞如图,晶胞参数为apm,O2-和Zr4+间的最小距离为___________ pm,晶体密度为___________ g·cm-3。(列出计算式,阿伏加德罗常数的值用 表示)
表示)
(1)25℃时,CH4和CH3COOH的燃烧热分别为890.3kJ·mol-1和873.7kJ·mol-1,写出CO2和CH4合成CH3COOH(l)的热化学方程式
(2)在硫酸酸化的ZrO2催化剂表面发生反应时,涉及多个基元反应,反应经历pathA,pathB两个路径,其能量变化如下图所示。吸附在催化剂表面的物种用*标注,TS1、TS2、TS3表示过渡态。
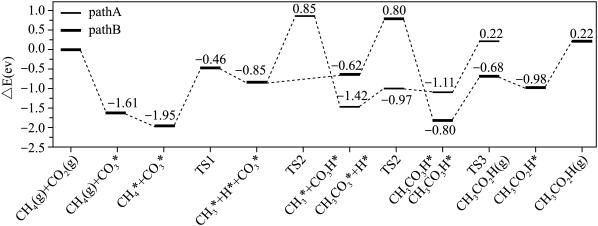
②上述基元反应pathA路径中,速率最慢的一步的反应方程式为
③pathA和pathB路径相比,
(3)已知
 能自发进行,
能自发进行,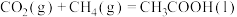
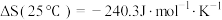 ,下列说法正确的是___________。
,下列说法正确的是___________。| A.25℃时,该反应能自发进行 |
| B.降低温度能提高CH4的平衡转化率 |
C. ,反应达平衡状态 ,反应达平衡状态 |
| D.温度越高反应速率越快 |
(4)以CuO-ZrO2作催化剂,CO2、CH4投料比为1:1,300℃反应,平衡时CH4转化率为12%,CH3COOH选择性为95%,则CH3COOH的平衡产率为
(5)立方ZrO2的晶胞如图,晶胞参数为apm,O2-和Zr4+间的最小距离为
 表示)
表示)
您最近半年使用:0次
2024-04-21更新
|
86次组卷
|
2卷引用:山西省平遥中学2023-2024学年高三二模考试化学试题
名校
解题方法
10 .  和甲醇在
和甲醇在 (钌铑)基催化剂表面加氢可以制取乙酸,其反应机理如图所示。下列说法错误的是
(钌铑)基催化剂表面加氢可以制取乙酸,其反应机理如图所示。下列说法错误的是
 和甲醇在
和甲醇在 (钌铑)基催化剂表面加氢可以制取乙酸,其反应机理如图所示。下列说法错误的是
(钌铑)基催化剂表面加氢可以制取乙酸,其反应机理如图所示。下列说法错误的是
| A.LiI起到催化作用 |
| B.反应①和⑤的反应类型不同 |
| C.反应③中有极性键的断裂和非极性键的形成 |
D.根据该反应机理,可以由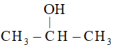 制备 制备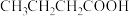 |
您最近半年使用:0次



