名校
1 . 根据实验操作和现象,不能得出相应结论的是
A.未知溶液中滴加 溶液出现不溶于硝酸的白色沉淀,说明该溶液中存在 溶液出现不溶于硝酸的白色沉淀,说明该溶液中存在 或 或 |
| B.将FeNO32样品溶于稀硫酸,滴加KSCN溶液变红,不能说明FeNO32样品溶于稀硫酸前已氧化变质 |
C.将充满 的密闭玻璃球没泡在热水中,红色加深,则 的密闭玻璃球没泡在热水中,红色加深,则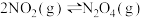 ,△H<0 ,△H<0 |
D.等体积 的 的 和 和 ,分别与足量的 ,分别与足量的 反应, 反应, 放出的氢气多,则酸性: 放出的氢气多,则酸性: |
您最近一年使用:0次
2022-11-03更新
|
202次组卷
|
2卷引用:安徽省宣城中学2023-2024学年高二上学期12月月考化学试题
解题方法
2 . 锶(Sr)和镁位于同主族,锶比镁更活泼,锶与氮气在加热条件下反应生成氮化锶(Sr3N2),已知氮化锶遇水剧烈反应。某同学设计如下装置制备氮化锶(Sr3N2相对分子质量:290.8)。
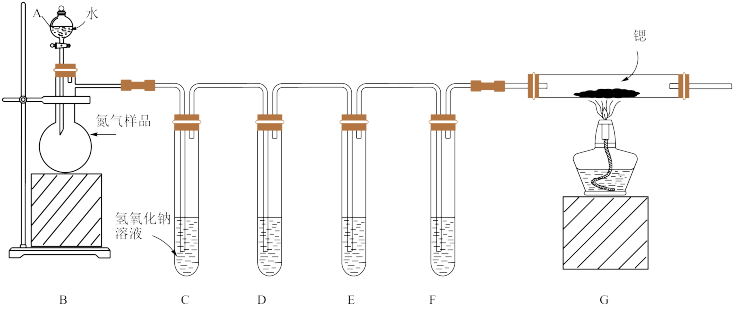
已知:①所使用的氮气样品可能含有少量CO、CO2、O2等气体杂质。
②醋酸二氨合亚铜(CH3COO[Cu(NH3)2])溶液能定量吸收CO,但易被O2氧化,失去吸收CO能力;连苯三酚碱性溶液能定量吸收O2。
试回答下列问题:
(1)仪器A的名称是___________
(2)打开分液漏斗的旋塞,装置B能持续提供N2,这是利用了N2___________ 的物理性质
(3)装置C中盛放NaOH溶液的作用为___________
(4)装置D、E、F中盛装的试剂分别是___________ (填代号)
①浓硫酸②连苯三酚碱性溶液③醋酸二氨合亚铜溶液
(5)为了制得纯净的氮气,实验室中可选用饱和氯化铵溶液和亚硝酸钠溶液共热制备氮气,其化学方程式为:___________
(6)上述实验设计存在明显的缺陷,可能会导致产品变质,提出改进方案为:___________
(7)产品纯度的测定:称取0.8000g实验所得产品,加入干燥的三颈瓶中,加入蒸馏水,并通入足量水蒸气,将产生的氨全部蒸出,用20.00mL1.00mol/L的盐酸标准溶液完全吸收,再用1.00mol/LNaOH标准溶液滴定过剩的HCl,到终点时消耗16.00mLNaOH溶液。则产品纯度为___________ %。

已知:①所使用的氮气样品可能含有少量CO、CO2、O2等气体杂质。
②醋酸二氨合亚铜(CH3COO[Cu(NH3)2])溶液能定量吸收CO,但易被O2氧化,失去吸收CO能力;连苯三酚碱性溶液能定量吸收O2。
试回答下列问题:
(1)仪器A的名称是
(2)打开分液漏斗的旋塞,装置B能持续提供N2,这是利用了N2
(3)装置C中盛放NaOH溶液的作用为
(4)装置D、E、F中盛装的试剂分别是
①浓硫酸②连苯三酚碱性溶液③醋酸二氨合亚铜溶液
(5)为了制得纯净的氮气,实验室中可选用饱和氯化铵溶液和亚硝酸钠溶液共热制备氮气,其化学方程式为:
(6)上述实验设计存在明显的缺陷,可能会导致产品变质,提出改进方案为:
(7)产品纯度的测定:称取0.8000g实验所得产品,加入干燥的三颈瓶中,加入蒸馏水,并通入足量水蒸气,将产生的氨全部蒸出,用20.00mL1.00mol/L的盐酸标准溶液完全吸收,再用1.00mol/LNaOH标准溶液滴定过剩的HCl,到终点时消耗16.00mLNaOH溶液。则产品纯度为
您最近一年使用:0次
名校
解题方法
3 . 下列与化学实验相关的说法正确的是
| A.向Na2O2样品中滴加过量的稀盐酸,将生成的气体通入BaCl2溶液中,无白色沉淀生成,说明样品未变质 |
| B.向2支盛有2 mL不同浓度的Na2SO3溶液的试管中同时加入1 mL2%的H2O2溶液,观察实验现象可得出浓度对反应速率的影响 |
C.向盛有Fe(NO3)2溶液的试管中加入0.1 mol/L的H2SO4溶液,试管口出现红棕色气体,说明NO 被还原成NO 被还原成NO |
| D.用标准HCl溶液滴定NaHCO3溶液来测定其浓度,选择酚酞作指示剂 |
您最近一年使用:0次
4 . 过氧化钠常作漂白剂、杀菌剂、消毒剂。能与水和二氧化碳等物质发生反应,保存不当容易变质。某实验小组以过氧化钠为研究对进行了如下实验,
(1)探究过氧化钠样品是否已经变质,取少量样品,溶解,加入__________ 溶液,充分振荡后有白色沉淀,证明Na2O2已经变质。
(2)该实验小组为了粗略测定过氧化钠的纯度,他们称取mg样品,并设计用如图装置来测定过氧化钠的质量分数。
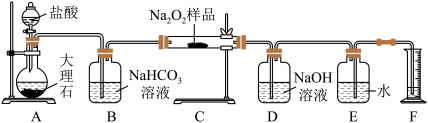
①将仪器连接好以后,必须进行的第一步操作是____________ 。
②D中NaOH溶液的作用____________ 。
③写出装置C中发生的反应的化学方程式____________ 。
④实验结束时,读取实验中生成气体的体积时,你认为合理的是_________ 。
a.读取气体体积,需冷却到室温
b.调整量筒使E. F中液面高度相同
c.视线与凹液面的最低点相平读取量筒中水的体积
⑤读出量筒内水的体积后,折算成氧气的质量为a g,则样品中过氧化钠的质量分数为______ 。
(1)探究过氧化钠样品是否已经变质,取少量样品,溶解,加入
(2)该实验小组为了粗略测定过氧化钠的纯度,他们称取mg样品,并设计用如图装置来测定过氧化钠的质量分数。

①将仪器连接好以后,必须进行的第一步操作是
②D中NaOH溶液的作用
③写出装置C中发生的反应的化学方程式
④实验结束时,读取实验中生成气体的体积时,你认为合理的是
a.读取气体体积,需冷却到室温
b.调整量筒使E. F中液面高度相同
c.视线与凹液面的最低点相平读取量筒中水的体积
⑤读出量筒内水的体积后,折算成氧气的质量为a g,则样品中过氧化钠的质量分数为
您最近一年使用:0次
5 . 实验室盛放NaOH的试剂瓶瓶口出现了大量的白色蘑菇云状物质。某化学兴趣小组对其成分进行探究,称取一定质量的样品溶于水配成1000mL溶液,取40mL溶液于小烧杯中并加入指示剂1用1.00 mol/L盐酸标准液滴定,第一次达到滴定终点时消耗盐酸的体积V1=1.70mL,加入指示剂2继续滴定,第二次达到滴定终点时又消耗盐酸体积V2=3.40mL。下列说法错误的是

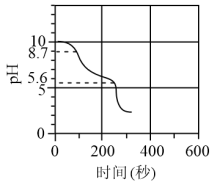


| A.久置NaOH变质后的固体主要成分为Na2CO3和NaHCO3,且物质的量之比为1:1 |
| B.指示剂1可能为酚酞,指示剂2可能为甲基橙 |
| C.原溶液中Na2CO3的浓度为0.0425 mol·L-1 |
D.第一次滴定终点时,溶液存在c(H2CO3)<c(CO ) ) |
您最近一年使用:0次
名校
解题方法
6 . 高铁酸钾(K2FeO4)是一种新型、高效、无毒的多功能水处理剂。查阅资料已知:K2FeO4为紫色固体,溶于KOH溶液,具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
(1)制备K2FeO4
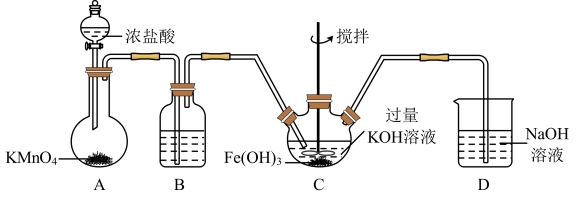
①在装置A中发生的化学反应中HCl显示出来的性质为___________ 。
②C为制备K2FeO4装置,写出次氯酸钾与氢氧化铁在碱性环境中反应的离子方程式:___________ 。
(2)探究K2FeO4的性质
取C中浅紫红色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明K2FeO4能否氧化Cl-而产生Cl2,设计如下方案:取少量溶液a,滴加KSCN溶液至过量,溶液呈红色。由方案中溶液变红可知a中含有Fe3+,该离子的产生不能判断一定是由K2FeO4被Cl-还原而形成的,原因是___________ 。
(3)使用时经常通过测定高铁酸钾的纯度来判断其是否变质。K2FeO4在硫酸溶液中反应如下: FeO
FeO +
+ H+=
H+= O2↑+
O2↑+ Fe3++
Fe3++ ___________
___________
①完成并配平上述离子方程式(方框内填化学计量数,横线上写物质)。___________
②现取C中洗涤并干燥后样品的质量10g,加入稀硫酸,收集到0.672L气体(标准状况)。则样品中高铁酸钾的质量分数为___________ 。(计算结果保留到0.1%)
(1)制备K2FeO4

①在装置A中发生的化学反应中HCl显示出来的性质为
②C为制备K2FeO4装置,写出次氯酸钾与氢氧化铁在碱性环境中反应的离子方程式:
(2)探究K2FeO4的性质
取C中浅紫红色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明K2FeO4能否氧化Cl-而产生Cl2,设计如下方案:取少量溶液a,滴加KSCN溶液至过量,溶液呈红色。由方案中溶液变红可知a中含有Fe3+,该离子的产生不能判断一定是由K2FeO4被Cl-还原而形成的,原因是
(3)使用时经常通过测定高铁酸钾的纯度来判断其是否变质。K2FeO4在硫酸溶液中反应如下:
 FeO
FeO +
+ H+=
H+= O2↑+
O2↑+ Fe3++
Fe3++ ___________
___________①完成并配平上述离子方程式(方框内填化学计量数,横线上写物质)。
②现取C中洗涤并干燥后样品的质量10g,加入稀硫酸,收集到0.672L气体(标准状况)。则样品中高铁酸钾的质量分数为
您最近一年使用:0次
2021-12-21更新
|
310次组卷
|
2卷引用:安徽省滁州市定远县育才学校2021-2022学年高一上学期期末考试化学试题
名校
解题方法
7 . 下列实验操作能达到实验目的的是
| 选项 | 操作 | 目的 |
| A | 取一张pH试纸放在表面皿上,用洁净的玻璃棒蘸取NaClO溶液滴于试纸的中部,与标准比色卡对比 | 测定NaClO溶液的pH |
| B | 向含有酚酞的 溶液中滴入 溶液中滴入 溶液,观察溶液颜色的变化 溶液,观察溶液颜色的变化 | 证明 溶液中存在水解平衡 溶液中存在水解平衡 |
| C | 取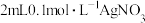 溶液,先后滴加3滴 溶液,先后滴加3滴 溶液和5滴 溶液和5滴 溶液,观察沉淀情况 溶液,观察沉淀情况 | 比较 、 、 的大小 的大小 |
| D | 将 样品溶于稀盐酸后,滴加KSCN溶液,观察溶液是否变红 样品溶于稀盐酸后,滴加KSCN溶液,观察溶液是否变红 | 检验 样品是否变质 样品是否变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-08-01更新
|
800次组卷
|
7卷引用:安徽省六安市第一中学2021-2022学年高二下学期开学考试化学试题
安徽省六安市第一中学2021-2022学年高二下学期开学考试化学试题选择性必修1(SJ)专题3专题综合检测(已下线)3.4.1 难溶电解质的沉淀溶解平衡(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)江西省赣州市赣县第三中学2021-2022学年高二上学期12月月考化学试卷河南省中原名校2021-2022学年高二上学期期末联考化学试题(已下线)第三章 水溶液中的离子反应与平衡(B卷·能力提升练)-【单元测试】2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修1)河南省南阳市第八中学校2022-2023学年高二上学期线上期末考试化学试题
名校
解题方法
8 . 氯化亚铜(CuCl)是一种见光易分解的白色固体,难溶于水,在潮湿的环境中易被氧气氧化为碱式氯化铜。实验室用SOCl2与CuCl2溶液混合制取CuCl的装置如图所示。
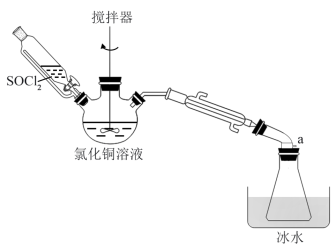
已知:①SOCl2是一种易发烟的液体,遇水剧烈水解生成SO2和HCl气体;
②CuCl在溶液中存在如下平衡:CuCl(s)+3Cl-(aq) [CuCl4]3-(aq)(无色)。
[CuCl4]3-(aq)(无色)。
回答下列问题:
(1)配制CuCl2溶液所需的蒸馏水需要去氧气,最简单的去氧操作是___ ,盛装SOCl2的仪器名称为___ 。
(2)SO2能在溶液中将CuCl2还原为CuCl,反应的离子方程式为___ 。
(3)当三颈烧瓶的溶液由___ 时(填实验现象),则说明反应已经完成,可以停止实验。
(4)实验结束后需要先向三颈烧瓶中加入蒸馏水,然后再进行过滤得到CuCl。加水的作用是___ ,过滤时需要在避光的条件下进行,原因是___ 。
(5)久置在空气中的CuCl可完全变质为碱式氯化铜[xCuCl2·yCu(OH)2,其x、y为整数],为探究该碱式氯化铜的组成,设计如下实验步骤:
①准确称取4.216g样品,溶于足量乙酸中,加蒸馏水配制成100mL溶液;
②取25mL溶液,向其中加入足量的AgNO3溶液,充分反应后过滤、洗涤、干燥,所得白色固体质量为0.574g;
③另取25mL溶液,向其中加入过量的KI溶液,再用0.400mol·L-1的Na2S2O3标准溶液滴定至终点,消耗标准溶液25.00mL。已知滴定过程涉及如下反应:2Cu2++4I-=2CuI↓+I2、2S2O +I2=2I-+S4O
+I2=2I-+S4O 。
。
计算碱式氯化铜中x=___ ;y=___ 。

已知:①SOCl2是一种易发烟的液体,遇水剧烈水解生成SO2和HCl气体;
②CuCl在溶液中存在如下平衡:CuCl(s)+3Cl-(aq)
 [CuCl4]3-(aq)(无色)。
[CuCl4]3-(aq)(无色)。回答下列问题:
(1)配制CuCl2溶液所需的蒸馏水需要去氧气,最简单的去氧操作是
(2)SO2能在溶液中将CuCl2还原为CuCl,反应的离子方程式为
(3)当三颈烧瓶的溶液由
(4)实验结束后需要先向三颈烧瓶中加入蒸馏水,然后再进行过滤得到CuCl。加水的作用是
(5)久置在空气中的CuCl可完全变质为碱式氯化铜[xCuCl2·yCu(OH)2,其x、y为整数],为探究该碱式氯化铜的组成,设计如下实验步骤:
①准确称取4.216g样品,溶于足量乙酸中,加蒸馏水配制成100mL溶液;
②取25mL溶液,向其中加入足量的AgNO3溶液,充分反应后过滤、洗涤、干燥,所得白色固体质量为0.574g;
③另取25mL溶液,向其中加入过量的KI溶液,再用0.400mol·L-1的Na2S2O3标准溶液滴定至终点,消耗标准溶液25.00mL。已知滴定过程涉及如下反应:2Cu2++4I-=2CuI↓+I2、2S2O
 +I2=2I-+S4O
+I2=2I-+S4O 。
。计算碱式氯化铜中x=
您最近一年使用:0次
9 . 室温下进行下列实验,根据实验操作和现象所得到的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向X溶液中滴加几滴新制氯水,振荡,再加入少量KSCN溶液,溶液变为红色 | X溶液中一定含有Fe2+ |
| B | 向3mLKI溶液中滴加几滴溴水,振荡,再滴加1mL淀粉溶液,溶液显蓝色 | Br2的氧化性比I2的强 |
| C | 用pH试纸测得: CH,COONa溶液的pH约为9,NaNO2溶液的pH约为8 | HNO2电离出H+的能力一定比CH3COOH的强 |
| D | 将Na2SO3样品溶于水,滴加稀盐酸酸化的Ba( NO3)2溶液,产生白色沉淀 | Na2SO3样品已变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-08-05更新
|
530次组卷
|
4卷引用:安徽省芜湖市第三中学2020-2021学年高二下学期期末调研测试化学试题
名校
解题方法
10 . 下列化学物质在实际生产生活和科技等方面的叙述正确的是
| A.SO2、漂白粉、Na2O2都能使品红溶液褪色,其作用原理相同 |
| B.在食品袋中放入装有硅胶、铁粉的透气小袋,可防止食物受潮、氧化变质 |
| C.高温结构陶瓷、压电陶瓷等新型陶瓷均属于硅酸盐材料 |
| D.某雨水样品放置一段时间酸性增强,是因为空气中的CO2溶解进入雨水 |
您最近一年使用:0次
2021-05-10更新
|
291次组卷
|
2卷引用:安徽省合肥市第一中学2020-2021学年高一下学期期中考试化学试题



