名校
解题方法
1 . 下列结论正确的是
①离子半径:K+>Al3+>S2->Cl-
②氢化物的稳定性:HF>HCl>H2S>PH3>SiH4
③离子的还原性:S2->Cl->Br->I-
④氧化性:Cl2>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>HClO4
⑥非金属性:O>N>P>Si
⑦碱性:NaOH>KOH>RbOH>CsOH
①离子半径:K+>Al3+>S2->Cl-
②氢化物的稳定性:HF>HCl>H2S>PH3>SiH4
③离子的还原性:S2->Cl->Br->I-
④氧化性:Cl2>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>HClO4
⑥非金属性:O>N>P>Si
⑦碱性:NaOH>KOH>RbOH>CsOH
| A.②④⑥ | B.②⑥⑦ | C.②④⑤⑥⑦ | D.②⑤⑦ |
您最近一年使用:0次
2022-04-03更新
|
205次组卷
|
3卷引用:四川省成都外国语学校2021-2022学年高一下学期3月月考化学试题
名校
解题方法
2 . 高铁酸钾是一种高效多功能的新型非氯绿色消毒剂,主要用于饮水处理。实验小组制备高铁酸钾(K2FeO4)并探究其性质。
资料:K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
(1)制备K2FeO4(夹持装置略)
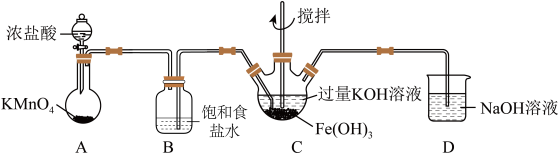
①如图所示,A为氯气发生装置。装置A、B、C、D中存在错误的是______________ (填序号)。
②C中得到紫色固体和溶液。C中通入氯气发生反应,生成高铁酸钾(K2FeO4)的化学方程式为_______ ,此外Cl2还可能与过量的KOH反应。
(2)探究K2FeO4的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明是否K2FeO4,氧化了Cl-而产生Cl2,设计以下方案:
i.由方案I中溶液变红可知溶液a中含有__________ 离子,但该离子的存在不能判断一定是K2FeO4,氧化了Cl2,因为K2FeO4,在酸性溶液中不稳定,请写出K2FeO4在酸性溶液中发生反应的离子方程式___________________________________ 。
ii.方案Ⅱ可证明K2FeO4,氧化了Cl-.用KOH溶液洗涤的目的是_______________ 。
②根据K2FeO4的制备实验得出:氧化性Cl2_____ FeO42- (填“>”或“<”),而方案Ⅱ实验表明,Cl2和FeO42-的氧化性强弱关系恰好相反,原因是_______________ 。
(3)若在制备装置C中加入Fe(OH)3的质量为14.0g,充分反应后经过滤、洗涤、干燥得K2FeO4固体19.3g,则K2FeO4的产率为______________ 。
资料:K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
(1)制备K2FeO4(夹持装置略)

①如图所示,A为氯气发生装置。装置A、B、C、D中存在错误的是
②C中得到紫色固体和溶液。C中通入氯气发生反应,生成高铁酸钾(K2FeO4)的化学方程式为
(2)探究K2FeO4的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明是否K2FeO4,氧化了Cl-而产生Cl2,设计以下方案:
| 方案I | 取少量溶液a,滴加KSCN溶液至过量,溶液呈红色。 |
| 方案II | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b。取少量b,滴加盐酸,有Cl2产生。 |
i.由方案I中溶液变红可知溶液a中含有
ii.方案Ⅱ可证明K2FeO4,氧化了Cl-.用KOH溶液洗涤的目的是
②根据K2FeO4的制备实验得出:氧化性Cl2
(3)若在制备装置C中加入Fe(OH)3的质量为14.0g,充分反应后经过滤、洗涤、干燥得K2FeO4固体19.3g,则K2FeO4的产率为
您最近一年使用:0次
2020-05-30更新
|
729次组卷
|
8卷引用:四川省重点高中2021届高三下学期入学考试化学试题
四川省重点高中2021届高三下学期入学考试化学试题河南省六市(南阳市、驻马店市、信阳市、漯河市、周口市、三门峡市)2020届高三第二次联合调研检测理综化学试题(已下线)专题16 化学实验综合题-2020年高考真题和模拟题化学分项汇编福建省连城县第一中学2021届高三上学期第一次月考化学试题(已下线)专题讲座(三)“铁三角”综合实验题解题策略(精练)——2021年高考化学一轮复习讲练测山东省济南市商河县第一中学2021届高三上学期阶段性考试化学试题(已下线)易错23 化学实验评价与探究-备战2021年高考化学一轮复习易错题福建省莆田二中2021-2022学年高三上学期期中考试化学试题
名校
3 . 硝酸是一种具有强氧化性、腐蚀性的强酸,其还原产物因硝酸浓度的不同而有变化,从总体上说,硝酸浓度越高,平均每分子硝酸得到的电子数越少,浓硝酸的还原产物主要为 、稀硝酸的还原产物为
、稀硝酸的还原产物为 。实验室中,常用
。实验室中,常用 与浓
与浓 反应制取
反应制取 ,用
,用 与稀
与稀 反应制取
反应制取 。
。
(1)浓硝酸具有以下性质:①强氧化性②酸性③还原性④不稳定性⑤挥发性,下列反应或者现象主要体现了硝酸的什么性质:
①久置浓硝酸显黄色___________ (填序号,下同),请写出反应的化学方程式___________ 。
②用稀硝酸清洗试管壁上的银___________ 。
(2) 与适量的浓
与适量的浓 反应,铜全部作用后,共收集到
反应,铜全部作用后,共收集到 气体(标准状况下),反应中消耗的
气体(标准状况下),反应中消耗的 的物质的量是___________(填字母代号)。
的物质的量是___________(填字母代号)。
(3)硝酸的还原产物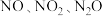 等对环境均有副作用,为了可持续发展,当今社会提出的一个新概念:“绿色化学”,它要求从经济、环保和技术上设计可行的化学反应,则下列由单质钢制取硝酸铜的方法可行且符合“绿色化学”的是_______ (填字母代号)。
等对环境均有副作用,为了可持续发展,当今社会提出的一个新概念:“绿色化学”,它要求从经济、环保和技术上设计可行的化学反应,则下列由单质钢制取硝酸铜的方法可行且符合“绿色化学”的是_______ (填字母代号)。
(4)实际上硝酸不仅可被还原为 或
或 ,浓度更稀时硝酸还可以被还原为
,浓度更稀时硝酸还可以被还原为 等,锌与很稀的硝酸反应生成硝酸锌、硝酸铵和水,写出该反应的化学方程式
等,锌与很稀的硝酸反应生成硝酸锌、硝酸铵和水,写出该反应的化学方程式___________ ,当生成 硝酸锌时,被还原的硝酸的物质的量为
硝酸锌时,被还原的硝酸的物质的量为___________ 。
(5)汽车彻底改变了我们生活,成为我们的不可成缺的交通工具之一,汽车尾气系统中的催化转化器,可有效降低尾气中的 和
和 等向大气的排放,在催化转化器的前半部发生的反应为
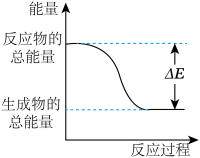
等向大气的排放,在催化转化器的前半部发生的反应为 ,已知汽车尾气处理反应能量过程如下图,下列说法正确的是___________。
,已知汽车尾气处理反应能量过程如下图,下列说法正确的是___________。
 、稀硝酸的还原产物为
、稀硝酸的还原产物为 。实验室中,常用
。实验室中,常用 与浓
与浓 反应制取
反应制取 ,用
,用 与稀
与稀 反应制取
反应制取 。
。(1)浓硝酸具有以下性质:①强氧化性②酸性③还原性④不稳定性⑤挥发性,下列反应或者现象主要体现了硝酸的什么性质:
①久置浓硝酸显黄色
②用稀硝酸清洗试管壁上的银
(2)
 与适量的浓
与适量的浓 反应,铜全部作用后,共收集到
反应,铜全部作用后,共收集到 气体(标准状况下),反应中消耗的
气体(标准状况下),反应中消耗的 的物质的量是___________(填字母代号)。
的物质的量是___________(填字母代号)。A. | B. | C. | D. |
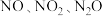 等对环境均有副作用,为了可持续发展,当今社会提出的一个新概念:“绿色化学”,它要求从经济、环保和技术上设计可行的化学反应,则下列由单质钢制取硝酸铜的方法可行且符合“绿色化学”的是_______ (填字母代号)。
等对环境均有副作用,为了可持续发展,当今社会提出的一个新概念:“绿色化学”,它要求从经济、环保和技术上设计可行的化学反应,则下列由单质钢制取硝酸铜的方法可行且符合“绿色化学”的是_______ (填字母代号)。A.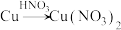 |
B. |
C.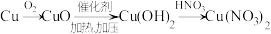 |
D.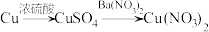 |
 或
或 ,浓度更稀时硝酸还可以被还原为
,浓度更稀时硝酸还可以被还原为 等,锌与很稀的硝酸反应生成硝酸锌、硝酸铵和水,写出该反应的化学方程式
等,锌与很稀的硝酸反应生成硝酸锌、硝酸铵和水,写出该反应的化学方程式 硝酸锌时,被还原的硝酸的物质的量为
硝酸锌时,被还原的硝酸的物质的量为(5)汽车彻底改变了我们生活,成为我们的不可成缺的交通工具之一,汽车尾气系统中的催化转化器,可有效降低尾气中的
 和
和 等向大气的排放,在催化转化器的前半部发生的反应为
等向大气的排放,在催化转化器的前半部发生的反应为 ,已知汽车尾气处理反应能量过程如下图,下列说法正确的是___________。
,已知汽车尾气处理反应能量过程如下图,下列说法正确的是___________。
| A.该反应为放热反应 | B.该反应为吸热反应 |
C.形成 化学键需要吸收热量 化学键需要吸收热量 | D.反应物的总能量小于生成物的总能量 |
您最近一年使用:0次
4 . 某兴趣小组研究亚硝酸钠,查阅下列资料,试根据信息回答下列问题。
(1)已知NaNO2能发生如下反应: 2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。请用双线桥表示电子转移的方向和数目。________________ ;该反应中氧化剂是_____ ;若有0.75mol电子转移,则被还原的氧化剂粒子数为_______ 。(用NA表示)
(2)误食NaNO2会导致血红蛋白中的Fe2+转化为Fe3+而中毒,可服用维生素C解毒。下列分析错误的是______ (填序号)。
A.NaNO2被还原 B.维生素C具有还原性
C.还原性: 维生素C > Fe2+ D.NaNO2是还原剂
(3)下列方法中,可用来区分NaNO2和NaCl的是______ (填序号)。
A. 焰色反应 B.分别滴加酸化FeSO4溶液和KSCN溶液
C.在酸性条件下加入KI 淀粉溶液 D.分别滴加AgNO3溶液
(4)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:_______________ 。
| 药品 | NaNO2 (亚硝酸钠) |
| 性质 | 1.在酸性溶液中有较强氧化性,能将Fe2+ 氧化成Fe3+ ; 2.AgNO2是一种难溶于水、易溶于酸的盐。 |
(1)已知NaNO2能发生如下反应: 2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。请用双线桥表示电子转移的方向和数目。
(2)误食NaNO2会导致血红蛋白中的Fe2+转化为Fe3+而中毒,可服用维生素C解毒。下列分析错误的是
A.NaNO2被还原 B.维生素C具有还原性
C.还原性: 维生素C > Fe2+ D.NaNO2是还原剂
(3)下列方法中,可用来区分NaNO2和NaCl的是
A. 焰色反应 B.分别滴加酸化FeSO4溶液和KSCN溶液
C.在酸性条件下加入KI 淀粉溶液 D.分别滴加AgNO3溶液
(4)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:
您最近一年使用:0次
2018-01-31更新
|
534次组卷
|
6卷引用:四川省成都市2017-2018学年高一上期期末调研考试化学试题
名校
解题方法
5 . 镁与稀硝酸的反应为:4Mg+10HNO3(稀)=4Mg(NO3)2+NH4NO3+3H2O
(1)该反应中,还原产物是___________ ,HNO3表现了___________ 。(选填“还原性”、“氧化性”、“酸性”、“碱性”)。氧化剂与还原剂的物质的量之比为___________ 。
(2)用“双线桥法”表示该反应中电子转移的方向和数目。___________ ,4Mg+10HNO3(稀)=4Mg(NO3)2+NH4NO3+3H2O
(3)若反应过程中转移的电子数为6.02×1023,则被还原的硝酸物质的量为___________ 。
(1)该反应中,还原产物是
(2)用“双线桥法”表示该反应中电子转移的方向和数目。
(3)若反应过程中转移的电子数为6.02×1023,则被还原的硝酸物质的量为
您最近一年使用:0次
名校
6 . 请回答下列问题:
(1)①配平并用“双线桥法”表示下列反应中电子转移的方向和数目。___________
Mg+ HNO3(稀) ——— Mg(NO3)2+ NO↑+ H2O
②该反应中HNO3表现了___________ (选填“还原性”、“氧化性”、“酸性”、“碱性”)。
③若反应过程中转移的电子为0.6 mol,则被还原的硝酸物质的量为___________ 。
(2)在KIO3+5KI+3H2SO4 = 3I2+3K2SO4+3H2O中,氧化产物与还原产物的物质的量之比:___________ 。
(3)Cl2是一种有毒气体,如果泄漏会造成严重的环境污染,化工厂可用浓氨水来检验Cl2是否泄漏,有关反应的化学方程式为:3Cl2(气)+8NH3(气)=6NH4Cl(固)+N2(气),若反应中消耗Cl2 1.5mol则被氧化的NH3在标准状况下的体积为___________ L。
(1)①配平并用“双线桥法”表示下列反应中电子转移的方向和数目。
Mg+ HNO3(稀) ——— Mg(NO3)2+ NO↑+ H2O
②该反应中HNO3表现了
③若反应过程中转移的电子为0.6 mol,则被还原的硝酸物质的量为
(2)在KIO3+5KI+3H2SO4 = 3I2+3K2SO4+3H2O中,氧化产物与还原产物的物质的量之比:
(3)Cl2是一种有毒气体,如果泄漏会造成严重的环境污染,化工厂可用浓氨水来检验Cl2是否泄漏,有关反应的化学方程式为:3Cl2(气)+8NH3(气)=6NH4Cl(固)+N2(气),若反应中消耗Cl2 1.5mol则被氧化的NH3在标准状况下的体积为
您最近一年使用:0次
名校
7 . 下列结论正确的是
①原子半径:K>Cl>S ②氢化物稳定性:HF<H2S<PH3;
③离子还原性:S2->Cl-> Br->I- ④单质氧化性:Cl2>S>Si;
⑤酸性:H2SO4>HClO ⑥碱性强弱:KOH>NaOH>Mg(OH)2
①原子半径:K>Cl>S ②氢化物稳定性:HF<H2S<PH3;
③离子还原性:S2->Cl-> Br->I- ④单质氧化性:Cl2>S>Si;
⑤酸性:H2SO4>HClO ⑥碱性强弱:KOH>NaOH>Mg(OH)2
| A.①④⑤ | B.③⑥ | C.③⑤⑥ | D.④⑤⑥ |
您最近一年使用:0次
解题方法
8 . 除第一周期外,关于同周期主族元素的下列变化规律的叙述中不正确的是
| A.从左到右,原子半径逐渐减小 |
| B.从左到右,元素原子的氧化性增强,还原性减弱 |
| C.从左到右,元素最高正价数从+1递增到+7,负价由-4递变到-1 |
| D.从左到右,元素最高价氧化物对应水化物碱性减弱,酸性增强 |
您最近一年使用:0次
2021-03-31更新
|
95次组卷
|
2卷引用:四川省成都东部新区养马中学2020-2021学年高一下学期第一次月考化学试题
解题方法
9 . 已知HNO3常温下能氧化金属Cu,反应的化学方程式如下:
3Cu+8HNO3(稀) = 3Cu(NO3)2+2NO↑+4H2O
(1)用双线桥法表示电子转移的方向和数目________ 。
(2)该反应中氧化剂是________ ,还原产物是________ (填化学式)。
(3)HNO3在上述反应中显示出来的性质是________ (填编号,下同)。
A.氧化性 B.还原性 C.酸性 D.碱性
(4)当转移9.03×1023个电子时,生成的NO气体的体积为(标准状况)_____ L。
(5)与15g NO所含原子总数相同的氨气是________ g。
3Cu+8HNO3(稀) = 3Cu(NO3)2+2NO↑+4H2O
(1)用双线桥法表示电子转移的方向和数目
(2)该反应中氧化剂是
(3)HNO3在上述反应中显示出来的性质是
A.氧化性 B.还原性 C.酸性 D.碱性
(4)当转移9.03×1023个电子时,生成的NO气体的体积为(标准状况)
(5)与15g NO所含原子总数相同的氨气是
您最近一年使用:0次
10 . 实验小组制备高铁酸钾(K2FeO4)并探究其性质。
资料:K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
(1)制备K2FeO4(夹持装置略)
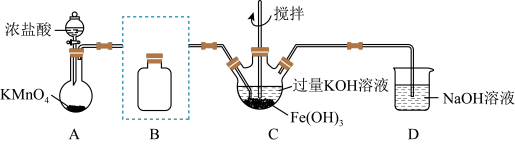
①A为氯气发生装置。A中反应方程式是___________________________________ (锰被还原为Mn2+)。
②将除杂装置B补充完整并标明所用试剂 :______________________________
③C中得到紫色固体和溶液。C中Cl2发生的反应有3Cl2+2Fe(OH)3+10KOH 2K2FeO4+6KCl+8H2O,另外还有
2K2FeO4+6KCl+8H2O,另外还有____________________________________ (写离子方程式)。
(2)探究K2FeO4的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明是否K2FeO4氧化了Cl-而产生Cl2,设计以下方案:
i.由方案Ⅰ中溶液变红可知a中含有_______ 离子,但该离子的产生不能判断一定是K2FeO4将Cl-氧化,还可能由__________________________________________ 产生(用方程式表示)。
ii.方案Ⅱ可证明K2FeO4氧化了Cl-。用KOH溶液洗涤的目的是______________________________ 。
②根据K2FeO4的制备实验得出:氧化性Cl2_______ FeO42-(填“>”或“<”),而方案Ⅱ实验表明,Cl2和FeO42-的氧化性强弱关系相反,原因是________________ 。
资料:K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
(1)制备K2FeO4(夹持装置略)
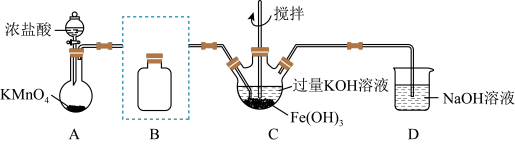
①A为氯气发生装置。A中反应方程式是
②将除杂装置B补充完整并标明所用试剂 :
③C中得到紫色固体和溶液。C中Cl2发生的反应有3Cl2+2Fe(OH)3+10KOH
 2K2FeO4+6KCl+8H2O,另外还有
2K2FeO4+6KCl+8H2O,另外还有(2)探究K2FeO4的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明是否K2FeO4氧化了Cl-而产生Cl2,设计以下方案:
| 方案Ⅰ | 取少量a,滴加KSCN溶液至过量,溶液呈红色。 |
| 方案Ⅱ | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b。取少量b,滴加盐酸,有Cl2产生。 |
ii.方案Ⅱ可证明K2FeO4氧化了Cl-。用KOH溶液洗涤的目的是
②根据K2FeO4的制备实验得出:氧化性Cl2
您最近一年使用:0次
2018-09-20更新
|
630次组卷
|
4卷引用:四川省内江市威远县威远中学2019届高三上学期第一次月考理科综合化学试题



