1 . 高铁酸钾(K2FeO4)是一种新型绿色、高效的水处理剂,对病毒的去除率可达99.95%。已知K2FeO4在低于常温的碱性环境中稳定,酸性条件下,其氧化性强于KMnO4、Cl2等。某小组设计制备K2FeO4并测定其纯度的实验步骤如下:
I.制备次氯酸钾。在搅拌和冰水浴条件下,将Cl2通入浓KOH溶液,同时补加一定量KOH,产生了大量白色沉淀,抽滤后得到浓KClO滤液。
II.制备高铁酸钾(装置如图)
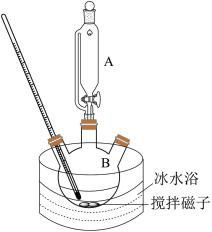
碱性条件下,向如图装置加入上述浓KClO 溶液与冰水浴磁子搅拌Fe(NO3)3;饱和溶液,反应一段时间,得到紫黑色溶液和大量白色沉淀,抽滤分离,用冰盐浴进一步冷却滤液得到K2FeO4粗品。
III.测定高铁酸钾样品的纯度。取0.300g上述步骤制备的K2FeO4样品于锥形瓶,在强碱性溶液中,用过量CrO2-与FeO42-反应生成 CrO42-和Fe(OH)3。稀硫酸酸化后加入指示剂,以0.150mol/L(NH)2Fe(SO4)2标准溶液滴定 Cr(VI)至 Cr3+,终点消耗 20.0mL。
(1)步骤I制备次氯酸钾的化学方程式为_____ ;“补加一定量KOH”的目的除了与过量Cl2继续反应生成更多KClO外,还在步骤II中起到___________ 的作用。
(2)根据 K2FeO4理论合成产率与合成条件响应曲面投影图(见图,虚线上的数据表示K2FeO4的理论合成产率),步骤II中控制的条件应是:温度______ (序号,下同),反应时间_____________ 。
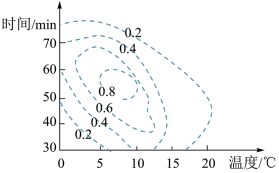
a.0.0~5.0℃ b.5.0~10℃ c.10~15℃ d.40~50 min e.50~60 min f.60~70 min
(3)步骤II中,为了避免副产物K3FeO4的产生,Fe(NO3)3饱和溶液应放在仪器A中,A的名称是________ ;写出实验刚开始时生成FeO42-的离子方程式________ 。
(4)根据步骤皿I的测定数据,计算高铁酸钾样品纯度为_____ (保留3位有效数字)。
(5)为探究酸性条件下FeO42-氧化性强弱,甲同学取步骤II所得K2FeO4粗品加入到少量盐酸中,观察到产生黄绿色气体,经检验气体为Cl2。该现象能否证明“酸性条件下FeO42-氧化性强于Cl2”,并说明理由_______________________________ 。
I.制备次氯酸钾。在搅拌和冰水浴条件下,将Cl2通入浓KOH溶液,同时补加一定量KOH,产生了大量白色沉淀,抽滤后得到浓KClO滤液。
II.制备高铁酸钾(装置如图)

碱性条件下,向如图装置加入上述浓KClO 溶液与冰水浴磁子搅拌Fe(NO3)3;饱和溶液,反应一段时间,得到紫黑色溶液和大量白色沉淀,抽滤分离,用冰盐浴进一步冷却滤液得到K2FeO4粗品。
III.测定高铁酸钾样品的纯度。取0.300g上述步骤制备的K2FeO4样品于锥形瓶,在强碱性溶液中,用过量CrO2-与FeO42-反应生成 CrO42-和Fe(OH)3。稀硫酸酸化后加入指示剂,以0.150mol/L(NH)2Fe(SO4)2标准溶液滴定 Cr(VI)至 Cr3+,终点消耗 20.0mL。
(1)步骤I制备次氯酸钾的化学方程式为
(2)根据 K2FeO4理论合成产率与合成条件响应曲面投影图(见图,虚线上的数据表示K2FeO4的理论合成产率),步骤II中控制的条件应是:温度

a.0.0~5.0℃ b.5.0~10℃ c.10~15℃ d.40~50 min e.50~60 min f.60~70 min
(3)步骤II中,为了避免副产物K3FeO4的产生,Fe(NO3)3饱和溶液应放在仪器A中,A的名称是
(4)根据步骤皿I的测定数据,计算高铁酸钾样品纯度为
(5)为探究酸性条件下FeO42-氧化性强弱,甲同学取步骤II所得K2FeO4粗品加入到少量盐酸中,观察到产生黄绿色气体,经检验气体为Cl2。该现象能否证明“酸性条件下FeO42-氧化性强于Cl2”,并说明理由
您最近一年使用:0次
解题方法
2 . I.高铁酸钠(Na2FeO4)是一种多功能、高效无毒的新型绿色水处理剂。
(1)Na2FeO4中铁元素的化合价是____ 价,Na2FeO4具有较强的____ (填“氧化性”或“还原性”)。
(2)工业上可用FeCl3、NaOH、NaClO三种物质在一定条件下反应制得Na2FeO4,完成下列化学方程式:____ 。
2FeCl3+10NaOH+3NaClO=2____+5____+9____
II.钒触媒(V2O5)是催化氧化所常用的催化剂,为综合利用,科研人员最新研制了一种离子交换法回收废钒的新工艺,回收率达90%以上。已知废钒催化剂中含有V2O5、VOSO4及不溶性残渣。查阅资料可知:VOSO4可溶于水,V2O5难溶于水,NH4VO3难溶于水。该工艺的流程如图。
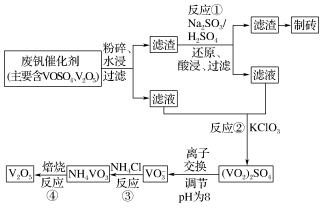
(3)水浸时,为了提高废钒的浸出率,除了粉碎,还可以采取的措施:____ 、____ (写出2条)。
(4)写出反应①的离子方程式____ 。
(5)该工艺中反应③的沉矾率是回收钒的关键,沉钒率的高低除受溶液pH影响外,还需要控制氯化铵系数(NH4Cl加入质量与料液中V2O5的质量比)和温度。根据如图建议最合适的氯化铵系数和温度:氯化铵系数为____ ,温度为____ 。
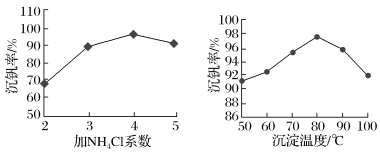
(6)写出“焙烧反应④”中由NH4VO3制备V2O5的化学方程式____ 。
(1)Na2FeO4中铁元素的化合价是
(2)工业上可用FeCl3、NaOH、NaClO三种物质在一定条件下反应制得Na2FeO4,完成下列化学方程式:
2FeCl3+10NaOH+3NaClO=2____+5____+9____
II.钒触媒(V2O5)是催化氧化所常用的催化剂,为综合利用,科研人员最新研制了一种离子交换法回收废钒的新工艺,回收率达90%以上。已知废钒催化剂中含有V2O5、VOSO4及不溶性残渣。查阅资料可知:VOSO4可溶于水,V2O5难溶于水,NH4VO3难溶于水。该工艺的流程如图。

(3)水浸时,为了提高废钒的浸出率,除了粉碎,还可以采取的措施:
(4)写出反应①的离子方程式
(5)该工艺中反应③的沉矾率是回收钒的关键,沉钒率的高低除受溶液pH影响外,还需要控制氯化铵系数(NH4Cl加入质量与料液中V2O5的质量比)和温度。根据如图建议最合适的氯化铵系数和温度:氯化铵系数为

(6)写出“焙烧反应④”中由NH4VO3制备V2O5的化学方程式
您最近一年使用:0次
名校
3 . 某小组同学探究不同条件下 与
与 的反应产物,设计的实验装置如图所示(夹持装置已省略)。
的反应产物,设计的实验装置如图所示(夹持装置已省略)。

已知:Ⅰ. 在一定条件下被
在一定条件下被 或
或 氧化成
氧化成 (棕黑色)、
(棕黑色)、 (绿色)、
(绿色)、 (紫色)。
(紫色)。
Ⅱ.浓碱条件下, 可与
可与 反应生成
反应生成 和
和 。
。
Ⅲ. 的氧化性与溶液的酸碱性无关,
的氧化性与溶液的酸碱性无关, 的氧化性随碱性增强而减弱。
的氧化性随碱性增强而减弱。
回答下列问题:
(1)仪器m的名称为___________ 。
(2)装置A中发生反应的化学方程式为___________ 。
(3)装置B中盛放的试剂为___________ 。
(4)装置D的作用为___________ 。
(5)根据表格推断,通入 前,实验Ⅱ、Ⅲ中产生的白色沉淀为
前,实验Ⅱ、Ⅲ中产生的白色沉淀为___________ (填化学式)。
(6)对比实验Ⅰ、Ⅱ通入 后的实验现象,在碱性条件下
后的实验现象,在碱性条件下___________ 能被 氧化为
氧化为___________ 。
(7)根据资料ⅱ,实验Ⅲ中应得到绿色溶液,但实验中得到紫色溶液,分析现象与资料不符的原因。
原因一:可能是通入 导致溶液的碱性减弱。
导致溶液的碱性减弱。
原因二:可能是氧化剂过量,氧化剂将 氧化为
氧化为 。
。
①用化学方程式表示可能导致溶液碱性减弱的原因:___________ 。
②取Ⅲ中放置后的1mL悬浊液,加入4mL40%NaOH溶液,紫色溶液迅速变为绿色,且绿色缓慢加深。溶液由紫色变为绿色的离子方程式为___________ ,溶液绿色缓慢加深,原因是 被
被___________ (填“化学式”)氧化,可证明Ⅲ的悬浊液中氧化剂过量。
 与
与 的反应产物,设计的实验装置如图所示(夹持装置已省略)。
的反应产物,设计的实验装置如图所示(夹持装置已省略)。
已知:Ⅰ.
 在一定条件下被
在一定条件下被 或
或 氧化成
氧化成 (棕黑色)、
(棕黑色)、 (绿色)、
(绿色)、 (紫色)。
(紫色)。Ⅱ.浓碱条件下,
 可与
可与 反应生成
反应生成 和
和 。
。Ⅲ.
 的氧化性与溶液的酸碱性无关,
的氧化性与溶液的酸碱性无关, 的氧化性随碱性增强而减弱。
的氧化性随碱性增强而减弱。| 实验 | 物质a | 装置C中实验现象 | |
通入 前 前 | 通入 后 后 | ||
| Ⅰ | 水 | 得到无色溶液 | 产生棕黑色沉淀,且放置后不发生变化 |
| Ⅱ | 5%NaOH溶液 | 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,但仍有棕黑色沉淀 |
| Ⅲ | 40%NaOH溶液 | 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,但仍有棕黑色沉淀 |
(1)仪器m的名称为
(2)装置A中发生反应的化学方程式为
(3)装置B中盛放的试剂为
(4)装置D的作用为
(5)根据表格推断,通入
 前,实验Ⅱ、Ⅲ中产生的白色沉淀为
前,实验Ⅱ、Ⅲ中产生的白色沉淀为(6)对比实验Ⅰ、Ⅱ通入
 后的实验现象,在碱性条件下
后的实验现象,在碱性条件下 氧化为
氧化为(7)根据资料ⅱ,实验Ⅲ中应得到绿色溶液,但实验中得到紫色溶液,分析现象与资料不符的原因。
原因一:可能是通入
 导致溶液的碱性减弱。
导致溶液的碱性减弱。原因二:可能是氧化剂过量,氧化剂将
 氧化为
氧化为 。
。①用化学方程式表示可能导致溶液碱性减弱的原因:
②取Ⅲ中放置后的1mL悬浊液,加入4mL40%NaOH溶液,紫色溶液迅速变为绿色,且绿色缓慢加深。溶液由紫色变为绿色的离子方程式为
 被
被
您最近一年使用:0次
2023-11-06更新
|
137次组卷
|
2卷引用:四川省泸县第一中学2023-2024学年高一上学期11月期中化学试题
名校
4 . 除第一周期外,关于同周期主族元素的下列变化规律的叙述中不正确的是
| A.从左到右,原子半径逐渐减小 |
| B.从左到右,元素原子的氧化性减弱,还原性增强 |
| C.从左到右,元素最高正价数从+1递增到+7,负价由-4递变到-1 |
| D.从左到右,元素最高价氧化物对应水化物碱性减弱,酸性增强 |
您最近一年使用:0次
2018-05-06更新
|
277次组卷
|
6卷引用:四川省内江市市中区天立学校2019-2020学年高一下学期第二次月考化学试题
四川省内江市市中区天立学校2019-2020学年高一下学期第二次月考化学试题【全国百强校】贵州省铜仁市第一中学2017-2018学年高一下学期期中考试化学试题黑龙江省绥滨县第一中学2018-2019学年高一(理)下学期期中考试化学试题湖南省常德市2019-2020学年高一上学期第一次月考化学试题贵州省铜仁市思南中学2019-2020学年高一下学期5月月考化学试题(已下线)【全国百强校】贵州省思南中学2018-2019学年2018-2019学年高一下学期期中考试化学试题
名校
5 . 下表是元素周期表的一部分。
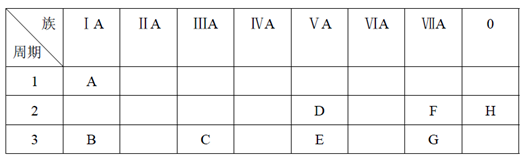
根据A~G元素在周期表中的位置,用化学式填写空白。
(1)氧化性最强的单质是______ ,还原性最强的单质是______ ,化学性质最不活泼的单质是______ 。(填相应的化学式)
(2)最稳定的氢化物是______ 。(填相应的化学式)
(3)一个E原子的核外电子总共有______ 种运动状态。
(4)按碱性逐渐减弱、酸性逐渐增强的顺序,将B、C、E、G四种元素的最高价氧化物对应水化物的化学式排列成序是_______ 。(填相应的化学式)

根据A~G元素在周期表中的位置,用化学式填写空白。
(1)氧化性最强的单质是
(2)最稳定的氢化物是
(3)一个E原子的核外电子总共有
(4)按碱性逐渐减弱、酸性逐渐增强的顺序,将B、C、E、G四种元素的最高价氧化物对应水化物的化学式排列成序是
您最近一年使用:0次
2018-05-28更新
|
555次组卷
|
2卷引用:【全国百强校】四川省南充高级中学2017-2018学年高二下学期期中化学试题
6 . 二氧化氯(ClO2)是一种黄绿色气体,易溶于水,在混合气体中的体积分数大于10%就可能发生爆炸,在工业上常用作水处理剂、漂白剂。回答下列问题:
(1)某小组通过查阅资料发现可以使用SO2和NaClO3反应的方法制备ClO2。写出该过程的离子方程式:______________ 。
(2)某小组按照文献中制备ClO2的方法设计了如图所示的实验装置用于制备ClO2。______ ,装置B中的试剂X为______ 。
②D装置通入氮气的主要作用有2个,一是可以起到搅拌作用,二是__________ 。
③装置D用于生成ClO2气体,该反应的化学方程式为___________ 。
(3)ClO2气体具有强氧化性,其还原产物 、Cl-的转化率与pH关系如图所示。ClO2对污水中S2-、CN-等也有明显的去除效果,请写出pH≥7时,ClO2与S2-反应的离子方程式
、Cl-的转化率与pH关系如图所示。ClO2对污水中S2-、CN-等也有明显的去除效果,请写出pH≥7时,ClO2与S2-反应的离子方程式_______ 。 =2I-+
=2I-+ ),当看到
),当看到____________ 现象时,测得标准液消耗的体积为20.00mL,通过计算可知D中ClO2溶液的浓度为_____ 。
(1)某小组通过查阅资料发现可以使用SO2和NaClO3反应的方法制备ClO2。写出该过程的离子方程式:
(2)某小组按照文献中制备ClO2的方法设计了如图所示的实验装置用于制备ClO2。
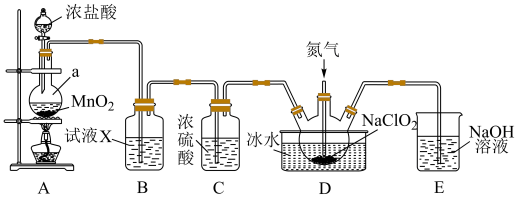
②D装置通入氮气的主要作用有2个,一是可以起到搅拌作用,二是
③装置D用于生成ClO2气体,该反应的化学方程式为
(3)ClO2气体具有强氧化性,其还原产物
 、Cl-的转化率与pH关系如图所示。ClO2对污水中S2-、CN-等也有明显的去除效果,请写出pH≥7时,ClO2与S2-反应的离子方程式
、Cl-的转化率与pH关系如图所示。ClO2对污水中S2-、CN-等也有明显的去除效果,请写出pH≥7时,ClO2与S2-反应的离子方程式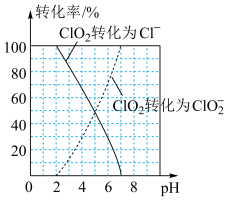
 =2I-+
=2I-+ ),当看到
),当看到
您最近一年使用:0次
7 . 氧化还原反应知识贯穿于中学化学教材,从初中阶段的简单了解,到高中基本理论知识,再到元素化合物部分的实际应用,再到化学电源本质的理解,再到有机化学中物质类型的变化关系,层层推进,高潮迭起。分析氧化还原反应常用双线桥法和单线桥法来表示电子转移的方向和数目。
I.在KClO3+6HCl=KCl+3Cl2↑+3H2O的反应中:
(1)请用单线桥 法标出电子转移的方向和数目________ ;
(2)该反应中,氧化产物与还原产物的物质的量之比为_____________ ;
(3)若生成 0.3 mol Cl2,则转移的电子的数目为________________ ;
II.已知硫化亚铁是一种黑色块状固体,在空气中煅烧时生成二氧化硫气体和烧渣;硫化亚铁常温下难溶于水,易溶于稀盐酸、稀硫酸而生成能溶于水的硫化氢气体。硫化亚铁与浓硫酸加热条件下,可发生反应:2FeS+6H2SO4(浓) Fe2(SO4)3+3SO2↑ +2S+6H2O:
Fe2(SO4)3+3SO2↑ +2S+6H2O:
(4)请用双线桥 法标出电子转移的方向和数目_______ 。
(5)H2SO4在该反应中显示出来的性质是___________ ;(填序号)
A.氧化性 B.还原性 C.酸性 D.碱性
(6)该反应中,氧化产物是________________ 。
I.在KClO3+6HCl=KCl+3Cl2↑+3H2O的反应中:
(1)请用
(2)该反应中,氧化产物与还原产物的物质的量之比为
(3)若生成 0.3 mol Cl2,则转移的电子的数目为
II.已知硫化亚铁是一种黑色块状固体,在空气中煅烧时生成二氧化硫气体和烧渣;硫化亚铁常温下难溶于水,易溶于稀盐酸、稀硫酸而生成能溶于水的硫化氢气体。硫化亚铁与浓硫酸加热条件下,可发生反应:2FeS+6H2SO4(浓)
 Fe2(SO4)3+3SO2↑ +2S+6H2O:
Fe2(SO4)3+3SO2↑ +2S+6H2O:(4)请用
(5)H2SO4在该反应中显示出来的性质是
A.氧化性 B.还原性 C.酸性 D.碱性
(6)该反应中,氧化产物是
您最近一年使用:0次
名校
解题方法
8 . 高铁酸钾(K2FeO4,极易溶于水)是常见的水处理剂,其原理如图所示。
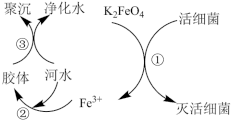
【查阅资料】向胶体中加入电解质后,胶体因失去稳定性而发生离子的聚集以至沉淀,称为电解质对胶体的聚沉作用,简称胶体的聚沉。
请回答下列问题:
(1) 中铁元素的化合价为
中铁元素的化合价为_______ 。
(2)过程①中活性菌表现了_______ (填“氧化”或“还原”)性;过程③属于______ (填“物理”或“化学”)变化。
(3)根据上述原理分析,作水处理剂时, 的作用有
的作用有________ 、_________ (填两个)。
(4)制备高铁酸钾常用的反应原理为 (未配平)。
(未配平)。
①通过该反应说明:在碱性条件下,氧化性:
_______ (填“>”、“=”或“<”) 。
。
②配平该反应的化学方程式,并用双线桥法表示电子转移的方向和数目:_______ 。

【查阅资料】向胶体中加入电解质后,胶体因失去稳定性而发生离子的聚集以至沉淀,称为电解质对胶体的聚沉作用,简称胶体的聚沉。
请回答下列问题:
(1)
 中铁元素的化合价为
中铁元素的化合价为(2)过程①中活性菌表现了
(3)根据上述原理分析,作水处理剂时,
 的作用有
的作用有(4)制备高铁酸钾常用的反应原理为
 (未配平)。
(未配平)。①通过该反应说明:在碱性条件下,氧化性:

 。
。②配平该反应的化学方程式,并用双线桥法表示电子转移的方向和数目:
您最近一年使用:0次
2022-12-17更新
|
163次组卷
|
2卷引用:四川省绵阳市东辰学校2022-2023学年高一上学期期末模拟化学试卷
名校
9 . 硫脲 是一种杀菌剂。某小组设计实验制备硫脲并探究其性质。
是一种杀菌剂。某小组设计实验制备硫脲并探究其性质。
实验(一):制备硫脲。装置如图所示(加热装置已省略)。

已知:① ;
;
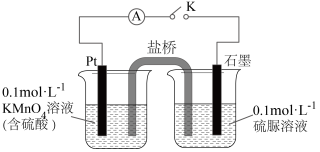
②25℃时硫脲溶解度为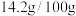 水;
水;
③实验室常用FeS与稀 在常温下制
在常温下制 。
。
(1)盛放石灰乳的仪器的名称是_______ ,B的加热方式宜选择_______ (填标号)。
a.直接用酒精灯加热 b.油浴加热(100~250℃) c.热水浴加热
(2)当C装置中出现_______ (填实验现象)时表明B中生成了 。
。
(3)实验发现,硫脲产率与投料比 的关系如图所示。
的关系如图所示。
最佳投料比为_______ 。
实验(二):探究硫脲的性质。
资料显示:①150℃时 转化成
转化成 。
。
②酸性 溶液和硫脲反应,还原产物为
溶液和硫脲反应,还原产物为 ,氧化产物为
,氧化产物为 和
和 。
。
(4)取少量 溶于水,加热至150℃,一段时间后再冷却至室温时,滴加
溶于水,加热至150℃,一段时间后再冷却至室温时,滴加_______ ,可检验是否有 生成。
生成。
(5)取少量 溶于NaOH溶液,加入
溶于NaOH溶液,加入 溶液,过滤、洗涤,得到黑色固体,由此推知,
溶液,过滤、洗涤,得到黑色固体,由此推知, 在碱性条件下会生成
在碱性条件下会生成_______ (填离子符号)。
(6)甲同学取少量 溶于水,滴加几滴酸性
溶于水,滴加几滴酸性 溶液,振荡,溶液褪色;再滴加
溶液,振荡,溶液褪色;再滴加 和盐酸溶液,产生白色沉淀。
和盐酸溶液,产生白色沉淀。
①乙同学认为甲同学的实验不能证明生成了 ,理由是
,理由是_______ 。
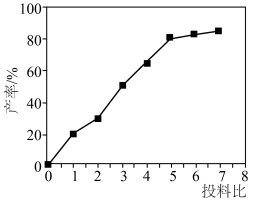
②乙同学设计如图装置验证氧化产物中含有 。
。
关闭K,发现电流计指针偏转。一段时间后,左烧杯中酸性高锰酸钾溶液褪色。铂电极上的反应式为_______ ,经检验石墨电极附近还有 和
和 生成,总反应的离子方程式为
生成,总反应的离子方程式为_______ 。
 是一种杀菌剂。某小组设计实验制备硫脲并探究其性质。
是一种杀菌剂。某小组设计实验制备硫脲并探究其性质。实验(一):制备硫脲。装置如图所示(加热装置已省略)。

已知:①
 ;
;②25℃时硫脲溶解度为
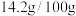 水;
水;③实验室常用FeS与稀
 在常温下制
在常温下制 。
。(1)盛放石灰乳的仪器的名称是
a.直接用酒精灯加热 b.油浴加热(100~250℃) c.热水浴加热
(2)当C装置中出现
 。
。(3)实验发现,硫脲产率与投料比
 的关系如图所示。
的关系如图所示。
最佳投料比为
实验(二):探究硫脲的性质。
资料显示:①150℃时
 转化成
转化成 。
。②酸性
 溶液和硫脲反应,还原产物为
溶液和硫脲反应,还原产物为 ,氧化产物为
,氧化产物为 和
和 。
。(4)取少量
 溶于水,加热至150℃,一段时间后再冷却至室温时,滴加
溶于水,加热至150℃,一段时间后再冷却至室温时,滴加 生成。
生成。(5)取少量
 溶于NaOH溶液,加入
溶于NaOH溶液,加入 溶液,过滤、洗涤,得到黑色固体,由此推知,
溶液,过滤、洗涤,得到黑色固体,由此推知, 在碱性条件下会生成
在碱性条件下会生成(6)甲同学取少量
 溶于水,滴加几滴酸性
溶于水,滴加几滴酸性 溶液,振荡,溶液褪色;再滴加
溶液,振荡,溶液褪色;再滴加 和盐酸溶液,产生白色沉淀。
和盐酸溶液,产生白色沉淀。①乙同学认为甲同学的实验不能证明生成了
 ,理由是
,理由是②乙同学设计如图装置验证氧化产物中含有
 。
。
关闭K,发现电流计指针偏转。一段时间后,左烧杯中酸性高锰酸钾溶液褪色。铂电极上的反应式为
 和
和 生成,总反应的离子方程式为
生成,总反应的离子方程式为
您最近一年使用:0次
2024-04-01更新
|
240次组卷
|
2卷引用:四川省雅安市雅安中学等校联考2023-2024学年高三下学期开学考试理综试题-高中化学
名校
10 . 食品容易被空气氧化而变质,放在装有月饼的袋子里常放有干燥剂及铁粉,这是利月了铁粉的
| A.酸性 | B.碱性 | C.氧化性 | D.还原性 |
您最近一年使用:0次
2017-12-12更新
|
291次组卷
|
9卷引用:四川省雅安市2019-2020学年高一上学期期末检测化学试题
四川省雅安市2019-2020学年高一上学期期末检测化学试题四川省眉山市仁寿第二中学等四校2020-2021学年高一上学期12月月考化学试题辽宁省葫芦岛市六校协作体2017-2018学年高一12月考化学试题内蒙古自治区巴彦淖尔市临河区第三中学2018-2019学年高一上学期第二次月考化学试题广西北海市北海中学2019-2020学年高一上学期期末考试化学试题海南省海南枫叶国际学校2019-2020学年高一上学期期末考试化学试题陕西省武功县普集高级中学2021-2022学年高一上学期第二次月考化学试题广西北海市2019-2020学年高一上学期期末教学质量测查化学试题湖南省邵阳市隆回县2022-2023学年高一上学期期末考试化学试题



