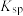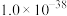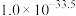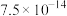名校
解题方法
1 . 工业上以方铅矿( ,含少量
,含少量 和软锰矿
和软锰矿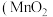 ,含少量
,含少量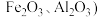 为原料,制备
为原料,制备 和
和 的工艺流程如图所示。
的工艺流程如图所示。 难溶于冷水,易溶于热水;
难溶于冷水,易溶于热水;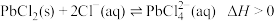
②常温下,某些难溶物质的 如下表:
如下表:
回答下列问题:
(1)方铅矿和软锰矿预先粉碎的目的是_____________ ;“热浸取”时, 参与反应的离子方程式为
参与反应的离子方程式为__________________________ 。
(2)“操作X”是_____________ ;若溶液中 的浓度为
的浓度为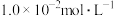 ,则“调
,则“调 ”的范围是
”的范围是_____________ (当离子浓度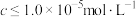 时,可认为该离子沉淀完全;忽略溶液体积变化)。
时,可认为该离子沉淀完全;忽略溶液体积变化)。
(3)“转化”过程中反应能够发生的原因是_______________________ ;“滤液”可循环使用,应当将其导入到____________ 操作中(填操作单元的名称)。
(4)“沉锰”过程中发生反应的离子方程式为____________________________________ 。
 ,含少量
,含少量 和软锰矿
和软锰矿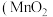 ,含少量
,含少量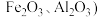 为原料,制备
为原料,制备 和
和 的工艺流程如图所示。
的工艺流程如图所示。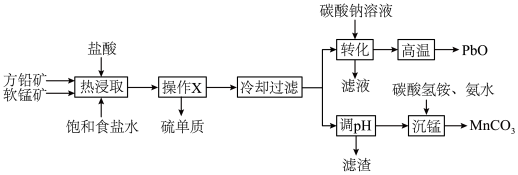
 难溶于冷水,易溶于热水;
难溶于冷水,易溶于热水;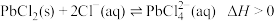
②常温下,某些难溶物质的
 如下表:
如下表:物质 |
|
|
|
|
|
|
|
|
|
|
|
(1)方铅矿和软锰矿预先粉碎的目的是
 参与反应的离子方程式为
参与反应的离子方程式为(2)“操作X”是
 的浓度为
的浓度为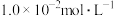 ,则“调
,则“调 ”的范围是
”的范围是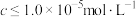 时,可认为该离子沉淀完全;忽略溶液体积变化)。
时,可认为该离子沉淀完全;忽略溶液体积变化)。(3)“转化”过程中反应能够发生的原因是
(4)“沉锰”过程中发生反应的离子方程式为
您最近一年使用:0次
解题方法
2 .  是有毒的污染性气体,可将其与氧气的混合气体通入
是有毒的污染性气体,可将其与氧气的混合气体通入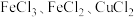 的混合溶液中进行处理,其物质转化如图所示。下列说法正确的是
的混合溶液中进行处理,其物质转化如图所示。下列说法正确的是
 是有毒的污染性气体,可将其与氧气的混合气体通入
是有毒的污染性气体,可将其与氧气的混合气体通入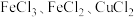 的混合溶液中进行处理,其物质转化如图所示。下列说法正确的是
的混合溶液中进行处理,其物质转化如图所示。下列说法正确的是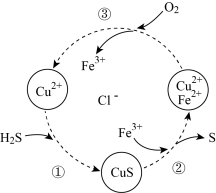
| A.过程①中发生的反应是复分解反应 |
B.过程②中每生成 转移 转移 个电子 个电子 |
C.过程③中每转化 ,需 ,需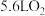 |
D.总反应为 |
您最近一年使用:0次
解题方法
3 . 从某铋(Bi)、锌的冶炼厂的高铟烟灰(主要含ZnO、 、
、 、
、 、
、 )中提取铟和铋的流程如图:
)中提取铟和铋的流程如图:
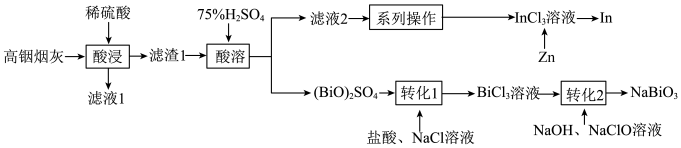
已知: 不溶于稀硫酸;
不溶于稀硫酸; 难溶于水。
难溶于水。
回答下列问题:
(1)“滤液1”中含有的金属阳离子有_______ (填离子符号)。
(2)“酸浸”过程中使用稀硫酸而不用75%的) 溶液,其原因是
溶液,其原因是_______ 。
(3)“酸溶”生成的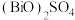 中,Bi元素的化合价为
中,Bi元素的化合价为_______ 。
(4)“转化2”时发生反应的化学方程式为_______ 。
(5)“系列操作”的流程如下:
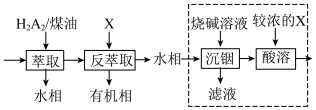
已知:“萃取”时发生反应: (金属阳离子)
(金属阳离子)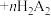 (有机液)
(有机液) (有机液)
(有机液)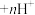 ;
; 与
与 相似,易水解。
相似,易水解。
①试剂X的名称为_______ ,“萃取”和“反萃取”的目的是_______ 。
②关于虚线框内的实验步骤,下列说法正确的是_______ (填标号)。
A.可以提高 溶液的浓度
溶液的浓度
B.烧碱溶液可用纯碱溶液代替
C.需用到分液漏斗、烧杯、玻璃棒等仪器
(6)akg的高铟烟灰经上述流程后,得到 质量分数为w的产品bg,则高铟烟灰中Bi的百分含量为
质量分数为w的产品bg,则高铟烟灰中Bi的百分含量为_______ (用含a、b、w的计算式表示)。
 、
、 、
、 、
、 )中提取铟和铋的流程如图:
)中提取铟和铋的流程如图:
已知:
 不溶于稀硫酸;
不溶于稀硫酸; 难溶于水。
难溶于水。回答下列问题:
(1)“滤液1”中含有的金属阳离子有
(2)“酸浸”过程中使用稀硫酸而不用75%的)
 溶液,其原因是
溶液,其原因是(3)“酸溶”生成的
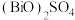 中,Bi元素的化合价为
中,Bi元素的化合价为(4)“转化2”时发生反应的化学方程式为
(5)“系列操作”的流程如下:

已知:“萃取”时发生反应:
 (金属阳离子)
(金属阳离子)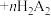 (有机液)
(有机液) (有机液)
(有机液)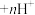 ;
; 与
与 相似,易水解。
相似,易水解。①试剂X的名称为
②关于虚线框内的实验步骤,下列说法正确的是
A.可以提高
 溶液的浓度
溶液的浓度B.烧碱溶液可用纯碱溶液代替
C.需用到分液漏斗、烧杯、玻璃棒等仪器
(6)akg的高铟烟灰经上述流程后,得到
 质量分数为w的产品bg,则高铟烟灰中Bi的百分含量为
质量分数为w的产品bg,则高铟烟灰中Bi的百分含量为
您最近一年使用:0次
解题方法
4 . 根据下列实验操作及现象,所得结论或解释正确的是
| 选项 | 实验操作和现象 | 结论或解释 |
| A | 将 和另一气体的混合物通入 和另一气体的混合物通入 溶液中,产生白色沉淀 溶液中,产生白色沉淀 | 白色沉淀为 |
| B | 向盛有 和 和 的试管中分别滴加浓盐酸,盛 的试管中分别滴加浓盐酸,盛 的试管中产生黄绿色气体 的试管中产生黄绿色气体 | 氧化性: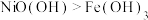 |
| C | 取久置的 粉末,向其中滴加过量的盐酸,得到的气体使澄清石灰水变浑浊 粉末,向其中滴加过量的盐酸,得到的气体使澄清石灰水变浑浊 |  粉末完全变质 粉末完全变质 |
| D | 取两份新制氯水,分别滴加 溶液和淀粉KI溶液,前者有白色沉淀,后者溶液变蓝色 溶液和淀粉KI溶液,前者有白色沉淀,后者溶液变蓝色 | 氯气与水的反应存在限度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 .  为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.1.8g甲基 中含有的中子数目为 中含有的中子数目为 |
B. 与足量Fe反应,转移的电子数目为 与足量Fe反应,转移的电子数目为 |
C. 和 和 的混合气体22g中,含原子总数目为 的混合气体22g中,含原子总数目为 |
D. 与Na反应生成2.24L 与Na反应生成2.24L ,断裂和生成的共价键数目共 ,断裂和生成的共价键数目共 |
您最近一年使用:0次
名校
6 . 某白色粉末由两种物质组成,对其进行如下实验。
①取少量白色粉末加入足量水充分溶解,过滤并洗涤得到滤液和滤渣;
②取少量①的滤液,加入 溶液,有白色沉淀;
溶液,有白色沉淀;
③取少量①的滤渣,加入稀盐酸,滤渣溶解得无色溶液,同时有无色无味气体产生。
该白色粉末中可能存在的是
①取少量白色粉末加入足量水充分溶解,过滤并洗涤得到滤液和滤渣;
②取少量①的滤液,加入
 溶液,有白色沉淀;
溶液,有白色沉淀;③取少量①的滤渣,加入稀盐酸,滤渣溶解得无色溶液,同时有无色无味气体产生。
该白色粉末中可能存在的是
A. 、 、 | B.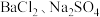 |
C.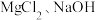 | D.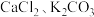 |
您最近一年使用:0次
2024-03-12更新
|
129次组卷
|
3卷引用:四川省德阳市什邡中学2023-2024学年高一下学期3月月考化学试题
名校
解题方法
7 . 利用固体表面催化工艺进行NO分解的过程如图所示,下列说法不正确的是

| A.NO属于共价化合物 |
| B.O2含有非极性共价键 |
| C.过程②释放能量,过程③吸收能量 |
| D.标准状况下,NO 分解生成11.2LN2转移电子数约为2NA |
您最近一年使用:0次
2024-02-25更新
|
881次组卷
|
3卷引用:四川省德阳市什邡中学2023-2024学年高一下学期3月月考化学试题
解题方法
8 . 废旧金属的综合利用有利于节约资源、保护环境。工业上以赤铁矿(主要含 ,还含少量
,还含少量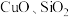 等杂质)为原料,制备
等杂质)为原料,制备 、回收
、回收 的工艺流程如下:
的工艺流程如下:
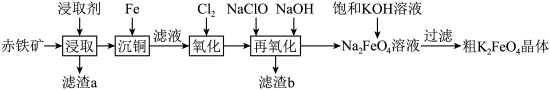
已知: 为难溶于盐酸、易溶于
为难溶于盐酸、易溶于 溶液的固体。
溶液的固体。
(1)“浸取”的方式为_________ (填“酸浸”“碱浸”或“水浸”)。
(2)“沉铜”过程中,发生还原反应的物质为_______ (填化学式)。
(3)“再氧化”中需要配制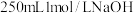 溶液。实验中除了量筒、烧杯、玻璃棒之外,还需要的玻璃仪器有
溶液。实验中除了量筒、烧杯、玻璃棒之外,还需要的玻璃仪器有______ ;“再氧化”制备 的离子方程式为:
的离子方程式为: ,
, 的名称为
的名称为______ ,X、Y代表的粒子符号依次为_______ 。
(4) 可将氨氮废水中的
可将氨氮废水中的 转化为
转化为 。从价态角度分析,
。从价态角度分析, 能处理氨氮废水的原因是
能处理氨氮废水的原因是________ 。
(5)“氧化”后,利用色度传感器测定其对光的透过率或者吸收率,颜色越深,吸收率越高。已知不同浓度 的标准液吸收率如下图。
的标准液吸收率如下图。
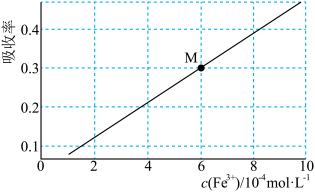
取 “氧化”后的溶液,稀释至
“氧化”后的溶液,稀释至 ,测得吸收率为上图中
,测得吸收率为上图中 点,则
点,则 该溶液中含铁元素的质量为
该溶液中含铁元素的质量为_____  ;已知色度传感器测定准确,实验制备的粗
;已知色度传感器测定准确,实验制备的粗 中铁元素质量偏低,其原因可能为
中铁元素质量偏低,其原因可能为___________ (任意回答一条原因)。
 ,还含少量
,还含少量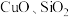 等杂质)为原料,制备
等杂质)为原料,制备 、回收
、回收 的工艺流程如下:
的工艺流程如下:
已知:
 为难溶于盐酸、易溶于
为难溶于盐酸、易溶于 溶液的固体。
溶液的固体。(1)“浸取”的方式为
(2)“沉铜”过程中,发生还原反应的物质为
(3)“再氧化”中需要配制
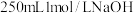 溶液。实验中除了量筒、烧杯、玻璃棒之外,还需要的玻璃仪器有
溶液。实验中除了量筒、烧杯、玻璃棒之外,还需要的玻璃仪器有 的离子方程式为:
的离子方程式为: ,
, 的名称为
的名称为(4)
 可将氨氮废水中的
可将氨氮废水中的 转化为
转化为 。从价态角度分析,
。从价态角度分析, 能处理氨氮废水的原因是
能处理氨氮废水的原因是(5)“氧化”后,利用色度传感器测定其对光的透过率或者吸收率,颜色越深,吸收率越高。已知不同浓度
 的标准液吸收率如下图。
的标准液吸收率如下图。
取
 “氧化”后的溶液,稀释至
“氧化”后的溶液,稀释至 ,测得吸收率为上图中
,测得吸收率为上图中 点,则
点,则 该溶液中含铁元素的质量为
该溶液中含铁元素的质量为 ;已知色度传感器测定准确,实验制备的粗
;已知色度传感器测定准确,实验制备的粗 中铁元素质量偏低,其原因可能为
中铁元素质量偏低,其原因可能为
您最近一年使用:0次
解题方法
9 . 纳米 在生物医学等方面具有广泛的用途。利用废旧镀锌铁皮(含
在生物医学等方面具有广泛的用途。利用废旧镀锌铁皮(含 、
、 、
、 、
、 )制备纳米
)制备纳米 及副产物
及副产物 的流程如下:
的流程如下:
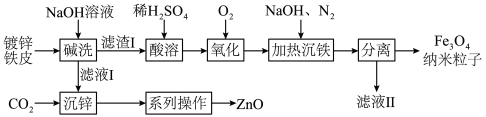
查阅资料: 、
、 、
、 的化学性质与铝及其化合物类似。
的化学性质与铝及其化合物类似。
回答下列问题:
(1)“碱洗”时, 溶液的作用是
溶液的作用是___________________ 。
(2)“沉锌”时,选用 而不用盐酸的依据是
而不用盐酸的依据是___________________ ,该反应的离子方程式为__________________________ 。
(3)“系列操作”包括过滤、____________ 。
(4)“氧化”后的溶液中所含金属阳离子有________________________ (填离子符号)。
(5)文献表明,若“氧化”时,溶液 过低,
过低, 容易转化为
容易转化为 ,该反应的化学方程式为
,该反应的化学方程式为_______________________ 。
(6)检验“分离”得到的 是否洗净的操作为
是否洗净的操作为______________________ 。
(7)某化学兴趣小组用 废旧镀锌铁皮(
废旧镀锌铁皮( 元素的质量分数为
元素的质量分数为 )制备纳米
)制备纳米 ,最终得到
,最终得到 产品,则产率为
产品,则产率为______ (保留三位有效数字)。
 在生物医学等方面具有广泛的用途。利用废旧镀锌铁皮(含
在生物医学等方面具有广泛的用途。利用废旧镀锌铁皮(含 、
、 、
、 、
、 )制备纳米
)制备纳米 及副产物
及副产物 的流程如下:
的流程如下:
查阅资料:
 、
、 、
、 的化学性质与铝及其化合物类似。
的化学性质与铝及其化合物类似。回答下列问题:
(1)“碱洗”时,
 溶液的作用是
溶液的作用是(2)“沉锌”时,选用
 而不用盐酸的依据是
而不用盐酸的依据是(3)“系列操作”包括过滤、
(4)“氧化”后的溶液中所含金属阳离子有
(5)文献表明,若“氧化”时,溶液
 过低,
过低, 容易转化为
容易转化为 ,该反应的化学方程式为
,该反应的化学方程式为(6)检验“分离”得到的
 是否洗净的操作为
是否洗净的操作为(7)某化学兴趣小组用
 废旧镀锌铁皮(
废旧镀锌铁皮( 元素的质量分数为
元素的质量分数为 )制备纳米
)制备纳米 ,最终得到
,最终得到 产品,则产率为
产品,则产率为
您最近一年使用:0次
10 .  常用于制钡盐和立德粉,也作橡胶硫化剂。实验室利用下图装置探究制取
常用于制钡盐和立德粉,也作橡胶硫化剂。实验室利用下图装置探究制取 时气体产物的成分(夹持仪器略去),并测定固体产品的纯度。
时气体产物的成分(夹持仪器略去),并测定固体产品的纯度。
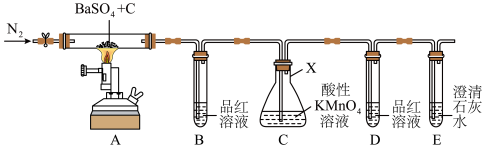
(1)仪器 的名称为
的名称为____________ 。
(2)一段时间后, 中品红溶液褪色,
中品红溶液褪色, 中溶液颜色变淡,
中溶液颜色变淡, 、
、 中无明显现象,则实验生成的气体为
中无明显现象,则实验生成的气体为____________ (填化学式),装置 中发生反应的离子方程式是
中发生反应的离子方程式是____________________________________ 。
(3)该装置的明显缺陷是____________________________________ 。
(4)测定 样品纯度的实验步骤如下:
样品纯度的实验步骤如下:
Ⅰ.称取 样品,加水溶解,配制成
样品,加水溶解,配制成 溶液;
溶液;
Ⅱ.取一锥形瓶,向其中加入 醋酸溶液、
醋酸溶液、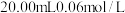 碘溶液、
碘溶液、 Ⅰ中所配制的溶液,待其充分反应(硫元素完全转化为硫单质);
Ⅰ中所配制的溶液,待其充分反应(硫元素完全转化为硫单质);
Ⅲ.向充分反应后的溶液中,加入 滴淀粉溶液,用
滴淀粉溶液,用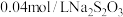 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 溶液
溶液 (
( )。
)。
①滴定终点时的现象为____________________________________________________________ 。
②样品中 的纯度为
的纯度为____________  (保留三位有效数字)。
(保留三位有效数字)。
③下列情况会导致测定 的纯度偏小的是
的纯度偏小的是____________ (填标号)。
a.称量样品时,发生了潮解
b.配制 溶液时,未洗涤烧杯
溶液时,未洗涤烧杯
c.达滴定终点时,俯视读数
 常用于制钡盐和立德粉,也作橡胶硫化剂。实验室利用下图装置探究制取
常用于制钡盐和立德粉,也作橡胶硫化剂。实验室利用下图装置探究制取 时气体产物的成分(夹持仪器略去),并测定固体产品的纯度。
时气体产物的成分(夹持仪器略去),并测定固体产品的纯度。
(1)仪器
 的名称为
的名称为(2)一段时间后,
 中品红溶液褪色,
中品红溶液褪色, 中溶液颜色变淡,
中溶液颜色变淡, 、
、 中无明显现象,则实验生成的气体为
中无明显现象,则实验生成的气体为 中发生反应的离子方程式是
中发生反应的离子方程式是(3)该装置的明显缺陷是
(4)测定
 样品纯度的实验步骤如下:
样品纯度的实验步骤如下:Ⅰ.称取
 样品,加水溶解,配制成
样品,加水溶解,配制成 溶液;
溶液;Ⅱ.取一锥形瓶,向其中加入
 醋酸溶液、
醋酸溶液、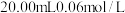 碘溶液、
碘溶液、 Ⅰ中所配制的溶液,待其充分反应(硫元素完全转化为硫单质);
Ⅰ中所配制的溶液,待其充分反应(硫元素完全转化为硫单质);Ⅲ.向充分反应后的溶液中,加入
 滴淀粉溶液,用
滴淀粉溶液,用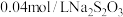 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 溶液
溶液 (
( )。
)。①滴定终点时的现象为
②样品中
 的纯度为
的纯度为 (保留三位有效数字)。
(保留三位有效数字)。③下列情况会导致测定
 的纯度偏小的是
的纯度偏小的是a.称量样品时,发生了潮解
b.配制
 溶液时,未洗涤烧杯
溶液时,未洗涤烧杯c.达滴定终点时,俯视读数
您最近一年使用:0次