2011·江苏·高考真题
1 . 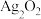 是银锌碱性电池的正极活性物质,可通过下列方法制备:在
是银锌碱性电池的正极活性物质,可通过下列方法制备:在 溶液中加入适量
溶液中加入适量 溶液,生成
溶液,生成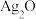 沉淀,保持反应温度为80
沉淀,保持反应温度为80 ,边搅拌边将一定量
,边搅拌边将一定量 溶液缓慢加到上述混合物中,反应完全后,过滤、洗涤、真空干燥得到固体样品。反应方程式为2AgNO3+ 4KOH+K2S2O8
溶液缓慢加到上述混合物中,反应完全后,过滤、洗涤、真空干燥得到固体样品。反应方程式为2AgNO3+ 4KOH+K2S2O8 Ag2O2↓+ 2KNO3+ 2K2SO4+ 2H2O。
Ag2O2↓+ 2KNO3+ 2K2SO4+ 2H2O。
回答下列问题:
(1)上述制备过程中,检验洗涤是否完全的方法是___________ 。
(2)银锌碱性电池的电解质溶液为 溶液,电池放电时正极的
溶液,电池放电时正极的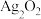 转化为
转化为 ,负极的
,负极的 转化为
转化为 ,写出该电池反应方程式:
,写出该电池反应方程式:___________ 。
(3)准确称取上述制备的样品(设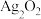 仅含和
仅含和 )2.558g,在一定的条件下完全分解为
)2.558g,在一定的条件下完全分解为 和
和 ,得到224.0mL
,得到224.0mL (标准状况下)。计算样品中
(标准状况下)。计算样品中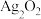 的质量分数
的质量分数_____ (计算结果精确到小数点后两位)。
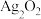 是银锌碱性电池的正极活性物质,可通过下列方法制备:在
是银锌碱性电池的正极活性物质,可通过下列方法制备:在 溶液中加入适量
溶液中加入适量 溶液,生成
溶液,生成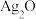 沉淀,保持反应温度为80
沉淀,保持反应温度为80 ,边搅拌边将一定量
,边搅拌边将一定量 溶液缓慢加到上述混合物中,反应完全后,过滤、洗涤、真空干燥得到固体样品。反应方程式为2AgNO3+ 4KOH+K2S2O8
溶液缓慢加到上述混合物中,反应完全后,过滤、洗涤、真空干燥得到固体样品。反应方程式为2AgNO3+ 4KOH+K2S2O8 Ag2O2↓+ 2KNO3+ 2K2SO4+ 2H2O。
Ag2O2↓+ 2KNO3+ 2K2SO4+ 2H2O。回答下列问题:
(1)上述制备过程中,检验洗涤是否完全的方法是
(2)银锌碱性电池的电解质溶液为
 溶液,电池放电时正极的
溶液,电池放电时正极的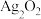 转化为
转化为 ,负极的
,负极的 转化为
转化为 ,写出该电池反应方程式:
,写出该电池反应方程式:(3)准确称取上述制备的样品(设
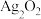 仅含和
仅含和 )2.558g,在一定的条件下完全分解为
)2.558g,在一定的条件下完全分解为 和
和 ,得到224.0mL
,得到224.0mL (标准状况下)。计算样品中
(标准状况下)。计算样品中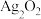 的质量分数
的质量分数
您最近半年使用:0次
2016-12-09更新
|
1391次组卷
|
4卷引用:2012-2013学年陕西省西安市第一中学高二上学期期末考试理科化学卷
(已下线)2012-2013学年陕西省西安市第一中学高二上学期期末考试理科化学卷2011年普通高等学校招生全国统一考试化学卷(江苏)(已下线)2014-2015学年河南省南阳市新野三中上学期10月月考高二化学试卷【全国百强校】湖南师范大学附属中学2017-2018学年高一下学期期末考试化学试题
2011·陕西·模拟预测
解题方法
2 . 完成下列各题:
⑴K2Cr2O7(橙色)、Cr2(SO4)3(绿色)、K2SO4、H2SO4、C2H5OH、CH3COOH和H2O分别属于同一氧化还原反应中的反应物和生成物,该反应原理可以用于检查司机是否酒后开车。
①若司机酒后开车,检测仪器内物质显示出______________ 色。
②写出并配平该反应的化学方程式:________________ 。
③如果在反应中生成1mol氧化产物,转移的电子总数为_______________________ 。
⑵在汽车上安装三效催化转化器,可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染。
已知:N2(g)+ O2(g)=2NO(g) △H=+180.5 kJ/mol
2C(s)+ O2(g)=2CO(g) △H=-221.0 kJ/mol
C(s)+ O2(g)=CO2(g) △H=-393.5 kJ/mol
①尾气转化的反应之一:2NO(g)+2CO(g)=N2(g)+2CO2(g) △H =___________ 。
②为了提高尾气转化的反应的速率和NO的转化率,采取的正确措施为_________ 。
A.加催化剂同时升高温度 B.加催化剂同时增大压强
C.升高温度同时充入N2 D.降低温度同时增大压强
③该反应达到平衡时若增大压强,则混合气体的平均相对分子质量___________ ,若升高温度,则该反应的平衡常数____________ (均填“增大”、“减小”或“不变”)。
⑶已知NH4A溶液为中性,又知将HA溶液加到Na2CO3溶液中有气体放出,试推断:①(NH4)2CO3溶液的pH____________ 7(填<、>、=)。
②相同温度下,等物质的量浓度的下列四种盐溶液按pH由大到小的排列顺序为____________ 。(填序号)
a.NH4HCO3 b.NH4A c.(NH4)2CO3 d.NH4Cl
⑴K2Cr2O7(橙色)、Cr2(SO4)3(绿色)、K2SO4、H2SO4、C2H5OH、CH3COOH和H2O分别属于同一氧化还原反应中的反应物和生成物,该反应原理可以用于检查司机是否酒后开车。
①若司机酒后开车,检测仪器内物质显示出
②写出并配平该反应的化学方程式:
③如果在反应中生成1mol氧化产物,转移的电子总数为
⑵在汽车上安装三效催化转化器,可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染。
已知:N2(g)+ O2(g)=2NO(g) △H=+180.5 kJ/mol
2C(s)+ O2(g)=2CO(g) △H=-221.0 kJ/mol
C(s)+ O2(g)=CO2(g) △H=-393.5 kJ/mol
①尾气转化的反应之一:2NO(g)+2CO(g)=N2(g)+2CO2(g) △H =
②为了提高尾气转化的反应的速率和NO的转化率,采取的正确措施为
A.加催化剂同时升高温度 B.加催化剂同时增大压强
C.升高温度同时充入N2 D.降低温度同时增大压强
③该反应达到平衡时若增大压强,则混合气体的平均相对分子质量
⑶已知NH4A溶液为中性,又知将HA溶液加到Na2CO3溶液中有气体放出,试推断:①(NH4)2CO3溶液的pH
②相同温度下,等物质的量浓度的下列四种盐溶液按pH由大到小的排列顺序为
a.NH4HCO3 b.NH4A c.(NH4)2CO3 d.NH4Cl
您最近半年使用:0次
2011·陕西西安·三模
解题方法
3 . 各物质之间的转化关系如下图,图中部分生成物省略,有相关信息如下:
①X为红褐色沉淀;②A为单质,B为溶液,D和F为气体;③反应I的产物只有Y和H O;
O;
④B、D、F和Y中均含有同一元素。

请回答下列问题:
(1)组成A的元素在周期表中属于_______ (选填序号)。
A.主族元素 B.副族元素 C.短周期元素 D.过渡元素
(2)写出溶液B中溶质的化学式:_______ 。
(3)写出反应I的化学反应方程式:_______ 。
(4)以石墨为两极材料,电解C的水溶液,写出电解初期阴极的电极反应式:______ 。
(5)28g单质A与一定浓度的B溶液反应,当生成n(C) ∶n(E)=2∶3时,反应中转移电子__ mol.
(6)给E溶液中加入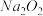 也能生成X,写出当n(E) ∶n(
也能生成X,写出当n(E) ∶n(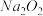 )=1∶1时,反应的离子方程式
)=1∶1时,反应的离子方程式__________________ 。
①X为红褐色沉淀;②A为单质,B为溶液,D和F为气体;③反应I的产物只有Y和H
 O;
O;④B、D、F和Y中均含有同一元素。

请回答下列问题:
(1)组成A的元素在周期表中属于
A.主族元素 B.副族元素 C.短周期元素 D.过渡元素
(2)写出溶液B中溶质的化学式:
(3)写出反应I的化学反应方程式:
(4)以石墨为两极材料,电解C的水溶液,写出电解初期阴极的电极反应式:
(5)28g单质A与一定浓度的B溶液反应,当生成n(C) ∶n(E)=2∶3时,反应中转移电子
(6)给E溶液中加入
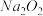 也能生成X,写出当n(E) ∶n(
也能生成X,写出当n(E) ∶n(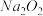 )=1∶1时,反应的离子方程式
)=1∶1时,反应的离子方程式
您最近半年使用:0次
10-11高三上·浙江金华·阶段练习
名校
解题方法
4 .
(1)请将5种物质:N2O、FeSO4、Fe(NO3)3、HNO3和Fe2(SO4)3分别填入下面对应的横线上,组成一个未配平的化学方程式。_______
_______+_______→_______+_______+_______+H2O
(2)反应物中发生氧化反应的物质_______ ,被还原的元素是_______ 。
(3)反应中1 mol氧化剂_______ (填“得到”或“失去”)_______ mol电子。
(4)请将反应物的化学式及配平后的系数填入下列相应的位置中:_______

(1)请将5种物质:N2O、FeSO4、Fe(NO3)3、HNO3和Fe2(SO4)3分别填入下面对应的横线上,组成一个未配平的化学方程式。
_______+_______→_______+_______+_______+H2O
(2)反应物中发生氧化反应的物质
(3)反应中1 mol氧化剂
(4)请将反应物的化学式及配平后的系数填入下列相应的位置中:

您最近半年使用:0次
2010·陕西汉中·三模
5 . 黑火药是我国古代科技四大发明之一,在化学史上占有重要地位,黑火药主要是硝酸钾、硫磺、木炭三者粉末的混合物,在点燃条件下,其化学反应式主要为:KNO3+S+C →N2↑+CO2↑+K2S
试填下列空白:
(1)在黑火药燃烧的反应中,氧化剂为_________ ,被氧化的物质为___________________
(2)根据化学反应式分析,KNO3、S和C恰好完全反应时,它们的物质的量之比为_________
(3)黑火药燃烧后的固体残留物中,除了K2S外,还有少许K2CO3、K2SO4和未燃烧的炭末,请设计一个简单的实验证明,黑火药燃烧的固体产物中存在K2CO3和K2SO4
[实验方案]
①取黑火药燃烧后的固体残留物于烧杯中,加适量水溶解,过滤,得无色澄清溶液;
②用洁净的铂丝蘸取滤液,将铂丝放在酒精灯火焰上灼烧,透过蓝色钴玻璃片观察火焰,若火焰呈紫色,则证明含K+;
③________________________________________________________________________
试填下列空白:
(1)在黑火药燃烧的反应中,氧化剂为
(2)根据化学反应式分析,KNO3、S和C恰好完全反应时,它们的物质的量之比为
(3)黑火药燃烧后的固体残留物中,除了K2S外,还有少许K2CO3、K2SO4和未燃烧的炭末,请设计一个简单的实验证明,黑火药燃烧的固体产物中存在K2CO3和K2SO4
[实验方案]
①取黑火药燃烧后的固体残留物于烧杯中,加适量水溶解,过滤,得无色澄清溶液;
②用洁净的铂丝蘸取滤液,将铂丝放在酒精灯火焰上灼烧,透过蓝色钴玻璃片观察火焰,若火焰呈紫色,则证明含K+;
③
您最近半年使用:0次
10-11高三上·北京朝阳·期末
名校
6 . 水热法制备纳米颗粒Y(化合物)的反应为3Fe2++2S2O32-+O2+aOH-=Y+S4O62-+2H2O,下列说法中,不正确的是
| A.a = 4 | B.Y的化学式为Fe2O3 |
| C.S2O32-是还原剂 | D.每有1molO2参加反应,转移的电子总数为4mol |
您最近半年使用:0次
名校
7 . 1994年度诺贝尔化学奖授予为研究臭氧做出贡献的化学家。O3能吸收有害紫外线,保护人类赖以生存的空间。O3的分子结构如图,呈V型,两个O----O键的夹角为116.5o。三个原子以一个O原子为中心,另外两个O原子分别构成一个共价键;中间O原子提供2个电子,旁边两个O原子各提供一个电子,构成一个特殊的化学键——三个O原子均等地享有这个电子。请回答:
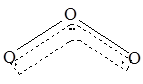
(1)臭氧与氧气的关系是_____________ 。
(2)写出下列分子与O3分子的结构最相似的是_______________ 。
(3)分子中某原子有一对或几对没有跟其他原子共用的价电子叫孤对电子,那么O3分子有________ 对孤对电子。
(4)O3分子是否为极性分子____________ (填是或否)。
(5)O3具有强氧化性,它能氧化PbS为PbSO4而O2不能,试配平:
_____ PbS +___ O3=________ PbSO4+_______ O2
生成1mol O2的转移电子物质的量为___________ mol。
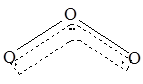
(1)臭氧与氧气的关系是
(2)写出下列分子与O3分子的结构最相似的是
| A.H2O | B.CO2 | C.SO2 | D.BeCl2 |
(3)分子中某原子有一对或几对没有跟其他原子共用的价电子叫孤对电子,那么O3分子有
(4)O3分子是否为极性分子
(5)O3具有强氧化性,它能氧化PbS为PbSO4而O2不能,试配平:
生成1mol O2的转移电子物质的量为
您最近半年使用:0次
名校
8 . 某离子反应涉及H2O、ClO-、NH4+ 、H+、N2、Cl-六种微粒。其中c(NH4+ )随反应进行逐渐减小。下列判断正确的是
| A.反应的还原产物是N2 |
| B.消耗1 mol氧化剂,转移电子3 mol |
| C.氧化剂与还原剂的物质的量之比为2:3 |
| D.反应后溶液的酸性明显增强 |
您最近半年使用:0次
2016-11-23更新
|
364次组卷
|
15卷引用:陕西省西安中学2018届高三10月月考化学试题
陕西省西安中学2018届高三10月月考化学试题陕西省西安中学2018届高三上学期期中考试化学试题陕西省黄陵中学2019-2020学年高一上学期期末考试化学试题(普通班)2016届吉林省吉林大学附属中学高三上第四次摸底考试化学试卷2017届湖南省岳阳市华容县四校高三联考二化学试卷2017届福建省泉州市南安一中高三上学期第一次阶段考化学试卷2017届山东省菏泽市高三上学期期末学分认定考试B卷化学试卷(已下线)【中等生百日捷进提升系列-基础练测】专题2.4 氧化还原反应江西省上饶中学2019届高三上学期开学检测化学试题福建省晋江市季延中学2018-2019学年高二上学期开学考试化学试题江西省赣州市会昌中学2019届高三上学期第一次月考(10月)化学试题山西省运城市临猗中学2019届高三上学期第一次月考化学试题【校级联考】福建省泉州市永春县永春二中、永春五中2019届高三上学期期中联合考试化学试题辽宁省沈阳铁路实验中学2020届高三上学期开学考试化学试题甘肃省白银市第十中学2019-2020学年高一上学期期中考试化学试题
2011·陕西·二模
解题方法
9 . 将某些化学知识用数轴表示,可以收到直观、简明、易记的效果。用数轴表示的下列知识正确的是
A.硫及其化合物的化合价与氧化还原反应的关系: |
B.分散系的分类: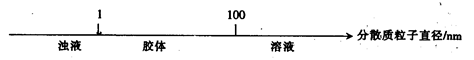 |
C.AlCl3溶液与NaOH溶液反应后铝元素的存在形式: |
D.CO2与NaOH溶液反应后的产物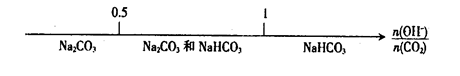 |
您最近半年使用:0次
2016-10-20更新
|
481次组卷
|
4卷引用:2012届陕西省铁一中高三第二次模拟考试化学试卷
(已下线)2012届陕西省铁一中高三第二次模拟考试化学试卷(已下线)2012届陕西省铁一中高三第二次模拟考试化学试卷 2017届陕西省西安市第七十中学高三上学期10月月考化学试卷四川省成都七中实验学校2016-2017学年高二下学期期中考试化学试题
10 . 草酸溶液能使酸性KMnO4溶液褪色,其离子方程式为:MnO4-+H2C2O4+H+→CO2↑+Mn2++__(未配平)。关于此反应的叙述正确的是
| A.该反应的还原产物是CO2 |
| B.该反应右框内的产物是OH- |
| C.配平该反应后,H+计量数是6 |
| D.1molMnO4-在反应中失去5mol电子 |
您最近半年使用:0次
2016-07-27更新
|
581次组卷
|
9卷引用:陕西省咸阳市泾阳县泾干中学2021-2022学年高一上学期期末考试化学试题



