名校
解题方法
1 . 钠的碘化物在生产和科学实验中有十分重要的应用。工业上利用碘、烧碱和铁屑为原料可生产碘化钠,其生产流程如图所示:
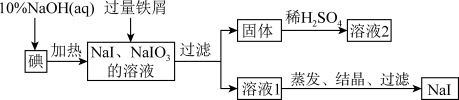
回答下列问题:
(1) 溶液和碘反应时需要严格控制温度,温度过低,获得副产物的化学式为
溶液和碘反应时需要严格控制温度,温度过低,获得副产物的化学式为__________ 。
(2)加入铁屑的目的是__________ ;过滤所得固体中除剩余铁屑外,还有红褐色固体,则加入铁屑时发生反应的离子方程式为__________ 。
(3)若参与流程的碘单质为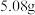 ,最终得到
,最终得到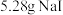 ,则反应的产率为
,则反应的产率为__________ 。
(4)溶液2经一系列操作得到硫酸亚铁晶体 ,称取该晶体样品放入下图所示装置高温加热,使其完全分解,对所得产物进行探究。
,称取该晶体样品放入下图所示装置高温加热,使其完全分解,对所得产物进行探究。
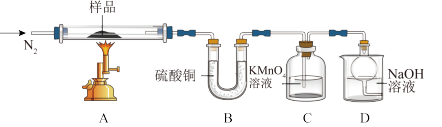
①硫酸亚铁晶体完全分解后,装置A中固体变为红棕色,装置B中硫酸铜粉末变蓝,装置C中高锰酸钾溶液褪色。根据化合价分析,产物中有还原性气体__________ (填化学式),装置D中球形干燥管的作用是__________ 。
②写出 分解的化学方程式
分解的化学方程式__________ 。
(5)用流程图的形式表示用溶液2制备 的过程
的过程__________ 。(用箭头表示转化关系,箭头上注明试剂、反应条件及操作,如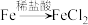 )
)

回答下列问题:
(1)
 溶液和碘反应时需要严格控制温度,温度过低,获得副产物的化学式为
溶液和碘反应时需要严格控制温度,温度过低,获得副产物的化学式为(2)加入铁屑的目的是
(3)若参与流程的碘单质为
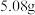 ,最终得到
,最终得到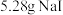 ,则反应的产率为
,则反应的产率为(4)溶液2经一系列操作得到硫酸亚铁晶体
 ,称取该晶体样品放入下图所示装置高温加热,使其完全分解,对所得产物进行探究。
,称取该晶体样品放入下图所示装置高温加热,使其完全分解,对所得产物进行探究。
①硫酸亚铁晶体完全分解后,装置A中固体变为红棕色,装置B中硫酸铜粉末变蓝,装置C中高锰酸钾溶液褪色。根据化合价分析,产物中有还原性气体
②写出
 分解的化学方程式
分解的化学方程式(5)用流程图的形式表示用溶液2制备
 的过程
的过程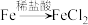 )
)
您最近半年使用:0次
2024-01-13更新
|
64次组卷
|
2卷引用:陕西省咸阳市实验中学2023-2024学年高一上学期11月期中考试化学试题
解题方法
2 . 下列有关电极方程式或离子方程式错误的是
A.铅蓄电池放电时,正极反应: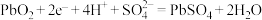 |
B.向碘化亚铁溶液中滴加少量稀硝酸: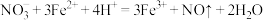 |
C.向0.1mol·L NaHA溶液( NaHA溶液( )加入NaOH溶液: )加入NaOH溶液: |
D.铜片上电镀银的总反应(银作阳极,硝酸银溶液作电镀液):Ag(阳极) (阴极) (阴极) |
您最近半年使用:0次
2024-01-13更新
|
781次组卷
|
5卷引用:陕西省渭南市2023-2024学年高三上学期教学质量检测化学试卷
陕西省渭南市2023-2024学年高三上学期教学质量检测化学试卷 陕西省渭南市2023-2024学年高三教学质量检测(Ⅰ)化学试题(已下线)化学(九省联考考后提升卷,吉林、黑龙江卷)-2024年1月“九省联考”真题完全解读与考后提升(已下线)热点03 离子方程式的正误判断、离子共存(已下线)专题01 基本概念-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)
名校
3 . 工业利用闪锌矿(主要成分 ZnS,还含有FeS、 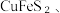 石英及F-、Cl⁻等杂质)富氧酸浸提取锌,同时实现环保除铁的工艺流程如下:
石英及F-、Cl⁻等杂质)富氧酸浸提取锌,同时实现环保除铁的工艺流程如下:
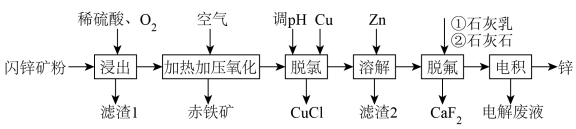
已知:①酸性条件下,亚铜离子易发生歧化反应;② 易形成胶体;③碱性环境下
易形成胶体;③碱性环境下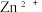 以
以  形式存在。回答下列问题:
形式存在。回答下列问题:
(1)“浸出”前闪锌矿石要碾碎为粉末的原因是___________ 。
(2)“浸出”过程原理如图所示,ZnS“浸出”的总反应化学方程式为___________ 。
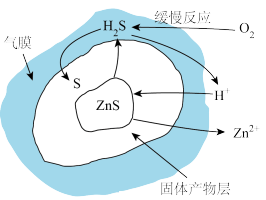
(3)“滤渣1”主要成分为S和___________ ;“加热加压氧化”发生反应的离子方程式为___________ 。
(4)“电积”时,F、Cl⁻会腐蚀电极板,需提前除净。
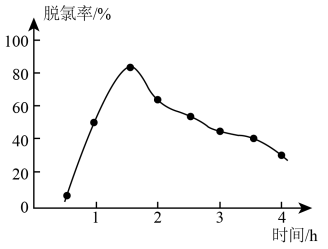
①“脱氯”时,脱氯率随时间变化如图所示,约1.5h后脱氯率减小的原因可能为___________ 。
②“脱氟时,先按物质的量之比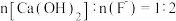 加入
加入  脱氟,充分反应后,
脱氟,充分反应后, 

___________ 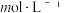 [已知
[已知  且不考虑
且不考虑  沉淀];后加入石灰石,目的为
沉淀];后加入石灰石,目的为___________ 。
(5)写出“电积”生成锌的电极反应式:___________ 。
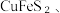 石英及F-、Cl⁻等杂质)富氧酸浸提取锌,同时实现环保除铁的工艺流程如下:
石英及F-、Cl⁻等杂质)富氧酸浸提取锌,同时实现环保除铁的工艺流程如下:
已知:①酸性条件下,亚铜离子易发生歧化反应;②
 易形成胶体;③碱性环境下
易形成胶体;③碱性环境下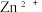 以
以  形式存在。回答下列问题:
形式存在。回答下列问题:(1)“浸出”前闪锌矿石要碾碎为粉末的原因是
(2)“浸出”过程原理如图所示,ZnS“浸出”的总反应化学方程式为

(3)“滤渣1”主要成分为S和
(4)“电积”时,F、Cl⁻会腐蚀电极板,需提前除净。
①“脱氯”时,脱氯率随时间变化如图所示,约1.5h后脱氯率减小的原因可能为

②“脱氟时,先按物质的量之比
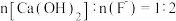 加入
加入  脱氟,充分反应后,
脱氟,充分反应后, 

 [已知
[已知  且不考虑
且不考虑  沉淀];后加入石灰石,目的为
沉淀];后加入石灰石,目的为(5)写出“电积”生成锌的电极反应式:
您最近半年使用:0次
4 . 连二亚硫酸钠( )也叫做保险粉,是一种重要的化工产品,易溶于水、难溶于甲醇,在碱性介质中比较稳定,在空气中易被氧化。某化学小组用如图所示装置(夹持仪器已省略)制取
)也叫做保险粉,是一种重要的化工产品,易溶于水、难溶于甲醇,在碱性介质中比较稳定,在空气中易被氧化。某化学小组用如图所示装置(夹持仪器已省略)制取 。
。
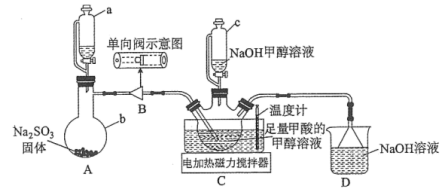
回答下列问题:
(1)仪器a的名称是___________ ,用装置A制备 时所选用的酸,你认为下列最适宜选用的是
时所选用的酸,你认为下列最适宜选用的是___________ (填字母)。
A.浓盐酸 B.质量分数为70%的
C.稀硝酸 D.质量分数为10%的稀硫酸
(2)单向阀的作用是___________ ,制备保险粉前先打开仪器a的活塞的目的是___________ 。
(3)已知三颈烧瓶中的甲酸转化为 ,写出生成
,写出生成 的化学方程式:
的化学方程式:___________ 。
(4) 是一种常用的还原剂,写出它与酸性高锰酸钾溶液反应的离子方程式:
是一种常用的还原剂,写出它与酸性高锰酸钾溶液反应的离子方程式:___________ 。
(5) 固体隔绝空气加热使之完全分解得到固体产物
固体隔绝空气加热使之完全分解得到固体产物 、
、 和
和 气体,设计实验方案检验产物中含有的
气体,设计实验方案检验产物中含有的 :
:___________ (写出实验操作、现象及结论)。
(6)称取粗产品 加水溶解,用NaOH溶液碱化后,加入一定量的
加水溶解,用NaOH溶液碱化后,加入一定量的 溶液恰好完全反应(
溶液恰好完全反应( ),将溶液中生成的纳米级的银粉过滤、洗涤、干燥后称重,得到
),将溶液中生成的纳米级的银粉过滤、洗涤、干燥后称重,得到 银,则粗产品中连二亚硫酸钠的纯度为
银,则粗产品中连二亚硫酸钠的纯度为___________ (含 、
、 的表达式)。
的表达式)。
 )也叫做保险粉,是一种重要的化工产品,易溶于水、难溶于甲醇,在碱性介质中比较稳定,在空气中易被氧化。某化学小组用如图所示装置(夹持仪器已省略)制取
)也叫做保险粉,是一种重要的化工产品,易溶于水、难溶于甲醇,在碱性介质中比较稳定,在空气中易被氧化。某化学小组用如图所示装置(夹持仪器已省略)制取 。
。
回答下列问题:
(1)仪器a的名称是
 时所选用的酸,你认为下列最适宜选用的是
时所选用的酸,你认为下列最适宜选用的是A.浓盐酸 B.质量分数为70%的

C.稀硝酸 D.质量分数为10%的稀硫酸
(2)单向阀的作用是
(3)已知三颈烧瓶中的甲酸转化为
 ,写出生成
,写出生成 的化学方程式:
的化学方程式:(4)
 是一种常用的还原剂,写出它与酸性高锰酸钾溶液反应的离子方程式:
是一种常用的还原剂,写出它与酸性高锰酸钾溶液反应的离子方程式:(5)
 固体隔绝空气加热使之完全分解得到固体产物
固体隔绝空气加热使之完全分解得到固体产物 、
、 和
和 气体,设计实验方案检验产物中含有的
气体,设计实验方案检验产物中含有的 :
:(6)称取粗产品
 加水溶解,用NaOH溶液碱化后,加入一定量的
加水溶解,用NaOH溶液碱化后,加入一定量的 溶液恰好完全反应(
溶液恰好完全反应( ),将溶液中生成的纳米级的银粉过滤、洗涤、干燥后称重,得到
),将溶液中生成的纳米级的银粉过滤、洗涤、干燥后称重,得到 银,则粗产品中连二亚硫酸钠的纯度为
银,则粗产品中连二亚硫酸钠的纯度为 、
、 的表达式)。
的表达式)。
您最近半年使用:0次
名校
5 . 实现碳达峰、碳中和是党中央做出的重大战略决策。恒压、  时,
时, 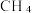 和
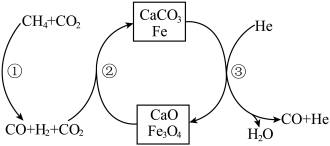
和  按物质的量之比1:3 投料,反应经如下流程(主要产物已标出)可实现
按物质的量之比1:3 投料,反应经如下流程(主要产物已标出)可实现 高效转化。下列说法正确的是
高效转化。下列说法正确的是
 时,
时, 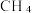 和
和  按物质的量之比1:3 投料,反应经如下流程(主要产物已标出)可实现
按物质的量之比1:3 投料,反应经如下流程(主要产物已标出)可实现 高效转化。下列说法正确的是
高效转化。下列说法正确的是
A.过程②中  的吸收,不利于CO还原 的吸收,不利于CO还原  的平衡正向移动 的平衡正向移动 |
B.过程③中通入 He 的作用是催化剂,加快  分解 分解 |
| C.过程①、②、③均涉及到了氧化还原反应 |
D. 可循环利用,而 CaO不可循环利用 可循环利用,而 CaO不可循环利用 |
您最近半年使用:0次
6 . 碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等方面。 的一种制备方法如图1所示:
的一种制备方法如图1所示: 可将
可将 氧化成
氧化成 。下列说法错误的是
。下列说法错误的是
 的一种制备方法如图1所示:
的一种制备方法如图1所示: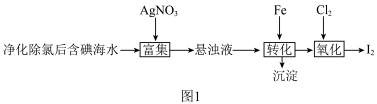
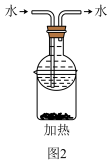
 可将
可将 氧化成
氧化成 。下列说法错误的是
。下列说法错误的是A.“转化”反应的离子方程式为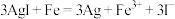 |
B.“转化”产生的沉淀可用 处理后循环使用 处理后循环使用 |
C.“氧化”时,应控制 的量,过多或过少,都会降低单质碘的收率 的量,过多或过少,都会降低单质碘的收率 |
| D.获得的粗碘可采用图2装置进行纯化 |
您最近半年使用:0次
2024-01-10更新
|
91次组卷
|
2卷引用:2024届陕西省安康市安康中学高新分校,安康市高新中学高三上学期模拟预测理综试题
名校
7 . 能正确表示下列反应的离子方程式是
A.向稀硫酸酸化的KMnO4溶液中滴加少量H2O2溶液:2MnO +6H++3H2O2=2Mn2++4O2↑+6H2O +6H++3H2O2=2Mn2++4O2↑+6H2O |
B.向明矾[KAl(SO4)2]溶液中逐滴加入Ba(OH)2溶液至SO 恰好沉淀完全:2Al3++3SO 恰好沉淀完全:2Al3++3SO +3Ba2++6OH- =2Al(OH)3↓+3BaSO4↓ +3Ba2++6OH- =2Al(OH)3↓+3BaSO4↓ |
C.用铜做电极电解CuSO4溶液:2Cu2++2H2O 2Cu+O2↑+4H+ 2Cu+O2↑+4H+ |
D.将ClO2气体通入H2O2、NaOH的混合溶液中制NaClO2:2ClO2+H2O2+2OH-=2ClO +O2+2H2O +O2+2H2O |
您最近半年使用:0次
名校
8 . 物质类别和核心元素的价态是学习元素及其化合物性质的两个重要认识视角。图为钠及其化合物的“价-类”二维图,请回答下列问题:
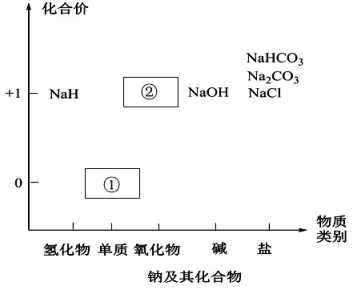
(1)物质①与水反应的离子方程式为________________________________________ 。
(2)淡黄色固体②与水反应的化学方程式为__________________________________ 。
(3)从核心元素价态的视角分析: 中H元素的化合价为
中H元素的化合价为________ ,在化学反应中, 常用作
常用作_________________ 。(填“氧化剂”或“还原剂”)
(4) 投入
投入 中,发生反应的化学方程式为
中,发生反应的化学方程式为______________________________ 。反应若生0.5克 ,则反应中转移电子数目为
,则反应中转移电子数目为________  。
。

(1)物质①与水反应的离子方程式为
(2)淡黄色固体②与水反应的化学方程式为
(3)从核心元素价态的视角分析:
 中H元素的化合价为
中H元素的化合价为 常用作
常用作(4)
 投入
投入 中,发生反应的化学方程式为
中,发生反应的化学方程式为 ,则反应中转移电子数目为
,则反应中转移电子数目为 。
。
您最近半年使用:0次
名校
9 . 含氯化合物在生产生活中具有重要用途,不同价态的含氯化合物在适当条件下可以相互转化。回答下列问题:
(1)氯胺是由氯气遇到氨气反应生成的一类化合物,是常用的饮用水二级消毒剂,主要包括一氯胺、二氯胺和三氯胺( 、
、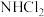 和
和 )等。
)等。
①氯胺作饮用水消毒剂是因为其与水反应生成了具有强烈杀菌作用的物质A。该物质(A)属于________ (填“强酸”或“弱酸”);其中二氯胺与水反应的化学方程式为_________________________________________ 。
②将
 通入足量
通入足量 溶液中,
溶液中, 被氧化为
被氧化为 ,则反应中转移电子的数目为
,则反应中转移电子的数目为________  。
。
(2) 有强氧化性,在强碱性介质中,
有强氧化性,在强碱性介质中, 与
与 反应生成紫红色高铁酸钾(
反应生成紫红色高铁酸钾( )溶液,
)溶液, 是一种优良的水处理剂。在制备反应中,氧化产物与还原产物的物质的量之比为
是一种优良的水处理剂。在制备反应中,氧化产物与还原产物的物质的量之比为________ 。
(3)把 溶液滴入沸水中,可得到一种红褐色、能发生丁达尔效应的分散系,该过程中发生反应的离子方程式为
溶液滴入沸水中,可得到一种红褐色、能发生丁达尔效应的分散系,该过程中发生反应的离子方程式为________________________________________________ 。
(4)二氧化氯( )气体是高效低毒的消毒剂。
)气体是高效低毒的消毒剂。 的稳定性差,因此常将其制成
的稳定性差,因此常将其制成 固体便于运输和贮存,其制备方法:将
固体便于运输和贮存,其制备方法:将 通入含
通入含 的
的 溶液中。该反应的化学方程式
溶液中。该反应的化学方程式_________________ 。
(1)氯胺是由氯气遇到氨气反应生成的一类化合物,是常用的饮用水二级消毒剂,主要包括一氯胺、二氯胺和三氯胺(
 、
、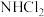 和
和 )等。
)等。①氯胺作饮用水消毒剂是因为其与水反应生成了具有强烈杀菌作用的物质A。该物质(A)属于
②将

 通入足量
通入足量 溶液中,
溶液中, 被氧化为
被氧化为 ,则反应中转移电子的数目为
,则反应中转移电子的数目为 。
。(2)
 有强氧化性,在强碱性介质中,
有强氧化性,在强碱性介质中, 与
与 反应生成紫红色高铁酸钾(
反应生成紫红色高铁酸钾( )溶液,
)溶液, 是一种优良的水处理剂。在制备反应中,氧化产物与还原产物的物质的量之比为
是一种优良的水处理剂。在制备反应中,氧化产物与还原产物的物质的量之比为(3)把
 溶液滴入沸水中,可得到一种红褐色、能发生丁达尔效应的分散系,该过程中发生反应的离子方程式为
溶液滴入沸水中,可得到一种红褐色、能发生丁达尔效应的分散系,该过程中发生反应的离子方程式为(4)二氧化氯(
 )气体是高效低毒的消毒剂。
)气体是高效低毒的消毒剂。 的稳定性差,因此常将其制成
的稳定性差,因此常将其制成 固体便于运输和贮存,其制备方法:将
固体便于运输和贮存,其制备方法:将 通入含
通入含 的
的 溶液中。该反应的化学方程式
溶液中。该反应的化学方程式
您最近半年使用:0次
名校
10 . 按要求填空:
(1)现有下列物质:①盐酸;②胆矾晶体;③熔融氯化钠;④稀盐酸;⑤氨水;⑥蔗糖;⑦二氧化碳;⑧氯水;⑨铜。其中属于能导电强电解质的是________ 。(填序号)
(2)已知在太阳光作用下,植物体内的叶绿素能将水、 转化为葡萄糖。如图为海水吸收
转化为葡萄糖。如图为海水吸收 并进行碳循环的原理示意图。其中“钙化”过程中发生的化学反应方程式为:
并进行碳循环的原理示意图。其中“钙化”过程中发生的化学反应方程式为:

①_________________________________ ;②_________________________________ 。
(3)硫化氢( )是一种有毒、有害的不良气体。处理某废气中的
)是一种有毒、有害的不良气体。处理某废气中的 ,是将废气与空气混合通入
,是将废气与空气混合通入 、
、 、
、 的混合液中,其转化的流程如图所示。
的混合液中,其转化的流程如图所示。
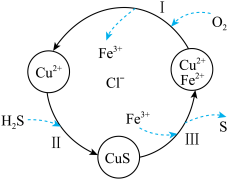
其中过程Ⅲ中发生反应的离子方程式为______________________________________ 。
(4)某课外活动小组设计了如图所示装置,验证 与
与 反应时需要与水接触。
反应时需要与水接触。
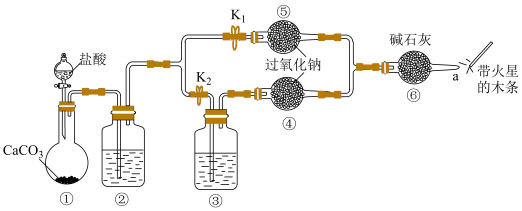
其中②中试剂为__________ ,⑤中发生的主要 反应化学方程式为_______________ 。
(1)现有下列物质:①盐酸;②胆矾晶体;③熔融氯化钠;④稀盐酸;⑤氨水;⑥蔗糖;⑦二氧化碳;⑧氯水;⑨铜。其中属于能导电强电解质的是
(2)已知在太阳光作用下,植物体内的叶绿素能将水、
 转化为葡萄糖。如图为海水吸收
转化为葡萄糖。如图为海水吸收 并进行碳循环的原理示意图。其中“钙化”过程中发生的化学反应方程式为:
并进行碳循环的原理示意图。其中“钙化”过程中发生的化学反应方程式为:
①
(3)硫化氢(
 )是一种有毒、有害的不良气体。处理某废气中的
)是一种有毒、有害的不良气体。处理某废气中的 ,是将废气与空气混合通入
,是将废气与空气混合通入 、
、 、
、 的混合液中,其转化的流程如图所示。
的混合液中,其转化的流程如图所示。
其中过程Ⅲ中发生反应的离子方程式为
(4)某课外活动小组设计了如图所示装置,验证
 与
与 反应时需要与水接触。
反应时需要与水接触。
其中②中试剂为
您最近半年使用:0次



