名校
1 . 恒容密闭容器中,反应NH4HS(s) NH3(g)+H2S(g)在某一温度下达到平衡状态,其他条件不变,仅改变下列条件,不会使化学平衡发生移动的是
NH3(g)+H2S(g)在某一温度下达到平衡状态,其他条件不变,仅改变下列条件,不会使化学平衡发生移动的是
①减少部分NH4HS固体 ②充入少量氨气 ③充入氦气 ④充入SO2气体
 NH3(g)+H2S(g)在某一温度下达到平衡状态,其他条件不变,仅改变下列条件,不会使化学平衡发生移动的是
NH3(g)+H2S(g)在某一温度下达到平衡状态,其他条件不变,仅改变下列条件,不会使化学平衡发生移动的是①减少部分NH4HS固体 ②充入少量氨气 ③充入氦气 ④充入SO2气体
| A.①② | B.②③ | C.①③ | D.②④ |
您最近一年使用:0次
2022-12-03更新
|
370次组卷
|
5卷引用:福建省厦门市厦门英才学校2021-2022学年高二上学期期中考试化学试题
解题方法
2 . 完成下列问题
(1)一定条件下,在体积为5 L的密闭容器中,A、B、C三种气体的物质的量n(mol)随时间t(min)的变化如图1所示。已知达到平衡后,降低温度,A的体积分数将减小。
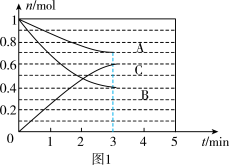
①该反应的化学方程式为_______ ,此反应平衡常数表达式为K=_______ 。
②该反应的△H_______ 0(填“>”“<”或“=”)。
③该反应的反应速率v随时间t的变化关系如图2所示:根据图2判断,在t3时刻改变的外界条件是_______ 。在恒温恒容密闭容器中发生该反应,下列能作为达到平衡状态的判断依据是_______ (填标号)。

a.体系压强不变 b.气体的平均摩尔质量保持不变
c.气体的密度保持不变 d.A的消耗速率等于B的生成速率
(2)习近平主席在《中央城镇化工作会议》发出号召:“让居民望得见山、看得见水、记得住乡愁”。消除含氮、硫、氯等化合物对大气和水体的污染对建设美丽家乡,打造宜居环境具有重要意义。NO2和CO是常见的环境污染气体,汽车尾气中CO、NO2在一定条件下可以发生反应:4CO(g)+2NO2(g) 4CO2(g)+N2(g)
4CO2(g)+N2(g)  kJ·mol–1,在一定温度下,向容积固定为2 L的密闭容器中充入一定量的CO和NO2,NO2的物质的量随时间的变化曲线如图所示。
kJ·mol–1,在一定温度下,向容积固定为2 L的密闭容器中充入一定量的CO和NO2,NO2的物质的量随时间的变化曲线如图所示。

①从反应开始到10 min的平衡状态,N2的平均反应速率为_______ 。从11 min起,其他条件不变,压缩容器的容积为1 L,则n(NO2)的变化曲线可能为图中的_______ (填字母)。
②对于该反应,温度不同(T2>T1)、其他条件相同时,下列图像表示正确的是_______ (填序号)。
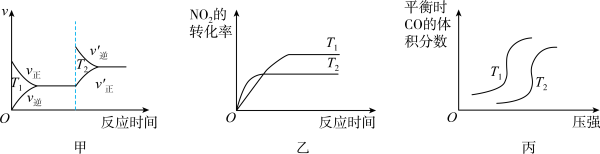
(3)甲醇是一种重要的化工原料,又是一种可再生能源,在开发和应用方面具有广阔前景。在一容积为2 L的密闭容器内,充入0.2 mol CO与0.4 mol H2发生反应CO(g) + 2H2(g) CH3OH(g),CO的平衡转化率与温度、压强的关系如图所示。
CH3OH(g),CO的平衡转化率与温度、压强的关系如图所示。
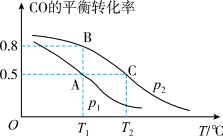
①p1_______ p2(填“>”“<”或“=”)。
②在p1、T1℃时,该反应的压强平衡常数Kp =_______ 。
③相同温度下,在两个相同的体积可变的容器a、b中分别投入容器a.0.1 mol CO(g),0.2 mol H2(g);容器b.0.2 mol CO(g),0.4 mol H2(g),0.1 mol CH3OH(g),则达到平衡后a、b容器的体积比为_______ 。
(1)一定条件下,在体积为5 L的密闭容器中,A、B、C三种气体的物质的量n(mol)随时间t(min)的变化如图1所示。已知达到平衡后,降低温度,A的体积分数将减小。

①该反应的化学方程式为
②该反应的△H
③该反应的反应速率v随时间t的变化关系如图2所示:根据图2判断,在t3时刻改变的外界条件是

a.体系压强不变 b.气体的平均摩尔质量保持不变
c.气体的密度保持不变 d.A的消耗速率等于B的生成速率
(2)习近平主席在《中央城镇化工作会议》发出号召:“让居民望得见山、看得见水、记得住乡愁”。消除含氮、硫、氯等化合物对大气和水体的污染对建设美丽家乡,打造宜居环境具有重要意义。NO2和CO是常见的环境污染气体,汽车尾气中CO、NO2在一定条件下可以发生反应:4CO(g)+2NO2(g)
 4CO2(g)+N2(g)
4CO2(g)+N2(g)  kJ·mol–1,在一定温度下,向容积固定为2 L的密闭容器中充入一定量的CO和NO2,NO2的物质的量随时间的变化曲线如图所示。
kJ·mol–1,在一定温度下,向容积固定为2 L的密闭容器中充入一定量的CO和NO2,NO2的物质的量随时间的变化曲线如图所示。
①从反应开始到10 min的平衡状态,N2的平均反应速率为
②对于该反应,温度不同(T2>T1)、其他条件相同时,下列图像表示正确的是

(3)甲醇是一种重要的化工原料,又是一种可再生能源,在开发和应用方面具有广阔前景。在一容积为2 L的密闭容器内,充入0.2 mol CO与0.4 mol H2发生反应CO(g) + 2H2(g)
 CH3OH(g),CO的平衡转化率与温度、压强的关系如图所示。
CH3OH(g),CO的平衡转化率与温度、压强的关系如图所示。
①p1
②在p1、T1℃时,该反应的压强平衡常数Kp =
③相同温度下,在两个相同的体积可变的容器a、b中分别投入容器a.0.1 mol CO(g),0.2 mol H2(g);容器b.0.2 mol CO(g),0.4 mol H2(g),0.1 mol CH3OH(g),则达到平衡后a、b容器的体积比为
您最近一年使用:0次
名校
解题方法
3 . 在一定温度下,向aL密闭容器中加入1molX气体和2molY气体,发生如下反应:X(g)+2Y(g)⇌2Z(g)此反应达到平衡的标志是
| A.容器内压强不随时间变化 |
| B.容器内X、Y、Z的浓度之比为1︰2︰2 |
| C.容器内各物质的浓度随时间变化 |
| D.单位时间消耗0.1molX同时生成0.2molZ |
您最近一年使用:0次
2022-12-02更新
|
214次组卷
|
2卷引用:陕西省安康市汉滨区五里高级中学2021-2022学年高二上学期期中考试化学试题
解题方法
4 . 在2 L容器中500℃时下列关于反应2SO2+O2 2SO3 ΔH<0,叙述中正确的是
2SO3 ΔH<0,叙述中正确的是
 2SO3 ΔH<0,叙述中正确的是
2SO3 ΔH<0,叙述中正确的是| A.当v(SO2)正=2v(O2)逆时达到化学平衡状态 |
| B.当气体密度不变时达到化学平衡状态 |
| C.工业上常用10MPa的条件反应 |
| D.高温可提高SO2的转化率 |
您最近一年使用:0次
名校
解题方法
5 .  在KI溶液中存在下列平衡:
在KI溶液中存在下列平衡:
 。某
。某 、KI混合溶液中,
、KI混合溶液中, 的物质的量浓度
的物质的量浓度 与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法不正确的是
与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法不正确的是
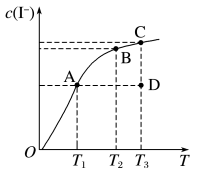
 在KI溶液中存在下列平衡:
在KI溶液中存在下列平衡:
 。某
。某 、KI混合溶液中,
、KI混合溶液中, 的物质的量浓度
的物质的量浓度 与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法不正确的是
与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法不正确的是
A.该反应 |
B.若在 、 、 温度下,反应的平衡常数分别为 温度下,反应的平衡常数分别为 、 、 ,则 ,则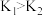 |
C.若反应进行到状态D时,一定有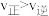 |
D.状态A与状态B相比,状态A的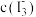 大 大 |
您最近一年使用:0次
2022-11-27更新
|
267次组卷
|
9卷引用:黑龙江省实验中学2021-2022学年高二上学期期中考试化学试题
黑龙江省实验中学2021-2022学年高二上学期期中考试化学试题【市级联考】山东省烟台市2019届高三上学期期末考试化学试题【全国百强校】福建省厦门市双十中学2018-2019学年高二下学期第一次月考化学试题黑龙江省牡丹江市东宁市第一中学2020-2021学年高二上学期第一次月考化学试题河北省衡水市第十四中学2020-2021学年高二上学期三调考试(校内)化学试题黑龙江省哈尔滨市第二十四中学2022-2023学年高二10月月考化学试题四川省成都市树德中学2022-2023学年高二上学期11月阶段性测试化学试题吉林省延边第二中学2022-2023学年高二上学期期末考试化学试题新疆阿克苏市实验中学2022-2023学年高二上学期期末考试化学试题
解题方法
6 . 某温度时,向某VL的密闭容器中充入3mol 和3mol
和3mol ,发生反应:
,发生反应: ,测得各物质的物质的量浓度与时间变化的关系如图所示。请回答下列问题:
,测得各物质的物质的量浓度与时间变化的关系如图所示。请回答下列问题:

(1)V=_______ L。
(2)该反应达到最大限度的时间是_______ s,该时间内平均反应速率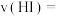
_______  。
。
(3)该反应达到平衡状态时,_______ (填“吸收”或“放出”)的热量为_______ kJ。
(4)判断该反应达到平衡的依据是_______ (填序号)。
①H2消耗的速率和 消耗的速率相等
消耗的速率相等
②H2、I2、HI的浓度比为1:1:2
③H2、I2、HI的浓度都不再发生变化
④该条件下正、逆反应速率都为零
(5)增大压强平衡移动方向_______ (正向、逆向、不移动)。
 和3mol
和3mol ,发生反应:
,发生反应: ,测得各物质的物质的量浓度与时间变化的关系如图所示。请回答下列问题:
,测得各物质的物质的量浓度与时间变化的关系如图所示。请回答下列问题:
(1)V=
(2)该反应达到最大限度的时间是
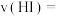
 。
。(3)该反应达到平衡状态时,
(4)判断该反应达到平衡的依据是
①H2消耗的速率和
 消耗的速率相等
消耗的速率相等②H2、I2、HI的浓度比为1:1:2
③H2、I2、HI的浓度都不再发生变化
④该条件下正、逆反应速率都为零
(5)增大压强平衡移动方向
您最近一年使用:0次
名校
解题方法
7 . H2NCOONH4是工业上由氨合成尿素的中间产物。在一定温度下、容积不变的密闭容器中发生反应H2NCOONH4(s)  2NH3(g)+CO2(g),能说明该反应达到平衡状态的是
2NH3(g)+CO2(g),能说明该反应达到平衡状态的是
①每生成34gNH3的同时消耗44 gCO2
②混合气体的平均相对分子质量不变
③NH3的体积分数保持不变
④混合气体的密度保持不变
⑤c(NH3):c(CO2)=2:1
 2NH3(g)+CO2(g),能说明该反应达到平衡状态的是
2NH3(g)+CO2(g),能说明该反应达到平衡状态的是①每生成34gNH3的同时消耗44 gCO2
②混合气体的平均相对分子质量不变
③NH3的体积分数保持不变
④混合气体的密度保持不变
⑤c(NH3):c(CO2)=2:1
| A.①③⑤ | B.①④ | C.①②④ | D.①③④ |
您最近一年使用:0次
2022-11-03更新
|
252次组卷
|
6卷引用:山东省济南市商河县第三中学2021-2022学年高二10月月考化学试题
名校
解题方法
8 . 某温度下,在一个2 L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,填写下列空白:

(1)从开始至2 min,X的平均反应速率为_______ 。
(2)该反应的化学方程式为_______ 。
(3)1 min时,v(正)__ v(逆),2 min时,v(正)__ v(逆)。(填“>”或“<”或“ ”)。
”)。
(4)上述反应在甲、乙两个相同容器内同时进行,分别测得甲中v(X)=9 mol/(L·min),乙中v(Y)=0.5 mol/(L·s),则__ 中反应更快。
(5)若X、Y、Z均为气体,在2 min时,向容器中通入氩气(容器体积不变),X的化学反应速率将_______ ,若加入适合的催化剂,Y的化学反应速率将_______ 。(填“变大”或“不变”或“变小”)。
(6)若X、Y、Z均为气体(容器体积不变),下列能说明反应已达平衡的是_______ 。
a.X、Y、Z三种气体的浓度相等
b.气体混合物物质的量不再改变
c.混合气体的总压强不随时间变化
d.反应速率v(X):v(Y)=3:1
e.单位时间内消耗X的物质的量:单位时间内消耗Z的物质的量=3:2
f.混合气体的密度不随时间变化
g.混合气体的平均相对分子质量不随时间变化

(1)从开始至2 min,X的平均反应速率为
(2)该反应的化学方程式为
(3)1 min时,v(正)
 ”)。
”)。(4)上述反应在甲、乙两个相同容器内同时进行,分别测得甲中v(X)=9 mol/(L·min),乙中v(Y)=0.5 mol/(L·s),则
(5)若X、Y、Z均为气体,在2 min时,向容器中通入氩气(容器体积不变),X的化学反应速率将
(6)若X、Y、Z均为气体(容器体积不变),下列能说明反应已达平衡的是
a.X、Y、Z三种气体的浓度相等
b.气体混合物物质的量不再改变
c.混合气体的总压强不随时间变化
d.反应速率v(X):v(Y)=3:1
e.单位时间内消耗X的物质的量:单位时间内消耗Z的物质的量=3:2
f.混合气体的密度不随时间变化
g.混合气体的平均相对分子质量不随时间变化
您最近一年使用:0次
23-24高一上·全国·假期作业
名校
解题方法
9 . 在恒温的密闭容器中,可逆反应 2SO2(g)+ O2(g)  2SO3(g)达到平衡状态的标志
2SO3(g)达到平衡状态的标志
 2SO3(g)达到平衡状态的标志
2SO3(g)达到平衡状态的标志| A.容器中SO2、O2和SO3共存 |
| B.反应器内各组分的浓度不再随时间发生变化 |
| C.容器中SO2、O2、SO3的物质的量之比为2:1:2 |
| D.SO2和SO3的物质的量浓度相等 |
您最近一年使用:0次
2022-11-01更新
|
538次组卷
|
6卷引用:安徽工业大学附属中学2020-2021学年高一下学期(高二文理分科考试)化学试题
安徽工业大学附属中学2020-2021学年高一下学期(高二文理分科考试)化学试题(已下线)第10讲 化学反应限度(讲义)-【寒假自学课】2023年高一化学寒假精品课(人教版2019必修第二册)(已下线)化学反应与能量——进阶学习6.1.4化学平衡状态(课中)-2019苏教版必修2课前课中课后(已下线)6.2.2化学反应的限度-随堂练习(已下线)专题06 化学反应的速率与限度(考题猜想)(8大题型)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)
名校
10 . 液氨作为一种潜在的汽车燃料已受到人们的普遍重视。它在安全性、价格等方面比化石燃料和氢燃料有着较大的优势,氨的燃烧实验涉及下列两个反应:
①4NH3(g)+5O2(g)=4NO(g)+6H2O(l) △H1
②4NH3(g)+6NO(g)=5N2(g)+6H2O(l) △H2
(1)反应4NH3(g)+3O2(g)=2N2(g)+6H2O(l)的△H=_______ (用含有△H1、△H2的式子表示)。
(2)若NH3(g)⇌ N2(g)+
N2(g)+ H2(g) K=A,则N2(g)+3H2(g) ⇌ 2NH3(g) K′=
H2(g) K=A,则N2(g)+3H2(g) ⇌ 2NH3(g) K′=____ (用A表示)。
(3)一定温度下,在恒容密闭容器中按照n(NH3)∶n(NO)=1∶3充入反应物,发生反应4NH3(g)+6NO(g)=5N2(g)+6H2O(l)。下列不能判断该反应达到平衡状态的是_______ 。
A.混合气体的平均摩尔质量保持不变
B.容器内物质的总质量保持不变
C. c(H2O)保持不变
D. n(NH3)∶n(NO)保持不变
E.有1molN-H键断裂的同时,有1molO-H键断裂
(4)向容积为3L的恒容密闭容器中投入4.0molN2和9.0molH2,在一定条件下发生反应N2(g)+3H2(g)⇌2NH3(g),仅改变温度测得平衡时的数据如表所示:
已知:断裂1.0molN2(g)和3.0molH2(g)中的化学键消耗的总能量小于断裂2.0molNH3(g)中的化学键消耗的能量。
①则T1_______ T2(填“>”“<”或“=”)。
②在T2 K下,经过10min达到化学平衡状态,则0~10min内,H2的平均反应速率v(H2)=_______ mol/(L·min),平衡时N2的转化率α(N2)=_______ 。
①4NH3(g)+5O2(g)=4NO(g)+6H2O(l) △H1
②4NH3(g)+6NO(g)=5N2(g)+6H2O(l) △H2
(1)反应4NH3(g)+3O2(g)=2N2(g)+6H2O(l)的△H=
(2)若NH3(g)⇌
 N2(g)+
N2(g)+ H2(g) K=A,则N2(g)+3H2(g) ⇌ 2NH3(g) K′=
H2(g) K=A,则N2(g)+3H2(g) ⇌ 2NH3(g) K′=(3)一定温度下,在恒容密闭容器中按照n(NH3)∶n(NO)=1∶3充入反应物,发生反应4NH3(g)+6NO(g)=5N2(g)+6H2O(l)。下列不能判断该反应达到平衡状态的是
A.混合气体的平均摩尔质量保持不变
B.容器内物质的总质量保持不变
C. c(H2O)保持不变
D. n(NH3)∶n(NO)保持不变
E.有1molN-H键断裂的同时,有1molO-H键断裂
(4)向容积为3L的恒容密闭容器中投入4.0molN2和9.0molH2,在一定条件下发生反应N2(g)+3H2(g)⇌2NH3(g),仅改变温度测得平衡时的数据如表所示:
| 温度/K | 平衡时NH3的物质的量/mol |
| T1 | 2.4 |
| T2 | 2.0 |
①则T1
②在T2 K下,经过10min达到化学平衡状态,则0~10min内,H2的平均反应速率v(H2)=
您最近一年使用:0次



