名校
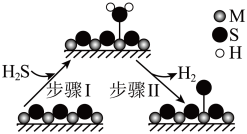
1 . 金属硫化物(MxSy)催化反应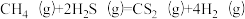 ,既可以除去天然气中的H2S,又可以获得H2.下列说法正确的是
,既可以除去天然气中的H2S,又可以获得H2.下列说法正确的是
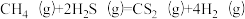 ,既可以除去天然气中的H2S,又可以获得H2.下列说法正确的是
,既可以除去天然气中的H2S,又可以获得H2.下列说法正确的是
A.该反应的 S<0 S<0 |
B.该反应的平衡常数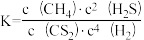 |
| C.其他条件相同,增大体系压强,能提高H2S的平衡转化率 |
| D.题图所示的反应机理中,步骤I可理解为H2S中带部分负电荷的S与催化剂中的M之间发生作用 |
您最近半年使用:0次
名校
2 . 下列叙述不能用勒夏特列原理解释的是
| A.氯气在饱和食盐水中的溶解度比在水中小 |
| B.利用TiCl4水解制备TiO2时,需加入大量水并加热 |
| C.由H2、I2(g)和HI组成的平衡体系,加压后颜色变深 |
| D.在含有Fe(SCN)3的红色溶液中加铁粉,振荡静置后溶液颜色变浅或褪去 |
您最近半年使用:0次
名校
3 . 一定条件下,1-苯基丙炔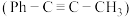 与HCl发生催化加成,反应如下:
与HCl发生催化加成,反应如下:
反应Ⅰ: 产物A:
产物A: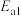 ;
;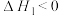
反应Ⅱ: 产物B:
产物B: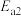 ;
;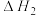
反应Ⅲ: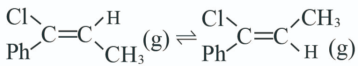 ;
;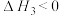
T℃,向密闭容器中通入2molPh-C≡C-CH3(g)和3molHCl(g),平衡时测得Ph-C≡C-CH3(g)的转化率为 ,反应Ⅲ的平衡常数
,反应Ⅲ的平衡常数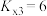 ,反应过程中有机物的物质的量分数随时间变化如图。下列说法错误的是
,反应过程中有机物的物质的量分数随时间变化如图。下列说法错误的是
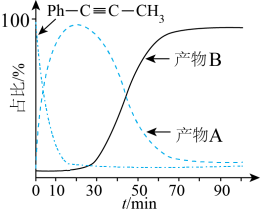
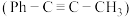 与HCl发生催化加成,反应如下:
与HCl发生催化加成,反应如下:反应Ⅰ:
 产物A:
产物A: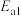 ;
;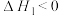
反应Ⅱ:
 产物B:
产物B: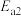 ;
;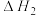
反应Ⅲ:
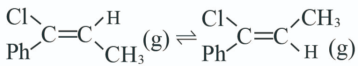 ;
;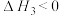
T℃,向密闭容器中通入2molPh-C≡C-CH3(g)和3molHCl(g),平衡时测得Ph-C≡C-CH3(g)的转化率为
 ,反应Ⅲ的平衡常数
,反应Ⅲ的平衡常数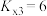 ,反应过程中有机物的物质的量分数随时间变化如图。下列说法错误的是
,反应过程中有机物的物质的量分数随时间变化如图。下列说法错误的是
A.活化能: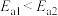 |
B.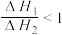 |
C.T℃反应的平衡常数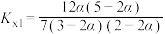 |
| D.若保持温度和压强不变,再向容器中通N2,反应I的化学平衡将逆向移动 |
您最近半年使用:0次
名校
解题方法
4 . 下列说法正确的是
A.25℃时,0.1 的醋酸溶液加水稀释,所有离子的浓度均减小 的醋酸溶液加水稀释,所有离子的浓度均减小 |
B.保持温度不变,向稀氨水中缓慢通入 ,溶液中 ,溶液中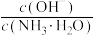 的值减少 的值减少 |
C.反应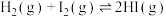 达平衡时,将容积缩小一半,混合气体颜色不变 达平衡时,将容积缩小一半,混合气体颜色不变 |
D.反应 在一定条件下能自发进行,该反应一定为放热反应 在一定条件下能自发进行,该反应一定为放热反应 |
您最近半年使用:0次
解题方法
5 . 环氧乙烷(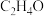 )被广泛地应用于洗涤、制药、印染等行业。工业上通常采用乙烯(
)被广泛地应用于洗涤、制药、印染等行业。工业上通常采用乙烯( )直接氧化法制取环氧乙烷,体系中发生的反应如下:
)直接氧化法制取环氧乙烷,体系中发生的反应如下:
主反应:


副反应: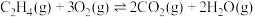

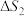
回答下列问题:
(1)已知几种化学键的键能如表所示:
试计算
___________ 。
(2)主反应与副反应的吉布斯自由能变( )与温度T的关系如图所示,则副反应的
)与温度T的关系如图所示,则副反应的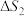
___________ (填“>”“<”或“=”)0,
___________ (填“>”“<”或“=”)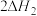 。
。

(3)在250℃、101kPa下,向某密闭容器中充入一定量的 和
和 ,同时发生上述两个反应,充分反应后,体系中含碳组分含量最高的是
,同时发生上述两个反应,充分反应后,体系中含碳组分含量最高的是 ,增大压强,
,增大压强, 的含量将
的含量将___________ (填“增大”“减小”或“不变”)。工业生产中常采用的反应条件为250℃、2.0MPa,并选择Ag作催化剂,充分反应后体系中含碳组分含量最高的是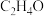 ,则Ag所起的作用可能为
,则Ag所起的作用可能为___________ 。
(4)一定条件下,用富氧空气(只含 和
和 ,且
,且 的体积分数为55%)代替
的体积分数为55%)代替 ,将
,将 、
、 、
、 按物质的量之比为11:11:1通入某恒容密闭容器中,发生上述两个反应,平衡时测得容器内总压为2.0MPa,
按物质的量之比为11:11:1通入某恒容密闭容器中,发生上述两个反应,平衡时测得容器内总压为2.0MPa, 的体积分数为31.25%,
的体积分数为31.25%,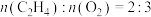 ,则
,则 和
和 的平衡转化率之比为
的平衡转化率之比为___________ ,该条件下主反应的压强平衡常数
___________  (
( 为用分压代替浓度的平衡常数,各组分分压=各组分物质的量分数×总压)。
为用分压代替浓度的平衡常数,各组分分压=各组分物质的量分数×总压)。
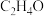 )被广泛地应用于洗涤、制药、印染等行业。工业上通常采用乙烯(
)被广泛地应用于洗涤、制药、印染等行业。工业上通常采用乙烯( )直接氧化法制取环氧乙烷,体系中发生的反应如下:
)直接氧化法制取环氧乙烷,体系中发生的反应如下:主反应:



副反应:
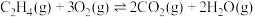

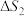
回答下列问题:
(1)已知几种化学键的键能如表所示:
| 化学键 | C-H | C=C | C-C | C-O | O=O |
键能 | 423 | 682 | 368 | 335 | 498 |

(2)主反应与副反应的吉布斯自由能变(
 )与温度T的关系如图所示,则副反应的
)与温度T的关系如图所示,则副反应的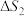

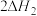 。
。
(3)在250℃、101kPa下,向某密闭容器中充入一定量的
 和
和 ,同时发生上述两个反应,充分反应后,体系中含碳组分含量最高的是
,同时发生上述两个反应,充分反应后,体系中含碳组分含量最高的是 ,增大压强,
,增大压强, 的含量将
的含量将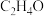 ,则Ag所起的作用可能为
,则Ag所起的作用可能为(4)一定条件下,用富氧空气(只含
 和
和 ,且
,且 的体积分数为55%)代替
的体积分数为55%)代替 ,将
,将 、
、 、
、 按物质的量之比为11:11:1通入某恒容密闭容器中,发生上述两个反应,平衡时测得容器内总压为2.0MPa,
按物质的量之比为11:11:1通入某恒容密闭容器中,发生上述两个反应,平衡时测得容器内总压为2.0MPa, 的体积分数为31.25%,
的体积分数为31.25%,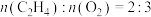 ,则
,则 和
和 的平衡转化率之比为
的平衡转化率之比为
 (
( 为用分压代替浓度的平衡常数,各组分分压=各组分物质的量分数×总压)。
为用分压代替浓度的平衡常数,各组分分压=各组分物质的量分数×总压)。
您最近半年使用:0次
解题方法
6 . H2O2俗称双氧水,是常用的绿色氧化剂,在生产和生活中发挥重要的作用。
(1)富勒烯C60颗粒对H2O2液相氧化:SO2具有明显的促进效果,该反应机理和能量变化如下:
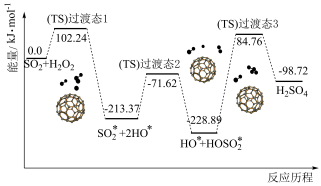
①H2O2液相氧化:SO2生成H2SO4的热化学方程式为________ 。
②图示历程包含________ 个基元反应,写出决速步骤的化学方程式________________ 。
③C60间的作用力是________ 。
(2) H2O2可用于工业源氮氧化物(NOx)的催化氧化,H2O2去除NO的反应存在平衡:
(i)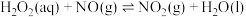
(ii)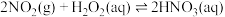
(iii)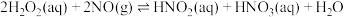
(iv)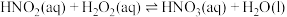
①上述反应体系在一定条件下建立平衡后,下列说法正确的有________ (填序号)。
A.其他条件不变时,温度越高,NO的转化率越大
B.加入催化剂,c(HNO3)与c(HNO2)比值保持不变
C.恒温恒压下,充入Ar,平衡(i)、(ii)向正反应方向移动
D.增大H2O2浓度,反应(i)、(ii)、(iii)、(iv)正反应速率都增加
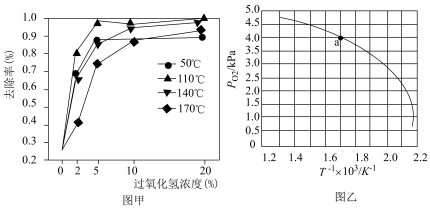
②一定范围内,催化剂光热协同辅助H2O2降解NO的去除率变化如图甲所示,NO去除率最佳的反应条件为________ 。
(3)过碳酸钠(2Na2CO3∙3H2O2)又称固体过氧化氢,是碳酸钠和过氧化氢的加成复合物。将2Na2CO3∙3H2O2置入真空的刚性容器中,升高温度发生分解反应:
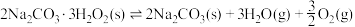 平衡时
平衡时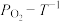 的关系如上图乙所示。a点时,该反应的平衡总压=
的关系如上图乙所示。a点时,该反应的平衡总压=________ kPa,平衡常数Kp=________ 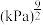 (列出算式),Kp随温度升高而
(列出算式),Kp随温度升高而________ (填“增大”、“减少”或“不变”)。
(1)富勒烯C60颗粒对H2O2液相氧化:SO2具有明显的促进效果,该反应机理和能量变化如下:

①H2O2液相氧化:SO2生成H2SO4的热化学方程式为
②图示历程包含
③C60间的作用力是
(2) H2O2可用于工业源氮氧化物(NOx)的催化氧化,H2O2去除NO的反应存在平衡:
(i)
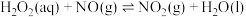
(ii)
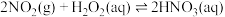
(iii)
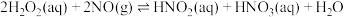
(iv)
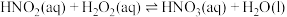
①上述反应体系在一定条件下建立平衡后,下列说法正确的有
A.其他条件不变时,温度越高,NO的转化率越大
B.加入催化剂,c(HNO3)与c(HNO2)比值保持不变
C.恒温恒压下,充入Ar,平衡(i)、(ii)向正反应方向移动
D.增大H2O2浓度,反应(i)、(ii)、(iii)、(iv)正反应速率都增加
②一定范围内,催化剂光热协同辅助H2O2降解NO的去除率变化如图甲所示,NO去除率最佳的反应条件为

(3)过碳酸钠(2Na2CO3∙3H2O2)又称固体过氧化氢,是碳酸钠和过氧化氢的加成复合物。将2Na2CO3∙3H2O2置入真空的刚性容器中,升高温度发生分解反应:
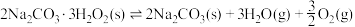 平衡时
平衡时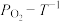 的关系如上图乙所示。a点时,该反应的平衡总压=
的关系如上图乙所示。a点时,该反应的平衡总压=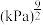 (列出算式),Kp随温度升高而
(列出算式),Kp随温度升高而
您最近半年使用:0次
名校
解题方法
7 . 生活中的一些现象常常涉及化学知识。下列分析中不正确 的是
| A.咀嚼米饭时,越嚼越甜,因为淀粉水解生成了麦芽糖 |
| B.木糖醇(C5H12O5)是一种天然甜味剂,属于糖类化合物 |
| C.维生素C又称为“抗坏血酸”,可以促进人体铁元素的吸收 |
| D.打开汽水瓶盖,有大量气泡冒出,因为减小压强后二氧化碳的溶解度减小 |
您最近半年使用:0次
名校
8 . 在一定温度下的可逆反应X(g) 2Y(g)
2Y(g)  >0,v正=k正c(X),v逆=k逆c2(Y)(k为速率常数),若在该温度下的k正=10k逆,下列说法错误的是
>0,v正=k正c(X),v逆=k逆c2(Y)(k为速率常数),若在该温度下的k正=10k逆,下列说法错误的是
 2Y(g)
2Y(g)  >0,v正=k正c(X),v逆=k逆c2(Y)(k为速率常数),若在该温度下的k正=10k逆,下列说法错误的是
>0,v正=k正c(X),v逆=k逆c2(Y)(k为速率常数),若在该温度下的k正=10k逆,下列说法错误的是| A.该温度下的平衡常数为10 |
| B.升高温度,k正增大的倍数小于k逆增大的倍数 |
| C.有利于测定X的相对分子质量的条件为高温低压 |
| D.恒压条件下,向平衡体系中充入惰性气体He,X的转化率增大 |
您最近半年使用:0次
2024-04-05更新
|
63次组卷
|
2卷引用:浙江省杭州市精诚联盟2023-2024学年高二上学期12月月考化学试题
解题方法
9 . 丙烯是重要的有机原料之一,可通过多种途径制备。回答下列问题:
Ⅰ.由丙烷直接脱氢法制备:

(1)已知键能: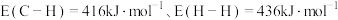 ;生成
;生成 碳碳
碳碳 键放出的能量为
键放出的能量为 ,则
,则
_____  。
。
(2)在一定温度下,保持总压为 ,将
,将 和
和 的混合气体分别按
的混合气体分别按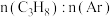 为
为 和
和 向密闭容器中投料,发生脱氢反应,测得
向密闭容器中投料,发生脱氢反应,测得 的转化率与时间的关系如图1所示(已知
的转化率与时间的关系如图1所示(已知 时反应处于平衡状态)。
时反应处于平衡状态)。

 点对应的投料方式为
点对应的投料方式为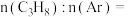
_____ ,原因是_____ 。 内,曲线
内,曲线_____ (填“ ”“
”“ ”)对应的平均反应速率最快。
”)对应的平均反应速率最快。 点对应的平衡常数
点对应的平衡常数
_____  (以分压表示,分压=总压×物质的量分数,保留一位小数)。
(以分压表示,分压=总压×物质的量分数,保留一位小数)。
Ⅱ.由丙烷氧化脱氢法制备。主要涉及反应: ;
;
(3)在一定条件下,将物质的量之比为 的
的 和
和 匀速通入体积可变的反应容器中发生上述反应,使总压强恒定为
匀速通入体积可变的反应容器中发生上述反应,使总压强恒定为 。在不同温度下反应相同时间,测得丙烷和氧气的转化率与温度倒数
。在不同温度下反应相同时间,测得丙烷和氧气的转化率与温度倒数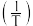 的关系如图2所示。
的关系如图2所示。
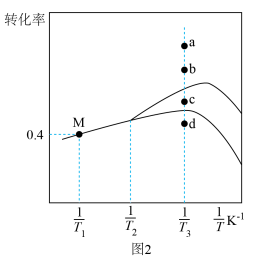
 时,容器内两种气体的物质的量之比
时,容器内两种气体的物质的量之比
_____  (填“>”“<”或“=”);若
(填“>”“<”或“=”);若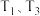 对应的点均处于平衡状态,保持其他条件不变,仅将容器更换为恒容的刚性容器,则图示点
对应的点均处于平衡状态,保持其他条件不变,仅将容器更换为恒容的刚性容器,则图示点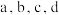 中,
中, 与
与 新的转化率点可能依次是
新的转化率点可能依次是_____ (填代号);M点丙烷的分压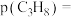
_____  (保留两位有效数字)。
(保留两位有效数字)。
Ⅰ.由丙烷直接脱氢法制备:


(1)已知键能:
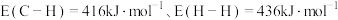 ;生成
;生成 碳碳
碳碳 键放出的能量为
键放出的能量为 ,则
,则
 。
。(2)在一定温度下,保持总压为
 ,将
,将 和
和 的混合气体分别按
的混合气体分别按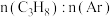 为
为 和
和 向密闭容器中投料,发生脱氢反应,测得
向密闭容器中投料,发生脱氢反应,测得 的转化率与时间的关系如图1所示(已知
的转化率与时间的关系如图1所示(已知 时反应处于平衡状态)。
时反应处于平衡状态)。
 点对应的投料方式为
点对应的投料方式为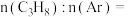
 内,曲线
内,曲线 ”“
”“ ”)对应的平均反应速率最快。
”)对应的平均反应速率最快。 点对应的平衡常数
点对应的平衡常数
 (以分压表示,分压=总压×物质的量分数,保留一位小数)。
(以分压表示,分压=总压×物质的量分数,保留一位小数)。Ⅱ.由丙烷氧化脱氢法制备。主要涉及反应:
 ;
;
(3)在一定条件下,将物质的量之比为
 的
的 和
和 匀速通入体积可变的反应容器中发生上述反应,使总压强恒定为
匀速通入体积可变的反应容器中发生上述反应,使总压强恒定为 。在不同温度下反应相同时间,测得丙烷和氧气的转化率与温度倒数
。在不同温度下反应相同时间,测得丙烷和氧气的转化率与温度倒数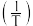 的关系如图2所示。
的关系如图2所示。
 时,容器内两种气体的物质的量之比
时,容器内两种气体的物质的量之比
 (填“>”“<”或“=”);若
(填“>”“<”或“=”);若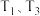 对应的点均处于平衡状态,保持其他条件不变,仅将容器更换为恒容的刚性容器,则图示点
对应的点均处于平衡状态,保持其他条件不变,仅将容器更换为恒容的刚性容器,则图示点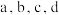 中,
中, 与
与 新的转化率点可能依次是
新的转化率点可能依次是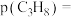
 (保留两位有效数字)。
(保留两位有效数字)。
您最近半年使用:0次
10 . 化学无处不在,下列有关说法正确的是
| A.淀粉、纤维素、油脂均属于天然高分子 |
| B.炒菜后铁锅不及时清理容易生锈,因为潮湿环境中铁锅发生析氢腐蚀 |
| C.打开汽水瓶盖有大量气泡冒出,可用勒夏特列原理解释 |
| D.向鸡蛋清溶液中加入食盐浓溶液有白色沉淀析出,因为食盐能使蛋白质变性 |
您最近半年使用:0次



