名校
1 . 下列说法中正确的个数为
①Cu的第二电离能大于Zn的第二电离能
②H与Cl以1﹕1的关系结合为HCl是因为共价键具有方向性
③ 的VSEPR模型与空间结构一致
的VSEPR模型与空间结构一致
④在冰晶体中,每个H2O分子周围紧邻的分子有4个,是因为水分子之间存在氢键,氢键也具有方向性和饱和性
①Cu的第二电离能大于Zn的第二电离能
②H与Cl以1﹕1的关系结合为HCl是因为共价键具有方向性
③
 的VSEPR模型与空间结构一致
的VSEPR模型与空间结构一致④在冰晶体中,每个H2O分子周围紧邻的分子有4个,是因为水分子之间存在氢键,氢键也具有方向性和饱和性
| A.1 | B.2 | C.3 | D.4 |
您最近一年使用:0次
名校
解题方法
2 . 下列说法正确的是
| A.杂化轨道只用于形成σ键 |
B. 分子N原子的杂化方式为 分子N原子的杂化方式为 |
C. 的VSEPR模型为三角锥形 的VSEPR模型为三角锥形 |
D.HF分子间氢键可表示为: |
您最近一年使用:0次
解题方法
3 . 下列离子的 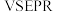 模型与其空间结构一致的是
模型与其空间结构一致的是
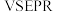 模型与其空间结构一致的是
模型与其空间结构一致的是A. | B. | C.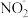 | D. |
您最近一年使用:0次
4 . 下列表示不正确 的是
A.硝化甘油的结构简式: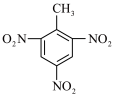 | B.中子数为20的氯离子: |
C.2-丁烯的实验式: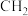 | D. 的价层电子对互斥(VSEPR)模型: 的价层电子对互斥(VSEPR)模型: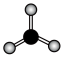 |
您最近一年使用:0次
2024-04-29更新
|
412次组卷
|
3卷引用:浙江绍兴市2023-2024学年高三下学期选考科目适应性考试化学试题
5 . 下列有关化学用语正确的是
A. 中的 中的 键电子云轮廓图: 键电子云轮廓图: |
B. 空间结构与VSEPR模型都是平面三角形 空间结构与VSEPR模型都是平面三角形 |
C. 分子的球棍模型: 分子的球棍模型: |
D.邻羟基苯甲醛分子内氢键示意图: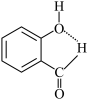 |
您最近一年使用:0次
名校
解题方法
6 . 用价层电子对互斥理论 可以预测许多分子或离子的立体构型,有时也能用来推测键角大小,下列判断正确的是
可以预测许多分子或离子的立体构型,有时也能用来推测键角大小,下列判断正确的是
 可以预测许多分子或离子的立体构型,有时也能用来推测键角大小,下列判断正确的是
可以预测许多分子或离子的立体构型,有时也能用来推测键角大小,下列判断正确的是| A.SO2、CS2都是直线形的分子 | B.键角由大到小顺序:CH4>NH3>H2O |
| C.BF3、NH3都是平面三角形的分子 | D.PCl3、SO3都是三角锥形的分子 |
您最近一年使用:0次
2024-04-29更新
|
134次组卷
|
2卷引用:湖北省鄂东南省级示范高中教育教学改革联盟学校2023-2024学年高二下学期期中联考化学试卷
7 . 氢氟酸可以溶蚀石英玻璃,反应方程式为: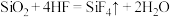 。设NA为阿伏加德罗常数的值,下列说法正确的是
。设NA为阿伏加德罗常数的值,下列说法正确的是
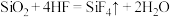 。设NA为阿伏加德罗常数的值,下列说法正确的是
。设NA为阿伏加德罗常数的值,下列说法正确的是| A.每60gSiO2含NA个SiO2分子 | B.标准状况下,1molHF体积为22.4L |
| C.1molH2O含有孤对电子数为2NA | D.0.1mol/L的氢氟酸中含H+数小于0.1NA |
您最近一年使用:0次
名校
8 . 侯氏制碱法的基本反应为NaCl + H2O + NH3 + CO2 = NaHCO3↓ + NH4Cl。下列说法正确的是
A.Na+的结构示意图为 | B.CO2的空间构型为V形 |
C.NH3的电子式为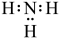 | D.NaHCO3既含离子键又含共价键 |
您最近一年使用:0次
名校
解题方法
9 . 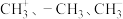 都是重要的有机反应中间体,有关它们的说法正确的是
都是重要的有机反应中间体,有关它们的说法正确的是
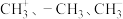 都是重要的有机反应中间体,有关它们的说法正确的是
都是重要的有机反应中间体,有关它们的说法正确的是A.它们的碳原子均采取 杂化,其中 杂化,其中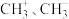 的结构示意图分别为: 的结构示意图分别为: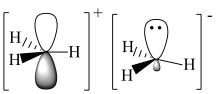 |
B. 与 与 形成的化合物中含有离子键 形成的化合物中含有离子键 |
C. 的键角和比 的键角和比 的键角小 的键角小 |
D. 与 与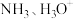 互为等电子体,VSEPR立体构型均为四面体形 互为等电子体,VSEPR立体构型均为四面体形 |
您最近一年使用:0次
解题方法
10 . 液氨是一种很好的溶剂,液氨可以微弱的电离产生NH 和NH
和NH 。NH3中的一个H原子若被-NH2取代可形成N2H4(联氨),若被-OH取代可形成NH2OH(羟胺)。在有NH
。NH3中的一个H原子若被-NH2取代可形成N2H4(联氨),若被-OH取代可形成NH2OH(羟胺)。在有NH 存在时,Cu(OH)2能溶于氨水形成[Cu(NH3)4]2+。NH3经过一定的转化可以形成N2、NO、NO2、N2O4(无色)、HNO3等。下列有关NH2OH、NH3、NH
存在时,Cu(OH)2能溶于氨水形成[Cu(NH3)4]2+。NH3经过一定的转化可以形成N2、NO、NO2、N2O4(无色)、HNO3等。下列有关NH2OH、NH3、NH 、NO
、NO 、[Cu(NH3)4]2+的说法正确的是
、[Cu(NH3)4]2+的说法正确的是
 和NH
和NH 。NH3中的一个H原子若被-NH2取代可形成N2H4(联氨),若被-OH取代可形成NH2OH(羟胺)。在有NH
。NH3中的一个H原子若被-NH2取代可形成N2H4(联氨),若被-OH取代可形成NH2OH(羟胺)。在有NH 存在时,Cu(OH)2能溶于氨水形成[Cu(NH3)4]2+。NH3经过一定的转化可以形成N2、NO、NO2、N2O4(无色)、HNO3等。下列有关NH2OH、NH3、NH
存在时,Cu(OH)2能溶于氨水形成[Cu(NH3)4]2+。NH3经过一定的转化可以形成N2、NO、NO2、N2O4(无色)、HNO3等。下列有关NH2OH、NH3、NH 、NO
、NO 、[Cu(NH3)4]2+的说法正确的是
、[Cu(NH3)4]2+的说法正确的是A.NO 的空间构型为三角锥形 的空间构型为三角锥形 | B.NH3中N原子的杂化方式皆为sp2 |
C.NH3的键角比NH 中的大 中的大 | D.1 mol [Cu(NH3)4]2+中含有σ键的数目为12 mol |
您最近一年使用:0次



