名校
1 . Cl2O是黄棕色具有强烈刺激性气味的气体,是一种强氧化剂,易溶于水且会与水反应生成次氯酸,与有机物、还原剂接触或加热时会发生燃烧并爆炸。制取Cl2O的装置如图所示。
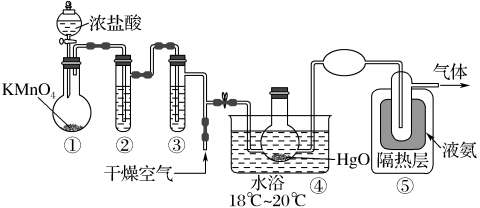
已知:Cl2O的熔点为-116℃,沸点为3.8℃,Cl2的沸点为-34.6℃;HgO+2Cl2=HgCl2+Cl2O
下列说法不正确的是

已知:Cl2O的熔点为-116℃,沸点为3.8℃,Cl2的沸点为-34.6℃;HgO+2Cl2=HgCl2+Cl2O
下列说法不正确的是
| A.装置②、③中盛装的试剂依次是饱和食盐水和浓硫酸 |
| B.通入干燥空气的目的是将生成的Cl2O稀释减少爆炸危险 |
| C.从装置⑤中逸出气体的主要成分是Cl2O |
| D.装置④与⑤之间不用橡皮管连接,是为了防止橡皮管燃烧和爆炸 |
您最近一年使用:0次
2020-12-27更新
|
1754次组卷
|
43卷引用:浙江省杭州市浙江大学附属中学2020-2021学年高一上学期10月份月测化学试题
浙江省杭州市浙江大学附属中学2020-2021学年高一上学期10月份月测化学试题(已下线)【浙江新东方】双师66云南省昆明市寻甸县民族中学2019-2020学年高一下学期第一次月考化学试题(已下线)第二章 海水中的重要元素——钠和氯(能力提升)-2020-2021学年高一化学单元测试定心卷(人教版2019必修第一册)安徽省六安市舒城中学2020-2021学年高一上学期第四次月考(12月)化学试题江苏省南京市六校联合2021-2022学年高一上学期期中调研考试化学试题天津市南开中学2021-2022学年高一上学期期中考试化学试题广东省广雅中学2021-2022学年高一上学期期中考试化学试题辽宁省实验中学2021-2022学年高一上学期12月月考化学试题辽宁省凌源市实验中学2021-2022学年高一上学期1月月考化学试题陕西省西北工业大学附属中学2021-2022学年高一下学期期中考试化学试题江苏省常州市第一中学2022-2023学年高一上学期期中质量调研化学试题福建省连城县第一中学2022-2023学年高一上学期第二次月考化学试题湖南省永州市第一中学2022-2023学年高一上学期期末考试化学试题章末检测卷(二) 海水中的重要元素——钠和氯湖南省长沙市第一中学2023-2024学年高一上学期期中考试化学试题福建省泉州市永春第一中学2023-2024学年高一上学期11月期中化学试题江西省信丰中学2023-2024学年高一上学期第二次月考化学试题天津市第二十中学2023-2024学年高一上学期期中考试化学试题山东省济宁市2017-2018学年度高三上学期期末考试化学试题山东省济宁市2018届高三上学期期末教学质量检测化学试题河北省定州中学2018届高三上学期期末考试化学试题(已下线)2019年8月13日 《每日一题》 (一轮复习) 氯气的制备及性质山西大学附中2020届高三上学期第二次模块诊断化学试题福建省漳平市第一中学2020届高三上学期第二次月考化学试题河北省衡水中学2020届高三上学期第四次调研考试化学试题2020届高三化学二轮冲刺新题专练——气体为载体的实验探究题(提升练)备考突破2020高三化学专题强化集训——基于气体的实验流程题湖南省衡阳市常宁五中2020届高三11月月考化学试题安徽省亳州市2019-2020学年高三上学期期末教学质量检测化学试题(已下线)【南昌新东方】 莲塘一中2020届高三10月质量检测山东省实验中学2020届高三下学期打靶模拟考试化学试题(已下线)第九单元 化学实验基础测试题-2021年高考化学一轮复习名师精讲练湖南省邵阳市邵东县创新实验学校2021届高三上学期10月月考化学试题(已下线)微专题21 新型含氯化合物的制备与性质探究(ClO2、NOCl等)-备战2022年高考化学考点微专题(已下线)考向11 氯及其化合物-备战2022年高考化学一轮复习考点微专题云南省大理州祥云四中2020届高三下学期3月线上模拟考试理综化学试题(已下线)第29讲 常见气体的制备与性质实验(练) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)考向33 从实验到化学-备战2022年高考化学一轮复习考点微专题(已下线)专题39 氯的氧化物、含氧酸及含氧酸盐-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)山东省枣庄市滕州市第一中学2022-2023学年高三上学期10月考试化学试题辽宁省铁岭市昌图县第一高级中学2022-2023学年高二下学期期末考试化学试题2024届河北省实验中学高三年级上学期第一次月考化学试题
19-20高一·浙江·期中
解题方法
2 . 常温常压下,一氧化二氯(Cl2O)为棕黄色气体,沸点为3.8℃,42℃以上会分解生成Cl2和O2,Cl2O易溶于水并与水反应生成HClO。将氯气和空气(不参与反应)按体积比1:3混合通入含水的碳酸钠中制备Cl2O(同时生成一种使澄清石灰水变浑浊的气体和一种盐),并用水吸收Cl2O(不含Cl2)制备次氯酸溶液。(Cl2在CCl4中的溶解度较大)

(1)各装置的连接顺序为___ 。
(2)装置B中多孔球泡和搅拌棒的作用是___ ;装置C的作用是___ 。
(3)B中的化学方程式为___ 。
(4)反应过程中,装置B需放在冷水中,其目的是___ 。

(1)各装置的连接顺序为
(2)装置B中多孔球泡和搅拌棒的作用是
(3)B中的化学方程式为
(4)反应过程中,装置B需放在冷水中,其目的是
您最近一年使用:0次
19-20高一·浙江·期中
解题方法
3 . TiCl4是制备钛及其化合物的重要中间体,某小组同学利用如图装置在实验室制备TiCl4,设计实验如图(夹持装置略去):
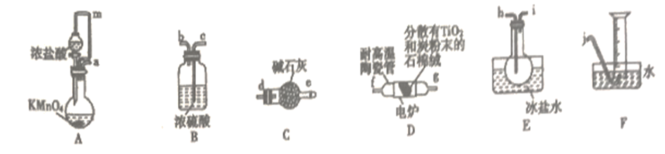
相关信息如表所示:
请回答下列问题:
(1)按照气流由左到右的方向,上述装置合理的连接顺序为a→___________ →___________ →f→g→___________ →___________ →d→e→j。(填仪器接口字母)
(2)根据完整的实验装置进行实验,实验步骤如下:检查装置气密性后,装入试剂,___________ (按正确的顺序填入下列操作的序号)。
①关闭分液漏斗活塞②打开分液漏斗活塞③停止加热,充分冷却④加热装置 D中陶瓷管
(3)装置A中导管m的作用是____________ 。
(4)装置D中除生成TiCl4外,还生成一种气态不成盐氧化物,该反应的化学方程式为___________ 。
(5)设计实验证明装置E中收集到的液体中含有TiCl4:___________ 。

相关信息如表所示:
| 化合物 | 熔点/℃ | 沸点/℃ | 密度/(g·cm-3) | 水溶性 |
| TiCl4 | -25 | 136 | 1.5 | 易与水反应,且生成难溶于水的物质,易升华,能溶于有机溶剂 |
| CCl4 | -25 | 76.8 | 1.6 | 难溶于水 |
(1)按照气流由左到右的方向,上述装置合理的连接顺序为a→
(2)根据完整的实验装置进行实验,实验步骤如下:检查装置气密性后,装入试剂,
①关闭分液漏斗活塞②打开分液漏斗活塞③停止加热,充分冷却④加热装置 D中陶瓷管
(3)装置A中导管m的作用是
(4)装置D中除生成TiCl4外,还生成一种气态不成盐氧化物,该反应的化学方程式为
(5)设计实验证明装置E中收集到的液体中含有TiCl4:
您最近一年使用:0次
20-21高一上·浙江·期中
解题方法
4 . 一氯化碘是一种红棕色液体,不溶于水,溶于乙醇和乙酸,能与KI反应生成I2,用于测定油脂中的碘值等(注:碘值表示有机物中不饱和程度的指标)。某校研究性学习小组的同学拟制备一氯化碘(沸点101℃)。回答下列问题:
(1)甲组同学拟利用干燥纯净的氯气与碘反应制备一氯化碘,已知碘与氯气的反应为放热反应,其装置如图:

①各装置连接顺序为A→___ 。
②B装置烧瓶需放在冷水中,其目的是___ ,D装置的作用是___ 。
(2)乙组同学采用最新报道制一氯化碘的方法,在三颈烧瓶中加入粗碘和盐酸,控制温度约50℃,在不断搅拌下逐滴加入氯酸钠溶液,生成一氯化碘,则发生反应的化学方程式为___ 。
(3)设计实验证明:ICl的氧化性比I2强:___ 。
(1)甲组同学拟利用干燥纯净的氯气与碘反应制备一氯化碘,已知碘与氯气的反应为放热反应,其装置如图:

①各装置连接顺序为A→
②B装置烧瓶需放在冷水中,其目的是
(2)乙组同学采用最新报道制一氯化碘的方法,在三颈烧瓶中加入粗碘和盐酸,控制温度约50℃,在不断搅拌下逐滴加入氯酸钠溶液,生成一氯化碘,则发生反应的化学方程式为
(3)设计实验证明:ICl的氧化性比I2强:
您最近一年使用:0次
19-20高一·浙江·阶段练习
解题方法
5 . 实验室里除了用二氧化锰和浓盐酸加热制取氯气,也可以利用反应:2KMnO4+16HCl(浓)=2KCl+2MnC12+5Cl2↑+8H2O制取并收集纯净、干燥的氯气,部分装置如图所示:
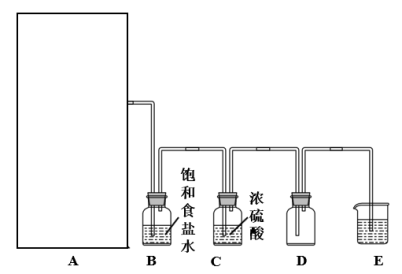
(1)若以KMnO4和浓盐酸为原料制取氯气,请根据反应原理从图中选择合适的制气装置___ (填代号)。
a.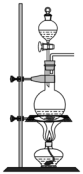 b.
b.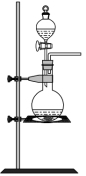 c.
c.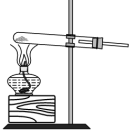
(2)装置B的作用___ 。
(3)E中的试剂选最好的是___ 。
A.NaOH溶液 B.NaCl溶液 C.Na2CO3溶液 D.水

(1)若以KMnO4和浓盐酸为原料制取氯气,请根据反应原理从图中选择合适的制气装置
a.
 b.
b. c.
c.
(2)装置B的作用
(3)E中的试剂选最好的是
A.NaOH溶液 B.NaCl溶液 C.Na2CO3溶液 D.水
您最近一年使用:0次
19-20高一·浙江·阶段练习
名校
解题方法
6 . 实验室用如图所示的仪器药品,对铁与氯气反应及产物进行如下的探究,已知氯化铁粉末很容易吸水生成结晶水化合物:FeCl3+6H2O= FeCl3·6H2O。

(1)按照气体流向从左到右顺序连接仪器应是(填仪器接口顺序)①接_____ ,_____ 接_____ ,_______ 接______ 。
(2)装置A中发生反应的离子方程式是___________ 。
(3)A、B中的酒精灯应先点燃________ 处(填“A”或“B”),装置C中的作用是 ____________ 。
(4)这套实验装置是否完整?________ (填“是”或“否”),若不完整还需补充___ 装置(若第一问填“是”,则此问不需要作答)。
(5)B中产物无水氯化铁与次氯酸钠、氢氧化钠共热可制取净水剂高铁酸钠(Na2FeO4,其中Fe元素为+6价),写出该反应的化学方程式_________ 。
(6)将反应后B中硬质玻璃管里的物质快速转移至锥形瓶中,并加入过量的稀盐酸和少许植物油(反应过程中不振荡),上述操作及后续实验如下:

请写出加入新制氯水时的离子方程式:____________ ;
根据上述实验现象与课本所学铁与氯气发生氧化还原反应的知识,判断B中硬质玻璃管里固体成分是_________ 。
A Fe和FeCl3 B FeCl2和FeCl3
C Fe、FeCl2和FeCl3 D Fe和FeCl2

(1)按照气体流向从左到右顺序连接仪器应是(填仪器接口顺序)①接
(2)装置A中发生反应的离子方程式是
(3)A、B中的酒精灯应先点燃
(4)这套实验装置是否完整?
(5)B中产物无水氯化铁与次氯酸钠、氢氧化钠共热可制取净水剂高铁酸钠(Na2FeO4,其中Fe元素为+6价),写出该反应的化学方程式
(6)将反应后B中硬质玻璃管里的物质快速转移至锥形瓶中,并加入过量的稀盐酸和少许植物油(反应过程中不振荡),上述操作及后续实验如下:

请写出加入新制氯水时的离子方程式:
根据上述实验现象与课本所学铁与氯气发生氧化还原反应的知识,判断B中硬质玻璃管里固体成分是
A Fe和FeCl3 B FeCl2和FeCl3
C Fe、FeCl2和FeCl3 D Fe和FeCl2
您最近一年使用:0次
名校
7 . ClO2与Cl2的氧化性相近,在自来水消毒和果蔬保鲜等方面应用广泛。某兴趣小组通过图1装置(夹持装置略)对其制备、吸收、释放和应用进行了研究。

(1)安装F中导管时,应选用图2中的________ 。
(2)打开B的活塞,A中发生反应:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O。为使ClO2在D中被稳定剂充分吸收,滴加稀盐酸的速度宜________ (填“快”或“慢”)。
(3)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为________ 。在ClO2释放实验中,打开E的活塞,D中发生反应,则装置F的作用是_________ 。
(4)已吸收ClO2气体的稳定剂Ⅰ和稳定剂Ⅱ,加酸后释放ClO2的浓度随时间的变化如图3所示。若将其用于水果保鲜,你认为效果较好的稳定剂是________ ,原因是_________ 。


(1)安装F中导管时,应选用图2中的
(2)打开B的活塞,A中发生反应:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O。为使ClO2在D中被稳定剂充分吸收,滴加稀盐酸的速度宜
(3)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为
(4)已吸收ClO2气体的稳定剂Ⅰ和稳定剂Ⅱ,加酸后释放ClO2的浓度随时间的变化如图3所示。若将其用于水果保鲜,你认为效果较好的稳定剂是

您最近一年使用:0次
8 . 无水AlCl3(183 ℃升华)遇潮湿空气即产生大量白雾,实验室可用Al和氯气通过下装置制备。已知A中产生的氯气混有少许HCl和水蒸气。则下列说法正确的是
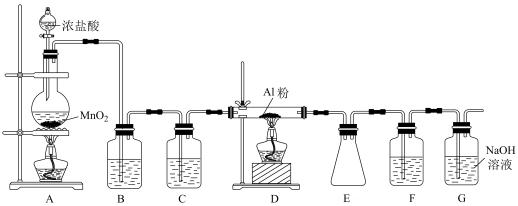

| A.试剂瓶B、C、F中分别盛饱和NaHCO3、浓硫酸、浓硫酸 |
| B.氯化铝产品最后在装置E中收集 |
| C.实验开始时应先点燃D处酒精灯 |
| D.装置F和G可用盛无水CaCl2的干燥管替换 |
您最近一年使用:0次
2020-11-19更新
|
895次组卷
|
16卷引用:浙江省宁波市2020-2021学年高一上学期期末九校联考化学试题
浙江省宁波市2020-2021学年高一上学期期末九校联考化学试题(已下线)【浙江新东方】高中化学20210304-029(已下线)【浙江新东方】在线化学53高一上广东省深圳市高级中学2020-2021学年高一上学期期中考试化学试题云南省曲靖市第二中学2020-2021学年高一上学期期末考试化学试题云南省曲靖市会泽县茚旺高级中学2020-2021学年高一下学期3月月考化学试题河北正定中学2020-2021学年高一上学期第二次半月考化学试题河北省辛集市第一中学2021-2022学年高一上学期第二次月考化学试题福建省龙岩第一中学2021-2022学年高一上学期第一次月考化学试题上海市奉贤区曙光中学2021-2022学年高一下学期期中检测化学试题黑龙江省勃利县高级中学2022-2023学年高一上学期11月期中考试化学试题广东省广州市广外、铁一、广大附中等三校2023~2024学年高一上学期期中联考化学试题广东省深圳外国语学校2022届高三上学期第一次月考化学试题河南省开封市杞县高中2021-2022学年高二下学期月考化学试题湖北省枣阳市第一中学2022-2023学年高三上学期9月月考化学试题黑龙江省佳木斯市第一中学2022-2023学年高三上学期第三次调研化学试题
19-20高一·浙江·阶段练习
9 . 下图是某位同学设计的实验装置, 制取 Cl2 并以 Cl2为原料制备纯净的无水 FeCl3粉末。已知:无水FeCl3 遇水强烈反应 。

(1)装置B的作用是_____________ 。
(2)实验时需要用到下列所有操作:
a.点燃 A 处的酒精灯;
b.打开分液漏斗旋塞,放入浓盐酸;
c.点燃 D 处的酒精灯;
d.检查装置气密性。
请给出上述操作的正确顺序_____________ (填字母)
(3)D中实验现象为______________________ 。
(4)装置E中倒置漏斗作用是________________ ,写出装置 E 中发生的反应的离子方程式:_________________________________________ 。
(5)某同学设计的上述实验装置示意图有一处不合理,请提出改进方案:___________ 。

(1)装置B的作用是
(2)实验时需要用到下列所有操作:
a.点燃 A 处的酒精灯;
b.打开分液漏斗旋塞,放入浓盐酸;
c.点燃 D 处的酒精灯;
d.检查装置气密性。
请给出上述操作的正确顺序
(3)D中实验现象为
(4)装置E中倒置漏斗作用是
(5)某同学设计的上述实验装置示意图有一处不合理,请提出改进方案:
您最近一年使用:0次
名校
解题方法
10 . Ⅰ“侯氏制碱法”是我国化工专家侯德榜为世界制碱工业作出的突出贡献。某实验小组模拟“侯氏法”的工艺流程及实验装置(部分夹持装置省略)如下:
气体A的饱和溶液 A与食盐的饱和溶液
A与食盐的饱和溶液 悬浊液
悬浊液 晶体
晶体 纯碱
纯碱
(1)气体A为______ (填化学式)。
(2)工业上粗盐(含Ca2+、Mg2+、SO 等杂质)经除杂得到氯化钠,判断氯化钠中的钠元素的具体操作为
等杂质)经除杂得到氯化钠,判断氯化钠中的钠元素的具体操作为___________ 。
(3)第Ⅲ步操作用到的主要玻璃仪器是________ 。
Ⅱ、某小组利用传感器探究Na2CO3和NaHCO3的性质。已知:氢氧根离子的浓度越小,溶液碱性越弱,(具体过程如图)
请回答:
(1)实验Ⅰ中,溶解时吸收热量的物质是_______ (填化学式)。
(2)实验Ⅱ中,滴加NaHCO3溶液的烧杯中溶液酸碱性变化与滴加Na2CO3溶液的有明显差异,原因是滴加NaHCO3溶液的烧杯中,_______ (填离子符号)参与了反应。
(3)若用方法Ⅲ验证Na2CO3和NaHCO3的稳定性,则试管B中装入的固体是____ (填化学式)。由此可知方法Ⅲ___ (填“能”或“不能”)鉴别Na2CO3和NaHCO3。
气体A的饱和溶液
 A与食盐的饱和溶液
A与食盐的饱和溶液 悬浊液
悬浊液 晶体
晶体 纯碱
纯碱(1)气体A为
(2)工业上粗盐(含Ca2+、Mg2+、SO
 等杂质)经除杂得到氯化钠,判断氯化钠中的钠元素的具体操作为
等杂质)经除杂得到氯化钠,判断氯化钠中的钠元素的具体操作为(3)第Ⅲ步操作用到的主要玻璃仪器是
Ⅱ、某小组利用传感器探究Na2CO3和NaHCO3的性质。已知:氢氧根离子的浓度越小,溶液碱性越弱,(具体过程如图)
| 编号 | 实验操作 |
| 实验Ⅰ | 测量下面实验过程中温度的变化 |
| 实验Ⅱ | 测量下面实验过程中溶液pH的变化 |
| 注:Na2CO3溶液和NaHCO3溶液的浓度相等 | |
| 实验Ⅲ |  |
(1)实验Ⅰ中,溶解时吸收热量的物质是
(2)实验Ⅱ中,滴加NaHCO3溶液的烧杯中溶液酸碱性变化与滴加Na2CO3溶液的有明显差异,原因是滴加NaHCO3溶液的烧杯中,
(3)若用方法Ⅲ验证Na2CO3和NaHCO3的稳定性,则试管B中装入的固体是
您最近一年使用:0次



