19-20高一·浙江·阶段练习
名校
解题方法
1 . 用金属钠制取氧化钠通常利用以下反应:2NaNO3+10Na=6Na2O+N2↑。下列说法正确的是
| A.该反应中Na为氧化剂 |
| B.该反应中氮气为氧化产物 |
| C.该反应中氧化钠为还原产物 |
| D.不用金属钠直接与空气中的氧气反应制备氧化钠的理由是NaNO3与Na反应生成的N2隔绝了空气中的O2,不会使Na2O被O2氧化为过氧化钠 |
您最近一年使用:0次
19-20高一·浙江·阶段练习
解题方法
2 . Cl2和Ca(OH)2制备少量漂粉精(一种含氨消毒剂)的装置如下。

(1)A为氯气发生装置,A中反应方程式是_____________ 。
(2)漂粉精常用于游泳池的消毒,起消毒作用的是HClO,漂粉精在水中释放HClO的途径如下:
途径一:Ca(ClO)2+2H2O=Ca(OH)2+2HClO
途径二:Ca(C1O)2+H2O+CO2=______ +____________ (把反应补充完整)。
(3)池水的酸碱性对漂粉精的消毒效果影响明显。
①池水碱性过强,杀毒作用会________ (填“增强"或“减弱")。
②池水酸性过强,会刺激眼睛和皮肤。通常加入Na2CO3、NaHCO3以降低酸性,起到降低酸性作用的离子分别是__________ (填离子符号)。
(4)定量检测实验中,规范的操作及实验步骤是确保结果准确性的关键。比如用36.5%、密度为1.19g/cm3的浓盐酸配制0.1mol/L的稀盐酸500mL,请回答:
①用量筒取所需要的浓盐酸的体积为____ mL。
②下列操作可能导致最终样品中所配溶液浓度偏高的是_______ (填字母)。
a.用量筒按事先计算结果量取一定量浓盐酸时,仰视刻度
b.配制过程中,第一次加水量太少,搅拌时间较长
c.浓盐酸在稀释后,但未等溶液冷却,就迅速转移、洗涤、定容
d.定容后摇匀,发现液面降低,再加水至刻度线

(1)A为氯气发生装置,A中反应方程式是
(2)漂粉精常用于游泳池的消毒,起消毒作用的是HClO,漂粉精在水中释放HClO的途径如下:
途径一:Ca(ClO)2+2H2O=Ca(OH)2+2HClO
途径二:Ca(C1O)2+H2O+CO2=
(3)池水的酸碱性对漂粉精的消毒效果影响明显。
①池水碱性过强,杀毒作用会
②池水酸性过强,会刺激眼睛和皮肤。通常加入Na2CO3、NaHCO3以降低酸性,起到降低酸性作用的离子分别是
(4)定量检测实验中,规范的操作及实验步骤是确保结果准确性的关键。比如用36.5%、密度为1.19g/cm3的浓盐酸配制0.1mol/L的稀盐酸500mL,请回答:
①用量筒取所需要的浓盐酸的体积为
②下列操作可能导致最终样品中所配溶液浓度偏高的是
a.用量筒按事先计算结果量取一定量浓盐酸时,仰视刻度
b.配制过程中,第一次加水量太少,搅拌时间较长
c.浓盐酸在稀释后,但未等溶液冷却,就迅速转移、洗涤、定容
d.定容后摇匀,发现液面降低,再加水至刻度线
您最近一年使用:0次
19-20高一·浙江·阶段练习
解题方法
3 . 高铁酸钾(K2FeO4)是一种理想的绿色高效水处理剂。某小组用如图所示能置(夹持仪器略去)制备KClO溶液,并通过KClO溶液与Fe(NO3)3溶液反应制备K2FeO4。
查资料知K2FeO4的部分性质如下:
①可溶于水、微溶于浓KOH溶液;
②在0~5℃、强碱性溶液中比校稳定;
③在Fe3+和Fe(OH)3催化作用下发生分解;
④在酸性至弱碱性条件下,能与水反应生成Fe(OH)3和O2。

请回答下列问题:
(1)仪器C和D中都盛有KOH溶液,其中C中KOH溶液的用途是_________ 。
(2)Cl2与KOH的浓溶液在较高温度下反应生成KClO3。为保证反应生成KClO,需要将反应温度控制在0-5℃下进行,在不改变KOH溶液浓度前提下,实验中可以采取的措施是__________________ 。
(3)在搅拌下,将Fe(NO3)3饱和溶液缓慢加到KClO饱和溶液中可制取K2FeO4。写出该反应的化学方程式:_________ 。该操作不能将KClO饱和溶液滴加到Fe(NO3)3饱和溶液中,其原因是__________ 。
查资料知K2FeO4的部分性质如下:
①可溶于水、微溶于浓KOH溶液;
②在0~5℃、强碱性溶液中比校稳定;
③在Fe3+和Fe(OH)3催化作用下发生分解;
④在酸性至弱碱性条件下,能与水反应生成Fe(OH)3和O2。

请回答下列问题:
(1)仪器C和D中都盛有KOH溶液,其中C中KOH溶液的用途是
(2)Cl2与KOH的浓溶液在较高温度下反应生成KClO3。为保证反应生成KClO,需要将反应温度控制在0-5℃下进行,在不改变KOH溶液浓度前提下,实验中可以采取的措施是
(3)在搅拌下,将Fe(NO3)3饱和溶液缓慢加到KClO饱和溶液中可制取K2FeO4。写出该反应的化学方程式:
您最近一年使用:0次
4 . 兴趣小组分析了用硫铁矿烧渣(主要成分Fe2O3、Fe3O4、FeO等)制备铁红(Fe2O3)的流程图并进行了铁红性质实验。
(一)铁红制备的流程图分析:
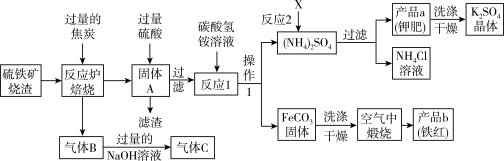
(1)若焙烧中碳与四氧化三铁反应后B中气体的比例恰好是1:1,其化学方程式:_________ 。
(2)实验室完成操作1,用到的玻璃仪器有烧杯、玻璃棒和____________ (填仪器名称)。
(3)你认为对气体C最佳的处理方法是________ (填选项序号)。
A.冷却后排入空气B.燃烧后排放C.再通入反应炉
(4)反应1的反应温度一般需控制在35℃以下,其目的是___________________ 。
(5)反应2中相关物质的溶解度如表,你认为该反应在常温下能实现的原因是:___________________ 。
洗涤干燥得到硫酸钾晶体时,可选用下列______ (选填序号,下同)洗涤剂
A.氯化钾饱和溶液B.水C.硫酸钾饱和溶液
为检验硫酸钾晶体是否洗涤干净,可取最后一次洗涤液,先加入________ ,振荡、静置,再向上层清液中滴加________ ,观察现象即可判断。
A.硝酸银溶液B.过量的氯化钡溶液C.过量的硝酸钡溶液
(二)铁红的性质实验
(6)实验装置:已知:草酸晶体(H2C2O4·3H2O)在浓H2SO4作用下受热分解,化学方程式为H2C2O4·3H2O CO2↑+CO↑+4H2O
CO2↑+CO↑+4H2O
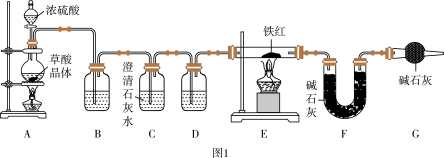
①实验前应先______________________ 。
②进入E中的气体是纯净、干燥的一氧化碳,则B、D中的试剂依次是______ 、______ (填字母编号)。
A.浓硫酸B.澄清的石灰水C.氢氧化钠溶液
③C装置的作用是________________________________ 。
(一)铁红制备的流程图分析:

(1)若焙烧中碳与四氧化三铁反应后B中气体的比例恰好是1:1,其化学方程式:
(2)实验室完成操作1,用到的玻璃仪器有烧杯、玻璃棒和
(3)你认为对气体C最佳的处理方法是
A.冷却后排入空气B.燃烧后排放C.再通入反应炉
(4)反应1的反应温度一般需控制在35℃以下,其目的是
(5)反应2中相关物质的溶解度如表,你认为该反应在常温下能实现的原因是:
| 物质 | X | K2SO4 | NH4C1 | (NH4)2SO4 |
| 溶解度g(25℃) | 34.0 | 11.1 | 37.2 | 19.2 |
洗涤干燥得到硫酸钾晶体时,可选用下列
A.氯化钾饱和溶液B.水C.硫酸钾饱和溶液
为检验硫酸钾晶体是否洗涤干净,可取最后一次洗涤液,先加入
A.硝酸银溶液B.过量的氯化钡溶液C.过量的硝酸钡溶液
(二)铁红的性质实验
(6)实验装置:已知:草酸晶体(H2C2O4·3H2O)在浓H2SO4作用下受热分解,化学方程式为H2C2O4·3H2O
 CO2↑+CO↑+4H2O
CO2↑+CO↑+4H2O
①实验前应先
②进入E中的气体是纯净、干燥的一氧化碳,则B、D中的试剂依次是
A.浓硫酸B.澄清的石灰水C.氢氧化钠溶液
③C装置的作用是
您最近一年使用:0次
名校
解题方法
5 . 已知无水AlCl3遇潮湿空气即产生大量白雾,实验室可用如图所示装置制备无水AlCl3。
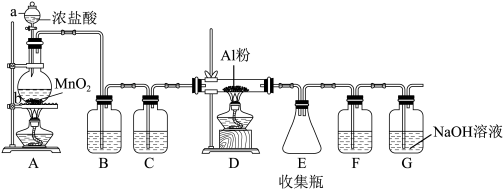
请回答:
(1)仪器a的名称是___ ,该仪器的优点有:减少浓盐酸的挥发和___ 。
(2)写出装置A中发生反应的化学方程式:___ ,该反应中浓盐酸体现的性质为___ 和___ ,两者的比例为___ 。
(3)装置B盛放的试剂是___ ,它的作用除降低氯气在水中的溶解量外还包括___ ;装置F中盛放的试剂是___ ,其作用是___ 。
(4)装置G的作用是___ (用离子方程式表示),检验氯气是否吸收完全,可以用___ (填试剂或用品名称)。
(5)已知无水AlCl3遇潮湿空气,能发生复分解反应,产生大量的白雾,请写出该反应的化学方程式___ 。
(6)已知氯酸钾和浓盐酸在不加热的条件下可以制备Cl2,反应如下:KClO3+6HCl=KCl+3Cl2↑+3H2O,回答下列小题:
①用双线桥标明该反应电子转移的方向和数目:___ ;
②KClO3和MnO2均能氧化HCl制备Cl2,比较KClO3和MnO2氧化性的强弱:KClO3___ MnO2(填“>”或“<”)。

请回答:
(1)仪器a的名称是
(2)写出装置A中发生反应的化学方程式:
(3)装置B盛放的试剂是
(4)装置G的作用是
(5)已知无水AlCl3遇潮湿空气,能发生复分解反应,产生大量的白雾,请写出该反应的化学方程式
(6)已知氯酸钾和浓盐酸在不加热的条件下可以制备Cl2,反应如下:KClO3+6HCl=KCl+3Cl2↑+3H2O,回答下列小题:
①用双线桥标明该反应电子转移的方向和数目:
②KClO3和MnO2均能氧化HCl制备Cl2,比较KClO3和MnO2氧化性的强弱:KClO3
您最近一年使用:0次
20-21高一上·浙江·期中
6 . 氯气是一种重要的化工原料,自来水的消毒、农药的生产、药物的合成都需要用它。
(1)工业上通常采用电解法制氯气,请观察图后回答下列问题:
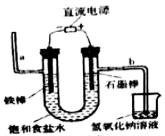
请写出该反应的化学方程式___________ 。
(2)某学生设计如图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉是一个放热反应,回答下列问题:
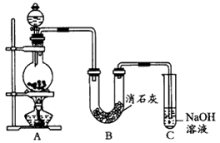
①漂白粉将在U形管中产生,其化学方程式是_________ ;
②装置C的作用是___________ ;
③此实验所得漂白粉的有效成分偏低,该学生经分析并查阅资料发现,温度较高时,氯气与消石灰发生副反应生成Ca(ClO3)2。有效成分偏低的可能原因有________ ,为提高产率,可采取的措施有_______ 。
(1)工业上通常采用电解法制氯气,请观察图后回答下列问题:

请写出该反应的化学方程式
(2)某学生设计如图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉是一个放热反应,回答下列问题:

①漂白粉将在U形管中产生,其化学方程式是
②装置C的作用是
③此实验所得漂白粉的有效成分偏低,该学生经分析并查阅资料发现,温度较高时,氯气与消石灰发生副反应生成Ca(ClO3)2。有效成分偏低的可能原因有
您最近一年使用:0次
20-21高一上·浙江·阶段练习
解题方法
7 . 如图是某位同学设计的实验装置,制取Cl2并以Cl2为原料制备无水FeCl3粉末。已知:无水FeCl3遇水强烈反应。
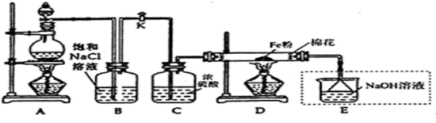
(1)A为氯气发生装置,写出反应的化学方程式:___ 。
(2)实验开始先点燃A处的酒精灯,打开旋塞K,让Cl2充满整个装置,再点燃D处的酒精灯Cl2通过C瓶后进入D,D装置内盛有铁粉,发生氧化还原反应,写出D装置中反应的化学方程式___ 。
(3)装置B的作用是___ 。
(4)某同学设计的上述实验装置示意图有一处不合理,会影响实验,请提出改进方案___ 。
(5)装置E的作用___ 。

(1)A为氯气发生装置,写出反应的化学方程式:
(2)实验开始先点燃A处的酒精灯,打开旋塞K,让Cl2充满整个装置,再点燃D处的酒精灯Cl2通过C瓶后进入D,D装置内盛有铁粉,发生氧化还原反应,写出D装置中反应的化学方程式
(3)装置B的作用是
(4)某同学设计的上述实验装置示意图有一处不合理,会影响实验,请提出改进方案
(5)装置E的作用
您最近一年使用:0次
名校
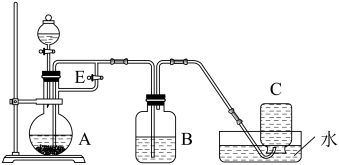
8 . 如图所示装置可用来制取 和观察
和观察 在空气中被氧化时的颜色变化。实验提供的试剂:铁屑、
在空气中被氧化时的颜色变化。实验提供的试剂:铁屑、 的硫酸溶液、
的硫酸溶液、 溶液。下列说法错误的是( )
溶液。下列说法错误的是( )
 和观察
和观察 在空气中被氧化时的颜色变化。实验提供的试剂:铁屑、
在空气中被氧化时的颜色变化。实验提供的试剂:铁屑、 的硫酸溶液、
的硫酸溶液、 溶液。下列说法错误的是( )
溶液。下列说法错误的是( )
A.已知B中盛有一定量的 溶液,则A中应预先加入的试剂是铁屑,C中收集到的气体主要是 溶液,则A中应预先加入的试剂是铁屑,C中收集到的气体主要是 |
B.实验开始时应先将 关闭 关闭 |
C.生成 的操作为:关闭 的操作为:关闭 ,将A中溶液压入B中 ,将A中溶液压入B中 |
| D.取下B的橡胶塞,使空气进入,颜色变化为白色变成灰绿色,最终变成红褐色 |
您最近一年使用:0次
2020-09-05更新
|
774次组卷
|
7卷引用:浙江省余姚中学2022-2023学年高一上学期期中考试化学试题
解题方法
9 . CuCl广泛应用于化工和印染等行业。某研究性学习小组拟热分解结晶水合物CuCl·2H2O制备CuCl,并进行相关探究。
查阅资料:CuCl2•2H2O CuCl2
CuCl2  CuCl+Cl2;CuCl2•2H2O
CuCl+Cl2;CuCl2•2H2O Cu2(OH)2Cl2
Cu2(OH)2Cl2 CuO
CuO
(实验探究)该小组用下图所示装置进行实验(夹持仪器略)。

请回答下列问题:
(1)仪器X的名称是___ ;装置D中倒扣的三角漏斗的作用是_____ ;
(2)实验操作的先后顺序是a→____ →____ →____ →e (填操作的编号)。
a.检查装置的气密性后加入药品 b.熄灭酒精灯,冷却 c.在“气体入口”处通入干燥HCl d.点燃酒精灯,加热 e.停止通入HCl,然后通入N2
(3)在实验过程中,观察到B中物质由白色变为蓝色,C中试纸的颜色变化是____ ;
(4)装置D中发生的氧化还原反应的离子方程式是_____ ;
(5)反应结束后,取出CuCl产品进行实验,发现其中含有少量的CuCl2或CuO杂质,根据资料信息分析:
①若杂质是CuCl2,则产生的原因是____ ;
②若杂质是CuO,则产生的原因是____ 。
查阅资料:CuCl2•2H2O
 CuCl2
CuCl2  CuCl+Cl2;CuCl2•2H2O
CuCl+Cl2;CuCl2•2H2O Cu2(OH)2Cl2
Cu2(OH)2Cl2 CuO
CuO(实验探究)该小组用下图所示装置进行实验(夹持仪器略)。

请回答下列问题:
(1)仪器X的名称是
(2)实验操作的先后顺序是a→
a.检查装置的气密性后加入药品 b.熄灭酒精灯,冷却 c.在“气体入口”处通入干燥HCl d.点燃酒精灯,加热 e.停止通入HCl,然后通入N2
(3)在实验过程中,观察到B中物质由白色变为蓝色,C中试纸的颜色变化是
(4)装置D中发生的氧化还原反应的离子方程式是
(5)反应结束后,取出CuCl产品进行实验,发现其中含有少量的CuCl2或CuO杂质,根据资料信息分析:
①若杂质是CuCl2,则产生的原因是
②若杂质是CuO,则产生的原因是
您最近一年使用:0次
名校
10 . 已知:2Al+3Cl2=2AlCl3,无水氯化铝遇潮湿的空气即产生大量白雾,实验室可用下列装置按一定的顺序连接,制备无水氯化铝。
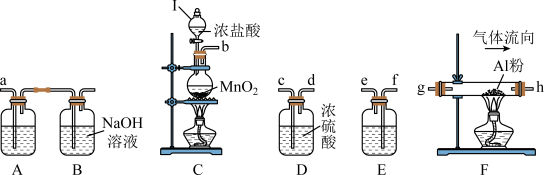
(1)写出仪器Ⅰ的名称___ 。装置C中发生反应的化学方程式为___ 。
(2)为达到实验目的,装置的连接顺序为(用字母“a”~“h”填写):b→___ →a。
(3)装置A盛放的试剂是___ ;装置E中盛放的试剂是___ 。装置B的作用是___ 。
(4)装置C的气密性检查的操作是___ 。

(1)写出仪器Ⅰ的名称
(2)为达到实验目的,装置的连接顺序为(用字母“a”~“h”填写):b→
(3)装置A盛放的试剂是
(4)装置C的气密性检查的操作是
您最近一年使用:0次



