名校
1 . 为测定某种铝镁合金中铝的质量分数,探究小组进行了实验:称取质量为20g的合金,加入300g的稀盐酸,合金恰好被溶解,并产生了质量为2g的氢气。以下问题均需要写出计算过程:
(1)铝镁合金中铝的质量分数是多少_______ ?
(2)所用稀盐酸的溶质质量分数是多少_______ ?
(3)若要将反应后的溶液中的溶质全部转变为MgCl2,至少需要加入多少质量的镁_______ ?
(1)铝镁合金中铝的质量分数是多少
(2)所用稀盐酸的溶质质量分数是多少
(3)若要将反应后的溶液中的溶质全部转变为MgCl2,至少需要加入多少质量的镁
您最近一年使用:0次
2 . 实验室通常利用质量分数36.5%盐酸(密度为1.14g/mL)与二氧化锰通过反应制取Cl2。通过计算回答下列问题:
(1)质量分数36.5%(密度为1.14g/mL)盐酸的物质的量浓度为_______ 。
(2)若要制取2.24L Cl2(标准状况),理论上需要消耗MnO2质量为_______ 克。
(3)此时,被氧化HCl的物质的量为_______ 。
(1)质量分数36.5%(密度为1.14g/mL)盐酸的物质的量浓度为
(2)若要制取2.24L Cl2(标准状况),理论上需要消耗MnO2质量为
(3)此时,被氧化HCl的物质的量为
您最近一年使用:0次
3 . 某纯碱样品中含有少量氯化钠。江津中学化学兴趣小组为测定样品中碳酸钠的质量分数,现称取该样品 ,加入到盛有
,加入到盛有 稀盐酸的烧杯中,恰好完全反应,最后称得烧杯中溶液的质量为
稀盐酸的烧杯中,恰好完全反应,最后称得烧杯中溶液的质量为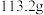 。计算:
。计算:
(1)产生的二氧化碳质量是多少_____ ?
(2)纯碱样品中碳酸钠的质量分数_____ ;(结果精确到 )
)
(3)反应后所得溶液的溶质质量分数_____ 。(结果精确到 )
)
 ,加入到盛有
,加入到盛有 稀盐酸的烧杯中,恰好完全反应,最后称得烧杯中溶液的质量为
稀盐酸的烧杯中,恰好完全反应,最后称得烧杯中溶液的质量为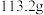 。计算:
。计算:(1)产生的二氧化碳质量是多少
(2)纯碱样品中碳酸钠的质量分数
 )
)(3)反应后所得溶液的溶质质量分数
 )
)
您最近一年使用:0次
解题方法
4 . 完成下列填空:
(1)某市售的浓氨水, 的质量分数为
的质量分数为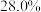 ,密度为
,密度为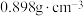 ,则该氨水的物质的量浓度为
,则该氨水的物质的量浓度为___________ 。
(2)已知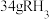 气体中含有
气体中含有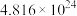 个原子,则该气体的摩尔质量为
个原子,则该气体的摩尔质量为___________ 。
(3)质量为___________  的
的 所含的电子的物质的量为
所含的电子的物质的量为 。
。
(4)质量比为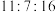 的
的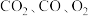 ,其物质的量之比为
,其物质的量之比为___________ 。
(5)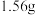 某金属与足量盐酸完全反应,生成
某金属与足量盐酸完全反应,生成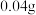 氢气,生成氯化物中金属显
氢气,生成氯化物中金属显 价,则该金属的摩尔质量为
价,则该金属的摩尔质量为___________ 。(写出计算过程)
(1)某市售的浓氨水,
 的质量分数为
的质量分数为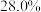 ,密度为
,密度为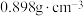 ,则该氨水的物质的量浓度为
,则该氨水的物质的量浓度为(2)已知
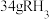 气体中含有
气体中含有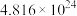 个原子,则该气体的摩尔质量为
个原子,则该气体的摩尔质量为(3)质量为
 的
的 所含的电子的物质的量为
所含的电子的物质的量为 。
。(4)质量比为
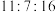 的
的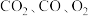 ,其物质的量之比为
,其物质的量之比为(5)
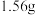 某金属与足量盐酸完全反应,生成
某金属与足量盐酸完全反应,生成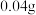 氢气,生成氯化物中金属显
氢气,生成氯化物中金属显 价,则该金属的摩尔质量为
价,则该金属的摩尔质量为
您最近一年使用:0次
名校
解题方法
5 . 请根据物质的量的相关概念及计算公式,完成下列各题:
(1)请填写下表:
(2)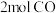 与
与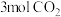 的质量之比
的质量之比__________ ;分子数之比为__________ ;含氧原子的数目之比为__________ 。
(3)将含杂质软锰矿粉末 与足量浓盐酸共热(杂质不与盐酸反应),完全反应后,制得
与足量浓盐酸共热(杂质不与盐酸反应),完全反应后,制得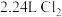 (标准状况下)。请回答下列问题:
(标准状况下)。请回答下列问题:
反应中被氧化的 的物质的量为
的物质的量为__________ mol,软锰矿中 的质量分数为
的质量分数为__________ 。
(1)请填写下表:
物质 | 摩尔质量 | 物质的量 | 质量 | 分子或离子数目 |
|
| |||
|
|
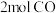 与
与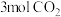 的质量之比
的质量之比(3)将含杂质软锰矿粉末
 与足量浓盐酸共热(杂质不与盐酸反应),完全反应后,制得
与足量浓盐酸共热(杂质不与盐酸反应),完全反应后,制得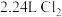 (标准状况下)。请回答下列问题:
(标准状况下)。请回答下列问题:反应中被氧化的
 的物质的量为
的物质的量为 的质量分数为
的质量分数为
您最近一年使用:0次
名校
6 . 按要求解答问题。
(1)已知标准状况下,气体A的密度为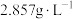 ,则气体A的相对分子质量约为
,则气体A的相对分子质量约为___________ 。
(2)两个相同容积的密闭容器X、Y,在25℃下,X中充入 A气体,Y中充入
A气体,Y中充入
 气体,X与Y内的压强之比是4:11,则A的摩尔质量为
气体,X与Y内的压强之比是4:11,则A的摩尔质量为___________ 。
(3)相同条件下,体积比为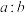 和质量比为
和质量比为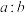 的
的 和
和 的混合气体,其平均摩尔质量分别是
的混合气体,其平均摩尔质量分别是___________ 和___________ 。
(4)在标准状况下,将
 气体溶于
气体溶于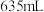 水中,所得盐酸的密度为
水中,所得盐酸的密度为 。试计算:
。试计算:
①所得盐酸的质量分数和物质的量浓度分别是___________ 、___________ 。
②取这种盐酸 ,稀释至
,稀释至 ,所得稀盐酸的物质的量浓度
,所得稀盐酸的物质的量浓度___________ 。
③在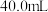

 溶液中,逐滴加入上述稀释后的稀盐酸,边加边振荡。若使反应不产生
溶液中,逐滴加入上述稀释后的稀盐酸,边加边振荡。若使反应不产生 气体,加入稀盐酸的体积最多不超过
气体,加入稀盐酸的体积最多不超过___________ mL。
(1)已知标准状况下,气体A的密度为
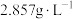 ,则气体A的相对分子质量约为
,则气体A的相对分子质量约为(2)两个相同容积的密闭容器X、Y,在25℃下,X中充入
 A气体,Y中充入
A气体,Y中充入
 气体,X与Y内的压强之比是4:11,则A的摩尔质量为
气体,X与Y内的压强之比是4:11,则A的摩尔质量为(3)相同条件下,体积比为
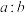 和质量比为
和质量比为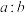 的
的 和
和 的混合气体,其平均摩尔质量分别是
的混合气体,其平均摩尔质量分别是(4)在标准状况下,将

 气体溶于
气体溶于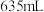 水中,所得盐酸的密度为
水中,所得盐酸的密度为 。试计算:
。试计算:①所得盐酸的质量分数和物质的量浓度分别是
②取这种盐酸
 ,稀释至
,稀释至 ,所得稀盐酸的物质的量浓度
,所得稀盐酸的物质的量浓度③在
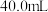

 溶液中,逐滴加入上述稀释后的稀盐酸,边加边振荡。若使反应不产生
溶液中,逐滴加入上述稀释后的稀盐酸,边加边振荡。若使反应不产生 气体,加入稀盐酸的体积最多不超过
气体,加入稀盐酸的体积最多不超过
您最近一年使用:0次
7 . 将质量为15g锌片浸入100.2克硫酸铜溶液中,一段时间后,取出锌片,洗涤、干燥、称量,锌片的质量为14.8克。(写出计算过程)
(1)生成铜的质量为多少?_______
(2)剩余的溶液中生成硫酸锌的质量分数为多少?_________
(1)生成铜的质量为多少?
(2)剩余的溶液中生成硫酸锌的质量分数为多少?
您最近一年使用:0次
23-24高二下·全国·课前预习
8 . 某种含C、H、O三种元素的未知物A,经燃烧分析实验测得其中碳的质量分数为52.16%,氢的质量分数为13.14%。则:
(1)氧的质量分数为___________ 。
(2)C、H、O的原子个数比N(C)∶N(H)∶N(O)≈___________ 。
(3)该未知物A的实验式为___________ 。
(1)氧的质量分数为
(2)C、H、O的原子个数比N(C)∶N(H)∶N(O)≈
(3)该未知物A的实验式为
您最近一年使用:0次
名校
解题方法
9 . 由N2与O2组成的混和气体对H2的相对密度为14.5,求混和气体中N2的体积分数与质量分数__________ (请写出计算过程)。
您最近一年使用:0次
2024高三下·全国·专题练习
解题方法
10 . 硫脲[CS(NH2)2]的分离及产品含量的测定。
装置C反应后的液体过滤后,将滤液减压蒸发浓缩,之后冷却结晶,离心分离,烘干即可得到产品。称取mg产品,加水溶解配成500mL溶液,量取25mL于锥形瓶中,滴加一定量的稀硫酸使溶液显酸性,用cmol·L-1 KMnO4标准溶液滴定,滴定至终点时消耗KMnO4标准溶液VmL。
(1)硫脲[CS(NH2)2]易溶于水,除硫脲和水都是极性分子外,其原因还有___________ 。
(2)滴定时,硫脲转化为CO2、N2、SO ,则
,则
___________ 。
(3)样品中硫脲的质量分数为___________ %(用含“m、c、V”的式子表示)。
装置C反应后的液体过滤后,将滤液减压蒸发浓缩,之后冷却结晶,离心分离,烘干即可得到产品。称取mg产品,加水溶解配成500mL溶液,量取25mL于锥形瓶中,滴加一定量的稀硫酸使溶液显酸性,用cmol·L-1 KMnO4标准溶液滴定,滴定至终点时消耗KMnO4标准溶液VmL。
(1)硫脲[CS(NH2)2]易溶于水,除硫脲和水都是极性分子外,其原因还有
(2)滴定时,硫脲转化为CO2、N2、SO
 ,则
,则
(3)样品中硫脲的质量分数为
您最近一年使用:0次