解题方法
1 . I.填空。
(1)同温同压下,同体积的氨气和硫化氢( )气体的质量比为
)气体的质量比为___________ ,若二者氢原子数相等,则它们的体积比为___________ 。
(2)在一定条件下44.8g某金属单质A与1.2mol 恰好完全反应,生成0.8molAClx,则x=
恰好完全反应,生成0.8molAClx,则x=___________ ,A的摩尔质量为___________ 。
II.常温下,将20.0g质量分数为14.0%的 溶液与30.0g质量分数为24.0%的
溶液与30.0g质量分数为24.0%的 溶液混合,得到的密度为
溶液混合,得到的密度为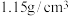 的混合溶液。计算:
的混合溶液。计算:
(3)混合后溶液的质量分数___________ ;
(4)混合后溶液的物质的量浓度___________ 。
(1)同温同压下,同体积的氨气和硫化氢(
 )气体的质量比为
)气体的质量比为(2)在一定条件下44.8g某金属单质A与1.2mol
 恰好完全反应,生成0.8molAClx,则x=
恰好完全反应,生成0.8molAClx,则x=II.常温下,将20.0g质量分数为14.0%的
 溶液与30.0g质量分数为24.0%的
溶液与30.0g质量分数为24.0%的 溶液混合,得到的密度为
溶液混合,得到的密度为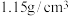 的混合溶液。计算:
的混合溶液。计算:(3)混合后溶液的质量分数
(4)混合后溶液的物质的量浓度
您最近一年使用:0次
2 . Ⅰ.根据物质的组成、结构、性质等进行分类,可预测物质的性质及变化:
(1)SiO2是普通玻璃的主要成分,与CO2一样是酸性氧化物,写出SiO2溶于NaOH溶液的化学方程式:___________ 。
(2)现有:①固体KOH②稀硫酸③氨气④熔融NaCl⑤蔗糖⑥铜;其中能导电的是___________ (填序号,下同)属于电解质的是___________ 。
(3)写出NaClO在水溶液中的电离方程式:___________ 。
Ⅱ.物质的量是联系宏观和微观的桥梁:
(4)40.5g某金属氯化物MCl2中含0.6molCl-,则该氯化物的摩尔质量为___________ 。
(5)标准状况下,与34g的H2S气体含相同H原子数的CH4的体积为___________ 。
(6)由CO、CO2两气体组成的混合气体12.8g,标准状况下,体积为8.96L。则CO、CO2的物质的量之比为___________ 。
(7)在VmL的硫酸铁溶液中,含有mgFe3+离子,则此溶液中 的物质的量浓度为
的物质的量浓度为_______ 。
(8)若用容量瓶以质量分数98%、密度为1.84g/cm3的浓硫酸配制480mL浓度0.2mol/L稀硫酸,计算需要用量筒量取___________ mL的浓硫酸。
(9)用4×10-3mol的KZO4恰好将60mL0.1mol/L的Na2SO3溶液氧化为Na2SO4,则元素Z在还原产物中的化合价是___________ 。
(1)SiO2是普通玻璃的主要成分,与CO2一样是酸性氧化物,写出SiO2溶于NaOH溶液的化学方程式:
(2)现有:①固体KOH②稀硫酸③氨气④熔融NaCl⑤蔗糖⑥铜;其中能导电的是
(3)写出NaClO在水溶液中的电离方程式:
Ⅱ.物质的量是联系宏观和微观的桥梁:
(4)40.5g某金属氯化物MCl2中含0.6molCl-,则该氯化物的摩尔质量为
(5)标准状况下,与34g的H2S气体含相同H原子数的CH4的体积为
(6)由CO、CO2两气体组成的混合气体12.8g,标准状况下,体积为8.96L。则CO、CO2的物质的量之比为
(7)在VmL的硫酸铁溶液中,含有mgFe3+离子,则此溶液中
 的物质的量浓度为
的物质的量浓度为(8)若用容量瓶以质量分数98%、密度为1.84g/cm3的浓硫酸配制480mL浓度0.2mol/L稀硫酸,计算需要用量筒量取
(9)用4×10-3mol的KZO4恰好将60mL0.1mol/L的Na2SO3溶液氧化为Na2SO4,则元素Z在还原产物中的化合价是
您最近一年使用:0次
2024高三下·全国·专题练习
3 .  作为绿色氧化剂应用广泛,氢醌法制备
作为绿色氧化剂应用广泛,氢醌法制备 原理及装置如下:
原理及装置如下: 、
、 等杂质易使
等杂质易使 催化剂中毒。回答下列问题:
催化剂中毒。回答下列问题:
(1)取 产品,加蒸馏水定容至
产品,加蒸馏水定容至 摇匀,取
摇匀,取 于锥形瓶中,用
于锥形瓶中,用 酸性
酸性 标准溶液滴定。平行滴定三次,消耗标准溶液体积分别为
标准溶液滴定。平行滴定三次,消耗标准溶液体积分别为 、
、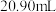 、
、 。假设其他杂质不干扰结果,产品中
。假设其他杂质不干扰结果,产品中 质量分数为
质量分数为_______ 。
 作为绿色氧化剂应用广泛,氢醌法制备
作为绿色氧化剂应用广泛,氢醌法制备 原理及装置如下:
原理及装置如下: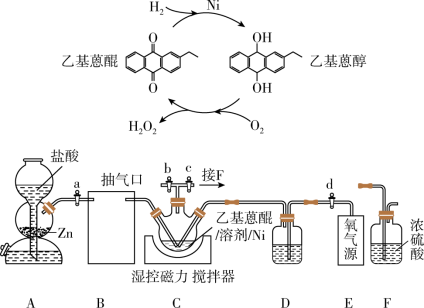
 、
、 等杂质易使
等杂质易使 催化剂中毒。回答下列问题:
催化剂中毒。回答下列问题:(1)取
 产品,加蒸馏水定容至
产品,加蒸馏水定容至 摇匀,取
摇匀,取 于锥形瓶中,用
于锥形瓶中,用 酸性
酸性 标准溶液滴定。平行滴定三次,消耗标准溶液体积分别为
标准溶液滴定。平行滴定三次,消耗标准溶液体积分别为 、
、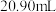 、
、 。假设其他杂质不干扰结果,产品中
。假设其他杂质不干扰结果,产品中 质量分数为
质量分数为
您最近一年使用:0次
4 . 填空
(1)在标准状况下,5.6LCO的物质的量是_____ 。
(2)相同质量的CO和CO2所含的原子个数比是_____ 。
(3)同温同压下,SO2气体和CO2气体的密度之比_____ 。
(4)瓦斯中甲烷与氧气的质量比为1∶4时极易发生爆炸,此时甲烷与氧气的体积比为_____ 。
(5)标准状况下VL氯化氢溶解在100mL水中(水的密度近似为1g/mL),所得溶液的密度为dg/mL,质量分数为w,物质的量浓度可以表示为_____ 。
(6)有下列物质:①氢氧化钠固体;②铝丝;③稀硫酸;④饱和食盐水;⑤氯化氢;⑥Na2CO3 ∙10H2O;⑦酒精;⑧熔融的KCl;⑨胆矾;⑩石墨,其中属于电解质,但不能导电的是_____ 。
(7)标准状况下,NH3与CH4组成的混合气体的平均密度为0.75g/L,该混合气体的中 的体积分数为
的体积分数为_____ 。
(1)在标准状况下,5.6LCO的物质的量是
(2)相同质量的CO和CO2所含的原子个数比是
(3)同温同压下,SO2气体和CO2气体的密度之比
(4)瓦斯中甲烷与氧气的质量比为1∶4时极易发生爆炸,此时甲烷与氧气的体积比为
(5)标准状况下VL氯化氢溶解在100mL水中(水的密度近似为1g/mL),所得溶液的密度为dg/mL,质量分数为w,物质的量浓度可以表示为
(6)有下列物质:①氢氧化钠固体;②铝丝;③稀硫酸;④饱和食盐水;⑤氯化氢;⑥Na2CO3 ∙10H2O;⑦酒精;⑧熔融的KCl;⑨胆矾;⑩石墨,其中属于电解质,但不能导电的是
(7)标准状况下,NH3与CH4组成的混合气体的平均密度为0.75g/L,该混合气体的中
 的体积分数为
的体积分数为
您最近一年使用:0次
解题方法
5 . 试回答下列问题
(1)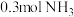 ,分子中所含质子数与
,分子中所含质子数与___________ 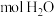 分子中所含质子数相等。
分子中所含质子数相等。
(2)正常人的血液中葡萄糖(简称血糖,分子式为 )的浓度在
)的浓度在 之间,今测得某病人1mL血液中含葡萄糖0.60mg,相当于
之间,今测得某病人1mL血液中含葡萄糖0.60mg,相当于___________ 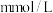 。
。
(3)质量分数为36.5%浓盐酸(密度为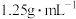 )的物质的量浓度为
)的物质的量浓度为___________ ,若配制250mL 的盐酸,需要量取浓盐酸的体积为
的盐酸,需要量取浓盐酸的体积为___________ mL。
(1)
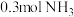 ,分子中所含质子数与
,分子中所含质子数与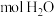 分子中所含质子数相等。
分子中所含质子数相等。(2)正常人的血液中葡萄糖(简称血糖,分子式为
 )的浓度在
)的浓度在 之间,今测得某病人1mL血液中含葡萄糖0.60mg,相当于
之间,今测得某病人1mL血液中含葡萄糖0.60mg,相当于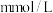 。
。(3)质量分数为36.5%浓盐酸(密度为
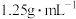 )的物质的量浓度为
)的物质的量浓度为 的盐酸,需要量取浓盐酸的体积为
的盐酸,需要量取浓盐酸的体积为
您最近一年使用:0次
解题方法
6 . 硫代硫酸钠 的俗名是大苏打,在化学实验中有广泛应用。
的俗名是大苏打,在化学实验中有广泛应用。
(1)实验室可通过向含 和
和 的溶液中通入
的溶液中通入 来制备
来制备 (其简单流程如图所示)。
(其简单流程如图所示)。

①写出制备 的化学方程式:
的化学方程式:________________ 。
②“一系列操作”包括________ 、________ 、过滤、洗涤、干燥。(填操作名称)
(2)工业上,常用 溶液吸收尾气中的
溶液吸收尾气中的 ,氧化产物为
,氧化产物为 。写出发生反应的离子方程式:
。写出发生反应的离子方程式:_______ 。
(3)临床上, 可用于氰化物解毒,解毒原理:
可用于氰化物解毒,解毒原理: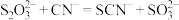 。检验该转化生成了
。检验该转化生成了 的操作为
的操作为________________ 。
(4)工业上,测定 样品纯度的方法:取
样品纯度的方法:取 样品溶于稀硫酸,加入足量
样品溶于稀硫酸,加入足量 溶液,再加入
溶液,再加入 的
的 溶液至恰好完全反应,消耗
溶液至恰好完全反应,消耗 溶液
溶液 。
。
相关反应: ;
;
 。
。
①该样品中 的质量分数为
的质量分数为________ (假设杂质不参与反应)。
②如果稀硫酸过多,测得结果会________ (填“偏高”、“偏低”或“无影响”)。
 的俗名是大苏打,在化学实验中有广泛应用。
的俗名是大苏打,在化学实验中有广泛应用。(1)实验室可通过向含
 和
和 的溶液中通入
的溶液中通入 来制备
来制备 (其简单流程如图所示)。
(其简单流程如图所示)。
①写出制备
 的化学方程式:
的化学方程式:②“一系列操作”包括
(2)工业上,常用
 溶液吸收尾气中的
溶液吸收尾气中的 ,氧化产物为
,氧化产物为 。写出发生反应的离子方程式:
。写出发生反应的离子方程式:(3)临床上,
 可用于氰化物解毒,解毒原理:
可用于氰化物解毒,解毒原理: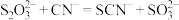 。检验该转化生成了
。检验该转化生成了 的操作为
的操作为(4)工业上,测定
 样品纯度的方法:取
样品纯度的方法:取 样品溶于稀硫酸,加入足量
样品溶于稀硫酸,加入足量 溶液,再加入
溶液,再加入 的
的 溶液至恰好完全反应,消耗
溶液至恰好完全反应,消耗 溶液
溶液 。
。相关反应:
 ;
; 。
。①该样品中
 的质量分数为
的质量分数为②如果稀硫酸过多,测得结果会
您最近一年使用:0次
解题方法
7 . 根据要求回答下列问题:
(1)amol单质碳和16g氧气恰好在某恒容密闭容器中发生反应: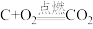 、
、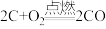 ,当恢复到原来的温度时,测得容器内的压强增大了0.5倍(忽略固体对压强的影响)。
,当恢复到原来的温度时,测得容器内的压强增大了0.5倍(忽略固体对压强的影响)。
①a=_______ ;16g氧气的体积为_______ L(标准状况下)
②若将反应后的气体通过盛有足量Na2O2的U形管,发生反应的化学方程式为_______ 。
(2)二氧化氯(ClO2)是一种广谱杀菌消毒剂。某工厂以213gNaClO3固体、117gNaCl固体和876g一定溶质质量分数的稀硫酸为原料制取ClO2,反应的化学方程式为2NaClO3+2NaCl+2H2SO4=2ClO2 +Cl2↑+2H2O+2Na2SO4,假设反应物均恰好完全反应。
+Cl2↑+2H2O+2Na2SO4,假设反应物均恰好完全反应。
①NaClO2中Cl的化合价是_______
②“84消毒液”也是一种含氯消毒剂,写出实验室制备“84消毒液”的化学方程式:_______
③876g稀硫酸中H2SO4的质量分数是_______ %(结果保留1位小数)。
④30℃时,将所得的硫酸钠溶液蒸发掉_______ g水可以恰好形成该温度下的饱和溶液(已知:30℃时,Na2SO4的溶解度为40g)。
(1)amol单质碳和16g氧气恰好在某恒容密闭容器中发生反应:
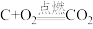 、
、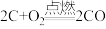 ,当恢复到原来的温度时,测得容器内的压强增大了0.5倍(忽略固体对压强的影响)。
,当恢复到原来的温度时,测得容器内的压强增大了0.5倍(忽略固体对压强的影响)。①a=
②若将反应后的气体通过盛有足量Na2O2的U形管,发生反应的化学方程式为
(2)二氧化氯(ClO2)是一种广谱杀菌消毒剂。某工厂以213gNaClO3固体、117gNaCl固体和876g一定溶质质量分数的稀硫酸为原料制取ClO2,反应的化学方程式为2NaClO3+2NaCl+2H2SO4=2ClO2
 +Cl2↑+2H2O+2Na2SO4,假设反应物均恰好完全反应。
+Cl2↑+2H2O+2Na2SO4,假设反应物均恰好完全反应。①NaClO2中Cl的化合价是
②“84消毒液”也是一种含氯消毒剂,写出实验室制备“84消毒液”的化学方程式:
③876g稀硫酸中H2SO4的质量分数是
④30℃时,将所得的硫酸钠溶液蒸发掉
您最近一年使用:0次
8 . 现有含HCl和 的混合溶液50g,向该溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成沉淀的质量与加入NaOH溶液的质量关系如图:
的混合溶液50g,向该溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成沉淀的质量与加入NaOH溶液的质量关系如图:
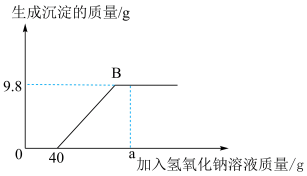
(1)当加入 溶液质量为ag时,溶液中的溶质有
溶液质量为ag时,溶液中的溶质有___________ (写出化学式);
(2)NaOH中Na元素的质量分数___________ (写出计算式);
(3)求混合溶液中 的质量分数
的质量分数___________ (写出计算过程);
(4)求恰好完全反应时,消耗NaOH溶液的总质量___________ (写出计算过程)。
 的混合溶液50g,向该溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成沉淀的质量与加入NaOH溶液的质量关系如图:
的混合溶液50g,向该溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成沉淀的质量与加入NaOH溶液的质量关系如图:
(1)当加入
 溶液质量为ag时,溶液中的溶质有
溶液质量为ag时,溶液中的溶质有(2)NaOH中Na元素的质量分数
(3)求混合溶液中
 的质量分数
的质量分数(4)求恰好完全反应时,消耗NaOH溶液的总质量
您最近一年使用:0次
2023-10-11更新
|
161次组卷
|
3卷引用:北京市首都师范大学附属中学2023-2024学年高一上学期10月月考化学试题
北京市首都师范大学附属中学2023-2024学年高一上学期10月月考化学试题(已下线)【精品卷】3.2.2 物质的量在化学方程式计算中的应用课堂例题-人教版2023-2024学年必修第一册12-2023新东方高二上期中考化学12
名校
解题方法
9 . 将一块质量为 表面(常温时)已被氧化的金属钠投入
表面(常温时)已被氧化的金属钠投入 水中,产生
水中,产生 气体,计算:
气体,计算:
(1)氧化钠的质量___________ g;
(2)所得溶液的质量分数___________ 。
 表面(常温时)已被氧化的金属钠投入
表面(常温时)已被氧化的金属钠投入 水中,产生
水中,产生 气体,计算:
气体,计算:(1)氧化钠的质量
(2)所得溶液的质量分数
您最近一年使用:0次
解题方法
10 . 工业上常用电解 溶液制得
溶液制得 ,反应方程式为:
,反应方程式为: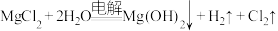 。现将
。现将 溶质质量分数为
溶质质量分数为 的
的 溶液通电一段时间后停止通电,将溶液中物质过滤,得到固体
溶液通电一段时间后停止通电,将溶液中物质过滤,得到固体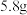 和若干滤液。试计算:
和若干滤液。试计算:
(1) 中
中 和
和 的质量比为
的质量比为________ 。
(2)滤液中 的质量分数(结果精确到
的质量分数(结果精确到 )
)_______ 。
(3)若要将滤液中的 恢复到原来的量分数,并把溶液质量增加到
恢复到原来的量分数,并把溶液质量增加到 。应在滤液中加入一定量水和
。应在滤液中加入一定量水和 固体,计算加入水的体积(水的密度为
固体,计算加入水的体积(水的密度为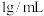 )
)_______ 。
 溶液制得
溶液制得 ,反应方程式为:
,反应方程式为: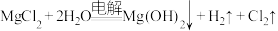 。现将
。现将 溶质质量分数为
溶质质量分数为 的
的 溶液通电一段时间后停止通电,将溶液中物质过滤,得到固体
溶液通电一段时间后停止通电,将溶液中物质过滤,得到固体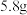 和若干滤液。试计算:
和若干滤液。试计算:(1)
 中
中 和
和 的质量比为
的质量比为(2)滤液中
 的质量分数(结果精确到
的质量分数(结果精确到 )
)(3)若要将滤液中的
 恢复到原来的量分数,并把溶液质量增加到
恢复到原来的量分数,并把溶液质量增加到 。应在滤液中加入一定量水和
。应在滤液中加入一定量水和 固体,计算加入水的体积(水的密度为
固体,计算加入水的体积(水的密度为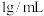 )
)
您最近一年使用:0次



