12-13高二上·上海·期末
1 . 石膏是一种节能建筑材料。某石膏样品是由二水石膏(CaSO4·2H2O)、半水石膏(CaSO4· H2O)、无水石膏(CaSO4)三种成分组成,各组分含量可用下列方法测定。
H2O)、无水石膏(CaSO4)三种成分组成,各组分含量可用下列方法测定。
①称取8.70 g该石膏试样,在400℃干燥失去全部结晶水,质量变为8.16 g。
②再称取8.70 g的该石膏试样,加入80%的酒精溶液,使CaSO4完全水化成CaSO4· H2O,此时,其它两组分与酒精溶液不起作用;将试样取出干燥后称量,试样质量变为8.97 g。
H2O,此时,其它两组分与酒精溶液不起作用;将试样取出干燥后称量,试样质量变为8.97 g。
③在②中所得8.97 g试样中加入蒸馏水,使全部的CaSO4· H2O都水化成CaSO4·2H2O,取出干燥后再次称量,质量变为10.32 g。
H2O都水化成CaSO4·2H2O,取出干燥后再次称量,质量变为10.32 g。
(1)试样中结晶水的质量分数为__________________ (用小数表示)。
(2)试样中无水石膏(CaSO4)的物质的量为____________ mol。
(3)试样中三种石膏的物质的量之比为:
n(CaSO4·2H2O)∶n(CaSO4· H2O)∶n(CaSO4)=
H2O)∶n(CaSO4)= __________________ 。
 H2O)、无水石膏(CaSO4)三种成分组成,各组分含量可用下列方法测定。
H2O)、无水石膏(CaSO4)三种成分组成,各组分含量可用下列方法测定。①称取8.70 g该石膏试样,在400℃干燥失去全部结晶水,质量变为8.16 g。
②再称取8.70 g的该石膏试样,加入80%的酒精溶液,使CaSO4完全水化成CaSO4·
 H2O,此时,其它两组分与酒精溶液不起作用;将试样取出干燥后称量,试样质量变为8.97 g。
H2O,此时,其它两组分与酒精溶液不起作用;将试样取出干燥后称量,试样质量变为8.97 g。③在②中所得8.97 g试样中加入蒸馏水,使全部的CaSO4·
 H2O都水化成CaSO4·2H2O,取出干燥后再次称量,质量变为10.32 g。
H2O都水化成CaSO4·2H2O,取出干燥后再次称量,质量变为10.32 g。(1)试样中结晶水的质量分数为
(2)试样中无水石膏(CaSO4)的物质的量为
(3)试样中三种石膏的物质的量之比为:
n(CaSO4·2H2O)∶n(CaSO4·
 H2O)∶n(CaSO4)=
H2O)∶n(CaSO4)=
您最近一年使用:0次
2 . 为测定钢铁中硫的含量,称取0.500g试样,高温下在氧气流中燃烧,使试样中的硫全部转化为二氧化硫。将燃烧后的气体通入加有淀粉指示剂的溶液中吸收,并用已知浓度的碘溶液进行滴定。
(1)滴定过程中反应的化学方程式是__________________________ 。
(2)若到达滴定终点时,消耗VmL浓度为amol·L-1的碘溶液,则试样中硫的质量分数的计算式(请化简)为_____________________________ 。
(3)为了快速测定结果,配制一定浓度的碘溶液时,要使每消耗0.1mL碘溶液相当于试样中含硫0.001%。则该碘溶液的物质的量浓度应是_________ (需列简要计算过程)
(1)滴定过程中反应的化学方程式是
(2)若到达滴定终点时,消耗VmL浓度为amol·L-1的碘溶液,则试样中硫的质量分数的计算式(请化简)为
(3)为了快速测定结果,配制一定浓度的碘溶液时,要使每消耗0.1mL碘溶液相当于试样中含硫0.001%。则该碘溶液的物质的量浓度应是
您最近一年使用:0次
10-11高三·黑龙江大庆·阶段练习
3 . 鸡蛋壳的主要成分是碳酸钙。某兴趣小组为了测定鸡蛋壳中CaCO3的含量,现取15 g鸡蛋壳,捣碎,放在烧杯中,然后向其中加入80 g某浓度的稀盐酸,使之充分反应(鸡蛋壳中除CaCO3外的其他成分都不溶于水,且不与稀盐酸反应),测得烧杯中的反应剩余物的质量(m)与反应时间(t)的关系如图所示(忽略水蒸气的挥发),其中当反应进行到B点时,所用盐酸刚好消耗了加入量的一半。试计算(计算结果精确到0.1%):
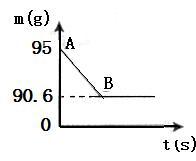
(1)产生CO2的质量为__________ g;
(2)该鸡蛋壳中CaCO3的质量分数__________ 。
(3)所用稀盐酸中溶质的质量分数__________ 。

(1)产生CO2的质量为
(2)该鸡蛋壳中CaCO3的质量分数
(3)所用稀盐酸中溶质的质量分数
您最近一年使用:0次
11-12高一上·江西宜春·阶段练习
4 . 下图是某厂生产的某种加钙食盐包装标签上的部分文字,请阅读后回答以下问题:

(1)为了检验此盐中是否含有碘酸钾,可用KI-淀粉溶液和稀盐酸作试剂进行检测。加入KI-淀粉溶液和稀盐酸后,若盐中含有碘酸钾,则会发生如下反应:KIO3+5KI+6HCl = 6KCl+3I2+3H2O,生成的I2遇淀粉变蓝。在上述反应中氧化剂与还原剂物质的量之比为______________ 。
(2)为了测定此盐的钙元素含量,取10克此盐溶于水,加入足量盐酸,生成标准状况下67.2ml二氧化碳气体。请计算此加钙食盐中钙元素的质量分数______ (取2位有效数字)。

(1)为了检验此盐中是否含有碘酸钾,可用KI-淀粉溶液和稀盐酸作试剂进行检测。加入KI-淀粉溶液和稀盐酸后,若盐中含有碘酸钾,则会发生如下反应:KIO3+5KI+6HCl = 6KCl+3I2+3H2O,生成的I2遇淀粉变蓝。在上述反应中氧化剂与还原剂物质的量之比为
(2)为了测定此盐的钙元素含量,取10克此盐溶于水,加入足量盐酸,生成标准状况下67.2ml二氧化碳气体。请计算此加钙食盐中钙元素的质量分数
您最近一年使用:0次
5 . 现有一种铜和氧化亚铁的混合物样品。为测定该样品中氧化亚铁的含量,某学生取20.0g此样品置于烧瓶中,分四次加入密度为1.22g/cm3的硫酸并做相关记录。有关数据记录如下表:
试计算:
(1)10.0g此样品中铜的质量____ 。
(2)样品中氧化亚铁的质量分数____ 。
(3)所用硫酸溶液溶质的质量分数_____ 和物质的量浓度____ 。
| 加硫酸的序号 | 每次加入硫酸的体积/mL | 剩余固体的质量/g |
| 1 | 20.0 | 16.0 |
| 2 | 20.0 | 12.0 |
| 3 | 20.0 | 8.0 |
| 4 | 20.0 | 8.0 |
试计算:
(1)10.0g此样品中铜的质量
(2)样品中氧化亚铁的质量分数
(3)所用硫酸溶液溶质的质量分数
您最近一年使用:0次
9-10高二下·浙江·期末
名校
6 . 氢氧化钡是一种使用广泛的化学试剂。某课外小组通过下列实验测定某试样中Ba(OH)2·nH2O的含量。
(1)称取3.50 g试样溶于蒸馏水配成100 mL溶液,从中取出10.0 mL溶液于锥形瓶中,加2滴指示剂,用0.100 mol/L HCl标准溶液滴定至终点,共消耗标准液20.0 mL(杂质不与酸反应),试样中氢氧化钡的物质的量为________ mol。
(2)另取5.25 g试样加热至失去全部结晶水(杂质不分解),称得质量为3.09 g,则Ba(OH)2·nH2O中的n的值为________ 。
(3)试样中Ba(OH)2·nH2O的质量分数为________ 。
(1)称取3.50 g试样溶于蒸馏水配成100 mL溶液,从中取出10.0 mL溶液于锥形瓶中,加2滴指示剂,用0.100 mol/L HCl标准溶液滴定至终点,共消耗标准液20.0 mL(杂质不与酸反应),试样中氢氧化钡的物质的量为
(2)另取5.25 g试样加热至失去全部结晶水(杂质不分解),称得质量为3.09 g,则Ba(OH)2·nH2O中的n的值为
(3)试样中Ba(OH)2·nH2O的质量分数为
您最近一年使用:0次
9-10高二·山东·假期作业
7 . 氯化钙是用途广泛的化学试剂,可作干燥剂、冷冻剂、防冻剂等。为了测定某氯化钙样品中钙的含量,进行如下实验:
①准确称取氯化钙样品0.2312g,放入烧杯中,加入适量6mol/L的盐酸和适量蒸馏水使样品完全溶解,再滴加35mL0.25mol/L (NH4)2C2O4溶液,水浴加热,逐渐生成CaC2O4沉淀,经检验,Ca2+已沉淀完全。
②过滤并洗涤①所得沉淀。
③加入足量的10% H2SO4和适量的蒸馏水,②中沉淀完全溶解,溶液呈酸性,加热至75℃,趁热加入0.05mol/L KMnO4溶液16mL,恰好完全反应。
回答下列问题:
(1)配平:___ MnO4-+___ H2C2O4+___ H+―___ Mn2++____ CO2↑+___ H2O
(2)0.05mol·L-1KMnO4标准溶液应置于_________ (选填“酸式”或“碱式”)滴定管中;判断滴定终点的现象为__________________________________________________ 。
(3)计算该氯化钙样品中钙元素的质量分数(精确到0.01%)________________ 。
①准确称取氯化钙样品0.2312g,放入烧杯中,加入适量6mol/L的盐酸和适量蒸馏水使样品完全溶解,再滴加35mL0.25mol/L (NH4)2C2O4溶液,水浴加热,逐渐生成CaC2O4沉淀,经检验,Ca2+已沉淀完全。
②过滤并洗涤①所得沉淀。
③加入足量的10% H2SO4和适量的蒸馏水,②中沉淀完全溶解,溶液呈酸性,加热至75℃,趁热加入0.05mol/L KMnO4溶液16mL,恰好完全反应。
回答下列问题:
(1)配平:
(2)0.05mol·L-1KMnO4标准溶液应置于
(3)计算该氯化钙样品中钙元素的质量分数(精确到0.01%)
您最近一年使用:0次
2010·上海徐汇·一模
8 . 粉煤灰是燃煤电厂排出的工业废渣,其中含莫来石(Al6Si2O13)的质量分数为43.4%,还有含量较多的SiO2(其他成分不含Al和Si)。用粉煤灰和纯碱在高温下烧结,可制取NaAlSiO4(霞石)、Na2SiO3和NaAlO2,有关化学方程式为:
Al6Si2O13 + 3Na2CO3→ 2NaAlSiO4+ 4NaAlO2+ 3CO2↑ ①
Al6Si2O13 + 5Na2CO3→ 2Na2SiO3 + 6NaAlO2+ 5CO2↑ ②
SiO2+ Na2CO3→ Na2SiO3+ CO2↑ ③
(1)粉煤灰中铝的质量分数为________ % 。
(2)用1 mol Al6Si2O13 和 4 mol SiO2制得5mol NaAlO2、1mol NaAlSiO4,还应制得Na2SiO3____________ mol,共消耗Na2CO3________ mol(得到的固体中无SiO2)。
(3)若粉煤灰中 Al6Si2O13 与 SiO2的物质的量之比为1:2,则1kg粉煤灰与6mol Na2CO3反应(反应物全部都参与反应),可制得NaAlO2_________________ mol。
(4)若用100 mol Al6Si2O13同时生产NaAlSiO4和NaAlO2,且n(NaAlSiO4):n(NaAlO2) =x,消耗Na2CO3 ymol,试确定y与x的关系式________________ 。
Al6Si2O13 + 3Na2CO3→ 2NaAlSiO4+ 4NaAlO2+ 3CO2↑ ①
Al6Si2O13 + 5Na2CO3→ 2Na2SiO3 + 6NaAlO2+ 5CO2↑ ②
SiO2+ Na2CO3→ Na2SiO3+ CO2↑ ③
(1)粉煤灰中铝的质量分数为
(2)用1 mol Al6Si2O13 和 4 mol SiO2制得5mol NaAlO2、1mol NaAlSiO4,还应制得Na2SiO3
(3)若粉煤灰中 Al6Si2O13 与 SiO2的物质的量之比为1:2,则1kg粉煤灰与6mol Na2CO3反应(反应物全部都参与反应),可制得NaAlO2
(4)若用100 mol Al6Si2O13同时生产NaAlSiO4和NaAlO2,且n(NaAlSiO4):n(NaAlO2) =x,消耗Na2CO3 ymol,试确定y与x的关系式
您最近一年使用:0次
名校
解题方法
9 . 工业上常用纯碱( )溶液吸收尾气中的NO、
)溶液吸收尾气中的NO、 。某纯碱样品中含杂质NaCl,取质量为a g的样品,加入足量的稀盐酸,充分反应后,加热、蒸干、灼烧,得到b g固体物质,则此样品中
。某纯碱样品中含杂质NaCl,取质量为a g的样品,加入足量的稀盐酸,充分反应后,加热、蒸干、灼烧,得到b g固体物质,则此样品中 的质量分数为
的质量分数为___________ 。
 )溶液吸收尾气中的NO、
)溶液吸收尾气中的NO、 。某纯碱样品中含杂质NaCl,取质量为a g的样品,加入足量的稀盐酸,充分反应后,加热、蒸干、灼烧,得到b g固体物质,则此样品中
。某纯碱样品中含杂质NaCl,取质量为a g的样品,加入足量的稀盐酸,充分反应后,加热、蒸干、灼烧,得到b g固体物质,则此样品中 的质量分数为
的质量分数为
您最近一年使用:0次
10 .  可用于光电材料,为测定某实验小组制得的产品中硫化氢的质量分数(设该产品中的其他成分不与
可用于光电材料,为测定某实验小组制得的产品中硫化氢的质量分数(设该产品中的其他成分不与 溶液反应):
溶液反应):
Ⅰ.取0.68000 g 产品,与足量
产品,与足量 溶液充分反应后。
溶液充分反应后。
Ⅱ.将生成的CuS置于已恒重、质量为31.230 g的坩埚中煅烧,恒重后总质量为32.814 g。
请计算:
(1)实验过程中化学科研工作者使用了950 mL 0.60000 mol/L 溶液,该试剂的物质的量为
溶液,该试剂的物质的量为___________ mol。
(2)Ⅱ中CuS煅烧成CuO,CuO的物质的量为___________ mol。
(3)产品中硫化氢的质量分数为___________ 。
 可用于光电材料,为测定某实验小组制得的产品中硫化氢的质量分数(设该产品中的其他成分不与
可用于光电材料,为测定某实验小组制得的产品中硫化氢的质量分数(设该产品中的其他成分不与 溶液反应):
溶液反应):Ⅰ.取0.68000 g
 产品,与足量
产品,与足量 溶液充分反应后。
溶液充分反应后。Ⅱ.将生成的CuS置于已恒重、质量为31.230 g的坩埚中煅烧,恒重后总质量为32.814 g。
请计算:
(1)实验过程中化学科研工作者使用了950 mL 0.60000 mol/L
 溶液,该试剂的物质的量为
溶液,该试剂的物质的量为(2)Ⅱ中CuS煅烧成CuO,CuO的物质的量为
(3)产品中硫化氢的质量分数为
您最近一年使用:0次



