解题方法
1 . 下列离子方程式中,错误 的是
A.NO2通入水中: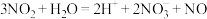 |
| B.Al投入少量NaOH溶液中:Al+OH-+2H2O=Al(OH)3↓+2H+ |
| C.Cl2通入石灰乳中:Cl2+Ca(OH)2=Ca2++Cl-+ClO-+H2O |
D.Pb放入Fe2(SO4)3溶液中: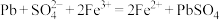 |
您最近一年使用:0次
名校
2 . 三草酸合铁( )酸钾晶体
)酸钾晶体 (
(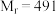 ),
), 时在水中溶解度为
时在水中溶解度为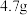 ,
, 时溶解度为
时溶解度为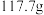 ,难溶于乙醇,是制备负载型活性铁催化剂的主要原料。实验室中先利用如图装置制备
,难溶于乙醇,是制备负载型活性铁催化剂的主要原料。实验室中先利用如图装置制备 (夹持装置略去),后续再制取三草酸合铁(
(夹持装置略去),后续再制取三草酸合铁( )酸钾晶体。
)酸钾晶体。
实验一: 晶体的制备
晶体的制备
(1)打开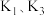 和
和 ,关闭
,关闭 ,向装置
,向装置 中加入稍过量的稀硫酸。
中加入稍过量的稀硫酸。
① 中盛放
中盛放 溶液的仪器名称为
溶液的仪器名称为___________ 。
②A中有气体产生,该气体的作用是___________ 。
(2)收集 并验纯后,打开
并验纯后,打开 ,关闭
,关闭___________ ,让A中浅绿色溶液流入 中,以生成
中,以生成 ,并分离得
,并分离得 晶体。
晶体。
实验二:三草酸合铁( )酸钾晶体的制备
)酸钾晶体的制备
(3)将实验一得到的 溶于水,加入
溶于水,加入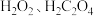 和
和 ,酒精灯微热并不断搅拌,反应制得
,酒精灯微热并不断搅拌,反应制得 ,冷却、过滤、洗涤、干燥。
,冷却、过滤、洗涤、干燥。
①写出该反应的化学方程式:___________ 。
②“微热、搅拌”过程中,温度不宜过高的原因是___________ 。
③过滤后需用___________ 洗涤,其优点是___________ 。
(4)产品纯度的测定
常温下,取 三草酸合铁(Ⅲ)酸钾晶体溶于水配制成
三草酸合铁(Ⅲ)酸钾晶体溶于水配制成 绿色溶液,取出25.00mL,用
绿色溶液,取出25.00mL,用 的酸性高锰酸钾标准液进行滴定,重复三次,平均消耗标准液20.00mL。
的酸性高锰酸钾标准液进行滴定,重复三次,平均消耗标准液20.00mL。
①滴定终点的判断依据是___________ 。
②该三草酸合铁( )酸钾晶体的纯度为
)酸钾晶体的纯度为___________ (保留三位有效数字)。
 )酸钾晶体
)酸钾晶体 (
( ),
), 时在水中溶解度为
时在水中溶解度为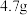 ,
, 时溶解度为
时溶解度为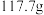 ,难溶于乙醇,是制备负载型活性铁催化剂的主要原料。实验室中先利用如图装置制备
,难溶于乙醇,是制备负载型活性铁催化剂的主要原料。实验室中先利用如图装置制备 (夹持装置略去),后续再制取三草酸合铁(
(夹持装置略去),后续再制取三草酸合铁( )酸钾晶体。
)酸钾晶体。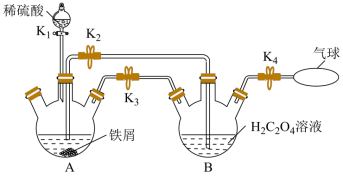
实验一:
 晶体的制备
晶体的制备(1)打开
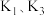 和
和 ,关闭
,关闭 ,向装置
,向装置 中加入稍过量的稀硫酸。
中加入稍过量的稀硫酸。①
 中盛放
中盛放 溶液的仪器名称为
溶液的仪器名称为②A中有气体产生,该气体的作用是
(2)收集
 并验纯后,打开
并验纯后,打开 ,关闭
,关闭 中,以生成
中,以生成 ,并分离得
,并分离得 晶体。
晶体。实验二:三草酸合铁(
 )酸钾晶体的制备
)酸钾晶体的制备(3)将实验一得到的
 溶于水,加入
溶于水,加入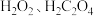 和
和 ,酒精灯微热并不断搅拌,反应制得
,酒精灯微热并不断搅拌,反应制得 ,冷却、过滤、洗涤、干燥。
,冷却、过滤、洗涤、干燥。①写出该反应的化学方程式:
②“微热、搅拌”过程中,温度不宜过高的原因是
③过滤后需用
(4)产品纯度的测定
常温下,取
 三草酸合铁(Ⅲ)酸钾晶体溶于水配制成
三草酸合铁(Ⅲ)酸钾晶体溶于水配制成 绿色溶液,取出25.00mL,用
绿色溶液,取出25.00mL,用 的酸性高锰酸钾标准液进行滴定,重复三次,平均消耗标准液20.00mL。
的酸性高锰酸钾标准液进行滴定,重复三次,平均消耗标准液20.00mL。①滴定终点的判断依据是
②该三草酸合铁(
 )酸钾晶体的纯度为
)酸钾晶体的纯度为
您最近一年使用:0次
3 . 工业上监测SO2含量是否达到排放标准的化学反应原理是:SO2+H2O2+BaCl2=BaSO4↓+2HCl,设NA为阿伏加德罗常数的值,下列说法正确的是
| A.标准状况下,11.2LSO2含有的原子总数为NA |
B.17gH2O2中含有 键数目为2NA 键数目为2NA |
| C.反应转移的电子数为0.2NA时,生成0.1mol的BaSO4沉淀 |
| D.常温下pH=1的HCl溶液中含有的H+数目为0.1NA |
您最近一年使用:0次
名校
4 . 反应CaC2+2H2O=Ca(OH)2+C2H2↑,可用于制取乙炔。下列说法正确的是
| A.H2O的空间结构为三角锥形 |
B.CaC2的电子式:Ca2+ |
C.C2H2的空间填充模型: |
D.基态碳原子的价层电子轨道表示式: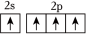 |
您最近一年使用:0次
5 . 赤铜矿(主要成分为 ,含少量
,含少量 、
、 )含铜量高达88.8%,是重要的冶金材料,某化学兴趣小组利用其制备
)含铜量高达88.8%,是重要的冶金材料,某化学兴趣小组利用其制备 晶体的流程为:
晶体的流程为:
(1) 晶体结构如下图所示。晶体中存在的作用力包括离子键、
晶体结构如下图所示。晶体中存在的作用力包括离子键、_______ 。_______ 。 发生反应的离子方程式为
发生反应的离子方程式为_______ 。检验氧化完全的试剂为_______ (填化学式)。
(4)沉铁。离子浓度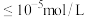 时,可认为该离子被沉淀完全。若室温下溶液pH应调节至略大于3.7,则
时,可认为该离子被沉淀完全。若室温下溶液pH应调节至略大于3.7,则 的
的 为
为_______ 。
(5)试从产率、试剂选择角度评价该制备流程并提出修改建议_______ 。
 ,含少量
,含少量 、
、 )含铜量高达88.8%,是重要的冶金材料,某化学兴趣小组利用其制备
)含铜量高达88.8%,是重要的冶金材料,某化学兴趣小组利用其制备 晶体的流程为:
晶体的流程为:

(1)
 晶体结构如下图所示。晶体中存在的作用力包括离子键、
晶体结构如下图所示。晶体中存在的作用力包括离子键、

 发生反应的离子方程式为
发生反应的离子方程式为(4)沉铁。离子浓度
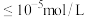 时,可认为该离子被沉淀完全。若室温下溶液pH应调节至略大于3.7,则
时,可认为该离子被沉淀完全。若室温下溶液pH应调节至略大于3.7,则 的
的 为
为(5)试从产率、试剂选择角度评价该制备流程并提出修改建议
您最近一年使用:0次
名校
6 . 设NA为阿伏加德罗常数的值。下列说法正确的是
| A.1molFe与水蒸气在高温下充分反应,转移的电子数为3NA |
| B.常温常压下,3.0g含甲醛的冰醋酸中含有的原子总数为0.4NA |
| C.1mol[Cu(H2O)4]2+中σ键的数目为8NA |
| D.1L 1mol/L的NaClO溶液中含有ClO-的数目为NA |
您最近一年使用:0次
名校
7 . 下列反应的离子方程式书写正确的是
A.向 溶液中滴加少量氯水: 溶液中滴加少量氯水: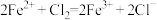 |
B.不用玻璃瓶盛装氢氟酸的原因: |
C.将稀硫酸加入硫代硫酸钠溶液中: |
D.Fe与稀硝酸反应,当 时, 时,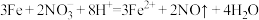 |
您最近一年使用:0次
解题方法
8 . 下列有关离子方程式错误 的是
A.向AgCl沉淀中加入过量氨水使AgCl溶解: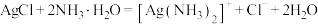 |
B.用 溶液处理锅炉水垢中的 溶液处理锅炉水垢中的 : : |
C.已知: 为二元弱碱,与足量浓 为二元弱碱,与足量浓 反应: 反应: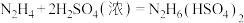 |
D.苯酚钠溶液中通入少量 气体: 气体: |
您最近一年使用:0次
名校
9 . 化学与生产、生活密切相关。回答下列问题:
I.家庭厨卫中有许多中学化学常见的物质,括号内为厨卫用品的主要成分。
①食盐(NaCl);②料酒(乙醇);③食醋(乙酸);④碱面( );⑤发酵粉(
);⑤发酵粉( 和明矾);⑥“84”消毒液(NaClO);⑦洁厕灵(HCl)。
和明矾);⑥“84”消毒液(NaClO);⑦洁厕灵(HCl)。
(1)当食盐不慎洒落在天然气的火焰上,观察到的现象是___________ 。
(2)②③的主要成分可以归为一类物质,其分类的依据是___________(填字母)。
(3)写出过量⑦和④反应的离子方程式:___________ 。
(4)“84”消毒液和洁厕灵不能混合使用,用离子方程式解释其原因:___________ 。
(5)某同学用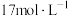 的浓硫酸配制480mL
的浓硫酸配制480mL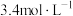 的稀硫酸用于增强“84”消毒液的消毒能力,需取用浓硫酸的体积为
的稀硫酸用于增强“84”消毒液的消毒能力,需取用浓硫酸的体积为___________ mL。
Ⅱ.汽车安全气囊内装有 等物质。
等物质。
(6)当汽车发生严重碰撞时,引发 分解:
分解: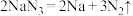 ,
, 的电子式为
的电子式为___________ ,若安全气囊内有65g ,其完全分解所释放的
,其完全分解所释放的 在标准状况下的体积为
在标准状况下的体积为___________ L,产生的Na立即与 发生置换反应生成
发生置换反应生成 ,其中氧化剂和还原剂的物质的量之比是
,其中氧化剂和还原剂的物质的量之比是___________ 。
I.家庭厨卫中有许多中学化学常见的物质,括号内为厨卫用品的主要成分。
①食盐(NaCl);②料酒(乙醇);③食醋(乙酸);④碱面(
 );⑤发酵粉(
);⑤发酵粉( 和明矾);⑥“84”消毒液(NaClO);⑦洁厕灵(HCl)。
和明矾);⑥“84”消毒液(NaClO);⑦洁厕灵(HCl)。(1)当食盐不慎洒落在天然气的火焰上,观察到的现象是
(2)②③的主要成分可以归为一类物质,其分类的依据是___________(填字母)。
| A.两种物质都是非电解质 | B.两种物质都是电解质 |
| C.两种物质都是氧化物 | D.两种物质都是含碳化合物 |
(3)写出过量⑦和④反应的离子方程式:
(4)“84”消毒液和洁厕灵不能混合使用,用离子方程式解释其原因:
(5)某同学用
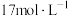 的浓硫酸配制480mL
的浓硫酸配制480mL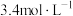 的稀硫酸用于增强“84”消毒液的消毒能力,需取用浓硫酸的体积为
的稀硫酸用于增强“84”消毒液的消毒能力,需取用浓硫酸的体积为Ⅱ.汽车安全气囊内装有
 等物质。
等物质。(6)当汽车发生严重碰撞时,引发
 分解:
分解: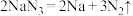 ,
, 的电子式为
的电子式为 ,其完全分解所释放的
,其完全分解所释放的 在标准状况下的体积为
在标准状况下的体积为 发生置换反应生成
发生置换反应生成 ,其中氧化剂和还原剂的物质的量之比是
,其中氧化剂和还原剂的物质的量之比是
您最近一年使用:0次
名校
解题方法
10 . 下列离子方程式书写错误的是
A. 用于治疗胃酸(主要为盐酸)过多症: 用于治疗胃酸(主要为盐酸)过多症: |
B.将少量金属钠加入硫酸铜溶液中: |
C.铝粉和NaOH用作管道疏通剂: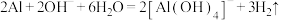 |
D.用湿润的淀粉-KI试纸检验 : : |
您最近一年使用:0次



