解题方法
1 . 以含钒钢渣(含 、
、 和少量
和少量 、
、 )和钛白废酸(含
)和钛白废酸(含 、
、 、
、 、
、 )为原料提取钒,实现“以废治废”。工艺流程如图:
)为原料提取钒,实现“以废治废”。工艺流程如图:
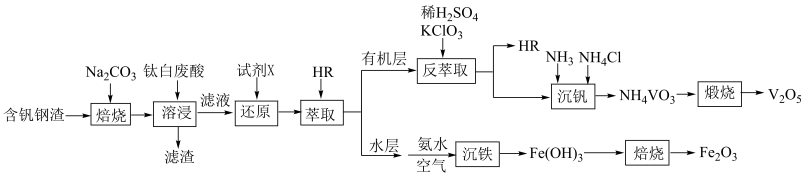
已知:有机萃取剂 的萃取原理为
的萃取原理为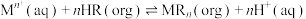 ,其中
,其中 表示有机溶液,酸性条件下
表示有机溶液,酸性条件下 能萃取
能萃取 而不能萃取
而不能萃取 ,
, 对+4价钒萃取能力强,而对+5价钒的萃取能力较弱。
对+4价钒萃取能力强,而对+5价钒的萃取能力较弱。
回答下列问题:
(1)在空气中“焙烧”时, 转化为
转化为 的化学方程式为
的化学方程式为___________ 。
(2)“溶浸”时生成的滤渣除了 外,还有
外,还有___________ (填化学式)。
(3)“还原”的目的是将溶液中的+5价钒和 分别转化为+4价钒与
分别转化为+4价钒与 ,利于+4价钒的萃取并实现钒和铁元素分离,加入的化学试剂
,利于+4价钒的萃取并实现钒和铁元素分离,加入的化学试剂 可能为___________(填标号)。
可能为___________(填标号)。
(4)在“萃取”操作后从水层中获得 的离子方程式是
的离子方程式是___________ 。
(5)在“反萃取”操作中 和
和 反应生成
反应生成 和
和 ,反应中氧化剂与还原剂的物质的量之比为
,反应中氧化剂与还原剂的物质的量之比为___________ 。
(6)上述流程中可循环利用的物质除 外,还有
外,还有___________ (填化学式)。
(7)常温“沉钒”,维持溶液中 的总浓度为
的总浓度为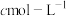 ,
, 。“沉钒”后溶液中
。“沉钒”后溶液中
___________  [已知
[已知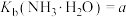 ;
; ]。
]。
 、
、 和少量
和少量 、
、 )和钛白废酸(含
)和钛白废酸(含 、
、 、
、 、
、 )为原料提取钒,实现“以废治废”。工艺流程如图:
)为原料提取钒,实现“以废治废”。工艺流程如图:
已知:有机萃取剂
 的萃取原理为
的萃取原理为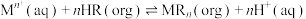 ,其中
,其中 表示有机溶液,酸性条件下
表示有机溶液,酸性条件下 能萃取
能萃取 而不能萃取
而不能萃取 ,
, 对+4价钒萃取能力强,而对+5价钒的萃取能力较弱。
对+4价钒萃取能力强,而对+5价钒的萃取能力较弱。回答下列问题:
(1)在空气中“焙烧”时,
 转化为
转化为 的化学方程式为
的化学方程式为(2)“溶浸”时生成的滤渣除了
 外,还有
外,还有(3)“还原”的目的是将溶液中的+5价钒和
 分别转化为+4价钒与
分别转化为+4价钒与 ,利于+4价钒的萃取并实现钒和铁元素分离,加入的化学试剂
,利于+4价钒的萃取并实现钒和铁元素分离,加入的化学试剂 可能为___________(填标号)。
可能为___________(填标号)。A. | B. | C. | D. |
(4)在“萃取”操作后从水层中获得
 的离子方程式是
的离子方程式是(5)在“反萃取”操作中
 和
和 反应生成
反应生成 和
和 ,反应中氧化剂与还原剂的物质的量之比为
,反应中氧化剂与还原剂的物质的量之比为(6)上述流程中可循环利用的物质除
 外,还有
外,还有(7)常温“沉钒”,维持溶液中
 的总浓度为
的总浓度为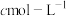 ,
, 。“沉钒”后溶液中
。“沉钒”后溶液中
 [已知
[已知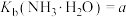 ;
; ]。
]。
您最近半年使用:0次
解题方法
2 . 低品位铜矿(主要含CuS、FeO)提铜是解决我国铜产量低这一问题的重要技术,利用低品位铜矿制备Cu2O的一种工艺流程如下图所示:

已知:Ⅰ.MnCO3难溶于水,CuS难溶于水及强酸。
Ⅱ.Cu2O是一种难溶于水的红色物质。
回答下列问题:
(1)“溶浸”包括以下操作:研磨、混合、加热并搅拌、冷却、______ 。“溶浸”中MnO2的作用是______ 。
(2)检验“溶浸”后所得溶液中是否含有 的试剂是
的试剂是______ 。
(3)“调pH”后判断 是否完全沉淀的操作是
是否完全沉淀的操作是______ 。
(4)“还原”中还原产物与氧化产物的物质的量之比为______ 。
(5)将Cu2O固体加入过量稀硫酸中,溶液变成蓝色,且仍有红色固体存在,发生反应的离子方程式为______ 。
(6)有人提出“将低品位铜矿灼烧后用酸溶解制得铜盐”的工艺流程,该流程不足之处有______ (写出一项即可)。

已知:Ⅰ.MnCO3难溶于水,CuS难溶于水及强酸。
Ⅱ.Cu2O是一种难溶于水的红色物质。
回答下列问题:
(1)“溶浸”包括以下操作:研磨、混合、加热并搅拌、冷却、
(2)检验“溶浸”后所得溶液中是否含有
 的试剂是
的试剂是(3)“调pH”后判断
 是否完全沉淀的操作是
是否完全沉淀的操作是(4)“还原”中还原产物与氧化产物的物质的量之比为
(5)将Cu2O固体加入过量稀硫酸中,溶液变成蓝色,且仍有红色固体存在,发生反应的离子方程式为
(6)有人提出“将低品位铜矿灼烧后用酸溶解制得铜盐”的工艺流程,该流程不足之处有
您最近半年使用:0次
3 . 湿法制备多功能水处理剂K2FeO4固体的工艺流程如下:
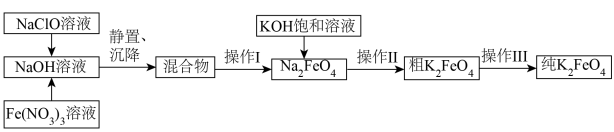
已知:NaCl、NaNO3在强碱中溶解度远小于Na2FeO4。
下列说法正确的是

已知:NaCl、NaNO3在强碱中溶解度远小于Na2FeO4。
下列说法正确的是
| A.溶解度:K2FeO4大于Na2FeO4 |
| B.“操作Ⅱ”所得副产物可循环使用 |
| C.“操作Ⅰ、Ⅱ、Ⅲ”都要使用的玻璃仪器有漏斗、玻璃棒、烧杯、酒精灯 |
D.生成Na2FeO4的离子方程式为 |
您最近半年使用:0次
名校
解题方法
4 . 亚硝酸钠是一种工业盐,在生产、生活中应用广泛。现用下图所示装置(夹持装置已省略)及药品,探究亚硝酸钠与硫酸反应及气体产物成分。
已知:① ;
;
②气体液化的温度: 为21℃,NO为-152℃,
为21℃,NO为-152℃,
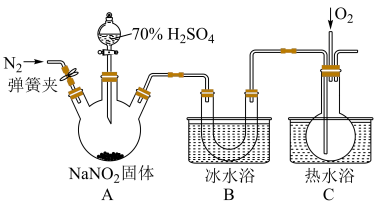
(1)反应前应打开弹簧夹,先通入一段时间氮气,排除装置中的空气,目的是___________ 。
(2)该实验装置的明显缺陷是___________ 。
(3)在关闭弹簧夹,打开分液漏斗活塞,滴入70%硫酸后,A中产生红棕色气体。
①确认A中产生的气体含有NO,依据的现象是___________ ;
②装置B的作用是___________ 。
(4)通过上述实验探究过程,可得出装置A中反应的化学方程式:___________ 。
(5)①水合肼( )是一种重要的化工原料,在医药、农业及燃料上都有着广泛的应用。目前,我国生产水合肼均采用尿素法,即利用NaClO溶液、NaOH溶液与尿素
)是一种重要的化工原料,在医药、农业及燃料上都有着广泛的应用。目前,我国生产水合肼均采用尿素法,即利用NaClO溶液、NaOH溶液与尿素 (尿素中的C为+4,N为-3)反应制得粗肼(
(尿素中的C为+4,N为-3)反应制得粗肼( ),则NaClO与尿素的物质的量之比为
),则NaClO与尿素的物质的量之比为___________ 。
②火箭发射时可用肼( )为燃料,二氧化氮作氧化剂,生成无毒害的物质,写出反应的化学方程式
)为燃料,二氧化氮作氧化剂,生成无毒害的物质,写出反应的化学方程式___________ 。
已知:①
 ;
;②气体液化的温度:
 为21℃,NO为-152℃,
为21℃,NO为-152℃,
(1)反应前应打开弹簧夹,先通入一段时间氮气,排除装置中的空气,目的是
(2)该实验装置的明显缺陷是
(3)在关闭弹簧夹,打开分液漏斗活塞,滴入70%硫酸后,A中产生红棕色气体。
①确认A中产生的气体含有NO,依据的现象是
②装置B的作用是
(4)通过上述实验探究过程,可得出装置A中反应的化学方程式:
(5)①水合肼(
 )是一种重要的化工原料,在医药、农业及燃料上都有着广泛的应用。目前,我国生产水合肼均采用尿素法,即利用NaClO溶液、NaOH溶液与尿素
)是一种重要的化工原料,在医药、农业及燃料上都有着广泛的应用。目前,我国生产水合肼均采用尿素法,即利用NaClO溶液、NaOH溶液与尿素 (尿素中的C为+4,N为-3)反应制得粗肼(
(尿素中的C为+4,N为-3)反应制得粗肼( ),则NaClO与尿素的物质的量之比为
),则NaClO与尿素的物质的量之比为②火箭发射时可用肼(
 )为燃料,二氧化氮作氧化剂,生成无毒害的物质,写出反应的化学方程式
)为燃料,二氧化氮作氧化剂,生成无毒害的物质,写出反应的化学方程式
您最近半年使用:0次
名校
5 . 现有以下物质:① ②Cu③
②Cu③ ④
④ 胶体⑤
胶体⑤ 溶液⑥干冰⑦稀硝酸⑧乙醇⑨熔融碳酸钠。回答下列问题:
溶液⑥干冰⑦稀硝酸⑧乙醇⑨熔融碳酸钠。回答下列问题:
(1)以上物质中属于电解质的是_______ (填序号,下同);上述状态下能导电的是________ 。
(2)①的电离方程式为___________ 。
(3)向④中逐滴滴加⑦,可观察到的现象是___________ 。
(4)⑤中混有少量①,除杂过程中选用的试剂为___________ 。
(5)③可发生如下反应 (未配平);配平该反应并用双线桥法分析电子转移的情况:
(未配平);配平该反应并用双线桥法分析电子转移的情况:________ ;每生成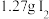 ,反应中转移电子的物质的量为
,反应中转移电子的物质的量为________ 。
 ②Cu③
②Cu③ ④
④ 胶体⑤
胶体⑤ 溶液⑥干冰⑦稀硝酸⑧乙醇⑨熔融碳酸钠。回答下列问题:
溶液⑥干冰⑦稀硝酸⑧乙醇⑨熔融碳酸钠。回答下列问题:(1)以上物质中属于电解质的是
(2)①的电离方程式为
(3)向④中逐滴滴加⑦,可观察到的现象是
(4)⑤中混有少量①,除杂过程中选用的试剂为
(5)③可发生如下反应
 (未配平);配平该反应并用双线桥法分析电子转移的情况:
(未配平);配平该反应并用双线桥法分析电子转移的情况: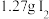 ,反应中转移电子的物质的量为
,反应中转移电子的物质的量为
您最近半年使用:0次
名校
6 . 二氧化氯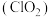 是一种新型的消毒杀剂,常用于饮用水的消毒,其消市效果优于传统的液氯消毒,除此之外,二氧化氯还具有漂白性,常用干纸浆和纸、纤维、小麦面粉、淀粉的漂白。常温常压下
是一种新型的消毒杀剂,常用于饮用水的消毒,其消市效果优于传统的液氯消毒,除此之外,二氧化氯还具有漂白性,常用干纸浆和纸、纤维、小麦面粉、淀粉的漂白。常温常压下 是一种带有辛辣气味的黄绿色气体,易溶于水和四氯化碳。工业上常用综合法制备
是一种带有辛辣气味的黄绿色气体,易溶于水和四氯化碳。工业上常用综合法制备 ,其工序包括制备氯酸钠,盐酸合成和
,其工序包括制备氯酸钠,盐酸合成和 制取,主要工艺流程如图所示。
制取,主要工艺流程如图所示。
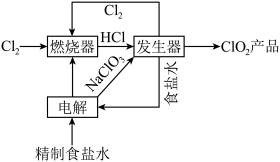
回答下列问题:
(1)工艺流程图涉及到的物质化学式或物质名称,其中能导电的是___________ ,属于电解质的是___________ 。
(2)实验室模拟“燃烧器”中发生的反应,观察到的现象有___________ 。
(3)“发生器”中发生反应的离子方程式为___________ ,若整个过程制得 ,则理论上分别向装置中补充
,则理论上分别向装置中补充___________ (填质量和物质名称)恢复至起始状态。
(4)粗盐中常常含有泥沙、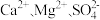 等杂质,粗盐提纯的步骤中加入稍过量的
等杂质,粗盐提纯的步骤中加入稍过量的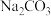 的目的是
的目的是___________ ,经一系列操作可得制食盐水,电解精制食盐水制得 同时还会获取轻质燃料氢气,则离子方程式为
同时还会获取轻质燃料氢气,则离子方程式为___________ 。
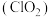 是一种新型的消毒杀剂,常用于饮用水的消毒,其消市效果优于传统的液氯消毒,除此之外,二氧化氯还具有漂白性,常用干纸浆和纸、纤维、小麦面粉、淀粉的漂白。常温常压下
是一种新型的消毒杀剂,常用于饮用水的消毒,其消市效果优于传统的液氯消毒,除此之外,二氧化氯还具有漂白性,常用干纸浆和纸、纤维、小麦面粉、淀粉的漂白。常温常压下 是一种带有辛辣气味的黄绿色气体,易溶于水和四氯化碳。工业上常用综合法制备
是一种带有辛辣气味的黄绿色气体,易溶于水和四氯化碳。工业上常用综合法制备 ,其工序包括制备氯酸钠,盐酸合成和
,其工序包括制备氯酸钠,盐酸合成和 制取,主要工艺流程如图所示。
制取,主要工艺流程如图所示。
回答下列问题:
(1)工艺流程图涉及到的物质化学式或物质名称,其中能导电的是
(2)实验室模拟“燃烧器”中发生的反应,观察到的现象有
(3)“发生器”中发生反应的离子方程式为
 ,则理论上分别向装置中补充
,则理论上分别向装置中补充(4)粗盐中常常含有泥沙、
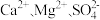 等杂质,粗盐提纯的步骤中加入稍过量的
等杂质,粗盐提纯的步骤中加入稍过量的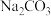 的目的是
的目的是 同时还会获取轻质燃料氢气,则离子方程式为
同时还会获取轻质燃料氢气,则离子方程式为
您最近半年使用:0次
名校
解题方法
7 . 天然气中因含有少量 等气体,使应用受限。
等气体,使应用受限。 菌在酸性
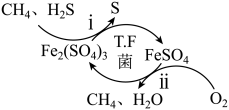
菌在酸性 溶液中可实现天然气的催化脱硫,其原理如图所示,总反应方程式为
溶液中可实现天然气的催化脱硫,其原理如图所示,总反应方程式为 。下列说法正确的是
。下列说法正确的是
 等气体,使应用受限。
等气体,使应用受限。 菌在酸性
菌在酸性 溶液中可实现天然气的催化脱硫,其原理如图所示,总反应方程式为
溶液中可实现天然气的催化脱硫,其原理如图所示,总反应方程式为 。下列说法正确的是
。下列说法正确的是
A.“反应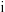 ”生成的 ”生成的 和 和 物质的量之比为 物质的量之比为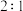 |
B.该脱硫过程中 是催化剂 是催化剂 |
C.若最终生成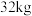 硫,则消耗 硫,则消耗 |
D.“反应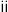 ”发生的反应为 ”发生的反应为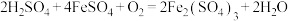 |
您最近半年使用:0次
8 . 某离子反应涉及 六种微粒,其中
六种微粒,其中 随反应进行逐渐减小,下列说法正确的是
随反应进行逐渐减小,下列说法正确的是
 六种微粒,其中
六种微粒,其中 随反应进行逐渐减小,下列说法正确的是
随反应进行逐渐减小,下列说法正确的是A.反应中每减少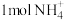 ,转移 ,转移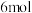 电子 电子 |
B.反应中 被还原 被还原 |
| C.反应前后溶液的酸碱性无明显变化 |
D.参加反应的氧化剂与还原剂的物质的量之比为 |
您最近半年使用:0次
名校
9 . 工业上用赤铁矿(主要成分为 ,含
,含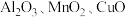 等杂质)制备绿矾
等杂质)制备绿矾 的流程如下:
的流程如下: 能与
能与 溶液反应生成可溶性盐
溶液反应生成可溶性盐 。
。
回答下列问题:
(1)试剂a为___________ 。
(2)试剂b需过量,其目的是___________ ;“滤渣”的成分是___________ 。
(3)“结晶”需隔绝空气,原因是___________ 。
(4)绿矾隔绝空气加强热可用于制备红色颜料铁红。取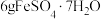 样品隔绝空气加热(杂质不反应),受热过程中样品质量随温度变化的曲线如图所示(已知固体
样品隔绝空气加热(杂质不反应),受热过程中样品质量随温度变化的曲线如图所示(已知固体 不含结晶水)。
不含结晶水)。 主要成分的化学式为
主要成分的化学式为___________ 。
②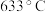 时,除生成铁红外,同时生成能使
时,除生成铁红外,同时生成能使 溶液变浑浊的气体和使品红溶液裉色的气体。该温度下反应的化学方程式为
溶液变浑浊的气体和使品红溶液裉色的气体。该温度下反应的化学方程式为___________ ;该样品中 的质量分数为
的质量分数为___________  (保留一位小数)。
(保留一位小数)。
 ,含
,含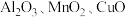 等杂质)制备绿矾
等杂质)制备绿矾 的流程如下:
的流程如下: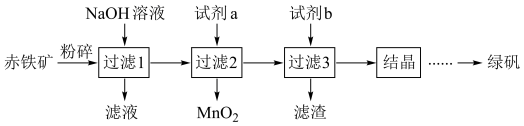
 能与
能与 溶液反应生成可溶性盐
溶液反应生成可溶性盐 。
。回答下列问题:
(1)试剂a为
(2)试剂b需过量,其目的是
(3)“结晶”需隔绝空气,原因是
(4)绿矾隔绝空气加强热可用于制备红色颜料铁红。取
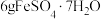 样品隔绝空气加热(杂质不反应),受热过程中样品质量随温度变化的曲线如图所示(已知固体
样品隔绝空气加热(杂质不反应),受热过程中样品质量随温度变化的曲线如图所示(已知固体 不含结晶水)。
不含结晶水)。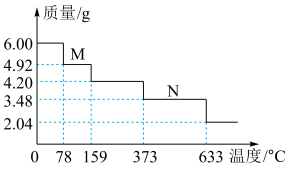
 主要成分的化学式为
主要成分的化学式为②
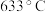 时,除生成铁红外,同时生成能使
时,除生成铁红外,同时生成能使 溶液变浑浊的气体和使品红溶液裉色的气体。该温度下反应的化学方程式为
溶液变浑浊的气体和使品红溶液裉色的气体。该温度下反应的化学方程式为 的质量分数为
的质量分数为 (保留一位小数)。
(保留一位小数)。
您最近半年使用:0次
2024-02-02更新
|
236次组卷
|
3卷引用:山东省潍坊市2023-2024学年高一上学期期末考试化学试题
解题方法
10 . 硝酸铈(Ⅳ)铵的化学式为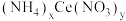 ,是一种橙红色结晶性粉末,易溶于水和乙醇,几乎不溶于浓硝酸,主要用作分析试剂和氧化剂。实验室设计如下实验进行制备并测定其化学式。
,是一种橙红色结晶性粉末,易溶于水和乙醇,几乎不溶于浓硝酸,主要用作分析试剂和氧化剂。实验室设计如下实验进行制备并测定其化学式。
步骤一:NH4HCO3溶液与CeCl3溶液反应制备Ce2(CO3)3。
已知:①氮化钙遇水可迅速产生NH3;②Ce(Ⅲ)易被空气氧化成Ce(Ⅳ)。___________ ,装置C的作用是___________ 。该实验以氮化钙和水制备NH3应选择装置___________ (填“A”或“D”)。
(2)实验时,“a”、“b”、“c”三个旋塞的打开顺序为___________ 。装置B中发生反应的离子方程式为___________ 。
(3)该实验装置存在的一处缺陷为___________ 。
步骤二:制备硝酸铈(Ⅳ)铵___________ 。
(5)“烘干”采取自然干燥的原因为___________ 。
步骤三:测定化学式
①称取一定质量的硝酸铈(Ⅳ)铵,充分灼烧得CeO2mg。
②另称取相同质量的硝酸铈(Ⅳ)铵,加入足量NaOH溶液微热,将产生的气体全部用V1mL水吸收。将吸收液滴入甲基橙,用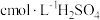 标准溶液滴定,重复2~3次,平均消耗H2SO4标准溶液V2mL。
标准溶液滴定,重复2~3次,平均消耗H2SO4标准溶液V2mL。
(6)计算y=___________ (用上述字母表示)。
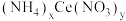 ,是一种橙红色结晶性粉末,易溶于水和乙醇,几乎不溶于浓硝酸,主要用作分析试剂和氧化剂。实验室设计如下实验进行制备并测定其化学式。
,是一种橙红色结晶性粉末,易溶于水和乙醇,几乎不溶于浓硝酸,主要用作分析试剂和氧化剂。实验室设计如下实验进行制备并测定其化学式。步骤一:NH4HCO3溶液与CeCl3溶液反应制备Ce2(CO3)3。
已知:①氮化钙遇水可迅速产生NH3;②Ce(Ⅲ)易被空气氧化成Ce(Ⅳ)。
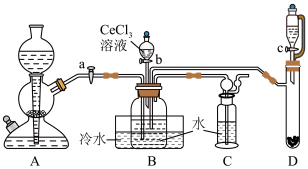
(2)实验时,“a”、“b”、“c”三个旋塞的打开顺序为
(3)该实验装置存在的一处缺陷为
步骤二:制备硝酸铈(Ⅳ)铵

(5)“烘干”采取自然干燥的原因为
步骤三:测定化学式
①称取一定质量的硝酸铈(Ⅳ)铵,充分灼烧得CeO2mg。
②另称取相同质量的硝酸铈(Ⅳ)铵,加入足量NaOH溶液微热,将产生的气体全部用V1mL水吸收。将吸收液滴入甲基橙,用
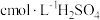 标准溶液滴定,重复2~3次,平均消耗H2SO4标准溶液V2mL。
标准溶液滴定,重复2~3次,平均消耗H2SO4标准溶液V2mL。(6)计算y=
您最近半年使用:0次
2024-02-02更新
|
246次组卷
|
3卷引用:山东省青岛市黄岛区2023-2024学年高三上学期期末考试化学试题



