名校
解题方法
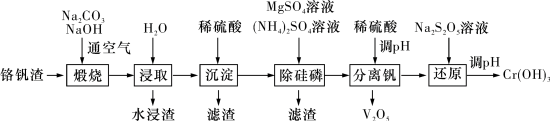
1 . 铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为铁、铝、硅、磷等氧化物,从铬钒渣中分离提取铬和钒的一种流程如图所示: 存在,在碱性介质中以
存在,在碱性介质中以 存在;
存在;
ii) 时,硅元素以
时,硅元素以 形式存在;
形式存在;
iii) 在
在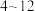 之间,铝元素以
之间,铝元素以 形式存在。
形式存在。
回答下列问题:
(1) 的基态价层电子轨道表示式为
的基态价层电子轨道表示式为_______ 。
(2)向浸取液中滴加稀硫酸过程中含铬离子转化反应的离子方程式为_______ 。
(3)水浸渣中主要物质为_______ (填化学式)。
(4)“沉淀”步骤调 到弱碱性,主要除去的杂质为
到弱碱性,主要除去的杂质为_______ (填化学式)。
(5)“除硅磷”步骤中,使硅、磷分别以 和
和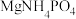 的形式沉淀,该步需要控制溶液的
的形式沉淀,该步需要控制溶液的 以达到最好的除杂效果,下列说法正确的是
以达到最好的除杂效果,下列说法正确的是_______ (填标号)。
a.若 过小,磷酸根离子会与
过小,磷酸根离子会与 反应使其浓度降低导致
反应使其浓度降低导致 无法完全沉淀
无法完全沉淀
b.若 过小,会抑制硅酸根离子水解,导致硅酸镁无法完全沉淀
过小,会抑制硅酸根离子水解,导致硅酸镁无法完全沉淀
c.若 过大,会导致镁离子生成氢氧化镁沉淀,不能形成
过大,会导致镁离子生成氢氧化镁沉淀,不能形成 沉淀,导致产品中混有杂质
沉淀,导致产品中混有杂质
d.若 过大,溶液中铵根离子浓度增大,导致
过大,溶液中铵根离子浓度增大,导致 无法完全沉淀
无法完全沉淀
(6)“分离钒”步骤中,将溶液 调到1.8左右得到
调到1.8左右得到 沉淀,
沉淀, 在
在 时,溶解为
时,溶解为 或
或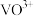 ,在碱性条件下,溶解为
,在碱性条件下,溶解为 或
或 ,上述性质说明
,上述性质说明 具有
具有_______ (填标号)。
A.酸性 B.碱性 C.两性
(7)“还原”步骤中加入焦亚硫酸钠 溶液,反应的离子方程式为
溶液,反应的离子方程式为_______ 。
 存在,在碱性介质中以
存在,在碱性介质中以 存在;
存在;ii)
 时,硅元素以
时,硅元素以 形式存在;
形式存在;iii)
 在
在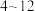 之间,铝元素以
之间,铝元素以 形式存在。
形式存在。回答下列问题:
(1)
 的基态价层电子轨道表示式为
的基态价层电子轨道表示式为(2)向浸取液中滴加稀硫酸过程中含铬离子转化反应的离子方程式为
(3)水浸渣中主要物质为
(4)“沉淀”步骤调
 到弱碱性,主要除去的杂质为
到弱碱性,主要除去的杂质为(5)“除硅磷”步骤中,使硅、磷分别以
 和
和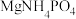 的形式沉淀,该步需要控制溶液的
的形式沉淀,该步需要控制溶液的 以达到最好的除杂效果,下列说法正确的是
以达到最好的除杂效果,下列说法正确的是a.若
 过小,磷酸根离子会与
过小,磷酸根离子会与 反应使其浓度降低导致
反应使其浓度降低导致 无法完全沉淀
无法完全沉淀b.若
 过小,会抑制硅酸根离子水解,导致硅酸镁无法完全沉淀
过小,会抑制硅酸根离子水解,导致硅酸镁无法完全沉淀c.若
 过大,会导致镁离子生成氢氧化镁沉淀,不能形成
过大,会导致镁离子生成氢氧化镁沉淀,不能形成 沉淀,导致产品中混有杂质
沉淀,导致产品中混有杂质d.若
 过大,溶液中铵根离子浓度增大,导致
过大,溶液中铵根离子浓度增大,导致 无法完全沉淀
无法完全沉淀(6)“分离钒”步骤中,将溶液
 调到1.8左右得到
调到1.8左右得到 沉淀,
沉淀, 在
在 时,溶解为
时,溶解为 或
或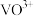 ,在碱性条件下,溶解为
,在碱性条件下,溶解为 或
或 ,上述性质说明
,上述性质说明 具有
具有A.酸性 B.碱性 C.两性
(7)“还原”步骤中加入焦亚硫酸钠
 溶液,反应的离子方程式为
溶液,反应的离子方程式为
您最近半年使用:0次
名校
2 . Cr2O 毒性较强,常用NaHSO3处理工业废水中的Cr2O
毒性较强,常用NaHSO3处理工业废水中的Cr2O ,反应的离子方程式为:H+ +Cr2O
,反应的离子方程式为:H+ +Cr2O +HSO
+HSO
 Cr3++SO
Cr3++SO +H2O(未配平),下列关于该反应的说法正确的是
+H2O(未配平),下列关于该反应的说法正确的是
 毒性较强,常用NaHSO3处理工业废水中的Cr2O
毒性较强,常用NaHSO3处理工业废水中的Cr2O ,反应的离子方程式为:H+ +Cr2O
,反应的离子方程式为:H+ +Cr2O +HSO
+HSO
 Cr3++SO
Cr3++SO +H2O(未配平),下列关于该反应的说法正确的是
+H2O(未配平),下列关于该反应的说法正确的是| A.氧化剂和还原剂的计量数之比为3:1 | B.Cr3+是氧化反应的产物 |
C. 发生还原反应 发生还原反应 | D.消耗5 molH+时转移6mol电子 |
您最近半年使用:0次
3 . 现有下列六种物质:①液态氯化氢;②二氧化碳;③硫酸铜溶液;④熔融氯化钠;⑤ 固体;⑥铁丝.
固体;⑥铁丝.
(1)上述六种物质中,属于非电解质的是__________ ,能导电的电解质是__________ (填序号)。
(2)③和⑥反应的基本反应类型为__________ ,其离子方程式为__________ 。
(3)氯化氢在水溶液中的电离方程式为__________ 。
(4)向③中加入⑤的水溶液的现象为__________ 。
(5) 与⑤可能会发生如下反应,配平该方程式,并用双线桥标出电子得失
与⑤可能会发生如下反应,配平该方程式,并用双线桥标出电子得失______ 。
__________ __________
__________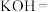 __________
__________ __________
__________ __________
__________
 固体;⑥铁丝.
固体;⑥铁丝.(1)上述六种物质中,属于非电解质的是
(2)③和⑥反应的基本反应类型为
(3)氯化氢在水溶液中的电离方程式为
(4)向③中加入⑤的水溶液的现象为
(5)
 与⑤可能会发生如下反应,配平该方程式,并用双线桥标出电子得失
与⑤可能会发生如下反应,配平该方程式,并用双线桥标出电子得失__________
 __________
__________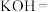 __________
__________ __________
__________ __________
__________
您最近半年使用:0次
名校
解题方法
4 . 下列反应的离子方程式书写正确的是
A.向 溶液中通入少量 溶液中通入少量 |
B. 溶解在 溶解在 溶液中: 溶液中: |
C.向 溶液中加过量的 溶液中加过量的 溶液: 溶液: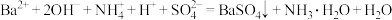 |
D.向 溶液中通入少量氯气: 溶液中通入少量氯气: |
您最近半年使用:0次
2024-04-10更新
|
264次组卷
|
2卷引用:湖南省长沙市长郡中学2023-2024学年高一下学期选科适应性检测化学试卷
名校
解题方法
5 . 铁的化合物有广泛用途,如碳酸亚铁( )可作补血剂。利用某硫酸厂产生的烧渣(主要含
)可作补血剂。利用某硫酸厂产生的烧渣(主要含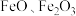 ,还有一定量的
,还有一定量的 )制备碳酸亚铁的流程如图所示:
)制备碳酸亚铁的流程如图所示:
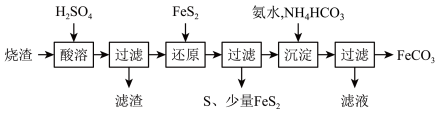
已知:① 不溶于稀硫酸;
不溶于稀硫酸;
②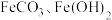 都难溶于水。
都难溶于水。
(1)加入稀硫酸溶解后得到的滤渣是_______________ (写化学式)。
(2)过滤操作需要用到的玻璃仪器有:烧杯、____________ 和____________ 。判断还原时溶液中是否含有 的试剂是
的试剂是______________ 。
(3)“还原”时,加入的 与
与 发生反应Ⅰ、Ⅱ两个氧化还原反应:
发生反应Ⅰ、Ⅱ两个氧化还原反应:
①配平反应Ⅰ的离子方程式:__________
反应Ⅰ:________ ________
________ ________
________ ________
________ ________
________ ________
________
②请写出反应Ⅱ的离子反应方程式:__________ 。
③还原前后溶液中部分离子的浓度见下表(溶液体积变化忽略不计):
则反应Ⅰ、Ⅱ中生成 的物质的量之比为
的物质的量之比为________________ 。
(4)“沉淀”时加入的氨水不宜过量,否则生成的 中可能混有
中可能混有____________ 杂质(写出一种即可)。
 )可作补血剂。利用某硫酸厂产生的烧渣(主要含
)可作补血剂。利用某硫酸厂产生的烧渣(主要含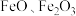 ,还有一定量的
,还有一定量的 )制备碳酸亚铁的流程如图所示:
)制备碳酸亚铁的流程如图所示:
已知:①
 不溶于稀硫酸;
不溶于稀硫酸;②
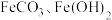 都难溶于水。
都难溶于水。(1)加入稀硫酸溶解后得到的滤渣是
(2)过滤操作需要用到的玻璃仪器有:烧杯、
 的试剂是
的试剂是(3)“还原”时,加入的
 与
与 发生反应Ⅰ、Ⅱ两个氧化还原反应:
发生反应Ⅰ、Ⅱ两个氧化还原反应:①配平反应Ⅰ的离子方程式:
反应Ⅰ:________
 ________
________ ________
________ ________
________ ________
________ ________
________②请写出反应Ⅱ的离子反应方程式:
③还原前后溶液中部分离子的浓度见下表(溶液体积变化忽略不计):
离子 | 离子浓度 | |
还原前 | 还原后 | |
| 0.10 | 2.50 |
| 3.50 | 3.70 |
 的物质的量之比为
的物质的量之比为(4)“沉淀”时加入的氨水不宜过量,否则生成的
 中可能混有
中可能混有
您最近半年使用:0次
名校
6 . 汽车尾气(含 、
、 、CO、
、CO、 、
、 等)是城市空气的污染源之一、
等)是城市空气的污染源之一、
(1)汽车尾气对环境的危害主要有温室效应、雾霾、_______ 等。
(2)在三元催化装置的作用下,汽车尾气可转化为无污染的物质。写出CO与 在此条件下反应的化学方程式:
在此条件下反应的化学方程式:_______ ,消耗14gCO时,转移电子的物质的量是_______ mol。
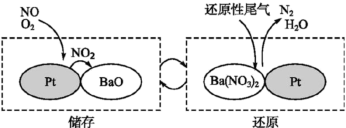
(3) 储存还原技术可有效降低柴油发动机在空气过量条件下
储存还原技术可有效降低柴油发动机在空气过量条件下 的排放。如图所示,
的排放。如图所示, 的储存和还原在不同时段交替进行,通过BaO和
的储存和还原在不同时段交替进行,通过BaO和 的相互转化实现
的相互转化实现 的储存和还原。储存
的储存和还原。储存 的物质是
的物质是_______ 。
(4) 也可以用于催化转化NOx,减少空气污染。请写出实验室用铵盐制备
也可以用于催化转化NOx,减少空气污染。请写出实验室用铵盐制备 的反应方程式
的反应方程式_______ 。
(5)若将 固体投入到含有下列离子的溶液中:
固体投入到含有下列离子的溶液中: 、
、 、
、 、
、 ,反应完毕后,溶液中上述离子数目几乎不变的有
,反应完毕后,溶液中上述离子数目几乎不变的有_______ (填离子符号)。
 、
、 、CO、
、CO、 、
、 等)是城市空气的污染源之一、
等)是城市空气的污染源之一、(1)汽车尾气对环境的危害主要有温室效应、雾霾、
(2)在三元催化装置的作用下,汽车尾气可转化为无污染的物质。写出CO与
 在此条件下反应的化学方程式:
在此条件下反应的化学方程式:(3)
 储存还原技术可有效降低柴油发动机在空气过量条件下
储存还原技术可有效降低柴油发动机在空气过量条件下 的排放。如图所示,
的排放。如图所示, 的储存和还原在不同时段交替进行,通过BaO和
的储存和还原在不同时段交替进行,通过BaO和 的相互转化实现
的相互转化实现 的储存和还原。储存
的储存和还原。储存 的物质是
的物质是
(4)
 也可以用于催化转化NOx,减少空气污染。请写出实验室用铵盐制备
也可以用于催化转化NOx,减少空气污染。请写出实验室用铵盐制备 的反应方程式
的反应方程式(5)若将
 固体投入到含有下列离子的溶液中:
固体投入到含有下列离子的溶液中: 、
、 、
、 、
、 ,反应完毕后,溶液中上述离子数目几乎不变的有
,反应完毕后,溶液中上述离子数目几乎不变的有
您最近半年使用:0次
名校
解题方法
7 .  是一种高效的水处理剂,下列用于解释事实的离子方程式不正确的是
是一种高效的水处理剂,下列用于解释事实的离子方程式不正确的是
 是一种高效的水处理剂,下列用于解释事实的离子方程式不正确的是
是一种高效的水处理剂,下列用于解释事实的离子方程式不正确的是A.工业上可用铁做阳极,电解浓 溶液的方法制 溶液的方法制 ,阳极的电极反应: ,阳极的电极反应: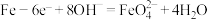 |
B.工业上用 、 、 、 、 三种物质反应制得 三种物质反应制得 的离子方程式: 的离子方程式: |
C. 消毒杀菌时得到的 消毒杀菌时得到的 可以净水, 可以净水, 能产生净水物质的原因: 能产生净水物质的原因: |
D. 在酸性溶液中不稳定,反应生成 在酸性溶液中不稳定,反应生成 和 和 ,离子方程式: ,离子方程式: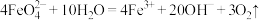 |
您最近半年使用:0次
2024-04-08更新
|
131次组卷
|
2卷引用:湖南省长沙市湖南师范大学附属中学2023-2024学年高三下学期第七次月考化学试题
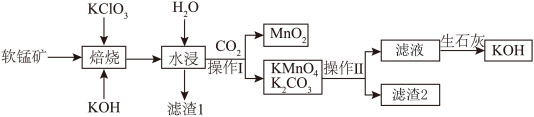
8 . 高锰酸钾在工业中广泛用作氧化剂。以软锰矿(主要成分是 ,含有
,含有 和
和 等杂质)为原料制备高锰酸钾的工艺流程如图所示:
等杂质)为原料制备高锰酸钾的工艺流程如图所示:
已知:
①“焙烧”中有 生成。
生成。
②20℃时各物质的溶解度如下表。
下列说法错误的是
 ,含有
,含有 和
和 等杂质)为原料制备高锰酸钾的工艺流程如图所示:
等杂质)为原料制备高锰酸钾的工艺流程如图所示:
已知:
①“焙烧”中有
 生成。
生成。②20℃时各物质的溶解度如下表。
| 物质 |  |  |  |
| 溶解度/g | 6.38 | 111 | 11.1 |
A.“焙烧”时,主要反应的化学方程式为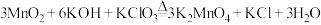 |
B.操作Ⅰ,若通入4mol  时,理论上转移电子数为2 时,理论上转移电子数为2 |
C.“焙烧”时加入的KOH应适量,否则制得的 中混有含Si元素的杂质 中混有含Si元素的杂质 |
D.操作Ⅱ为蒸发浓缩、冷却结晶、过滤,滤渣2的主要成分为 |
您最近半年使用:0次
名校
解题方法
9 . NOx是污染性气体,其性质的掌握及防污处理很重要。回答下列问题:
(1)写出NO2与水反应的离子方程式:___________ ,该反应中氧化剂与还原剂的质量比为____________ 。
(2)相同条件下,将10mL装满NO2与O2的试管倒扣在水槽中,充分反应。若试管中还剩余2mL无色气体,则原试管中NO2的体积可能为___________ mL(答出所有可能)。
(3)NaOH溶液可吸收硝酸工业尾气(含NO、NO2),并获得副产品。
已知: 、
、 。要使硝酸的工业尾气完全被吸收,
。要使硝酸的工业尾气完全被吸收, 的比值应满足
的比值应满足__________ 。
(4)尿素水溶液热解产生的NH3可去除汽车尾气中的NOx,流程如下:

①尿素[CO(NH2)2]中氮元素的化合价为_______________ 。
②写出“催化反应”过程中NH3还原NOx的化学方程式:__________ 。
③“催化反应”过程中需控制温度在250~380℃之间,温度过高,NOx的去除率下降,其原因可能是温度过高催化剂的活性降低和_____________________ 。
(1)写出NO2与水反应的离子方程式:
(2)相同条件下,将10mL装满NO2与O2的试管倒扣在水槽中,充分反应。若试管中还剩余2mL无色气体,则原试管中NO2的体积可能为
(3)NaOH溶液可吸收硝酸工业尾气(含NO、NO2),并获得副产品。
已知:
 、
、 。要使硝酸的工业尾气完全被吸收,
。要使硝酸的工业尾气完全被吸收, 的比值应满足
的比值应满足(4)尿素水溶液热解产生的NH3可去除汽车尾气中的NOx,流程如下:

①尿素[CO(NH2)2]中氮元素的化合价为
②写出“催化反应”过程中NH3还原NOx的化学方程式:
③“催化反应”过程中需控制温度在250~380℃之间,温度过高,NOx的去除率下降,其原因可能是温度过高催化剂的活性降低和
您最近半年使用:0次
10 . 联氨 是一种绿色环保还原剂,为二元弱碱,在水中的电离方程式与氨相似,可用于处理锅炉水中的溶解氧,防止锅炉被腐蚀,下列说法错误的是
是一种绿色环保还原剂,为二元弱碱,在水中的电离方程式与氨相似,可用于处理锅炉水中的溶解氧,防止锅炉被腐蚀,下列说法错误的是
 是一种绿色环保还原剂,为二元弱碱,在水中的电离方程式与氨相似,可用于处理锅炉水中的溶解氧,防止锅炉被腐蚀,下列说法错误的是
是一种绿色环保还原剂,为二元弱碱,在水中的电离方程式与氨相似,可用于处理锅炉水中的溶解氧,防止锅炉被腐蚀,下列说法错误的是A.向装有少量 的试管中加入联氨溶液,可观察到固体逐渐变黑,发生的反应为 的试管中加入联氨溶液,可观察到固体逐渐变黑,发生的反应为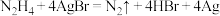 |
B.碱性: |
C.理论上1mol 可处理水中1mol 可处理水中1mol |
D. 是极性分子 是极性分子 |
您最近半年使用:0次