1 . 正高碘酸(H5IO6)是白色结晶性粉末,可溶于水,主要用作氧化剂和分析试剂。由NaI制取H5IO6的实验流程如图所示:
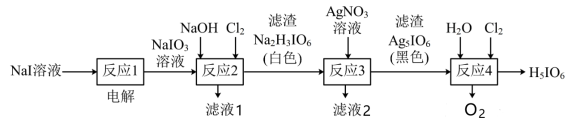
A.“反应1”中: |
B.“反应2”中: |
C.“反应3”中: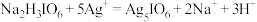 |
D.“反应4”中: |
您最近半年使用:0次
2 . 氧钒(Ⅳ)碱式碳酸铵晶体{化学式为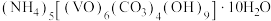 ,
,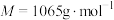 }是一种难溶于水的化合物,它是制备热敏材料VO2的原料。实验室以V2O5为原料,通过还原、转化、沉淀等步骤合成该晶体的流程如下:
}是一种难溶于水的化合物,它是制备热敏材料VO2的原料。实验室以V2O5为原料,通过还原、转化、沉淀等步骤合成该晶体的流程如下:

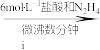
 溶液
溶液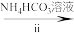 氧钒(Ⅳ)碱式碳酸铵晶体
氧钒(Ⅳ)碱式碳酸铵晶体
已知:+4价钒在弱酸性条件下具有还原性。
回答下列问题:
(1)N2H4为二元弱碱,其在水中的电离过程与NH3类似,其第一步电离方程式为_____ ,第二步电离方程式为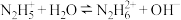 ;N2H4与液氧接触能自燃,产物对环境无污染,写出发生反应的化学方程式:
;N2H4与液氧接触能自燃,产物对环境无污染,写出发生反应的化学方程式:_____ 。
(2)步骤ii可通过如图装置完成。 的优点为
的优点为_____ ,检查其气密性的操作为_____ 。
②实验开始时,先打开_____ (填“K1”或“K2”)。
③盛装NH4HCO3溶液的仪器名称为_____ 。
(3)测定氧钒(Ⅳ)碱式碳酸铵晶体粗产品的纯度。
实验步骤:粗产品wg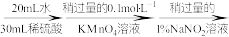
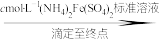 再重复实验两次。
再重复实验两次。
已知: 。
。
①滴入NaNO2溶液的目的是除去KMnO4,写出其反应的离子方程式:_____ 。
②若平均消耗cmol/L(NH4)2Fe(SO4)2标准溶液的体积为amL,则氧钒(Ⅳ)碱式碳酸铵晶体粗产品的纯度为_____  。
。
③若其他操作均正确,但NaNO2的加入量不足,会引起测定结果_____ (填“偏大”“偏小”或“无影响”)。
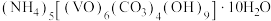 ,
,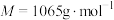 }是一种难溶于水的化合物,它是制备热敏材料VO2的原料。实验室以V2O5为原料,通过还原、转化、沉淀等步骤合成该晶体的流程如下:
}是一种难溶于水的化合物,它是制备热敏材料VO2的原料。实验室以V2O5为原料,通过还原、转化、沉淀等步骤合成该晶体的流程如下:
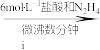
 溶液
溶液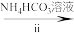 氧钒(Ⅳ)碱式碳酸铵晶体
氧钒(Ⅳ)碱式碳酸铵晶体已知:+4价钒在弱酸性条件下具有还原性。
回答下列问题:
(1)N2H4为二元弱碱,其在水中的电离过程与NH3类似,其第一步电离方程式为
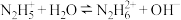 ;N2H4与液氧接触能自燃,产物对环境无污染,写出发生反应的化学方程式:
;N2H4与液氧接触能自燃,产物对环境无污染,写出发生反应的化学方程式:(2)步骤ii可通过如图装置完成。
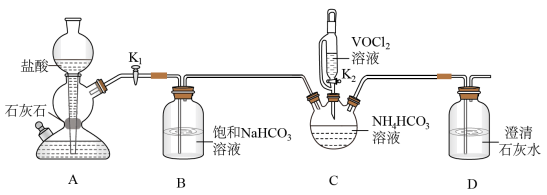
 的优点为
的优点为②实验开始时,先打开
③盛装NH4HCO3溶液的仪器名称为
(3)测定氧钒(Ⅳ)碱式碳酸铵晶体粗产品的纯度。
实验步骤:粗产品wg
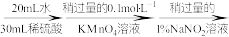
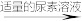
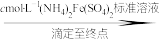 再重复实验两次。
再重复实验两次。已知:
 。
。①滴入NaNO2溶液的目的是除去KMnO4,写出其反应的离子方程式:
②若平均消耗cmol/L(NH4)2Fe(SO4)2标准溶液的体积为amL,则氧钒(Ⅳ)碱式碳酸铵晶体粗产品的纯度为
 。
。③若其他操作均正确,但NaNO2的加入量不足,会引起测定结果
您最近半年使用:0次
2024-05-08更新
|
182次组卷
|
2卷引用:湖南省衡阳市祁东县2024届高三第三次联考(三模)化学试题
解题方法
3 . 氧化锌为白色粉末,可用于湿疹、癣等皮肤病的治疗。纯化工业氧化锌[含有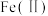 、
、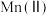 、
、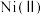 等杂质]的流程如下
等杂质]的流程如下


已知:①在本实验条件下,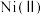 不能被氧化;高锰酸钾的还原产物是
不能被氧化;高锰酸钾的还原产物是 。
。
②不考虑操作过程中引起的质量损失。
回答下列问题:
(1)加稀硫酸酸浸时,常将工业 粉碎,其目的是
粉碎,其目的是_____ 。
(2)过滤时,主要用到的玻璃仪器有烧杯、玻璃棒和________ ,其中玻璃棒的作用为_________ 。
(3)②发生反应的离子方程式有 和
和________ 。
(4)若④中产物仅为 ,则发生反应的离子方程式为
,则发生反应的离子方程式为________ ;取干燥后的滤饼 ,煅烧后可得到产品(
,煅烧后可得到产品( )
) ,则
,则 等于
等于_____ (用含a、m的代数式表示)。
(5)④形成的沉淀要水洗,检验沉淀是否洗涤干净的操作和现象是________ 。
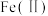 、
、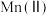 、
、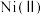 等杂质]的流程如下
等杂质]的流程如下

已知:①在本实验条件下,
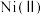 不能被氧化;高锰酸钾的还原产物是
不能被氧化;高锰酸钾的还原产物是 。
。②不考虑操作过程中引起的质量损失。
回答下列问题:
(1)加稀硫酸酸浸时,常将工业
 粉碎,其目的是
粉碎,其目的是(2)过滤时,主要用到的玻璃仪器有烧杯、玻璃棒和
(3)②发生反应的离子方程式有
 和
和(4)若④中产物仅为
 ,则发生反应的离子方程式为
,则发生反应的离子方程式为 ,煅烧后可得到产品(
,煅烧后可得到产品( )
) ,则
,则 等于
等于(5)④形成的沉淀要水洗,检验沉淀是否洗涤干净的操作和现象是
您最近半年使用:0次
4 . 以含锌废液(主要成分为 ,含少量的
,含少量的 、
、 )为原料制备
)为原料制备 的实验流程如下。设
的实验流程如下。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 ,含少量的
,含少量的 、
、 )为原料制备
)为原料制备 的实验流程如下。设
的实验流程如下。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是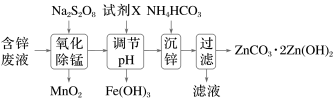
A.1mol过二硫酸钠( )中含有过氧键(-O-O-)数目为 )中含有过氧键(-O-O-)数目为 |
B.“氧化除锰”后的溶液中一定存在: 、 、 、 、 |
C.“调节pH”时试剂X可以选用Zn、ZnO、 等物质 等物质 |
D.“氧化除锰”过程中生成 的离子方程式: 的离子方程式: |
您最近半年使用:0次
解题方法
5 . 氧化钪( )在合金、电光源、催化剂和陶瓷等领域有广泛应用,以链锰矿石(含
)在合金、电光源、催化剂和陶瓷等领域有广泛应用,以链锰矿石(含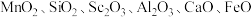 )为原料制备氧化钪的一种工艺流程如图所示。
)为原料制备氧化钪的一种工艺流程如图所示。 ;③草酸可与多种金属离子形成可溶性络合物。
;③草酸可与多种金属离子形成可溶性络合物。
回答下列问题:
(1)为了提高“浸取”效果,可采取的措施有___________ (写出一种)。
(2)“浸取”时铁屑被 氧化为
氧化为 ,该反应的离子方程式是
,该反应的离子方程式是___________ 。
(3)“萃取除铁”时铁和钪的萃取率与O/A(有机相与水相的体积比)的关系如图所示。该工艺中最佳O/A为___________ 。___________ 。
(5)常温下,“沉淀分离”时加入NaOH溶液调节pH至6,滤液中 的浓度为
的浓度为___________ 。
(6)已知 ,
,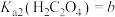 ,
,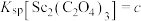 。“沉钪”时,发生反应
。“沉钪”时,发生反应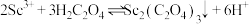 ,此反应的平衡常数
,此反应的平衡常数
___________ (用含a、b、c的代数式表示)。反应过程中,草酸用量过多时,航的沉淀率下降,原因可能是___________ 。
(7)草酸钪晶体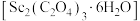 在空气中加热,
在空气中加热, 随温度的变化情况如图所示。550-850 ℃发生反应的化学方程式为
随温度的变化情况如图所示。550-850 ℃发生反应的化学方程式为___________ 。
 )在合金、电光源、催化剂和陶瓷等领域有广泛应用,以链锰矿石(含
)在合金、电光源、催化剂和陶瓷等领域有广泛应用,以链锰矿石(含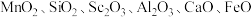 )为原料制备氧化钪的一种工艺流程如图所示。
)为原料制备氧化钪的一种工艺流程如图所示。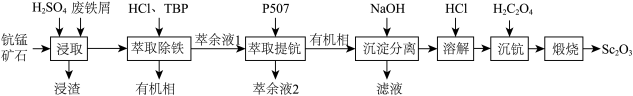
 ;③草酸可与多种金属离子形成可溶性络合物。
;③草酸可与多种金属离子形成可溶性络合物。回答下列问题:
(1)为了提高“浸取”效果,可采取的措施有
(2)“浸取”时铁屑被
 氧化为
氧化为 ,该反应的离子方程式是
,该反应的离子方程式是(3)“萃取除铁”时铁和钪的萃取率与O/A(有机相与水相的体积比)的关系如图所示。该工艺中最佳O/A为

(5)常温下,“沉淀分离”时加入NaOH溶液调节pH至6,滤液中
 的浓度为
的浓度为(6)已知
 ,
,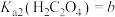 ,
,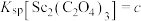 。“沉钪”时,发生反应
。“沉钪”时,发生反应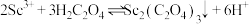 ,此反应的平衡常数
,此反应的平衡常数
(7)草酸钪晶体
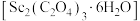 在空气中加热,
在空气中加热, 随温度的变化情况如图所示。550-850 ℃发生反应的化学方程式为
随温度的变化情况如图所示。550-850 ℃发生反应的化学方程式为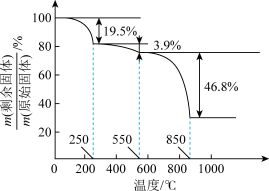
您最近半年使用:0次
名校
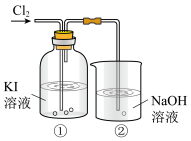
6 . 某研究小组利用下图所示装置探究卤素的性质。___________ (填“氧化性”或“还原性”)。
(2)①中溶液有I2生成,发生反应的化学方程式是___________ 。
(3)②中NaOH溶液的作用是吸收多余的氯气,发生反应的离子方程式是___________ 。
(2)①中溶液有I2生成,发生反应的化学方程式是
(3)②中NaOH溶液的作用是吸收多余的氯气,发生反应的离子方程式是
您最近半年使用:0次
名校
7 . 废旧磷酸铁锂电池中电极片主要由 、铝箔、少量铜及炭黑组成,回收
、铝箔、少量铜及炭黑组成,回收 、
、 的具体流程如下:
的具体流程如下: 溶于酸,不溶于碱;
溶于酸,不溶于碱; 、
、 在常温下的溶解度分别为
在常温下的溶解度分别为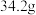 、
、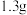 。
。
下列说法错误的是
 、铝箔、少量铜及炭黑组成,回收
、铝箔、少量铜及炭黑组成,回收 、
、 的具体流程如下:
的具体流程如下: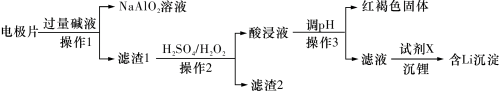
 溶于酸,不溶于碱;
溶于酸,不溶于碱; 、
、 在常温下的溶解度分别为
在常温下的溶解度分别为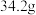 、
、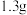 。
。下列说法错误的是
A. 中基态亚铁离子的电子排布式: 中基态亚铁离子的电子排布式: |
B.滤渣1中加入 和 和 可发生反应: 可发生反应: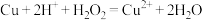 |
C.“调 ”和“沉锂”两个步骤都可以使用 ”和“沉锂”两个步骤都可以使用 ,但试剂的作用不同 ,但试剂的作用不同 |
| D.甲烷和三氧化硫都是由极性键构成的非极性分子 |
您最近半年使用:0次
2024-05-06更新
|
95次组卷
|
3卷引用:湖南省长沙市第一中学2023-2024学年高二下学期第一次月考化学试题
名校
8 . 下列离子方程式书写正确的是
A.向NaOH稀溶液中通入过量 气体: 气体: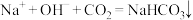 |
B.向 溶液中滴加稀硝酸: 溶液中滴加稀硝酸: |
C.向 溶液中滴加澄清石灰水: 溶液中滴加澄清石灰水: |
D.向 中加入浓盐酸: 中加入浓盐酸: |
您最近半年使用:0次
2024-05-05更新
|
320次组卷
|
3卷引用:湖南省衡阳市衡阳县第一中学2023-2024学年高三下学期4月月考化学试题
名校
解题方法
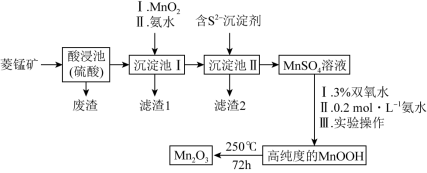
9 . Mn2O3是一种重要的化工产品。以菱锰矿(主要成分为MnCO3,还含有少量Fe3O4、FeO、CoO、Al2O3)为原料制备Mn2O3的工艺流程如图:
已知:氢氧化氧锰(MnOOH)难溶于水和碱性溶液。
(1)MnOOH中Mn的化合价为_______ 价。
(2)向“沉淀池I”中加入MnO2,MnO2的作用是_______ ,在“沉淀池I”中,滴加氨水调节溶液的pH,使溶液中铝、铁元素完全沉淀,则理论上pH的最小值为_______ (当溶液中某离子浓度c≤1.0×10-5mol•L-1时,可认为该离子沉淀完全)。
(3)MnSO4转化为MnOOH的离子方程式为_______ 。
(4)MnSO4转化为MnOOH中“III实验操作”包含过滤、洗涤、干燥,检验MnOOH是否洗涤干净,具体操作为_______ 。
(5)MnS晶胞与NaCl晶胞属于同种类型,MnS晶胞结构如图所示。_______ 。
②已知:MnS晶体的边长为bnm,NA为阿伏加德罗常数的值,则MnS晶胞密度为_______ g•cm-3(列出计算式即可)。
| 物质 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Mn(OH)2 | Co(OH)2 |
| Ksp | 1×10-16.3 | 1×10-38.6 | 1×10-32.3 | 1×10-12.7 | 1.09×10-15 |
(1)MnOOH中Mn的化合价为
(2)向“沉淀池I”中加入MnO2,MnO2的作用是
(3)MnSO4转化为MnOOH的离子方程式为
(4)MnSO4转化为MnOOH中“III实验操作”包含过滤、洗涤、干燥,检验MnOOH是否洗涤干净,具体操作为
(5)MnS晶胞与NaCl晶胞属于同种类型,MnS晶胞结构如图所示。
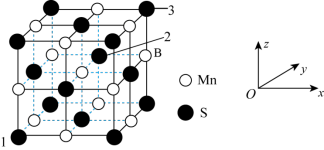
②已知:MnS晶体的边长为bnm,NA为阿伏加德罗常数的值,则MnS晶胞密度为
您最近半年使用:0次
名校
解题方法
10 . 化学小组实验探究 与
与 溶液的反应。
溶液的反应。
实验一:用如图装置制备 ,并将足量
,并将足量 通入
通入 溶液中,迅速反应,得到无色溶液A和白色沉淀B。
溶液中,迅速反应,得到无色溶液A和白色沉淀B。
(1)制备的 中会混有少量的
中会混有少量的 ,原因可能为浓硫酸或硫酸铜受热分解产生
,原因可能为浓硫酸或硫酸铜受热分解产生 ,为了排除
,为了排除 的干扰,试剂a可以为
的干扰,试剂a可以为___________ 。
a.浓硫酸 b.足量 溶液 c.足量NaHS溶液 d.足量饱和
溶液 c.足量NaHS溶液 d.足量饱和 溶液
溶液
请写出试剂a所有不能选择的试剂的理由(用相应的离子方程式回答):___________ 。
实验二:验证白色沉淀B的成分。
分析:沉淀B可能为 、
、 或两者混合物。滴加氨水可释出其阴离子,便于后续检验。
或两者混合物。滴加氨水可释出其阴离子,便于后续检验。
相关反应为:① ,
,
② 。
。
流程如下: 是否已经过量,请简述实验方法
是否已经过量,请简述实验方法___________ 。
(3)沉淀D加入过量盐酸后,只有少量沉淀剩余,则表明大部外沉淀为 。向滤液E中加入
。向滤液E中加入 溶液,产生的现象是
溶液,产生的现象是___________ ,可进一步证实B中含 。
。
实验三:探究 的产生途径。
的产生途径。
猜想1:实验一中, 在
在 溶液中被氧化生成
溶液中被氧化生成 ,随沉淀B进入D。
,随沉淀B进入D。
猜想2:实验二中, 被氧化为
被氧化为 进入D。
进入D。
(4)取少量溶液A,滴加过量盐酸,产生白色沉淀。静置后,取上层清液再滴加 溶液,未出现白色沉淀,可判断猜想1不合理。理由是:
溶液,未出现白色沉淀,可判断猜想1不合理。理由是:___________ 。
(5)不同反应的速率也有所不同。将实验一所得混合物放置一段时间,也会有 生成,同时生成单质Ag。请从化学反应速率的角度分析沉淀反应的速率比氧化还原反应的速率
生成,同时生成单质Ag。请从化学反应速率的角度分析沉淀反应的速率比氧化还原反应的速率___________ (填“快”或“慢”)。
(6)实验探究可知, 在
在___________ (选填“酸性”“中性”“碱性”)溶液中更易被氧化为 。
。
 与
与 溶液的反应。
溶液的反应。实验一:用如图装置制备
 ,并将足量
,并将足量 通入
通入 溶液中,迅速反应,得到无色溶液A和白色沉淀B。
溶液中,迅速反应,得到无色溶液A和白色沉淀B。
(1)制备的
 中会混有少量的
中会混有少量的 ,原因可能为浓硫酸或硫酸铜受热分解产生
,原因可能为浓硫酸或硫酸铜受热分解产生 ,为了排除
,为了排除 的干扰,试剂a可以为
的干扰,试剂a可以为a.浓硫酸 b.足量
 溶液 c.足量NaHS溶液 d.足量饱和
溶液 c.足量NaHS溶液 d.足量饱和 溶液
溶液请写出试剂a所有不能选择的试剂的理由(用相应的离子方程式回答):
实验二:验证白色沉淀B的成分。
分析:沉淀B可能为
 、
、 或两者混合物。滴加氨水可释出其阴离子,便于后续检验。
或两者混合物。滴加氨水可释出其阴离子,便于后续检验。相关反应为:①
 ,
,②
 。
。流程如下:

 是否已经过量,请简述实验方法
是否已经过量,请简述实验方法(3)沉淀D加入过量盐酸后,只有少量沉淀剩余,则表明大部外沉淀为
 。向滤液E中加入
。向滤液E中加入 溶液,产生的现象是
溶液,产生的现象是 。
。实验三:探究
 的产生途径。
的产生途径。猜想1:实验一中,
 在
在 溶液中被氧化生成
溶液中被氧化生成 ,随沉淀B进入D。
,随沉淀B进入D。猜想2:实验二中,
 被氧化为
被氧化为 进入D。
进入D。(4)取少量溶液A,滴加过量盐酸,产生白色沉淀。静置后,取上层清液再滴加
 溶液,未出现白色沉淀,可判断猜想1不合理。理由是:
溶液,未出现白色沉淀,可判断猜想1不合理。理由是:(5)不同反应的速率也有所不同。将实验一所得混合物放置一段时间,也会有
 生成,同时生成单质Ag。请从化学反应速率的角度分析沉淀反应的速率比氧化还原反应的速率
生成,同时生成单质Ag。请从化学反应速率的角度分析沉淀反应的速率比氧化还原反应的速率(6)实验探究可知,
 在
在 。
。
您最近半年使用:0次
2024-05-05更新
|
287次组卷
|
2卷引用:湖南省常德市汉寿县第一中学2023-2024学年高一下学期4月期中考试化学试题



