1 . 已知某反应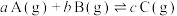 ,在其他条件不变的情况下,改变某一条件后的化学平衡图像如图(T表示温度,p表示压强且
,在其他条件不变的情况下,改变某一条件后的化学平衡图像如图(T表示温度,p表示压强且 ,
, 表示转化率)。下列说法正确的是
表示转化率)。下列说法正确的是
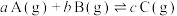 ,在其他条件不变的情况下,改变某一条件后的化学平衡图像如图(T表示温度,p表示压强且
,在其他条件不变的情况下,改变某一条件后的化学平衡图像如图(T表示温度,p表示压强且 ,
, 表示转化率)。下列说法正确的是
表示转化率)。下列说法正确的是
A. , , | B. , , |
C. , , | D. , , |
您最近半年使用:0次
名校
解题方法
2 . 下列有关化学反应速率、化学反应限度的说法中,正确的是
A.反应 ,其他条件不变时,增加碳的用量可加快反应速率 ,其他条件不变时,增加碳的用量可加快反应速率 |
| B.用铁片与稀硫酸反应制H2,改用98%的浓硫酸可加快生成H2的速率 |
| C.工业合成氨反应在密闭容器中进行,压缩容器体积,可使反应速率增大 |
D.当SO3的分子数等于SO2和O2分子数之和时,反应 达到平衡 达到平衡 |
您最近半年使用:0次
名校
3 . N2(g)+3H2(g) 2NH3(g) △H<0,反应达平衡时,下列措施能提高N2转化率的是
2NH3(g) △H<0,反应达平衡时,下列措施能提高N2转化率的是
①降温 ②恒压通入惰性气体 ③增加N2的浓度 ④加压 ⑤催化剂
 2NH3(g) △H<0,反应达平衡时,下列措施能提高N2转化率的是
2NH3(g) △H<0,反应达平衡时,下列措施能提高N2转化率的是①降温 ②恒压通入惰性气体 ③增加N2的浓度 ④加压 ⑤催化剂
| A.①④ | B.①②③⑤ | C.②③⑤ | D.③④ |
您最近半年使用:0次
名校
4 . 下列实验装置能够达到实验目的的是
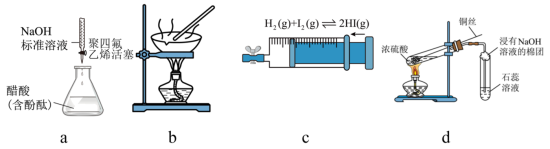
| A.图a测定醋酸的浓度 |
| B.图b由MgCl2溶液制取无水MgCl2 |
| C.图c探究压强对平衡的影响 |
| D.图d检验二氧化硫的漂白性 |
您最近半年使用:0次
5 . 下列方案设计、现象和结论都正确的是
| 实验 | 目的 | 方案设计 | 现象和结论 |
| ① | 探究压强对 与 与 平衡的影响 平衡的影响 | 快速压缩装有 、 、 平衡混合气体的针筒 平衡混合气体的针筒 | 如果气体颜色变深,则增大压强,平衡向生成 的方向移动 的方向移动 |
| ② | 探究 与 与 氧化性的强弱 氧化性的强弱 | 向 和 和 的混合溶液中滴入 的混合溶液中滴入 酸化的 酸化的 溶液 溶液 | 溶液变红,说明氧化性: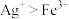 |
| ③ | 验证 溶液中存在水解平衡 溶液中存在水解平衡 | 取2  溶液于试管中,加2滴酚酞,再加入少量 溶液于试管中,加2滴酚酞,再加入少量 固体 固体 | 如果溶液红色变浅,则 溶液中存在水解平衡 溶液中存在水解平衡 |
| ④ | 相同温度下,比较 与 与 的酸性强弱 的酸性强弱 | 向等体积的水中分别通入 、 、 至饱和,再用 至饱和,再用 计测定两种溶液的 计测定两种溶液的 | 如果通 后所得溶液的 后所得溶液的 小,则 小,则 的酸性比弱 的酸性比弱 |
| A.① | B.② | C.③ | D.④ |
您最近半年使用:0次
6 . 下列实验操作、现象及结论都正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将铁锈溶于浓盐酸,再滴入KMnO4溶液 | 紫色褪去 | 铁锈中含有二价铁 |
| B | 向淀粉溶液中加入稀硫酸,加热一段时间后,再滴加银氨溶液,水浴加热 | 未产生银镜 | 淀粉未发生水解 |
| C | 向盛有10滴0.1mol/L AgNO3溶液的试管中滴加15滴0.1mol/L NaCl溶液,观察现象,再滴加2滴0.1mol/L KI溶液 | 先产生白色沉淀,后产生黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| D | 向一体积可变的密闭容器中充入NO2,发生反应:2NO2(g) N2O4(g),将容器体积压缩至原来的一半 N2O4(g),将容器体积压缩至原来的一半 | 相比压缩体积之前,气体颜色变浅 | 增大压强,平衡向气体分子数减小的方向移动 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
7 . 恒温下,反应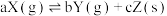 达到平衡状态,把容器容积缩小到原来的一半,且达到新的平衡状态时,X的物质的量浓度从0.1mol·L-1增大到0.19mol·L-1。下列判断中正确的是
达到平衡状态,把容器容积缩小到原来的一半,且达到新的平衡状态时,X的物质的量浓度从0.1mol·L-1增大到0.19mol·L-1。下列判断中正确的是
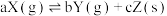 达到平衡状态,把容器容积缩小到原来的一半,且达到新的平衡状态时,X的物质的量浓度从0.1mol·L-1增大到0.19mol·L-1。下列判断中正确的是
达到平衡状态,把容器容积缩小到原来的一半,且达到新的平衡状态时,X的物质的量浓度从0.1mol·L-1增大到0.19mol·L-1。下列判断中正确的是| A.a>b | B.a<b+c | C.a=b+c | D.a<b |
您最近半年使用:0次
名校
8 . 在催化剂作用下, 氧化
氧化 可获得
可获得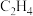
 其主要化学反应为
其主要化学反应为
反应Ⅰ: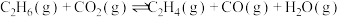
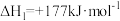
反应Ⅱ: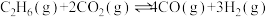

压强分别为 、
、 时,将2mol
时,将2mol 和4mol
和4mol  的混合气体置于的密闭容器中反应,不同温度下体系中乙烷的平衡转化率、乙烯的选择性(
的混合气体置于的密闭容器中反应,不同温度下体系中乙烷的平衡转化率、乙烯的选择性( 的选择性
的选择性 如图所示。已知:210℃时反应均达到平衡状态,容器的体积恒定为1L。
如图所示。已知:210℃时反应均达到平衡状态,容器的体积恒定为1L。
 氧化
氧化 可获得
可获得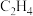
 其主要化学反应为
其主要化学反应为反应Ⅰ:
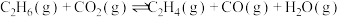
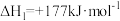
反应Ⅱ:
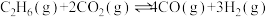

压强分别为
 、
、 时,将2mol
时,将2mol 和4mol
和4mol  的混合气体置于的密闭容器中反应,不同温度下体系中乙烷的平衡转化率、乙烯的选择性(
的混合气体置于的密闭容器中反应,不同温度下体系中乙烷的平衡转化率、乙烯的选择性( 的选择性
的选择性 如图所示。已知:210℃时反应均达到平衡状态,容器的体积恒定为1L。
如图所示。已知:210℃时反应均达到平衡状态,容器的体积恒定为1L。 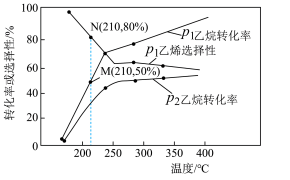
A.压强: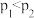 |
B.压强为 ,温度为210℃时,平衡状态 ,温度为210℃时,平衡状态 |
C.压强为 ,温度为210℃时,反应达到平衡时生成等物质的量的CO和 ,温度为210℃时,反应达到平衡时生成等物质的量的CO和 |
D.温度为300℃时,反应Ⅰ的平衡常数: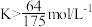 |
您最近半年使用:0次
名校
9 . 氢能作为一种清洁、高效、安全、可持续的新能源,被视为21世纪最具发展潜力的清洁能源,是人类的战略能源发展方向。目前,制备氢气有多种途径:途径一:甲醇产生氢气的反应为:
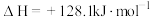
(1)已知相关物质的标准熵数值如下表:
该反应能自发进行的最低温度为___________ K。(保留小数点后1位)
途径二:乙酸制氢的反应为:
反应I: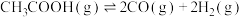
反应Ⅱ: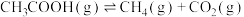
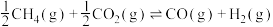

①由图1可得,
___________ kJ·mol-1;
②恒温恒容下发生上述反应,下列说法正确的是___________ 。
A.混合气体密度不变时,反应达到平衡
B.充入CO2,可提高CH4的转化率
C.加入催化剂,可提高H2的平衡产率
D.充入Ar,对H2的产率不产生影响
(3)一定条件下,在密闭容器中加入一定量的乙酸,只发生反应I和反应Ⅱ。
①在相同时间,测得温度与气体产率的关系如上图2所示。约650℃之前,氢气产率低于甲烷的可能原因是___________ 。
②设达到平衡时,体系总压强为p,乙酸体积分数为20%,反应I消耗的乙酸占投入量的20%,则反应Ⅱ的平衡常数 为
为___________ 。(用平衡分压代替平衡浓度计算)
途径三:热分解H2S制氢的反应为: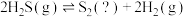
(4)不同温度和压强下,H2S的平衡转化率变化如图。生成物S2的状态为___________ (填“气态”或“非气态”),P1___________ P2(填“>”或“<”)。

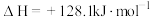
(1)已知相关物质的标准熵数值如下表:
| 化学式 |  |  |  |
标准熵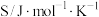 | 126.8 | 130.7 | 197.7 |
途径二:乙酸制氢的反应为:
反应I:
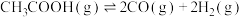
反应Ⅱ:
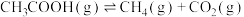
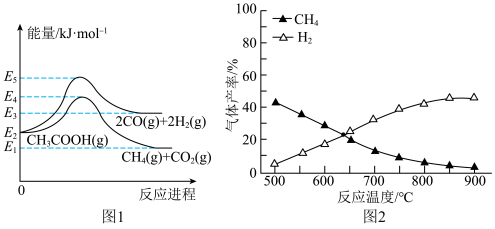
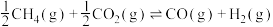

①由图1可得,

②恒温恒容下发生上述反应,下列说法正确的是
A.混合气体密度不变时,反应达到平衡
B.充入CO2,可提高CH4的转化率
C.加入催化剂,可提高H2的平衡产率
D.充入Ar,对H2的产率不产生影响
(3)一定条件下,在密闭容器中加入一定量的乙酸,只发生反应I和反应Ⅱ。
①在相同时间,测得温度与气体产率的关系如上图2所示。约650℃之前,氢气产率低于甲烷的可能原因是
②设达到平衡时,体系总压强为p,乙酸体积分数为20%,反应I消耗的乙酸占投入量的20%,则反应Ⅱ的平衡常数
 为
为途径三:热分解H2S制氢的反应为:
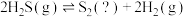
(4)不同温度和压强下,H2S的平衡转化率变化如图。生成物S2的状态为
您最近半年使用:0次
2024-04-21更新
|
116次组卷
|
2卷引用:东北三省四城市联考暨沈阳市高三下学期质量监测(二)化学试题
10 . 将 催化转化成CO是实现
催化转化成CO是实现 资源化利用的关键步骤,发生的反应有
资源化利用的关键步骤,发生的反应有
反应Ⅰ:

反应Ⅱ: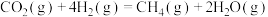

反应Ⅲ: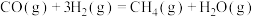
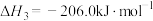 ,0.1MPa,在密闭容器中按
,0.1MPa,在密闭容器中按 投料,平衡时各组分的摩尔分数[物质i的摩尔分数:
投料,平衡时各组分的摩尔分数[物质i的摩尔分数: ,
, 未计入]随温度的变化如图。下列说法
未计入]随温度的变化如图。下列说法不正确 的是
 催化转化成CO是实现
催化转化成CO是实现 资源化利用的关键步骤,发生的反应有
资源化利用的关键步骤,发生的反应有反应Ⅰ:


反应Ⅱ:
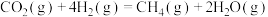

反应Ⅲ:
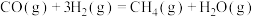
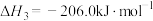 ,0.1MPa,在密闭容器中按
,0.1MPa,在密闭容器中按 投料,平衡时各组分的摩尔分数[物质i的摩尔分数:
投料,平衡时各组分的摩尔分数[物质i的摩尔分数: ,
, 未计入]随温度的变化如图。下列说法
未计入]随温度的变化如图。下列说法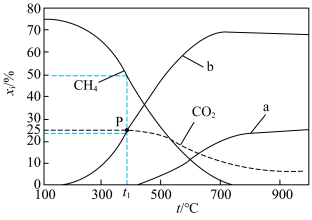
| A.低温下有利于反应Ⅱ正向进行 | B.曲线b为 |
C.P点时反应Ⅰ的 约为 约为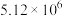 | D.900℃时,适当增大体系压强,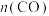 保持不变 保持不变 |
您最近半年使用:0次



