名校
1 . 太阳能电池是通过光电效应或者光化学效应直接把光能转化成电能的装置。其材料除单晶硅,还有铜、铟、镓、硒等化合物。
(1)镓的基态原子的价电子排布式是___________ 。
(2)已知硒为第4周期ⅥA族元素,则硒与其相邻的同周期元素中,第一电离能从大到小顺序为___ (用元素符号表示)。
(3)气态SeO3分子的立体构型为_____________________ 。
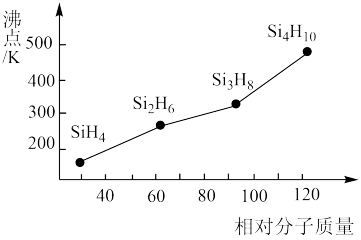
(4)硅烷(SinH2n+2)的沸点与其相对分子质量的变化关系如图所示,呈现这种变化关系的原因是:_________ 。
(5)与镓元素处于同一主族的硼元素具有缺电子性,其化合物往往具有加合性,因而硼酸(H3BO3)在水溶液中能与水反应生成[B(OH)4]-而体现一元弱酸的性质,则[B(OH)4]-中B的原子杂化类型为______ ;
(6)金属Cu单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,反应的离子方程式为_______ ;
(7)一种铜金合金晶体具有面心立方最密堆积的结构.在晶胞中,Au原子位于顶点,Cu原子位于面心,则该合金中Au原子与Cu原子个数之比为______ ,若Au的原子半径为a pm,Cu的原子半径为b pm,则合金的密度为________ g·cm-3(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)。
(1)镓的基态原子的价电子排布式是
(2)已知硒为第4周期ⅥA族元素,则硒与其相邻的同周期元素中,第一电离能从大到小顺序为
(3)气态SeO3分子的立体构型为
(4)硅烷(SinH2n+2)的沸点与其相对分子质量的变化关系如图所示,呈现这种变化关系的原因是:

(5)与镓元素处于同一主族的硼元素具有缺电子性,其化合物往往具有加合性,因而硼酸(H3BO3)在水溶液中能与水反应生成[B(OH)4]-而体现一元弱酸的性质,则[B(OH)4]-中B的原子杂化类型为
(6)金属Cu单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,反应的离子方程式为
(7)一种铜金合金晶体具有面心立方最密堆积的结构.在晶胞中,Au原子位于顶点,Cu原子位于面心,则该合金中Au原子与Cu原子个数之比为
您最近一年使用:0次
解题方法
2 . 铁及其化合物在生产生活及科学研究方面应用非常广泛。
(1)基态Fe原子的价层电子的电子排布图为_________________ ,其最外层电子的电子云形状为___________ 。
(2)(NH4)2Fe(SO4)2•6H2O俗称摩尔盐。
①O、S两元素的电负性由大到小的顺序为_____________ (用元素符号表示)。
②N、O两元素的的第一电离能由大到小的顺序为___________ (用元素符号表示)。
③SO42-中S原子的杂化方式为___________ ,VSEPR模型名称为___________________ 。
(3)Fe3+可与某阴离子发生特征的显色反应,用于鉴定Fe3+。该阴离子的电子式为_____ ,σ键和π键的数目之比为______________ 。其空间构型为__________ 。
(4)K3[Fe(CN)6]晶体中配离子的配位体为_____ (用化学符号表示)
(1)基态Fe原子的价层电子的电子排布图为
(2)(NH4)2Fe(SO4)2•6H2O俗称摩尔盐。
①O、S两元素的电负性由大到小的顺序为
②N、O两元素的的第一电离能由大到小的顺序为
③SO42-中S原子的杂化方式为
(3)Fe3+可与某阴离子发生特征的显色反应,用于鉴定Fe3+。该阴离子的电子式为
(4)K3[Fe(CN)6]晶体中配离子的配位体为
您最近一年使用:0次
2019-02-25更新
|
571次组卷
|
2卷引用:【区级联考】重庆市九龙坡区2018-2019学年高二上学期教育质量全面监测化学试题
解题方法
3 . 许多元素及它们的化合物在科学研究和工业生产中具有许多用途。请回答下列有关问题:
(1)现代化学中,常利用_________ 上的特征谱线来鉴定元素。
(2)某同学画出基态碳原子的核外电子排布图: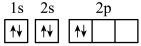 ,该电子排布图违背了
,该电子排布图违背了__ ;CH3+、—CH3、CH3—都是重要的有机反应中间体。CH3+、CH3—的空间构型分别为___ 、____ 。
(3)基态溴原子的价层电子轨道排布图为_______ ,第四周期中,与溴原子未成对电子数相同的金属元素有_______ 种。
(4)磷化硼是一种耐磨涂料,它可用作金属的表面保护层。
①磷化硼晶体晶胞如图甲所示:其中实心球为磷原子,在一个晶胞中磷原子空间堆积方式为_____ ,已知晶胞边长a pm,阿伏伽德罗常数为NA。则磷化硼晶体的密度为___________ g/cm3。
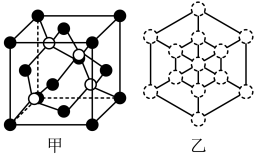
②磷化硼晶胞沿着体对角线方向的投影(图乙中 表示P原子的投影),用
表示P原子的投影),用 画出B原子的投影位置
画出B原子的投影位置_____ 。
(5)Fe3O4晶体中,O2-围成正四面体空隙(1、3、6、7号氧围成)和正八面体空隙(3、6、7、8、9、12号氧围成),Fe3O4中有一半的Fe3+填充在正四面体空隙中,Fe2+和另一半Fe3+填充在正八面体空隙中,晶体中正四面体空隙数与正八面体空隙数之比为__________ ,有__________ %的正八面体空隙没有填充阳离子。
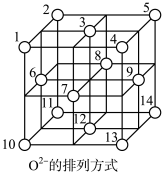
(6)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+填充其中(如图),已知O2-的半径为a pm,每平方米面积上分散的该晶体的质量为_____ g(用a、NA表示)

(1)现代化学中,常利用
(2)某同学画出基态碳原子的核外电子排布图:
 ,该电子排布图违背了
,该电子排布图违背了(3)基态溴原子的价层电子轨道排布图为
(4)磷化硼是一种耐磨涂料,它可用作金属的表面保护层。
①磷化硼晶体晶胞如图甲所示:其中实心球为磷原子,在一个晶胞中磷原子空间堆积方式为

②磷化硼晶胞沿着体对角线方向的投影(图乙中
 表示P原子的投影),用
表示P原子的投影),用 画出B原子的投影位置
画出B原子的投影位置(5)Fe3O4晶体中,O2-围成正四面体空隙(1、3、6、7号氧围成)和正八面体空隙(3、6、7、8、9、12号氧围成),Fe3O4中有一半的Fe3+填充在正四面体空隙中,Fe2+和另一半Fe3+填充在正八面体空隙中,晶体中正四面体空隙数与正八面体空隙数之比为

(6)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+填充其中(如图),已知O2-的半径为a pm,每平方米面积上分散的该晶体的质量为

您最近一年使用:0次
2019-02-05更新
|
781次组卷
|
2卷引用:重庆市2021届高三上学期第二次预测性考试化学试题
4 . W、X、Y、Z(W、X、Y、Z分别代表元素符号)均为元素周期表中前四周期的元素,其原子序数依次增大,其中W、X、Y、Z为短周期元素,它们的单质在通常情况下均为无色气体。X元素的基态原子在同周期元素基态原子中含有的未成对电子数最多,Y元素的基态原子中s能级上的电子数等于p能级上的电子数,Z为金属元素,其基态原子是具有4s1结构的基态原子中质子数最多的原子,试回答下列问题:
(1)写出X的基态原子的价电子排布式_________________ ;
(2)比较X、Y两元素基态原子的第一电离能大小:X__________ Y(填“>”、“<”或“=”),理由是________ ;
(3)W、X两元素能写出一种常见气体M,每个M分子中含有10个电子,M分子中心原子的杂化方式为_________ ;WX两种元素还能写出一种常见阳离子N,每个N中也含有10个电子,但在N与M中所含化学键的键角大小不同,其原因是__________ ;
(4)Z2+可与M分子在谁溶液中形成[Z(M)4]2+,其中M分子和Z2+通过__________ -结合;
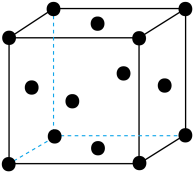
(5)单质Z的警报结构如图所示,已知两个最近的Z原子距离为a,Z的相对原子质量用Mr表示,则该晶体密度为_______________ (只列计算式)。
(1)写出X的基态原子的价电子排布式
(2)比较X、Y两元素基态原子的第一电离能大小:X
(3)W、X两元素能写出一种常见气体M,每个M分子中含有10个电子,M分子中心原子的杂化方式为
(4)Z2+可与M分子在谁溶液中形成[Z(M)4]2+,其中M分子和Z2+通过
(5)单质Z的警报结构如图所示,已知两个最近的Z原子距离为a,Z的相对原子质量用Mr表示,则该晶体密度为

您最近一年使用:0次
5 . 氮、磷、砷是同族元素,该族元素单质及其化合物在农药、化肥等方面有重要应用。回答下列问题:
(1)基态砷原子的电子排布式为______ 。
(2)K3[Fe(CN)6]晶体中Fe3+与CN一之间化学键类型为_____ 键,与CN一互为等电子体的化合物分子式为________ 。
(3)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾污染,光化学烟雾中含有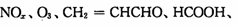
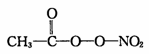 (PAN)等二次污染物。
(PAN)等二次污染物。
N2O结构式可表示为N=N=O,N2O中中心氮原子的杂化轨道类型为_____ ,1 mol PAN中含σ键数目为____ 。
测定大气中PM2.5的浓度方法之一是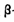 一射线吸收法,
一射线吸收法,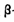 一射线放射源可用85 Kr。Kr晶体为面心立方晶体,若晶体中与每个Kr原子相紧邻的Kr原子有m个,晶胞中含Kr原子为n个,则
一射线放射源可用85 Kr。Kr晶体为面心立方晶体,若晶体中与每个Kr原子相紧邻的Kr原子有m个,晶胞中含Kr原子为n个,则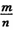 =
=_____ (填数字)。已知Kr晶体的密度为 g/cm3,摩尔质量为Mg/ mol,阿伏加德罗常数用NA表示,列式表示Kr晶胞参数a=
g/cm3,摩尔质量为Mg/ mol,阿伏加德罗常数用NA表示,列式表示Kr晶胞参数a=____ nm
(1)基态砷原子的电子排布式为
(2)K3[Fe(CN)6]晶体中Fe3+与CN一之间化学键类型为
(3)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾污染,光化学烟雾中含有
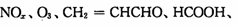
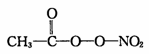 (PAN)等二次污染物。
(PAN)等二次污染物。N2O结构式可表示为N=N=O,N2O中中心氮原子的杂化轨道类型为
测定大气中PM2.5的浓度方法之一是
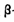 一射线吸收法,
一射线吸收法,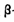 一射线放射源可用85 Kr。Kr晶体为面心立方晶体,若晶体中与每个Kr原子相紧邻的Kr原子有m个,晶胞中含Kr原子为n个,则
一射线放射源可用85 Kr。Kr晶体为面心立方晶体,若晶体中与每个Kr原子相紧邻的Kr原子有m个,晶胞中含Kr原子为n个,则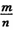 =
= g/cm3,摩尔质量为Mg/ mol,阿伏加德罗常数用NA表示,列式表示Kr晶胞参数a=
g/cm3,摩尔质量为Mg/ mol,阿伏加德罗常数用NA表示,列式表示Kr晶胞参数a=
您最近一年使用:0次
2019-01-30更新
|
164次组卷
|
3卷引用:2016届重庆市巴蜀中学高三下3月月考理综化学试卷
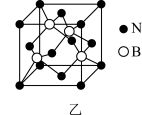
6 . 氮化硼(BN)是一种重要的功能陶瓷材料以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如下图所示:
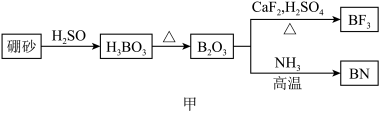
请回答下列问题:
(1)由B2O3制备BF3、BN的化学方程式依次是_________ 、__________ ;
(2)基态B原子的电子排布式为_________ ;B和N相比,电负性较大的是_________ ,BN中B元素的化合价为_________ ;
(3)在BF3分子中,F-B-F的建角是_______ ,B原子的杂化轨道类型为_______ ,BF3和过量NaF作用可生成NaBF,BF 的立体结构为
的立体结构为_______ ;
(4) 在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为________ ,层间作用力为________ ;
(5)六方氢化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,硬度与金刚石相当,晶胞边长为361.5pm,立方氮化硼晶胞中含有______ 各氮原子、________ 各硼原子,立方氮化硼的密度是_______ g· (只要求列算式,不必计算出数值,阿伏加德罗常数为NA)。
(只要求列算式,不必计算出数值,阿伏加德罗常数为NA)。


请回答下列问题:
(1)由B2O3制备BF3、BN的化学方程式依次是
(2)基态B原子的电子排布式为
(3)在BF3分子中,F-B-F的建角是
 的立体结构为
的立体结构为(4) 在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为
(5)六方氢化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,硬度与金刚石相当,晶胞边长为361.5pm,立方氮化硼晶胞中含有
 (只要求列算式,不必计算出数值,阿伏加德罗常数为NA)。
(只要求列算式,不必计算出数值,阿伏加德罗常数为NA)。
您最近一年使用:0次
2019-01-30更新
|
2642次组卷
|
14卷引用:2016届重庆市部分中学高三上学期第一次月考化学试卷
2016届重庆市部分中学高三上学期第一次月考化学试卷2011年普通高等学校招生全国统一考试化学卷(新课标)(已下线)2012-2013学年吉林省龙井市三中高二下学期期中考试化学试卷(已下线)2012-2013学年河南灵宝第三高级中学高二下学期第三次检测化学卷(已下线)2014高考名师推荐化学选做题练习22015-2016学年贵州省思南中学高二下第二次月考化学试卷2016-2017学年高中化学选修3(人教版)第三章 晶体结构与性质 章末检测内蒙古阿拉善左旗高级中学2017-2018学年高二下学期期末考试化学试题贵州省遵义育新高级中学2018-2019学年高二上学期11月月考化学试题云南省彝良县民族中学2018-2019学年高二上学期12月份考试化学试题云南省武定县第一中学2018-2019学年高二上学期12月份考试化学试题云南省昭通水田新区中学2018-2019学年高二上学期12月月考化学试题云南省凤庆县第一中学2019-2020学年高二12月月考化学试题云南省梁河县第一中学2019-2020学年高二上学期期末考试化学试题
7 . 氮族元素中的很多化合物在医疗上有广泛应用,比如NO,少量的NO可以防止血管堵塞。
Ⅰ.氨水在实验室是一种常见的试剂。
(1)稀氨水与稀盐酸反应,中和热∆H___ —57.3 kJ/mol(选填“>”“<”“=”)
(2)铜氨络合物的制备:烧杯中加入10 mL 0.2mol/L的硫酸铜溶液,再滴加8 mol/L的氨水,则有浅蓝色的碱式硫酸铜沉淀生成,继续滴加氨水至沉淀完全溶解,此时即得深蓝色的含有铜氨络离子的溶液,写出铜氨络离子的结构式___________ 。
Ⅱ.麻醉剂的发现和使用,是人类历史上了不起的一项成就,它可使患者在接受治疗时感觉不到疼痛。
(3)“笑气”(N2O)是人类最早应用于医疗的麻醉剂之一。有关理论认为N2O与CO2具有相似的结构(包括电子式)且都为非极性分子,则其空间构型是___________ 形;另一种常用麻醉剂氯仿,常因保存不慎而被氧化,产生剧毒物光气(COCl2):2CHCl3 + O2 =2HCl+ 2COCl2,为防止中毒事故,使用前可用于检验氯仿是否变质的试剂是___________ 。
Ⅲ.羟胺(NH2OH)可看做是氨分子内的1个氢原子被羟基取代的物质,常用作还原剂。也用作合成抗癌药(羟基脲)、磺胺药(新诺明)和农药(灭多威)的原料。
(4)羟胺的电子式为___________ 。
(5)以下关于羟胺说法正确的是___________ 。
Ⅳ.氮氧化物会污染环境,若用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4 (g)+4NO2 (g)=4NO(g)+CO2 (g)+2H2 O(g) ΔH=-574 kJ/mol
②CH4 (g)+4NO(g)=2N2 (g)+CO2 (g)+2H2 O(g) ΔH=-1160 kJ/mol
③H2O(g)=H2O(l) ΔH=-44.0 kJ/mol
(6)写出甲烷气体与NO2气体反应生成氮气、二氧化碳气体和液态水的热化学方程式:___________ 。
Ⅰ.氨水在实验室是一种常见的试剂。
(1)稀氨水与稀盐酸反应,中和热∆H
(2)铜氨络合物的制备:烧杯中加入10 mL 0.2mol/L的硫酸铜溶液,再滴加8 mol/L的氨水,则有浅蓝色的碱式硫酸铜沉淀生成,继续滴加氨水至沉淀完全溶解,此时即得深蓝色的含有铜氨络离子的溶液,写出铜氨络离子的结构式
Ⅱ.麻醉剂的发现和使用,是人类历史上了不起的一项成就,它可使患者在接受治疗时感觉不到疼痛。
(3)“笑气”(N2O)是人类最早应用于医疗的麻醉剂之一。有关理论认为N2O与CO2具有相似的结构(包括电子式)且都为非极性分子,则其空间构型是___________ 形;另一种常用麻醉剂氯仿,常因保存不慎而被氧化,产生剧毒物光气(COCl2):2CHCl3 + O2 =2HCl+ 2COCl2,为防止中毒事故,使用前可用于检验氯仿是否变质的试剂是___________ 。
| A.酚酞试液 | B.淀粉碘化钾溶液 | C.NaOH溶液 | D.硝酸银溶液 |
Ⅲ.羟胺(NH2OH)可看做是氨分子内的1个氢原子被羟基取代的物质,常用作还原剂。也用作合成抗癌药(羟基脲)、磺胺药(新诺明)和农药(灭多威)的原料。
(4)羟胺的电子式为
(5)以下关于羟胺说法正确的是___________ 。
| A.可做抗氧化剂 |
| B.羟胺晶体为分子晶体,其晶体内只有范德华力一种作用 |
| C.根据其结构特征,可推测羟胺难溶于水 |
| D.等物质的量的羟胺和乙烷所含电子数相等 |
Ⅳ.氮氧化物会污染环境,若用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4 (g)+4NO2 (g)=4NO(g)+CO2 (g)+2H2 O(g) ΔH=-574 kJ/mol
②CH4 (g)+4NO(g)=2N2 (g)+CO2 (g)+2H2 O(g) ΔH=-1160 kJ/mol
③H2O(g)=H2O(l) ΔH=-44.0 kJ/mol
(6)写出甲烷气体与NO2气体反应生成氮气、二氧化碳气体和液态水的热化学方程式:
您最近一年使用:0次
8 . A、B、C、D为原子序数依次增大的四种元素,A2-和B+具有相同的电子构型;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中电负性最大的是______ (填元素符号),其中C原子的核外电子排布式为__________ 。
(2)单质A有两种同素异形体,其中沸点高的是_____ (填分子式),原因是_______ ;A和B的氢化物所属的晶体类型分别为______ 和______ 。
(3)C和D反应可生成组成比为1:3的化合物E,E的立体构型为______ ,中心原子的杂化轨道类型为______ 。
(4)化合物D2A的立体构型为___ ,中心原子的价层电子对数为______ ,单质D与湿润的Na2CO3反应可制备D2A,其化学方程式为_________ 。
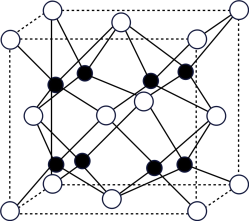
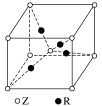
(5)A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数,a=0.566nm,F的化学式为______ :晶胞中A原子的配位数为_________ ;列式计算晶体F的密度(g.cm-3)_____ 。
(1)四种元素中电负性最大的是
(2)单质A有两种同素异形体,其中沸点高的是
(3)C和D反应可生成组成比为1:3的化合物E,E的立体构型为
(4)化合物D2A的立体构型为
(5)A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数,a=0.566nm,F的化学式为

您最近一年使用:0次
2019-01-30更新
|
7105次组卷
|
32卷引用:2016届重庆市第一中学高三上12月月考理综化学试卷
2016届重庆市第一中学高三上12月月考理综化学试卷2015年全国普通高等学校招生统一考试化学(新课标II卷)2016届广东省仲元中学高三11月月考理科综合化学试卷2016届宁夏六盘山中学高三上第一次模拟理综化学试卷2017届江西省九江市十校高三第二次联考理科综合化学试卷新疆生产建设兵团第二中学2016-2017学年高二下学期第二次月考化学试题宁夏六盘山高级中学2017届高三第五次模拟考试理科综合化学试题宁夏石嘴山市第三中学2018届高三9月月考化学试题河北省正定中学2017届高三上学期第三次月考化学试题四川省南充高级中学2018届高三上学期第四次检测理综化学试题山西省临猗县临晋中学2017-2018学年高二下学期期末考试化学试题西藏自治区日喀则市南木林高级中学2019届高三第一次月考理综化学试题河北省唐山市第十一中学2018-2019学年高二下学期期中考试化学试题鲁科版高中化学选修3模块综合测评卷山西省应县第一中学校2018-2019学年高二下学期期中考试化学试题云南省玉溪一中2020届高三上学期期中考试理综化学试题云南省西畴县第二中学2019-2020学年高三上学期期末考试化学试题四川省成都市双流棠湖中学2019-2020学年高二下学期第二次月考化学试题2020届浙江省杭州学军中学高三教学质量监测卷化学试题湖南省长沙市礼雅中学2020届高三下学期三月份网络教学质量监测理科综合化学试题吉林省长春市东北师大附中2020届高中毕业班三月份网络教学质量监测卷理科综合化学部分广东省广州市华南师范大学附属中学2020届高三教学质量监测卷理科综合化学试题广东省深圳外国语学校2021届高三上学期11月月考化学试题四川省成都市北大成都附属实验学校2021届高三上学期12月月考理科综合化学试题广东省2021届高三“六校联盟”第三次联考化学试题四川省成都龙泉中学2021届高三下学期4月月考理科综合化学试题吉林省松原市实验高级中学2021届高三5月月考化学试题(已下线)2020年海南卷化学高考真题变式题15-19山东省德州市2021-2022学年高二下学期物质结构与性质模块综合测评化学试题吉林省汪清县汪清四中2020-2021学年高二下学期期末考试化学试题河南省郑州市六校联盟2022-2023学年高二下学期4月期中考试化学试题内蒙古通辽市/科左中旗民族职专·实验高中2023-2024学年高三上学期第二次月考化学试卷
名校
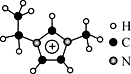
9 . 离子液体是一类具有很高应用价值的绿色溶剂和催化剂,其中的EMIM+离子由H、C、N三种元素组成,结构如图所示。回答下列问题:
(1)碳原子价层电子的轨道表达式为__________ ,基态碳原子中,核外电子占据的最高能级的电子云轮廓图为_________ 形。
(2)根据价层电子对互斥理论,NH3、NO3-、NO2-中,中心原子价层电子对数不同于其他两种粒子的是_______ 。NH3比PH3的沸点高,原因是_________ 。
(3)氮元素的第一电离能比同周期相邻元素都大的原因是____________ 。
(4)EMIM+离子中,碳原子的杂化轨道类型为______ 。分子中的大π键可用符号 表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中的大π键可表示为 ),则EMIM+离子中的大π键应表示为
),则EMIM+离子中的大π键应表示为________ 。
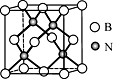
(5)立方氮化硼硬度仅次于金刚石,但热稳定性远高于金刚石,其晶胞结构如图所示。立方氮化硼属于_______ 晶体,其中硼原子的配位数为_______ 。已知:立方氮化硼密度为dg/cm3,B原子半径为xpm,N原子半径为ypm,阿伏伽德罗常数的值为NA,则该晶胞中原子的空间利用率为________ (列出化简后的计算式)。

(1)碳原子价层电子的轨道表达式为
(2)根据价层电子对互斥理论,NH3、NO3-、NO2-中,中心原子价层电子对数不同于其他两种粒子的是
(3)氮元素的第一电离能比同周期相邻元素都大的原因是
(4)EMIM+离子中,碳原子的杂化轨道类型为
 表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中的大π键可表示为 ),则EMIM+离子中的大π键应表示为
),则EMIM+离子中的大π键应表示为
(5)立方氮化硼硬度仅次于金刚石,但热稳定性远高于金刚石,其晶胞结构如图所示。立方氮化硼属于
您最近一年使用:0次
2019-01-14更新
|
1545次组卷
|
5卷引用:【全国百强校】重庆南开中学高2019届高三下学期4月考试理科综合化学试题
名校
10 . X、Y、Z、W、R是原子序数依次增大的前四周期元素,这五种元素的相关信息如下:
(1)基态R原子的电子排布式为________________ 。
(2)Y2分子中σ键和π键的数目比为________ 。
(3)X、Y、Z三种元素的第一电离能由小到大的顺序为____ (用元素符号表示),元素Y的简单气态氢化物的沸点比元素X的简单气态氢化物沸点高的主要原因是____ 。
(4)元素Z、W组成的微粒WZ42-的空间构型是_____ ,其中W原子的杂化轨道类型为_____ 。
(5)已知Z、R能形成一种化合物,其晶胞结构如图所示,该化合物的化学式为______ ;若相邻的Z原子和R原子间的距离为acm,设阿伏加德常数的值为NA,则该晶体的密度为______ g·cm-3(用含a、NA的代数式表示)。
| 元素 | 相关信息 |
| X | 其中一种核素在考古时常用来鉴定一些文物的年代 |
| Y | 原子核外电子有7种不同的运动状态 |
| Z | 地壳中含量最高的元素 |
| W | 价电子排布式为(n+1)sn(n+1)pn+2 |
| R | 基态原子最外能层只有一个电子,其他能层均已充满电子 |
(1)基态R原子的电子排布式为
(2)Y2分子中σ键和π键的数目比为
(3)X、Y、Z三种元素的第一电离能由小到大的顺序为
(4)元素Z、W组成的微粒WZ42-的空间构型是
(5)已知Z、R能形成一种化合物,其晶胞结构如图所示,该化合物的化学式为

您最近一年使用:0次



