名校
解题方法
1 . 利用微生物燃料电池(MFC)可以将废水中的 降解为N2。某课题组设计出如图所示的微生物燃料电池进行同步硝化和反硝化脱氮研究,下列说法不正确的是
降解为N2。某课题组设计出如图所示的微生物燃料电池进行同步硝化和反硝化脱氮研究,下列说法不正确的是
 降解为N2。某课题组设计出如图所示的微生物燃料电池进行同步硝化和反硝化脱氮研究,下列说法不正确的是
降解为N2。某课题组设计出如图所示的微生物燃料电池进行同步硝化和反硝化脱氮研究,下列说法不正确的是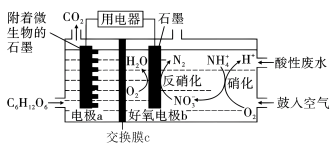
A.好氧电极b上发生的反硝化反应为2 +10e-+12H+=N2↑+6H2O +10e-+12H+=N2↑+6H2O |
| B.好氧电极b上的副反应为O2+4e-+4H+=2H2O |
| C.交换膜c为质子交换膜,质子从电极a区域通过质子交换膜移向电极b区域 |
D.理论上每消耗1molC6H12O6,可以处理 的物质的量为4.8mol 的物质的量为4.8mol |
您最近一年使用:0次
2024-04-02更新
|
1129次组卷
|
4卷引用:天津市第二十中学2023-2024学年高一下学期学情调研(二)(期中)化学试卷
名校
2 . 三氯化铬(CrCl3)为紫色晶体,熔点为83 ℃,易潮解,易升华,能溶于水但不易水解,高温下能被氧气氧化。其工业生产中应用广泛。
以Cr2O3、CCl4(沸点为76.8 ℃)为原料制备无水CrCl3的实验装置图如下所示。
(2)装置A中产生N2的作用为___________ 。
A.排尽装置中的空气 B.平衡气压 C.吹出CCl4 和CrCl3
(3)装置C和装置E水槽中盛有的液体分别为___________ 、___________ 。
A.沸水 B.冰水
(4)装置D中另一产物为光气(COCl2),D中反应的化学方程式为___________ 。
(5)三氯化铬属于___________ 。
A.分子晶体 B.离子晶体 C.共价晶体 D.金属晶体
实验中发现D、E之间的导管容易堵塞,原因是___________ 。
(6)为进一步探究CrCl3的性质,某同学取若干支试管,分别加入10滴0.1 mol·L-1 CrCl3溶液,再分别加入不同滴数的0.1 mol·L-1 KMnO4酸性溶液,并在不同的温度下进行实验,反应现象记录于表中。
通过对表中数据进行分析,在上述反应条件下,欲将Cr3+ 氧化为橙黄色的Cr2O ,CrCl3与KMnO4最佳用量比为
,CrCl3与KMnO4最佳用量比为___________ 。已知: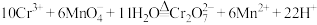 ,实验用量比理论用量更多,原因是
,实验用量比理论用量更多,原因是___________ 。
(7)Cr(Ⅲ)的存在形态的物质的量分数随溶液pH的分布如图所示,请补充完整由CrCl3溶液制备纯净的Cr(OH)3的实验方案。___________ 。
A.4~6 B.6 C.6~12 D.12
步骤二:充分反应后过滤、洗涤,检验沉淀已洗净的操作是___________ 。
步骤三:低温烘干沉淀,得到Cr(OH)3晶体。
以Cr2O3、CCl4(沸点为76.8 ℃)为原料制备无水CrCl3的实验装置图如下所示。
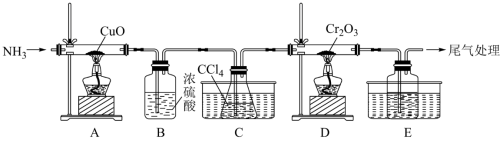
| A.加热氯化铵固体制备氨气 | B.使用无水氯化钙干燥氨气 |
| C.用排水法收集氨气 | D.用湿润的红色石蕊试纸检验氨气 |
A.排尽装置中的空气 B.平衡气压 C.吹出CCl4 和CrCl3
(3)装置C和装置E水槽中盛有的液体分别为
A.沸水 B.冰水
(4)装置D中另一产物为光气(COCl2),D中反应的化学方程式为
(5)三氯化铬属于
A.分子晶体 B.离子晶体 C.共价晶体 D.金属晶体
实验中发现D、E之间的导管容易堵塞,原因是
(6)为进一步探究CrCl3的性质,某同学取若干支试管,分别加入10滴0.1 mol·L-1 CrCl3溶液,再分别加入不同滴数的0.1 mol·L-1 KMnO4酸性溶液,并在不同的温度下进行实验,反应现象记录于表中。
| KMnO4酸性溶液的用量(滴数) | 在不同温度下的反应现象 | |
| 25 ℃ | 90~100 ℃ | |
| 1 | 紫红色 | 蓝绿色溶液 |
| 3 | 紫红色 | 黄绿色溶液 |
| 10 | 紫红色 | 橙黄色溶液 |
| 11 | 紫红色 | 橙黄色溶液,有少量棕褐色沉淀 |
| 25 | 紫红色 | 紫红色溶液,有较多的棕褐色沉淀 |
 ,CrCl3与KMnO4最佳用量比为
,CrCl3与KMnO4最佳用量比为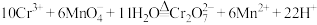 ,实验用量比理论用量更多,原因是
,实验用量比理论用量更多,原因是(7)Cr(Ⅲ)的存在形态的物质的量分数随溶液pH的分布如图所示,请补充完整由CrCl3溶液制备纯净的Cr(OH)3的实验方案。
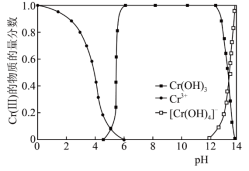
A.4~6 B.6 C.6~12 D.12
步骤二:充分反应后过滤、洗涤,检验沉淀已洗净的操作是
步骤三:低温烘干沉淀,得到Cr(OH)3晶体。
您最近一年使用:0次
2024-04-01更新
|
599次组卷
|
3卷引用:2024届天津市第四十七中学高三下学期模拟预测化学试题
3 .  是电解铝烟气的主要组分之一,属于强温室气体,其温室效应指数为
是电解铝烟气的主要组分之一,属于强温室气体,其温室效应指数为 的7390倍。我国科学家用
的7390倍。我国科学家用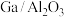 作为催化剂实现了
作为催化剂实现了 100%催化水解,其历程如下图所示。
100%催化水解,其历程如下图所示。
 是电解铝烟气的主要组分之一,属于强温室气体,其温室效应指数为
是电解铝烟气的主要组分之一,属于强温室气体,其温室效应指数为 的7390倍。我国科学家用
的7390倍。我国科学家用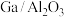 作为催化剂实现了
作为催化剂实现了 100%催化水解,其历程如下图所示。
100%催化水解,其历程如下图所示。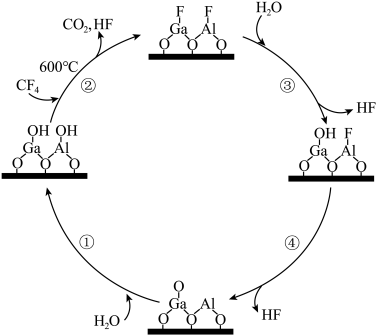
A.总反应为 |
B.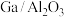 不能改变总反应的 不能改变总反应的 |
| C.反应过程中,Ga-F、C-F键既有断裂又有形成 |
| D.反应过程中涉及的小分子包含两种非极性分子 |
您最近一年使用:0次
2024-04-01更新
|
432次组卷
|
6卷引用:选择题7-12
(已下线)选择题7-12河南省周口市2024届高三二模理综-化学试题河南省2024届高三下学期第二次质量检测(二模)理综-化学试卷(已下线)提升练03 反应历程探究与催化原理-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)2024届河南省许昌市禹州市高级中学高三下学期第三次专题考试理综试题-高中化学安徽省六安第一中学2024届高三下学期质量检测(二 )化学试题
名校
解题方法
4 . 向碘水、淀粉的混合液中加入 溶液,蓝色褪去。为探究褪色原因,实验如图:
溶液,蓝色褪去。为探究褪色原因,实验如图:不正确 的是
 溶液,蓝色褪去。为探究褪色原因,实验如图:
溶液,蓝色褪去。为探究褪色原因,实验如图:
A.过程①中蓝色褪去的原因可能是 氧化了 氧化了 | B.过程①后溶液 可能明显变小 可能明显变小 |
C.过程③中加入 溶液的目的是除去 溶液的目的是除去 | D.过程④说明过程①生成含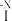 的粒子 的粒子 |
您最近一年使用:0次
5 . 实验室制取A并进一步制取无水FeCl3的实验装置如图所示。
已知:无水FeCl3在空气中易与水发生作用,加热易升华。
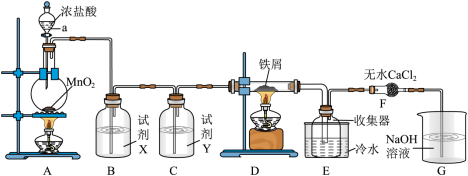
回答下列问题:
(1)仪器a的名称是_______ ,装置A所发生的氧化还原反应中,氧化剂与还原剂的物质的量之比为_______ 。
(2)试剂X是_______ 。
(3)装置F中无水CaCl2的作用是_______
(4)某温度下,将氯气通入G装置中,反应得到NaCl,NaClO和NaClO3的混合溶液,经测定ClO-与ClO 的物质的量之比为4∶1,写出该反应总的离子方程式:
的物质的量之比为4∶1,写出该反应总的离子方程式:_______ 。
已知:无水FeCl3在空气中易与水发生作用,加热易升华。

回答下列问题:
(1)仪器a的名称是
(2)试剂X是
(3)装置F中无水CaCl2的作用是
(4)某温度下,将氯气通入G装置中,反应得到NaCl,NaClO和NaClO3的混合溶液,经测定ClO-与ClO
 的物质的量之比为4∶1,写出该反应总的离子方程式:
的物质的量之比为4∶1,写出该反应总的离子方程式:
您最近一年使用:0次
解题方法
6 . 下列指定反应的离子方程式书写正确的是
A.将 溶液滴入 溶液滴入 溶液中: 溶液中: |
B. 溶液中通入过量的 溶液中通入过量的 : : |
C.用铜作电极电解饱和食盐水: |
D.碳酸氢铵溶液中加入足量石灰水: |
您最近一年使用:0次
7 .  和
和 在工农业。科研等方面应用广泛。按要求回答下列问题。
在工农业。科研等方面应用广泛。按要求回答下列问题。
(1)工业合成 时用到含铁催化剂。
时用到含铁催化剂。
①基态Fe原子的简化电子排布式为___________ 。
②我国科学家研发得Fe-LiH等双中心催化剂,在合成 中显示出高催化活性。Li、H元素的第一电离能(
中显示出高催化活性。Li、H元素的第一电离能( )较小的是
)较小的是___________ (填元素符号)。
(2) (氨硼烷)是具有广泛应用前景的储氢材料。
(氨硼烷)是具有广泛应用前景的储氢材料。
① 中存在配位键,提供空轨道的原子是
中存在配位键,提供空轨道的原子是___________ 。
② 的沸点高于
的沸点高于 的可能原因是
的可能原因是___________ 。
(3)在侯德榜制碱流程中两处用到 。
。
①其一先将 通入饱和食盐水,再通入
通入饱和食盐水,再通入 ,得到小苏打沉淀。写出该反应的离子方程式:
,得到小苏打沉淀。写出该反应的离子方程式:___________ 。
②其二为提高食盐利用率,向析出大量小苏打后的母液中加入NaCl细粉,通入 ,析出X晶体。
,析出X晶体。 参与此反应的离子方程式为
参与此反应的离子方程式为___________ ;X晶体中阳离子的空间结构为___________ 。
(4)Fe-Mg合金是储氢密度很高的材料之一,其晶胞结构如图所示。若该晶体储氢时,H₂分子在晶胞的体心和棱的中心位置。___________ 个。
②要储存1 kg ,至少需要
,至少需要___________ kg Fe-Mg合金。
 和
和 在工农业。科研等方面应用广泛。按要求回答下列问题。
在工农业。科研等方面应用广泛。按要求回答下列问题。(1)工业合成
 时用到含铁催化剂。
时用到含铁催化剂。①基态Fe原子的简化电子排布式为
②我国科学家研发得Fe-LiH等双中心催化剂,在合成
 中显示出高催化活性。Li、H元素的第一电离能(
中显示出高催化活性。Li、H元素的第一电离能( )较小的是
)较小的是(2)
 (氨硼烷)是具有广泛应用前景的储氢材料。
(氨硼烷)是具有广泛应用前景的储氢材料。①
 中存在配位键,提供空轨道的原子是
中存在配位键,提供空轨道的原子是②
 的沸点高于
的沸点高于 的可能原因是
的可能原因是(3)在侯德榜制碱流程中两处用到
 。
。①其一先将
 通入饱和食盐水,再通入
通入饱和食盐水,再通入 ,得到小苏打沉淀。写出该反应的离子方程式:
,得到小苏打沉淀。写出该反应的离子方程式:②其二为提高食盐利用率,向析出大量小苏打后的母液中加入NaCl细粉,通入
 ,析出X晶体。
,析出X晶体。 参与此反应的离子方程式为
参与此反应的离子方程式为(4)Fe-Mg合金是储氢密度很高的材料之一,其晶胞结构如图所示。若该晶体储氢时,H₂分子在晶胞的体心和棱的中心位置。
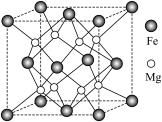
②要储存1 kg
 ,至少需要
,至少需要
您最近一年使用:0次
解题方法
8 . 锌在工业中有重要作用,也是人体必需的微量元素。回答下列问题:
(1)Zn原子核外电子排布式为___________ 。
(2)《中华本草》等中医典籍中,记载了炉甘石( )可入药。
)可入药。 中,阴离子空间构型为
中,阴离子空间构型为___________ ,C原子的杂化形式为___________ 。
(3) 具有较高的熔点(872℃),其化学键类型是
具有较高的熔点(872℃),其化学键类型是___________ ; 不溶于有机溶剂
不溶于有机溶剂 、
、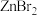 、
、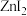 能够溶于乙醇、乙醚等有机溶剂,原因是
能够溶于乙醇、乙醚等有机溶剂,原因是___________ 。
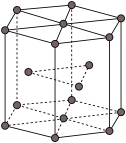
(4)金属Zn晶体中的原子堆积方式如图所示,六棱柱底边边长为a cm,高为c cm,阿伏加德罗常数的值为 ,Zn的密度为
,Zn的密度为___________  (列出计算式)。
(列出计算式)。
(5)铜转炉烟灰(主要成分为ZnO),加入氯化铵和氨水,浸出液中锌浸出液中锌以 形式存在,则浸取时反应的离子方程式为
形式存在,则浸取时反应的离子方程式为___________ 。氨分子的VSEPR模型为___________ 。
(6) 能活化ZnS,地表层原生铜的硫化物经氧化、淋滤作用后变成
能活化ZnS,地表层原生铜的硫化物经氧化、淋滤作用后变成 溶液,在地下深层遇到难溶的ZnS,慢慢转变为铜蓝(CuS),试推测其原因是
溶液,在地下深层遇到难溶的ZnS,慢慢转变为铜蓝(CuS),试推测其原因是___________ 。
(7)取m g活性氧化锌样品,预处理后配成待测液,加入指示剂3~4滴,再加入适量六亚甲基四胺,用a EDTA标准液进行滴定,消耗标准液V mL。若与1.0mL EDTA标准液[
EDTA标准液进行滴定,消耗标准液V mL。若与1.0mL EDTA标准液[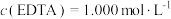 ]相当的以克表示的氧化锌质量为0.08139g,则样品中氧化锌的质量分数为
]相当的以克表示的氧化锌质量为0.08139g,则样品中氧化锌的质量分数为___________ (用代数式表示)。
(1)Zn原子核外电子排布式为
(2)《中华本草》等中医典籍中,记载了炉甘石(
 )可入药。
)可入药。 中,阴离子空间构型为
中,阴离子空间构型为(3)
 具有较高的熔点(872℃),其化学键类型是
具有较高的熔点(872℃),其化学键类型是 不溶于有机溶剂
不溶于有机溶剂 、
、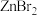 、
、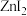 能够溶于乙醇、乙醚等有机溶剂,原因是
能够溶于乙醇、乙醚等有机溶剂,原因是(4)金属Zn晶体中的原子堆积方式如图所示,六棱柱底边边长为a cm,高为c cm,阿伏加德罗常数的值为
 ,Zn的密度为
,Zn的密度为 (列出计算式)。
(列出计算式)。
(5)铜转炉烟灰(主要成分为ZnO),加入氯化铵和氨水,浸出液中锌浸出液中锌以
 形式存在,则浸取时反应的离子方程式为
形式存在,则浸取时反应的离子方程式为(6)
 能活化ZnS,地表层原生铜的硫化物经氧化、淋滤作用后变成
能活化ZnS,地表层原生铜的硫化物经氧化、淋滤作用后变成 溶液,在地下深层遇到难溶的ZnS,慢慢转变为铜蓝(CuS),试推测其原因是
溶液,在地下深层遇到难溶的ZnS,慢慢转变为铜蓝(CuS),试推测其原因是(7)取m g活性氧化锌样品,预处理后配成待测液,加入指示剂3~4滴,再加入适量六亚甲基四胺,用a
 EDTA标准液进行滴定,消耗标准液V mL。若与1.0mL EDTA标准液[
EDTA标准液进行滴定,消耗标准液V mL。若与1.0mL EDTA标准液[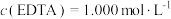 ]相当的以克表示的氧化锌质量为0.08139g,则样品中氧化锌的质量分数为
]相当的以克表示的氧化锌质量为0.08139g,则样品中氧化锌的质量分数为
您最近一年使用:0次
名校
9 . 高电压水系锌——有机混合液流电池的装置及其充放电原理示意图如下。
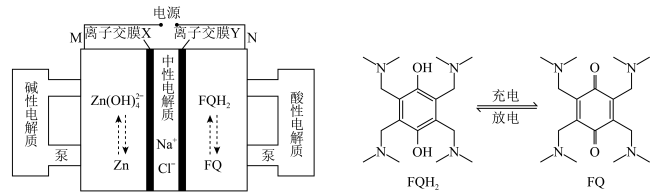
A.放电时,负极反应式: | B.放电时,1 mol FQ反应需转移4 mol  |
C.充电时, 可通过离子交换膜Y 可通过离子交换膜Y | D.充电时,M电极接电源负极 |
您最近一年使用:0次
2024-03-28更新
|
360次组卷
|
3卷引用:天津市河西区2023-2024学年高三下学期一模化学试题
解题方法
10 . 非天然氨基酸AHPA是一种重要的药物中间体,其合成路线之一如下: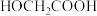 氧化得到,
氧化得到,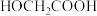 的化学名称是
的化学名称是_______ ;关于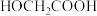 ,下列说法不正确的是
,下列说法不正确的是_______ 。
A.能发生取代反应 B.能发生消去反应 C.能与 反应 D.能进行缩取反应反应
反应 D.能进行缩取反应反应
(2)C的结构简式为_______ 。
(3)D中手性碳原子数目为_______ 。
(4)E转化为AHPA的反应类型为_______ 。
(5)AHPA中酸性官能团名称为_______ ,碱性官能团名称为_______ 。
(6)写出同时满足下列条件的AHPA的同分异构体的结构简式_______ 。
①含苯环且苯环只有一个取代基;
②红外光谱显示含氧官能团只有—OH和 ;
;
③核磁共振氢谱显示有6组峰,峰面积:4∶2∶2∶2∶2∶1。
(7)参照上述合成路线,补全下面的合成路线__________ (填写反应条件或结构简式)。
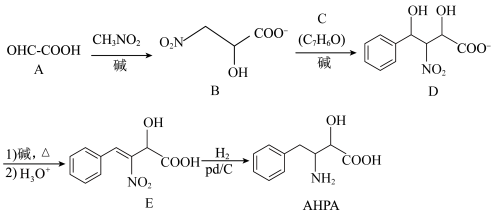
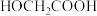 氧化得到,
氧化得到,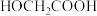 的化学名称是
的化学名称是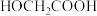 ,下列说法不正确的是
,下列说法不正确的是A.能发生取代反应 B.能发生消去反应 C.能与
 反应 D.能进行缩取反应反应
反应 D.能进行缩取反应反应(2)C的结构简式为
(3)D中手性碳原子数目为
(4)E转化为AHPA的反应类型为
(5)AHPA中酸性官能团名称为
(6)写出同时满足下列条件的AHPA的同分异构体的结构简式
①含苯环且苯环只有一个取代基;
②红外光谱显示含氧官能团只有—OH和
 ;
;③核磁共振氢谱显示有6组峰,峰面积:4∶2∶2∶2∶2∶1。
(7)参照上述合成路线,补全下面的合成路线

您最近一年使用:0次



