名校
1 . 化学小组探究Cu与Fe2(SO4)3溶液的反应,实验如下:
已知:经检验白色沉淀为CuSCN。
(1)实验i中发生反应的离子方程式为___________
(2)实验i中检测到Fe3+,依据的实验现象是___________
(3)对实验ii中Fe3+产生的原因作如下假设:
假设1:Cu与Fe2(SO4)3的反应是一个可逆反应
假设2:溶液中的Fe2+被___________ 氧化
假设3:在实验ii的条件下,Fe2+被Cu2+氧化
①将假设2补充完整
②通过查找___________ 数据,可定量判断Cu与Fe2(SO4)3的反应是否为可逆反应。
(4)设计实验验证假设。
资料:还原反应中,增大反应物浓度或降低生成物浓度,氧化剂氧化性增强,还原反应越易发生。
①假设1不成立的实验证据是___________
②实验iii的目的是___________
③溶液a是___________
④结合电极反应以及资料,解释实验ii中Fe3+产生的原因___________
| 序号 | 实验方案 | 实验现象 |
| 实验i |  | 振荡试管,观察到溶液变为蓝色,待反应充分后,试管底部有 Cu粉剩余。 |
| 实验ii | 取实验i中的上层清液,向其中滴加0.1mol·L-1 KSCN溶液 | 溶液局部变红,同时产生白色沉淀,振荡试管,红色消失。 |
(1)实验i中发生反应的离子方程式为
(2)实验i中检测到Fe3+,依据的实验现象是
(3)对实验ii中Fe3+产生的原因作如下假设:
假设1:Cu与Fe2(SO4)3的反应是一个可逆反应
假设2:溶液中的Fe2+被
假设3:在实验ii的条件下,Fe2+被Cu2+氧化
①将假设2补充完整
②通过查找
(4)设计实验验证假设。
资料:还原反应中,增大反应物浓度或降低生成物浓度,氧化剂氧化性增强,还原反应越易发生。
| 序号 | 实验iii | 实验iv |
| 方案 | 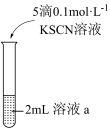 | 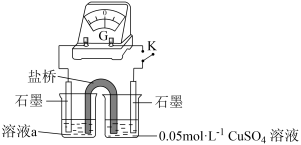 |
| 现象 | 放置较长时间,溶液颜色不变红 | 闭合开关K,电流计指针不动,向右侧CuSO4溶液中滴加0.1mol·L-1KSCN,指针向右大幅度偏转,溶液中有白色浑浊物产生。取出左侧溶液,滴加0.1mol·L-1KSCN,溶液变红。 |
②实验iii的目的是
③溶液a是
④结合电极反应以及资料,解释实验ii中Fe3+产生的原因
您最近一年使用:0次
名校
2 . 一定温度下,在三个1L的恒容密闭容器中分别进行反应:2X(g)+Y(g) Z(g),达到化学平衡状态时,相关数据如下表,下列说法不正确的是
Z(g),达到化学平衡状态时,相关数据如下表,下列说法不正确的是
 Z(g),达到化学平衡状态时,相关数据如下表,下列说法不正确的是
Z(g),达到化学平衡状态时,相关数据如下表,下列说法不正确的是| 实验 | 温度/K | 起始时各物质的浓度/(mol/L) | 平衡时浓度/(mol/L) | ||
| c(X) | c(Y) | c(Z) | c(Z) | ||
| I | 400 | 0.2 | 0.1 | 0 | 0.08 |
| Ⅱ | 400 | 0.4 | 0.2 | 0.2 | a |
| Ⅲ | 500 | 0.2 | 0.1 | 0 | 0.025 |
| A.达到化学平衡时,Ⅱ中X的转化率大于80% |
| B.化学平衡常数:K(Ⅱ)=K(Ⅰ) |
| C.达到化学平衡所需要的时间:IⅢ<I |
| D.按Ⅱ中的起始浓度进行实验,反应逆向进行 |
您最近一年使用:0次
名校
3 . 某实验小组同学依据资料深入探究Fe³+在水溶液中的行为。
资料:i.Fe³+在水溶液中以水合铁离子的形式存在,如[Fe(H2O)6]3+;[Fe(H2O)6] 3+发生如下水解反应:[Fe(H2O)6]3+(几乎无色)+nH2O [Fe(H2O)6-n(OH)n]3−n(黄色)+nH3O+(n=0~6)。
[Fe(H2O)6-n(OH)n]3−n(黄色)+nH3O+(n=0~6)。
ii.[FeCl4(H2O)2]-为黄色。
进行实验:【实验I】

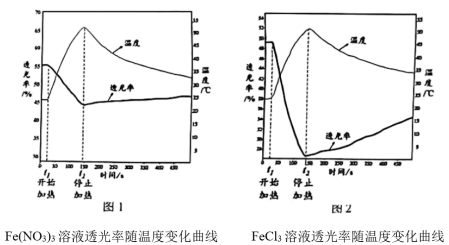
【实验Ⅱ】分别用试管①、③中的试剂作为待测液,用色度计测定其透光率。透光率越小,溶液颜色越深;透光率越大,溶液颜色越浅。
(1)实验1中,试管②溶液变为无色的原因是___________ 。
(2)实验I中,试管③溶液呈棕黄色与[FeCl4(H2O)2]-有关,支持此结论的实验现象是___________ 。
(3)由实验Ⅱ图1、2可知:加热时,溶液颜色___________ (填“变浅"、“变深”或“不变”)。
(4)由实验Ⅱ,可以得出如下结论:
[结论一]FeCl3溶液中存在可逆反应:[FeCl4(H2O)2]-+4H2O=[Fe(H2O)6]³++4Cl-得出此结论的理由是___________ 。
[结论二]结论一中反应的△H___________ (填“>0”或"<0")。
资料:i.Fe³+在水溶液中以水合铁离子的形式存在,如[Fe(H2O)6]3+;[Fe(H2O)6] 3+发生如下水解反应:[Fe(H2O)6]3+(几乎无色)+nH2O
 [Fe(H2O)6-n(OH)n]3−n(黄色)+nH3O+(n=0~6)。
[Fe(H2O)6-n(OH)n]3−n(黄色)+nH3O+(n=0~6)。ii.[FeCl4(H2O)2]-为黄色。
进行实验:【实验I】

【实验Ⅱ】分别用试管①、③中的试剂作为待测液,用色度计测定其透光率。透光率越小,溶液颜色越深;透光率越大,溶液颜色越浅。

(1)实验1中,试管②溶液变为无色的原因是
(2)实验I中,试管③溶液呈棕黄色与[FeCl4(H2O)2]-有关,支持此结论的实验现象是
(3)由实验Ⅱ图1、2可知:加热时,溶液颜色
(4)由实验Ⅱ,可以得出如下结论:
[结论一]FeCl3溶液中存在可逆反应:[FeCl4(H2O)2]-+4H2O=[Fe(H2O)6]³++4Cl-得出此结论的理由是
[结论二]结论一中反应的△H
您最近一年使用:0次
名校
4 . 卤代烃是重要的工业原料,同时对环境造成严重影响,如破坏臭氧层等,请回答下列问题:
I. 破坏臭氧层的机理为:
破坏臭氧层的机理为:
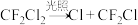
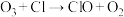

(1)活性氯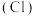 的作用是
的作用是___________ 。
(2)下列关于氟利昂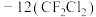 、氟利昂
、氟利昂 的推测错误的有
的推测错误的有___________ 。
A.两种氟利昂在 醇溶液中均可发生消去反应
醇溶液中均可发生消去反应
B.两种氟利昂均不存在同分异构体
C.直接用 溶液均可检验两种氟利昂中的氯元素
溶液均可检验两种氟利昂中的氯元素
II.Glaser反应是指端炔烃在催化剂存在下发生的偶联反应,例如: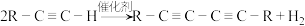 ,下面是以氯乙烷为原料利用Glaser反应制备化合物E的一种合成路线:
,下面是以氯乙烷为原料利用Glaser反应制备化合物E的一种合成路线:
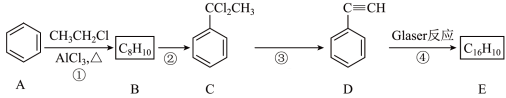
请回答下列问题:
(3)步骤①的反应类型为___________ ,步骤②的试剂和条件为___________ ,D的名称为___________ 。
(4)写出步骤③反应的化学方程式:___________ 。
(5)E的结构简式为___________ 。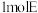 与
与 反应,理论上最多需要消耗
反应,理论上最多需要消耗
___________  。
。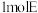 与溴水反应,理论上最多消耗
与溴水反应,理论上最多消耗
___________  。
。
(6)芳香族化合物F是C的同分异构体,其分子中只有两种氢原子,数目之比为 ,符合条件的F有5种,分别为
,符合条件的F有5种,分别为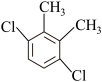
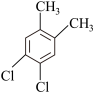
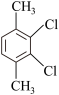
___________ 、___________ 。
(7)设计一条以环己醇(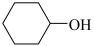 )为原料(其他无机试剂任取)合成
)为原料(其他无机试剂任取)合成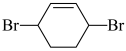 的合成路线
的合成路线_________ 。
(合成路线常用的表示方式为: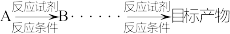 )
)
I.
 破坏臭氧层的机理为:
破坏臭氧层的机理为: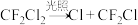
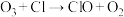

(1)活性氯
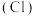 的作用是
的作用是(2)下列关于氟利昂
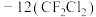 、氟利昂
、氟利昂 的推测错误的有
的推测错误的有A.两种氟利昂在
 醇溶液中均可发生消去反应
醇溶液中均可发生消去反应B.两种氟利昂均不存在同分异构体
C.直接用
 溶液均可检验两种氟利昂中的氯元素
溶液均可检验两种氟利昂中的氯元素II.Glaser反应是指端炔烃在催化剂存在下发生的偶联反应,例如:
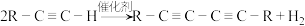 ,下面是以氯乙烷为原料利用Glaser反应制备化合物E的一种合成路线:
,下面是以氯乙烷为原料利用Glaser反应制备化合物E的一种合成路线:
请回答下列问题:
(3)步骤①的反应类型为
(4)写出步骤③反应的化学方程式:
(5)E的结构简式为
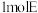 与
与 反应,理论上最多需要消耗
反应,理论上最多需要消耗
 。
。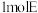 与溴水反应,理论上最多消耗
与溴水反应,理论上最多消耗
 。
。(6)芳香族化合物F是C的同分异构体,其分子中只有两种氢原子,数目之比为
 ,符合条件的F有5种,分别为
,符合条件的F有5种,分别为


(7)设计一条以环己醇(
 )为原料(其他无机试剂任取)合成
)为原料(其他无机试剂任取)合成 的合成路线
的合成路线(合成路线常用的表示方式为:
 )
)
您最近一年使用:0次
名校
5 . 有机玻璃(聚甲基丙烯酸甲酯,结构见流程)用途广泛。一种合成路线如下:
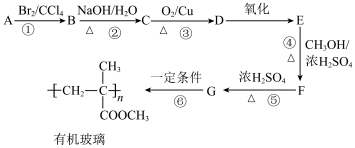
(1)已知原料A的分子式为C4H8,核磁共振氢谱中有两个吸收峰,并且面积比为1:3,则所属的物质类别为___________ 。
(2)写出流程中标有序号的六个反应中,属于取代反应的是___________ 。
(3)E中含有两种官能团,名称分别为___________ 。
(4)写出流程中反应的化学方程式②___________ ;③___________ 。
(5)G有多种同分异构体,写出期中一种链状的,含有-COOH且为顺式结构的同分异构体的结构简式___________ (写出一种即可)。

(1)已知原料A的分子式为C4H8,核磁共振氢谱中有两个吸收峰,并且面积比为1:3,则所属的物质类别为
(2)写出流程中标有序号的六个反应中,属于取代反应的是
(3)E中含有两种官能团,名称分别为
(4)写出流程中反应的化学方程式②
(5)G有多种同分异构体,写出期中一种链状的,含有-COOH且为顺式结构的同分异构体的结构简式
您最近一年使用:0次
名校
6 . 茶叶中含有丰富的有机物,通过不同提取方法可以获得不同的有机物成分。
I.从茶叶中提取咖啡因的主要流程如下:

资料:咖啡因能溶于乙醇等溶剂,120℃升华显著,熔点为238℃
(1)第①步使用乙醇提取咖啡因的原因是___________ 。
(2)步骤②使用的装置是___________ (填序号)。
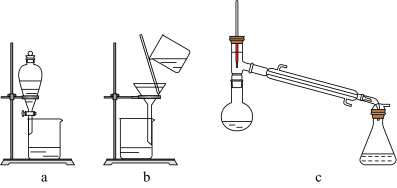
(3)上述步骤中主要利用化学变化进行物质分离的是___________ (填数字序号)。
(4)由液相色谱法从茶叶中可以分离得到B,为确定B的结构,进行如下实验:
综上所述,B的结构简式是___________ 。
I.从茶叶中提取咖啡因的主要流程如下:

资料:咖啡因能溶于乙醇等溶剂,120℃升华显著,熔点为238℃
(1)第①步使用乙醇提取咖啡因的原因是
(2)步骤②使用的装置是

(3)上述步骤中主要利用化学变化进行物质分离的是
(4)由液相色谱法从茶叶中可以分离得到B,为确定B的结构,进行如下实验:
| 实验步骤 | 解释或实验结论 |
| ①取适量B用质谱仪确定相对分子质量 | B的相对分子质量212 |
| ②将此2.12gB在足量纯O2中充分燃烧,使其产物依次缓缓通过浓硫酸,碱石灰,计算发现生成0.06mol H2O和0.10molCO2 | B的分子式为 |
| ③B能使FeCl3溶液变紫色,另取2.12gB与足量NaOH溶液反应,最多消耗0.04molNaOH,且产物之一是1-丙醇 | B中含有的官能团有: |
| ④B的核磁共振氢谱有6组信号峰且峰面积比为1:2:2:2:2:3,且环上有3个相同的取代基位于相邻位置。 | B中含 |
您最近一年使用:0次
名校
7 . I.某小组对Cu与浓HNO3的反应进行研究。记录如下:
(1)Cu与浓HNO3反应的化学方程式是___________ 。
II.探究实验1中溶液A呈绿色而不是蓝色的原因。
(2)甲认为溶液呈绿色是由Cu2+离子浓度较大引起的。乙根据实验记录,认为此观点不正确,乙的依据是___________ 。
(3)乙认为溶液呈绿色是由溶解的NO2引起的。
进行实验2:先将NO2通入B中,再鼓入N2,结果证实假设成立。
则以上两步操作对应的现象分别是___________ 、___________ 。
(4)为深入研究,丙查阅资料,有如下信息:
i.溶有NO2的浓HNO3呈黄色;水或稀HNO3中通少量NO2溶液呈无色。
ii.NO2溶于水,会发生反应2NO2+H2O= HNO3+HNO2;
HNO2是弱酸,只能稳定存在于冷、稀的溶液中,否则易分解。
iii. 能与Cu2+反应:Cu2+(蓝色)+4
能与Cu2+反应:Cu2+(蓝色)+4

 (绿色)
(绿色)
据此,丙进一步假设:
①可能是A中剩余的浓HNO3溶解了NO2得到的黄色溶液与Cu(NO3)2的蓝色溶液混合而形成的绿色;
②可能是A中生成了 使溶液呈绿色。
使溶液呈绿色。
丙进行如下实验:
①亚硝酸分解的化学方程式是___________ 。
②请用平衡原理解释加入H2SO4后绿色溶液变蓝的原因:___________ 。
(5)根据实验得出结论:实验1中溶液A呈绿色的主要原因是___________ 。请依据实验现象阐述理由:___________ 。
| 装置 | 药品 | 现象 | |
| 实验1 | 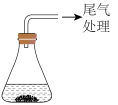 | 0.64gCu片(0.01mol) Cu片和20.0 mL浓HNO3 | Cu片消失,得到绿色溶液A,放置较长时间后得到蓝色溶 液B,…… |
(1)Cu与浓HNO3反应的化学方程式是
II.探究实验1中溶液A呈绿色而不是蓝色的原因。
(2)甲认为溶液呈绿色是由Cu2+离子浓度较大引起的。乙根据实验记录,认为此观点不正确,乙的依据是
(3)乙认为溶液呈绿色是由溶解的NO2引起的。
进行实验2:先将NO2通入B中,再鼓入N2,结果证实假设成立。
则以上两步操作对应的现象分别是
(4)为深入研究,丙查阅资料,有如下信息:
i.溶有NO2的浓HNO3呈黄色;水或稀HNO3中通少量NO2溶液呈无色。
ii.NO2溶于水,会发生反应2NO2+H2O= HNO3+HNO2;
HNO2是弱酸,只能稳定存在于冷、稀的溶液中,否则易分解。
iii.
 能与Cu2+反应:Cu2+(蓝色)+4
能与Cu2+反应:Cu2+(蓝色)+4

 (绿色)
(绿色)据此,丙进一步假设:
①可能是A中剩余的浓HNO3溶解了NO2得到的黄色溶液与Cu(NO3)2的蓝色溶液混合而形成的绿色;
②可能是A中生成了
 使溶液呈绿色。
使溶液呈绿色。丙进行如下实验:
| 操作 | 现象 | |
| 实验3 | i.配制与溶液A的c(H+)相同的HNO3溶液,取20.0mL,通入NO2气体 | 溶液呈黄色 |
| ii.再加0.01molCu(NO3)2固体搅拌至完全溶解 | 溶液变为绿色 | |
| iii.加水稀释 | 溶液立即变蓝 | |
| 实验4 | i.向20.0mL0.5mol/L Cu(NO3)2蓝色溶液中通入少量NO2 | 溶液呈绿色 |
| ii.加入稀H2SO4 | 有无色气体放出,遇空气变红棕色,溶液很快变为蓝色 |
②请用平衡原理解释加入H2SO4后绿色溶液变蓝的原因:
(5)根据实验得出结论:实验1中溶液A呈绿色的主要原因是
您最近一年使用:0次
名校
解题方法
8 . 回答下列问题:
(1)金属元素铁能形成多种配合物,如:[Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(III)]和Fe(CO)x等。
①基态氧原子的价电子排布式为___________ 。
②尿素(H2NCONH2)分子中C、N原子的杂化方式分别是___________ 、___________ 。
③配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=_____ 。Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于________ (填晶体类型)。
(2)O和Na形成的一种只含有离子键的离子化合物的晶胞结构如图,距一个阴离子周围最近的所有阳离子为顶点构成的几何体为___________ 。已知该晶胞的密度为 g/cm3,阿伏加德罗常数为NA,求晶胞边长a=
g/cm3,阿伏加德罗常数为NA,求晶胞边长a=___________ cm。(用含p、NA的计算式表示)___________ 。
a.第一电离能大小:S>P>Si
b.电负性顺序:C<N<O<F
c.因为晶格能CaO比KC1高,所以KCl比CaO熔点低
d.SO2与CO2的化学性质类似,分子结构也都呈直线形,相同条件下SO2的溶解度更大
(1)金属元素铁能形成多种配合物,如:[Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(III)]和Fe(CO)x等。
①基态氧原子的价电子排布式为
②尿素(H2NCONH2)分子中C、N原子的杂化方式分别是
③配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=
(2)O和Na形成的一种只含有离子键的离子化合物的晶胞结构如图,距一个阴离子周围最近的所有阳离子为顶点构成的几何体为
 g/cm3,阿伏加德罗常数为NA,求晶胞边长a=
g/cm3,阿伏加德罗常数为NA,求晶胞边长a=
a.第一电离能大小:S>P>Si
b.电负性顺序:C<N<O<F
c.因为晶格能CaO比KC1高,所以KCl比CaO熔点低
d.SO2与CO2的化学性质类似,分子结构也都呈直线形,相同条件下SO2的溶解度更大
您最近一年使用:0次
名校
解题方法
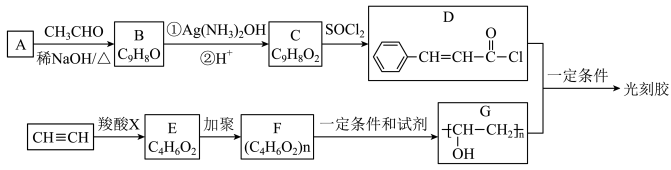
9 . 光刻胶是一种应用广泛的光敏材料,其合成路线如下(部分试剂和产物略去):_______ 。
(2)羧酸X的结构简式为_______ 。
(3)C物质可发生的反应类型为_______ (填字母序号)。
a.加聚反应 b.酯化反应 c.还原反应 d.缩聚反应
(4)B与Ag(NH3)2OH反应的化学方程式为_______ 。
(5)乙炔和羧酸X加成生成E,E的核磁共振氢谱为三组峰,且峰面积比为3:2:1,E能发生水解反应,则E的结构简式为_______ 。
(6)与C具有相同官能团且含有苯环的同分异构体有4种,其结构简式分别为_______ 、_______ 、_______ 和 _______ 。
(7)D和G反应生成光刻胶的化学方程为_______ 。
Ⅰ.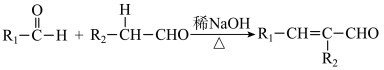 (R,R′为烃基或氢)
(R,R′为烃基或氢)
Ⅱ. (R,R′为烃基)
(R,R′为烃基)
(2)羧酸X的结构简式为
(3)C物质可发生的反应类型为
a.加聚反应 b.酯化反应 c.还原反应 d.缩聚反应
(4)B与Ag(NH3)2OH反应的化学方程式为
(5)乙炔和羧酸X加成生成E,E的核磁共振氢谱为三组峰,且峰面积比为3:2:1,E能发生水解反应,则E的结构简式为
(6)与C具有相同官能团且含有苯环的同分异构体有4种,其结构简式分别为
(7)D和G反应生成光刻胶的化学方程为
您最近一年使用:0次
名校
解题方法
10 . 实验小组制备硫代硫酸钠(Na2S2O3)并探究其性质。
资料:ⅰ.S2O +2H+=S↓+SO2↑+H2O
+2H+=S↓+SO2↑+H2O
ⅱ.Fe3++3S2O
 Fe(S2O3)
Fe(S2O3) (紫黑色)
(紫黑色)
ⅲ.Ag2S2O3是难溶于水、可溶于Na2S2O3溶液的白色固体。
(1)实验室可利用反应:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2制备Na2S2O3,装置如下图。

①用化学用语解释Na2S和Na2CO3的混合溶液呈碱性的原因:S2-+H2O HS-+OH-、
HS-+OH-、___________ 。
②为了保证Na2S2O3的产量,实验中通入的SO2不能过量。要控制SO2的生成速率,可以采取的措施有:___________ (写出一条)。
(2)探究Na2S2O3溶液与不同金属的硫酸盐溶液间反应的多样性。
①Ⅰ中产生白色沉淀的离子方程式为___________ 。
②经检验,现象Ⅱ中的沉淀有Al(OH)3和S,用平衡移动原理解释Ⅱ中的现象:___________ 。
③经检验,现象中的无色溶液中含有Fe2+。从化学反应速率和限度的角度解释Ⅲ中Fe3+与S2O 反应的实验现象:
反应的实验现象:___________ 。
以上实验说明:Na2S2O3溶液与金属阳离子反应的多样性和阳离子的性质有关。
资料:ⅰ.S2O
 +2H+=S↓+SO2↑+H2O
+2H+=S↓+SO2↑+H2O ⅱ.Fe3++3S2O

 Fe(S2O3)
Fe(S2O3) (紫黑色)
(紫黑色)ⅲ.Ag2S2O3是难溶于水、可溶于Na2S2O3溶液的白色固体。
(1)实验室可利用反应:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2制备Na2S2O3,装置如下图。

①用化学用语解释Na2S和Na2CO3的混合溶液呈碱性的原因:S2-+H2O
 HS-+OH-、
HS-+OH-、②为了保证Na2S2O3的产量,实验中通入的SO2不能过量。要控制SO2的生成速率,可以采取的措施有:
(2)探究Na2S2O3溶液与不同金属的硫酸盐溶液间反应的多样性。
| 实验 | 试剂 | 现象 | |
 | 试管 | 滴管 | |
| 2mL0.1mol/LNa2S2O3溶液 | Ag2SO4溶液(浓度约为0.03mol/L) | Ⅰ.局部生成白色沉淀,振荡后沉淀溶解,得到无色溶液 | |
| 0.03mol/LAl2(SO4)3溶液 | Ⅱ.一段时间后,生成沉淀 | ||
| 0.03mol/LFe2(SO4)3溶液 | Ⅲ.混合后溶液先变成紫黑色,30s时溶液几乎变为无色 | ||
②经检验,现象Ⅱ中的沉淀有Al(OH)3和S,用平衡移动原理解释Ⅱ中的现象:
③经检验,现象中的无色溶液中含有Fe2+。从化学反应速率和限度的角度解释Ⅲ中Fe3+与S2O
 反应的实验现象:
反应的实验现象:以上实验说明:Na2S2O3溶液与金属阳离子反应的多样性和阳离子的性质有关。
您最近一年使用:0次
2023-12-27更新
|
52次组卷
|
2卷引用:北京市第八中学2022-2023学年高二上学期期中考试化学试题



