真题
解题方法
1 . 液态氟化氢(HF)的电离方式为: ,其中X为
,其中X为_______ 。 的结构为
的结构为 ,其中
,其中 与HF依靠
与HF依靠_______ 相连接。
 ,其中X为
,其中X为 的结构为
的结构为 ,其中
,其中 与HF依靠
与HF依靠
您最近一年使用:0次
名校
解题方法
2 . 归纳、演绎和模型等是化学学习的重要方法,回答下列问题。
元素的“价-类”二维图是学习元素及其化合物的重要工具。下图是部分硫及其化合物的“价-类”二维图。
(1)Y的化学式为__________ 。
(2)根据“价-类”二维图预测,下列能与 反应且
反应且 表现氧化性的物质是
表现氧化性的物质是__________ (填序号), 与其反应的化学方程式是
与其反应的化学方程式是__________ 。
a. b.酸性
b.酸性 溶液 c.
溶液 c. 溶液 d.
溶液 d. 溶液
溶液
(3)分析 的物质类别,写出它和少量NaOH溶液反应的离子方程式
的物质类别,写出它和少量NaOH溶液反应的离子方程式_______________ 。
(4)从 转化为X的化学方程式为
转化为X的化学方程式为________ ,由 制备X的过程中,一般用
制备X的过程中,一般用___________ 吸收 ,防止反应放出大量的热导致形成酸雾,降低吸收效率且腐蚀设备。
,防止反应放出大量的热导致形成酸雾,降低吸收效率且腐蚀设备。
元素的“价-类”二维图是学习元素及其化合物的重要工具。下图是部分硫及其化合物的“价-类”二维图。

(1)Y的化学式为
(2)根据“价-类”二维图预测,下列能与
 反应且
反应且 表现氧化性的物质是
表现氧化性的物质是 与其反应的化学方程式是
与其反应的化学方程式是a.
 b.酸性
b.酸性 溶液 c.
溶液 c. 溶液 d.
溶液 d. 溶液
溶液(3)分析
 的物质类别,写出它和少量NaOH溶液反应的离子方程式
的物质类别,写出它和少量NaOH溶液反应的离子方程式(4)从
 转化为X的化学方程式为
转化为X的化学方程式为 制备X的过程中,一般用
制备X的过程中,一般用 ,防止反应放出大量的热导致形成酸雾,降低吸收效率且腐蚀设备。
,防止反应放出大量的热导致形成酸雾,降低吸收效率且腐蚀设备。
您最近一年使用:0次
3 . 与氮元素同主族的磷元素化合物有如下反应,其中反应物有:PH3、H2SO4、KClO3;生成物有:K2SO4、H3PO4、H2O和一种未知物质X。
(1)已知KClO3在反应中得到电子,则该反应的还原剂是___________ ,被氧化的元素是___________ 。
(2)已知0.2mol KClO3在反应中得到1mol电子生成X,则X的化学式为___________ 。
(3)完成并配平上述反应的化学方程式,标出电子转移方向和数目。___________
___________PH3+___________H2SO4+___________KClO3=___________K2SO4+___________H3PO4+___________H2O+___________
(4)根据上述反应可推知___________。
(5)在该反应中转移电子2mol时,生成H3PO4___________ mol。
(1)已知KClO3在反应中得到电子,则该反应的还原剂是
(2)已知0.2mol KClO3在反应中得到1mol电子生成X,则X的化学式为
(3)完成并配平上述反应的化学方程式,标出电子转移方向和数目。
___________PH3+___________H2SO4+___________KClO3=___________K2SO4+___________H3PO4+___________H2O+___________
(4)根据上述反应可推知___________。
| A.氧化性:KClO3 > H3PO4 | B.氧化性:KClO3 > H2O |
| C.还原性:PH3 > X | D.还原性:PH3 > K2SO4 |
您最近一年使用:0次
名校
解题方法
4 . 平衡思想是化学研究的一个重要观念,在电解质溶液中存在电离平衡、水解平衡、溶解平衡等多种平衡。
I.25℃时,三种弱酸的电离平衡常数如下:
回答下列问题:
(1)碳酸二级电离平衡常数的表达式为Ka2=___________ 。
(2)下列四种离子结合质子能力由大到小的顺序是___________ 。
A.CO B.ClO- C.CH3COO- D.HCO
B.ClO- C.CH3COO- D.HCO
(3)下列反应不能发生的是___________。
Ⅱ.体积均为10mL、pH均为2的醋酸溶液与HX溶液分别加水稀释至1000mL,稀释过程中pH变化如下图所示。___________ mol·L-1。
(5)用同浓度的NaOH溶液分别中和上述两种酸溶液,恰好中和时消耗NaOH溶液的体积:醋酸___________HX。
I.25℃时,三种弱酸的电离平衡常数如下:
| 弱酸 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.8×10-5 | Ka1=4.2×10-7,Ka2=4.8×10-11 | 3.0×10-8 |
(1)碳酸二级电离平衡常数的表达式为Ka2=
(2)下列四种离子结合质子能力由大到小的顺序是
A.CO
 B.ClO- C.CH3COO- D.HCO
B.ClO- C.CH3COO- D.HCO
(3)下列反应不能发生的是___________。
A.CO +2CH3COOH=2CH3COO-+CO2↑+H2O +2CH3COOH=2CH3COO-+CO2↑+H2O |
| B.ClO-+CH3COOH=CH3COO-+HClO |
C.CO +2HClO=CO2↑+H2O+2ClO- +2HClO=CO2↑+H2O+2ClO- |
D.2ClO-+CO2+H2O=CO +2HClO +2HClO |
Ⅱ.体积均为10mL、pH均为2的醋酸溶液与HX溶液分别加水稀释至1000mL,稀释过程中pH变化如下图所示。
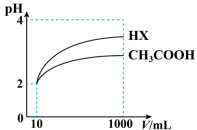
(5)用同浓度的NaOH溶液分别中和上述两种酸溶液,恰好中和时消耗NaOH溶液的体积:醋酸___________HX。
| A.大于 | B.等于 | C.小于 | D.无法比较 |
您最近一年使用:0次
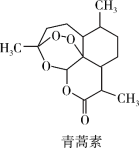
5 . 青蒿素是我国科学家从传统中药中发现的能治疗疟疾的有机化合物,可从黄花蒿茎叶中提取,它是无色针状晶体,其分子结构如图所示。___________ 。
②操作Ⅱ、Ⅲ的分离提纯方法名称分别是___________ 、___________ 。
(2)某同学发现青蒿素可以使湿润的淀粉碘化钾试纸变蓝,依据此现象在其键线式上圈出对应的基团_________ 。
(3)科学家在青蒿素的研究中发现,一定条件下可把青蒿素转化为双氢青蒿素。___________ (填字母)。
a.青蒿素分子式为C14H20O5
b.青蒿素含有酯基和醚键
c.青蒿素分子不存在手性异构体
d.青蒿素转化为双氢青蒿素时断裂π键
②因为双氢青蒿素的水溶性更好,所与青蒿素相比,双氢青蒿素具有更好的疗效,请从结构的角度推测主要原因___________ 。
(4)已知有机溶剂A只含C、H、O三种元素,使用现代分析仪器对A的分子结构进行测定,相关结果如下:___________ 仪器可测得A的相对分子质量,其数值为74。
②如图2所示,通过红外光谱法可推测A可能所属的有机化合物类别为___________ 。
③如图3所示,通过核磁共振氢谱法测得两个峰的面积比为2∶3,推测A的结构简式为___________ 。
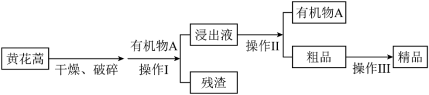
②操作Ⅱ、Ⅲ的分离提纯方法名称分别是
(2)某同学发现青蒿素可以使湿润的淀粉碘化钾试纸变蓝,依据此现象在其键线式上圈出对应的基团
(3)科学家在青蒿素的研究中发现,一定条件下可把青蒿素转化为双氢青蒿素。
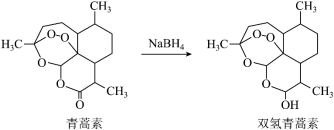
a.青蒿素分子式为C14H20O5
b.青蒿素含有酯基和醚键
c.青蒿素分子不存在手性异构体
d.青蒿素转化为双氢青蒿素时断裂π键
②因为双氢青蒿素的水溶性更好,所与青蒿素相比,双氢青蒿素具有更好的疗效,请从结构的角度推测主要原因
(4)已知有机溶剂A只含C、H、O三种元素,使用现代分析仪器对A的分子结构进行测定,相关结果如下:
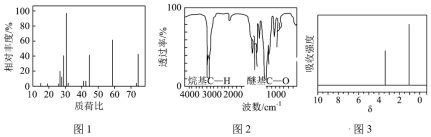

②如图2所示,通过红外光谱法可推测A可能所属的有机化合物类别为
③如图3所示,通过核磁共振氢谱法测得两个峰的面积比为2∶3,推测A的结构简式为
您最近一年使用:0次
名校
解题方法
6 . 高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。回答下列问题:
(1)SiO2属于___________ (填“酸性”“碱性”或“两性”)氧化物。盛装NaOH溶液的试剂瓶不能用玻璃塞,其原因为___________ (用离子方程式表示)。
(2)用氮化硅(Si3N4)陶瓷制造发动机,能大幅度提高发动机的热效率。工业上制备氮化硅的原理为:3SiCl4+2N2+6H2 Si3N4+12HCl。
Si3N4+12HCl。
①SiCl4是___________ (填“离子化合物”或“共价化合物”)。
②若该反应转移3mol电子,生成Si3N4的质量为___________ g。
(3)芯片制作中的部分流程如图:___________ 。
Na2SiO3可通过SiO2与纯碱混合高温熔融反应制得,高温熔融纯碱时下列坩埚可选用的是___________ 。
A.普通玻璃坩埚 B.石英玻璃坩埚 C.铁坩埚
②去除磷硅玻璃即除去扩散制结过程中产生的SiO2,下列试剂合适的为___________ (填标号),写出其化学方程式:___________ 。
a.浓硫酸 b.氢氟酸 c.稀硝酸
(1)SiO2属于
(2)用氮化硅(Si3N4)陶瓷制造发动机,能大幅度提高发动机的热效率。工业上制备氮化硅的原理为:3SiCl4+2N2+6H2
 Si3N4+12HCl。
Si3N4+12HCl。①SiCl4是
②若该反应转移3mol电子,生成Si3N4的质量为
(3)芯片制作中的部分流程如图:

Na2SiO3可通过SiO2与纯碱混合高温熔融反应制得,高温熔融纯碱时下列坩埚可选用的是
A.普通玻璃坩埚 B.石英玻璃坩埚 C.铁坩埚
②去除磷硅玻璃即除去扩散制结过程中产生的SiO2,下列试剂合适的为
a.浓硫酸 b.氢氟酸 c.稀硝酸
您最近一年使用:0次
名校
解题方法
7 . 如图所示,是原电池的装置图。请回答:___________ ;在反应中溶液中的阴离子移向___________ (填“A”或“B”),反应进行一段时间后溶液C中H+浓度___________ 。(填“增大”“减小”或“基本不变”)
(2)若需将反应Cu+2Fe3+=Cu2++2Fe2+设计成如图所示的原电池装置,则A极(负极)材料为___________ ,B极电极反应式为___________ 。
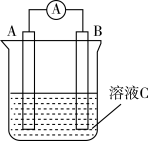
(2)若需将反应Cu+2Fe3+=Cu2++2Fe2+设计成如图所示的原电池装置,则A极(负极)材料为
您最近一年使用:0次
8 . 选择完成下列实验的装置。___________ (填序号,下同)。
(2)比较Na2CO3和NaHCO3的热稳定性,选用___________ 。
(3)加热MnO2和浓盐酸的混合物制Cl2,选用___________ 。
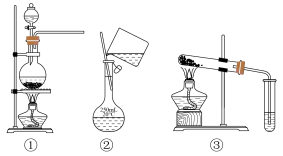
(2)比较Na2CO3和NaHCO3的热稳定性,选用
(3)加热MnO2和浓盐酸的混合物制Cl2,选用
您最近一年使用:0次
名校
9 . I.回答下列问题:
(1)对以下有机物进行系统命名: 的结构简式改写为键线式:
的结构简式改写为键线式:___________ 。
(3)上述(1)中分子②最多有___________ 个碳原子共平面。
(4)分子式为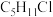 的同分异构体共有___________(不考虑立体异构)。
的同分异构体共有___________(不考虑立体异构)。
II.青蒿素是我国科学家从传统中药中发现的能治疗疟疾的有机化合物,其分子结构如图所示,它可以用有机溶剂A从中药中提取。
(5)下列关于青蒿素的说法不正确的是___________ (填字母)。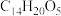
b.分子中含有酯基和醚键
c.易溶于有机溶剂A,不易溶于水
d.分子的空间结构不是平面形
(6)使用现代分析仪器对有机化合物A的分子结构进行测定,相关结果如下:___________ 。
②根据图2,推测A可能所属的有机化合物类别:___________ ,A的分子式:___________ 。
③根据以上结果和图3(两个峰的面积比为2:3),推测A的结构简式___________ 。
(1)对以下有机物进行系统命名:
①键线式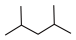 :
:
② :
:
 的结构简式改写为键线式:
的结构简式改写为键线式:(3)上述(1)中分子②最多有
(4)分子式为
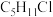 的同分异构体共有___________(不考虑立体异构)。
的同分异构体共有___________(不考虑立体异构)。| A.6种 | B.7种 | C.8种 | D.9种 |
II.青蒿素是我国科学家从传统中药中发现的能治疗疟疾的有机化合物,其分子结构如图所示,它可以用有机溶剂A从中药中提取。
(5)下列关于青蒿素的说法不正确的是

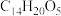
b.分子中含有酯基和醚键
c.易溶于有机溶剂A,不易溶于水
d.分子的空间结构不是平面形
(6)使用现代分析仪器对有机化合物A的分子结构进行测定,相关结果如下:
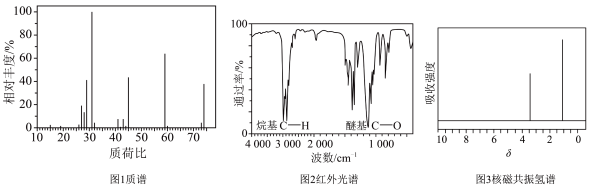
②根据图2,推测A可能所属的有机化合物类别:
③根据以上结果和图3(两个峰的面积比为2:3),推测A的结构简式
您最近一年使用:0次
名校
解题方法
10 . 化学电源是人类生产和生活的重要能量来源之一,回答下列问题。
(1)为了探究化学反应中的能量变化,某同学设计了如下两个实验。___________ (填序号)。
A.图1和图2的气泡均产生在锌棒表面
B.图1中温度计的示数高于图2的示数
C.图2中产生气体的速度比1快
D.图1和图2中温度计的示数相等,且均高于室温
②图②装置中,正极的电极反应方程式为___________ 。
(2)将反应2Fe3++Fe=3Fe2+设计成原电池装置,负极的电极反应方程式为___________ ,离子导体为___________ 。
(3)甲烷碱性燃料电池以KOH溶液为电解质溶液,电池反应为CH4+2O2+2OH- CO
CO +3H2O,该电池的负极电极反应方程式为
+3H2O,该电池的负极电极反应方程式为___________ ,K+向___________ 极(填正或负)移动,若电路中通过0.4mol电子,则理论上消耗甲烷的体积为(标况)___________ 。
(1)为了探究化学反应中的能量变化,某同学设计了如下两个实验。
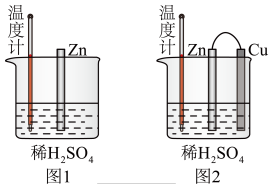
A.图1和图2的气泡均产生在锌棒表面
B.图1中温度计的示数高于图2的示数
C.图2中产生气体的速度比1快
D.图1和图2中温度计的示数相等,且均高于室温
②图②装置中,正极的电极反应方程式为
(2)将反应2Fe3++Fe=3Fe2+设计成原电池装置,负极的电极反应方程式为
(3)甲烷碱性燃料电池以KOH溶液为电解质溶液,电池反应为CH4+2O2+2OH-
 CO
CO +3H2O,该电池的负极电极反应方程式为
+3H2O,该电池的负极电极反应方程式为
您最近一年使用:0次



