解题方法
1 . 废旧铅蓄电池具有较高的回收利用价值。由废铅膏(含 、
、 、
、 和
和 以及少量的铁和铝的氧化物)制备
以及少量的铁和铝的氧化物)制备 的流程如下:
的流程如下: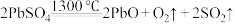 ;
;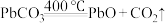
②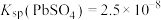 ,
,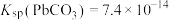
请回答下列问题:
(1)“浸取”时为增大浸取速率,可以采取的措施有___________ (请写一点)。
(2)“浸取”时 发生的主要反应的化学方程式为
发生的主要反应的化学方程式为___________ 。
(3)“浸取”时将 换成
换成 溶液效果会更好,
溶液效果会更好, 除作还原剂外,还有的作用为
除作还原剂外,还有的作用为___________ 。
(4)“脱硫”的目的是___________ 。
(5)“脱硫”时 转化反应的离子方程式为
转化反应的离子方程式为___________ ;用沉淀溶解平衡原理解释选择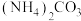 的原因
的原因___________ 。
(6)“焙烧”时会有中间产物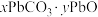 生成,固体残留率
生成,固体残留率 与温度的关系如图所示,则358℃时对应固体的成分为
与温度的关系如图所示,则358℃时对应固体的成分为___________ (填化学式)。
 、
、 、
、 和
和 以及少量的铁和铝的氧化物)制备
以及少量的铁和铝的氧化物)制备 的流程如下:
的流程如下: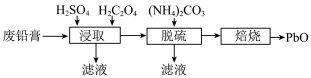
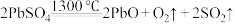 ;
;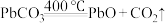
②
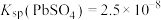 ,
,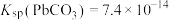
请回答下列问题:
(1)“浸取”时为增大浸取速率,可以采取的措施有
(2)“浸取”时
 发生的主要反应的化学方程式为
发生的主要反应的化学方程式为(3)“浸取”时将
 换成
换成 溶液效果会更好,
溶液效果会更好, 除作还原剂外,还有的作用为
除作还原剂外,还有的作用为(4)“脱硫”的目的是
(5)“脱硫”时
 转化反应的离子方程式为
转化反应的离子方程式为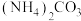 的原因
的原因(6)“焙烧”时会有中间产物
 生成,固体残留率
生成,固体残留率 与温度的关系如图所示,则358℃时对应固体的成分为
与温度的关系如图所示,则358℃时对应固体的成分为
您最近一年使用:0次
解题方法
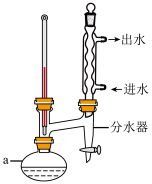
2 . 乙酸正丁酯是优良的有机溶剂,在石油加工、制药工程等领域均有广泛应用。某实验小组采用如图所示的实验装置制备乙酸正丁酯(加热及夹持装置略)。
具体步骤如下:
I.按如图所示装配仪器。
II.关闭分水器旋塞并在分水器带旋塞一侧预先加入适量的水,再向反应瓶中加入5.0mL(0.055mol)正丁醇、0.06mol冰醋酸和0.05mol浓疏酸,加入1粒沸石。
III.将反应液温度控制在80℃并保持15分钟,然后升温至回流状态进行分水。反应停止后,并仪器a和分水器中的液体,用分液漏斗将水层分出,得到乙酸正丁酯粗品。
IV.将乙酸正丁酯粗品纯化。
回答下列问题:
(1)仪器a的名称为___________ 。
(2)写出图中所示实验装置中的两处错误___________ 。
(3)若分水器带旋塞一侧加水不足,会导致的后果是___________ 。
(4)写出上述制备乙酸正丁酯的化学方程式___________ 。
(5)判断反应停止时的现象为___________ 。
(6)步骤IV包括以下操作,正确的操作顺序为___________ (填标号)。
a.无水硫酸镁干燥 b.饱和 溶液洗涤
溶液洗涤
c.常压蒸馏,收集124℃~126℃的馏分 d.水洗
(7)乙酸和甲酸都属于常见的有机酸,从结构的角度比较并解释二者酸性强弱的关系:_____ 。
| 化合物 | 乙酸 | 正丁醇 | 乙酸正丁酯 |
| 沸点/℃ | 117.9 | 117.3 | 126.6 |
| 共沸物 | 正丁醇—水 | 乙酸正丁酯—水 | 乙酸正丁酯—正丁醇—水 |
| 沸点/℃ | 92.7 | 90.7 | 90.7 |
I.按如图所示装配仪器。
II.关闭分水器旋塞并在分水器带旋塞一侧预先加入适量的水,再向反应瓶中加入5.0mL(0.055mol)正丁醇、0.06mol冰醋酸和0.05mol浓疏酸,加入1粒沸石。
III.将反应液温度控制在80℃并保持15分钟,然后升温至回流状态进行分水。反应停止后,并仪器a和分水器中的液体,用分液漏斗将水层分出,得到乙酸正丁酯粗品。
IV.将乙酸正丁酯粗品纯化。
回答下列问题:
(1)仪器a的名称为
(2)写出图中所示实验装置中的两处错误
(3)若分水器带旋塞一侧加水不足,会导致的后果是
(4)写出上述制备乙酸正丁酯的化学方程式
(5)判断反应停止时的现象为
(6)步骤IV包括以下操作,正确的操作顺序为
a.无水硫酸镁干燥 b.饱和
 溶液洗涤
溶液洗涤c.常压蒸馏,收集124℃~126℃的馏分 d.水洗
(7)乙酸和甲酸都属于常见的有机酸,从结构的角度比较并解释二者酸性强弱的关系:
您最近一年使用:0次
解题方法
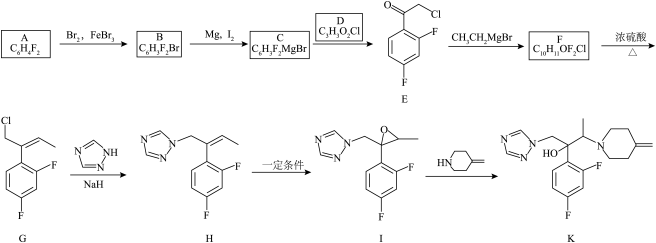
3 . 艾氟康唑(化合物K)是一种抗真菌药物,其合成路线如下。
(1)A→B的化学方程式为___________ 。
(2)D的名称为___________ 。
(3)E→F实现了___________ 到___________ 的转化(填官能团的名称)。
(4)F→G的反应类型为___________ ;该反应中另一种与G互为同分异构体的副产物的结构简式为___________ 。
(5)F的同分异构体能同时满足以下三个条件的有___________ 种(不考虑立体异构)。
①苯环上含有两个取代基
②与FeCl3溶液显紫色
③分子中含-CF2Cl
写出一种核磁共振氢谱有4组峰,且峰面积比为1:2:2:6的结构简式:___________ 。
已知:i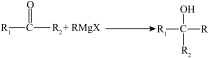
ii.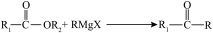
(1)A→B的化学方程式为
(2)D的名称为
(3)E→F实现了
(4)F→G的反应类型为
(5)F的同分异构体能同时满足以下三个条件的有
①苯环上含有两个取代基
②与FeCl3溶液显紫色
③分子中含-CF2Cl
写出一种核磁共振氢谱有4组峰,且峰面积比为1:2:2:6的结构简式:
您最近一年使用:0次
名校
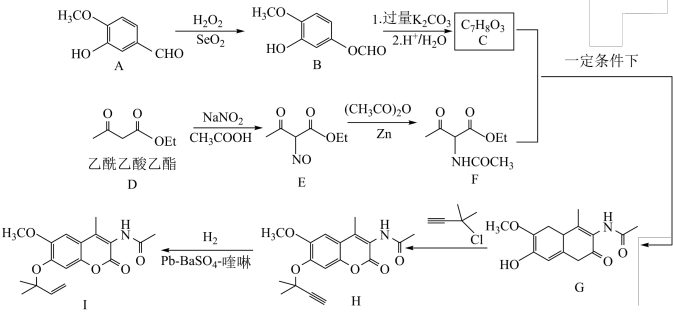
4 . 香豆素类化合物是一类有机杂环化合物,一种香豆素衍生物的合成路线如下。
(1)G中除羟基和醚键外的含氧官能团为________ 。
(2)A→B的反应类型为________ 。
(3)B-C第一步的化学反应方程式为________ 。
(4)H-1的反应中加入 的作用是
的作用是________ 。
(5)F的同分异构体中,满足下列要求的有________ 种。
①含有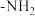 ;
;
②结构中含有六元环;
③1mol F与足量 反应,消耗2mol
反应,消耗2mol  。
。
其中核磁共振氢谱有6组峰,峰面积之比为4:2:2:2:2:1的结构简式为________ 。(写一种即可)
(6)以对甲基苯酚和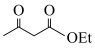 为原料,设计
为原料,设计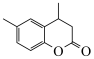 的合成路线
的合成路线_____ 。(其他无机试剂任选)
②
(1)G中除羟基和醚键外的含氧官能团为
(2)A→B的反应类型为
(3)B-C第一步的化学反应方程式为
(4)H-1的反应中加入
 的作用是
的作用是(5)F的同分异构体中,满足下列要求的有
①含有
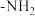 ;
;②结构中含有六元环;
③1mol F与足量
 反应,消耗2mol
反应,消耗2mol  。
。其中核磁共振氢谱有6组峰,峰面积之比为4:2:2:2:2:1的结构简式为
(6)以对甲基苯酚和
 为原料,设计
为原料,设计 的合成路线
的合成路线
您最近一年使用:0次
2024-05-30更新
|
272次组卷
|
3卷引用:湖北省黄冈中学2024届高三下学期5月第三次模拟考试化学试题
名校
5 . 某研究小组试探究1,6-己二硫醇(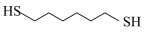 ,用HDT表示)与铜的反应历程。
,用HDT表示)与铜的反应历程。
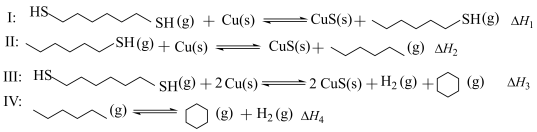
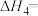
化学键 | C-H | C-C | H-H |
键能/ | 413 | 347 | 436 |
(2)温度一定时,在隔绝空气的条件下使HDT(g)以恒定的流速通过如甲图所示的反应器,仅发生反应Ⅰ、Ⅱ、Ⅲ,在反应器出口处实时检测各物质的相对含量如图乙所示。
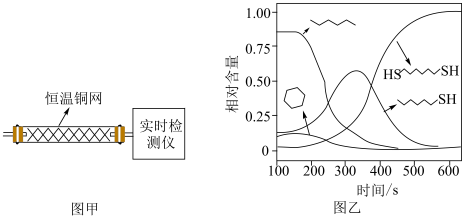
②推测
 在该实验条件下与Cu反应生成烃类产物的名称为
在该实验条件下与Cu反应生成烃类产物的名称为(3)向恒温刚性容器M中充入己烷(g)和HDT(g),初始总压为2.5Pa,己烷的体积分数为80%。容器M中只发生反应Ⅳ,达平衡时,己烷的转化率为50%,则反应Ⅳ的

(
 )
)
您最近一年使用:0次
2024-05-30更新
|
104次组卷
|
2卷引用:湖北省黄冈中学2024届高三下学期5月第三次模拟考试化学试题
6 . 三氯甲苯(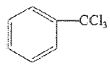 )可用于制取农药、染料等有机物,可利用甲苯的取代反应进行制备。
)可用于制取农药、染料等有机物,可利用甲苯的取代反应进行制备。
物质 | 熔点/℃ | 沸点/℃ | 密度/g· | 摩尔质量/g· |
甲苯 | -94.9 | 110.6 | 0.87 | 92 |
三氯甲苯 | -7.5 | 219.0 | 1.36 | 195.5 |
如图组装实验仪器,检验装置气密性后将138.0mL甲苯加入N中,__________,加热至100~110℃后通氯气反应1h。

(1)仪器N的名称是
(2)将甲苯加入三颈烧瓶后的操作是
(3)实验时,
(4)该实验采用
(5)反应结束后,混合溶液用
①蒸馏水 ②饱和
 溶液 ③饱和
溶液 ③饱和 溶液
溶液(6)粗产品经蒸馏后得138.0g三氯甲苯。该反应的产率最接近于
A.30% B.50% C.70%
您最近一年使用:0次
2024-05-30更新
|
254次组卷
|
3卷引用:湖北省黄冈中学2024届高三下学期5月第三次模拟考试化学试题
名校
7 . 氧化镓(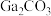 )是一种常用的无机催化剂.某兴趣小组设计以砷化镓废料(主要成分为GaAs、
)是一种常用的无机催化剂.某兴趣小组设计以砷化镓废料(主要成分为GaAs、 、
、 )为原料生产
)为原料生产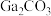 的工业流程如图所示:
的工业流程如图所示:
ⅱ. 对硝酸参与的氧化还原反应有催化作用。
对硝酸参与的氧化还原反应有催化作用。
回答下列问题:
(1)Ga元素的价电子排布式为_______ 。
(2)滤渣1的主要成分为_______ 。
(3)①“浸取”时GaAs发生反应的化学方程式_______ 。
②若取A、B两组样品分别进行“浸取”实验,向A中不断通入 ,其他条件、操作完全一样,得到镓元素的浸出率随时间变化情况如图所示:
,其他条件、操作完全一样,得到镓元素的浸出率随时间变化情况如图所示:___________ B(填>、=或<),其可能原因是___________ 。
(4)“沉镓”时的离子方程式为___________ ,需要控制硝酸用量的原因___________ 。
(5)查阅资料后发现,实际工业生产中,在“浸取”步骤除了加硝酸外,还需要加入 ,从绿色化学角度分析加入
,从绿色化学角度分析加入 的优点
的优点___________ 。
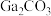 )是一种常用的无机催化剂.某兴趣小组设计以砷化镓废料(主要成分为GaAs、
)是一种常用的无机催化剂.某兴趣小组设计以砷化镓废料(主要成分为GaAs、 、
、 )为原料生产
)为原料生产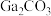 的工业流程如图所示:
的工业流程如图所示: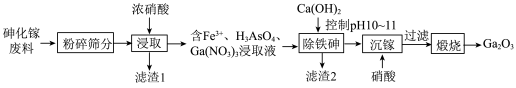
ⅱ.
 对硝酸参与的氧化还原反应有催化作用。
对硝酸参与的氧化还原反应有催化作用。回答下列问题:
(1)Ga元素的价电子排布式为
(2)滤渣1的主要成分为
(3)①“浸取”时GaAs发生反应的化学方程式
②若取A、B两组样品分别进行“浸取”实验,向A中不断通入
 ,其他条件、操作完全一样,得到镓元素的浸出率随时间变化情况如图所示:
,其他条件、操作完全一样,得到镓元素的浸出率随时间变化情况如图所示: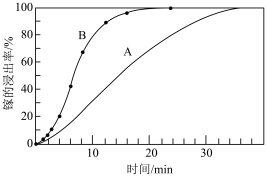
(4)“沉镓”时的离子方程式为
(5)查阅资料后发现,实际工业生产中,在“浸取”步骤除了加硝酸外,还需要加入
 ,从绿色化学角度分析加入
,从绿色化学角度分析加入 的优点
的优点
您最近一年使用:0次
2024-05-30更新
|
174次组卷
|
3卷引用:湖北省黄冈中学2024届高三下学期5月第三次模拟考试化学试题
解题方法
8 .  用途广泛。某实验小组同学围绕
用途广泛。某实验小组同学围绕 开展如下实验活动。
开展如下实验活动。
 .配制溶液
.配制溶液
(1)配制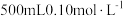 的
的 溶液,需要称量
溶液,需要称量 固体的质量为
固体的质量为___________  。
。
(2)上述配制溶液的过程中,用到的玻璃仪器除玻璃棒、量筒、胶头滴管外,还有___________ (填标号)。 .实验探究
.实验探究
探究温度对 溶液
溶液 的影响,进行如下实验(不考虑水的挥发)。
的影响,进行如下实验(不考虑水的挥发)。
(3) 溶液显碱性的原因是
溶液显碱性的原因是___________ (用离子方程式表示)。
(4)实验1中测得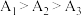 ,可知当
,可知当 时,
时, 溶液的
溶液的 随温度升高而减小,这主要是
随温度升高而减小,这主要是 改变与水解平衡移动共同作用的结果,其中
改变与水解平衡移动共同作用的结果,其中___________ 发挥主导作用。实验1中测得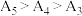 ,且当
,且当 时,实验过程中观察到有气泡产生。
时,实验过程中观察到有气泡产生。
(5)针对(4)中实验现象,小组同学继续开展探究。
查阅资料: 溶液中存在平衡:
溶液中存在平衡: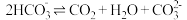 。
。
提出猜想:对于 溶液,当
溶液,当 时,该反应进行程度很小;当
时,该反应进行程度很小;当 时,该反应进行程度明显增大。
时,该反应进行程度明显增大。
实验验证:该小组同学设计如下方案进行实验,进一步验证猜想。补充表格内容。
实验结论:②根据实验1~3的结果,小组同学认为猜想成立,其判断依据是___________ 。
拓展总结:③ 溶液中存在
溶液中存在 的自偶电离平衡:
的自偶电离平衡: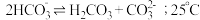 时,
时, 自偶电离的平衡常数为
自偶电离的平衡常数为___________ [保留两位有效数字;已知: 时,
时,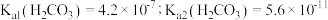 ]。当温度升高时,
]。当温度升高时, 更易分解,
更易分解, 从体系逸出,促进了
从体系逸出,促进了 在溶液中的分解。
在溶液中的分解。
(6)写出 在生产或生活中的一种应用
在生产或生活中的一种应用___________ 。
 用途广泛。某实验小组同学围绕
用途广泛。某实验小组同学围绕 开展如下实验活动。
开展如下实验活动。 .配制溶液
.配制溶液(1)配制
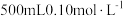 的
的 溶液,需要称量
溶液,需要称量 固体的质量为
固体的质量为 。
。(2)上述配制溶液的过程中,用到的玻璃仪器除玻璃棒、量筒、胶头滴管外,还有
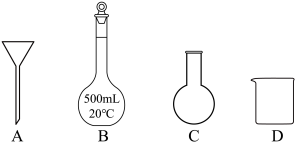
 .实验探究
.实验探究探究温度对
 溶液
溶液 的影响,进行如下实验(不考虑水的挥发)。
的影响,进行如下实验(不考虑水的挥发)。| 实验序号 | 操作 | 测试温度 |  |
| 1 | 采用水浴加热,将 溶液从 溶液从 持续升温至 持续升温至 ,每隔 ,每隔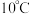 测量并记录溶液 测量并记录溶液 |  |  |
 |  | ||
 |  | ||
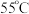 |  | ||
 | 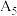 |
(3)
 溶液显碱性的原因是
溶液显碱性的原因是(4)实验1中测得
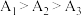 ,可知当
,可知当 时,
时, 溶液的
溶液的 随温度升高而减小,这主要是
随温度升高而减小,这主要是 改变与水解平衡移动共同作用的结果,其中
改变与水解平衡移动共同作用的结果,其中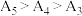 ,且当
,且当 时,实验过程中观察到有气泡产生。
时,实验过程中观察到有气泡产生。(5)针对(4)中实验现象,小组同学继续开展探究。
查阅资料:
 溶液中存在平衡:
溶液中存在平衡: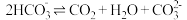 。
。提出猜想:对于
 溶液,当
溶液,当 时,该反应进行程度很小;当
时,该反应进行程度很小;当 时,该反应进行程度明显增大。
时,该反应进行程度明显增大。实验验证:该小组同学设计如下方案进行实验,进一步验证猜想。补充表格内容。
| 实验序号 | 操作 | 测试温度 |  |
| 2 | 采用水浴加热,① ,并记录溶液 ,并记录溶液 |  |  |
| 3 | 采用水浴加热,将 溶液从 溶液从 升温至 升温至 ,然后冷却至 ,然后冷却至 ,并记录溶液 ,并记录溶液 |  |  |
拓展总结:③
 溶液中存在
溶液中存在 的自偶电离平衡:
的自偶电离平衡: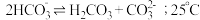 时,
时, 自偶电离的平衡常数为
自偶电离的平衡常数为 时,
时,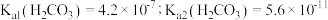 ]。当温度升高时,
]。当温度升高时, 更易分解,
更易分解, 从体系逸出,促进了
从体系逸出,促进了 在溶液中的分解。
在溶液中的分解。(6)写出
 在生产或生活中的一种应用
在生产或生活中的一种应用
您最近一年使用:0次
2024-05-29更新
|
687次组卷
|
2卷引用:2024届湖北省武汉市黄陂区第七高级中学高三下学期二模化学试题
解题方法
9 . 硫脲 为白色晶体,可溶于水,易溶于乙酸乙酯,可代替氰化物用于提炼金。合成硫脲的原理为
为白色晶体,可溶于水,易溶于乙酸乙酯,可代替氰化物用于提炼金。合成硫脲的原理为 。
。
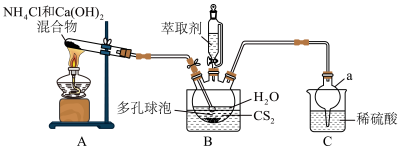
(1)仪器a的名称为__________ 。
(2)从结构角度分析,硫脲可溶于水的原因是__________ 。
(3)多孔球泡的作用是__________ 。
(4)B中反应完全的标志是__________ 。
(5)分离提纯的方法为萃取,应选用的绿色萃取剂为__________ (填标号)。
a.苯 b.四氯化碳 c.乙酸乙酯 d.乙醇
(6)滴定原理:
取mg硫脲的粗产品溶于水,用c mol∙L-1的酸性重铬酸钾标准溶液滴定到终点,平行三次实验平均消耗VmL标准溶液,则样品中硫脲的纯度为__________ 。
(7)在酸性溶液中,硫脲在Fe3+存在下能溶解金形成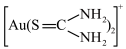 ,反应的离子方程式为
,反应的离子方程式为_______ 。溶解金的过程伴随着溶液变红的现象,原因可能为硫脲发生异构化生成__________ (填化学式)。
 为白色晶体,可溶于水,易溶于乙酸乙酯,可代替氰化物用于提炼金。合成硫脲的原理为
为白色晶体,可溶于水,易溶于乙酸乙酯,可代替氰化物用于提炼金。合成硫脲的原理为 。
。
(1)仪器a的名称为
(2)从结构角度分析,硫脲可溶于水的原因是
(3)多孔球泡的作用是
(4)B中反应完全的标志是
(5)分离提纯的方法为萃取,应选用的绿色萃取剂为
a.苯 b.四氯化碳 c.乙酸乙酯 d.乙醇
(6)滴定原理:

取mg硫脲的粗产品溶于水,用c mol∙L-1的酸性重铬酸钾标准溶液滴定到终点,平行三次实验平均消耗VmL标准溶液,则样品中硫脲的纯度为
(7)在酸性溶液中,硫脲在Fe3+存在下能溶解金形成
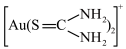 ,反应的离子方程式为
,反应的离子方程式为
您最近一年使用:0次
2024-05-29更新
|
190次组卷
|
3卷引用:湖北省武汉市2024届高三毕业生四月调研考试(二模)化学试题
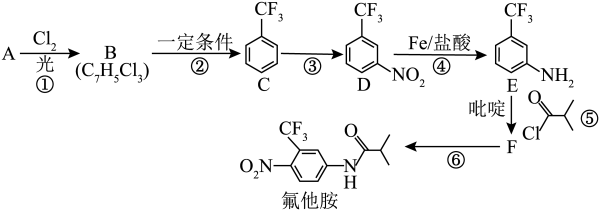
10 . I.氟他胺是一种抗肿瘤药,在实验室由芳香烃A制备氟他胺的合成路线如下所示:____________________ 。
(2)反应④的反应类型为____________________ 。
(3)请写出反应⑤的化学方程式____________________ 。
(4)吡啶是一种有机碱,请推测其在反应⑤中的作用____________________ 。
Ⅱ.取有机物A4.4g,完全燃烧后生成3.6gH2O和4.48LCO2(标准状况)。已知相同状况下,A蒸气的密度是氢气的44倍,其红外光谱图如下:__________ 。
(6)若A的核磁共振氢谱图有3组信号峰且A能与氢气加成,请写出A的结构简式____________________ 。
(2)反应④的反应类型为
(3)请写出反应⑤的化学方程式
(4)吡啶是一种有机碱,请推测其在反应⑤中的作用
Ⅱ.取有机物A4.4g,完全燃烧后生成3.6gH2O和4.48LCO2(标准状况)。已知相同状况下,A蒸气的密度是氢气的44倍,其红外光谱图如下:

(6)若A的核磁共振氢谱图有3组信号峰且A能与氢气加成,请写出A的结构简式
您最近一年使用:0次






