名校
解题方法
1 . 科学研究表明: 存储能量的能力是
存储能量的能力是 的12000倍左右,在大气中的寿命可达740年,如表所示是几种化学键的键能(断裂或形成1mol化学键时吸收或释放的热量)
的12000倍左右,在大气中的寿命可达740年,如表所示是几种化学键的键能(断裂或形成1mol化学键时吸收或释放的热量)
回答下列问题:
(1)①过程
___________ (填“吸收”或“放出”)能量。
②反应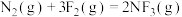
 =
=___________ 。
(2)已知:
①
 ;
;
②
 。
。
现有2mol由炭粉和氢气组成的悬浮气,在足量氧气中完全燃烧生成 (g)和
(g)和 (l),共放出679.0kJ的热量,则2mol悬浮气中C与
(l),共放出679.0kJ的热量,则2mol悬浮气中C与 的物质的量之比为
的物质的量之比为___________ 。
(3)电石( )可通过下列反应制备:
)可通过下列反应制备:
①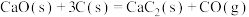
 ;
;
②
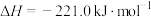 。
。
若不考虑热量损耗,物料转化率均为100%,最终炉中出来的气体只有CO。则为了维持热量平衡,每生产64g ,投料的量为56g CaO及
,投料的量为56g CaO及___________ mol C、___________ mol  。
。
 存储能量的能力是
存储能量的能力是 的12000倍左右,在大气中的寿命可达740年,如表所示是几种化学键的键能(断裂或形成1mol化学键时吸收或释放的热量)
的12000倍左右,在大气中的寿命可达740年,如表所示是几种化学键的键能(断裂或形成1mol化学键时吸收或释放的热量)| 化学键 | N≡N | F—F | N—F |
键能( ) ) | 946 | 154 | 283 |
(1)①过程

②反应
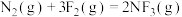
 =
=(2)已知:
①

 ;
;②

 。
。现有2mol由炭粉和氢气组成的悬浮气,在足量氧气中完全燃烧生成
 (g)和
(g)和 (l),共放出679.0kJ的热量,则2mol悬浮气中C与
(l),共放出679.0kJ的热量,则2mol悬浮气中C与 的物质的量之比为
的物质的量之比为(3)电石(
 )可通过下列反应制备:
)可通过下列反应制备:①
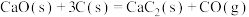
 ;
;②

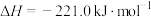 。
。若不考虑热量损耗,物料转化率均为100%,最终炉中出来的气体只有CO。则为了维持热量平衡,每生产64g
 ,投料的量为56g CaO及
,投料的量为56g CaO及 。
。
您最近半年使用:0次
2 . 化学反应过程中都伴随能量变化,吸热或放热是化学反应中能量变化的重要形式。回答下列问题:
(1)化学反应中伴随热量变化的本质原因是反应过程中形成化学键___________ ,断裂化学键___________ 。
(2)已知拆开1mol H—H键、1mol Cl—Cl键、1mol H—Cl键分别需要的能量是436kJ、243kJ、432kJ,则反应 的
的 =
=___________  。
。
(3)已知:
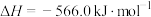 ;
;
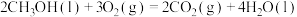
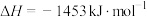 。
。
则 (l)不完全燃烧生成CO和
(l)不完全燃烧生成CO和 (l)的热化学方程式为
(l)的热化学方程式为___________ 。
(4)已知常温常压下,稀的强酸与稀的强碱溶液生成1mol (l)的反应热
(l)的反应热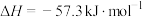 。
。
①表示稀硫酸与稀烧碱溶液生成1mol (l)的热化学方程式为
(l)的热化学方程式为___________ 。
②若用98%浓硫酸代替稀硫酸与稀烧碱溶液进行中和反应反应热测定,则所测得的
___________ (填“偏大”或“偏小”)。
(1)化学反应中伴随热量变化的本质原因是反应过程中形成化学键
(2)已知拆开1mol H—H键、1mol Cl—Cl键、1mol H—Cl键分别需要的能量是436kJ、243kJ、432kJ,则反应
 的
的 =
= 。
。(3)已知:

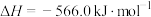 ;
;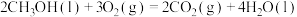
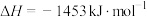 。
。则
 (l)不完全燃烧生成CO和
(l)不完全燃烧生成CO和 (l)的热化学方程式为
(l)的热化学方程式为(4)已知常温常压下,稀的强酸与稀的强碱溶液生成1mol
 (l)的反应热
(l)的反应热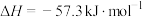 。
。①表示稀硫酸与稀烧碱溶液生成1mol
 (l)的热化学方程式为
(l)的热化学方程式为②若用98%浓硫酸代替稀硫酸与稀烧碱溶液进行中和反应反应热测定,则所测得的

您最近半年使用:0次
名校
解题方法
3 . 已知 (g)和
(g)和 (l)的燃烧热分别是1411.0
(l)的燃烧热分别是1411.0 和1366.8
和1366.8 ,则反应
,则反应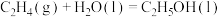 的
的 为
为
 (g)和
(g)和 (l)的燃烧热分别是1411.0
(l)的燃烧热分别是1411.0 和1366.8
和1366.8 ,则反应
,则反应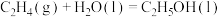 的
的 为
为A.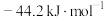 | B.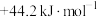 | C.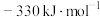 | D. |
您最近半年使用:0次
4 . 第五届硒博会主题为“健康中国·硒引天下”。硒(Se)是第四周期第VI A族元素,是人体内不可或缺的微量元素,H2Se是制备新型光伏太阳能电池、半导体材料和金属硒化物的重要原料。
(1)已知:①2H2Se(g)+O2(g) 2Se(s)+2H2O(l) △H =a kJ·mol-1
2Se(s)+2H2O(l) △H =a kJ·mol-1
②2H2(g)+O2(g) 2H2O(l) △H=b kJ·mol-1
2H2O(l) △H=b kJ·mol-1
反应H2(g)+Se(s) H2Se(g)的反应热△H=
H2Se(g)的反应热△H=___________ kJ·mol-1(用含a、b的代数式表示)。
(2)T℃时,向一恒容密闭容器中加入3molH2和1 mol Se,发生反应H2(g)+Se(s) H2Se(g),
H2Se(g),
①下列情况可判断反应达到平衡状态的是___________ (填字母代号)。
a.气体的密度不变 b.v(H2)=v(H2Se)
c.气体的压强不变 d.气体的平均摩尔质量不变
②以5小时内得到的H2Se为产量指标,且温度、压强对H2Se产率的影响如图所示:___________ 。
(3)已知常温下H2Se的电离平衡常数K1=1.3×10-4、K2=5.0×10-11,则NaHSe溶液呈___________ (填“酸性”或“碱性”),该溶液中的物料守恒关系式为___________ 。
(4)工业上从含硒废料中提取硒的方法是用硫酸和硝酸钠的混合溶液处理后获得亚硒酸和少量硒酸,再与盐酸共热,硒酸转化为亚硒酸,硒酸与盐酸反应的化学方程式为___________ ,最后通入SO2析出硒单质。
(5)H2 Se在一定条件下可以制备出CuSe,已知常温时CuSe的Ksp=7.9×10-49,CuS的Ksp=1.3×10-36,则反应CuS(s)+Se2-(aq) CuSe(s)+S2-(aq)的化学平衡常数K=
CuSe(s)+S2-(aq)的化学平衡常数K=___________ (保留2位有效数字)。
(1)已知:①2H2Se(g)+O2(g)
 2Se(s)+2H2O(l) △H =a kJ·mol-1
2Se(s)+2H2O(l) △H =a kJ·mol-1②2H2(g)+O2(g)
 2H2O(l) △H=b kJ·mol-1
2H2O(l) △H=b kJ·mol-1反应H2(g)+Se(s)
 H2Se(g)的反应热△H=
H2Se(g)的反应热△H=(2)T℃时,向一恒容密闭容器中加入3molH2和1 mol Se,发生反应H2(g)+Se(s)
 H2Se(g),
H2Se(g),①下列情况可判断反应达到平衡状态的是
a.气体的密度不变 b.v(H2)=v(H2Se)
c.气体的压强不变 d.气体的平均摩尔质量不变
②以5小时内得到的H2Se为产量指标,且温度、压强对H2Se产率的影响如图所示:
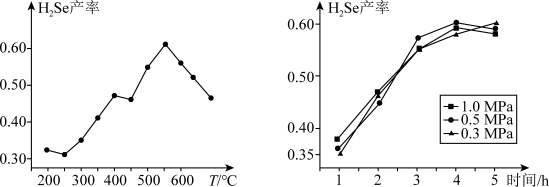
(3)已知常温下H2Se的电离平衡常数K1=1.3×10-4、K2=5.0×10-11,则NaHSe溶液呈
(4)工业上从含硒废料中提取硒的方法是用硫酸和硝酸钠的混合溶液处理后获得亚硒酸和少量硒酸,再与盐酸共热,硒酸转化为亚硒酸,硒酸与盐酸反应的化学方程式为
(5)H2 Se在一定条件下可以制备出CuSe,已知常温时CuSe的Ksp=7.9×10-49,CuS的Ksp=1.3×10-36,则反应CuS(s)+Se2-(aq)
 CuSe(s)+S2-(aq)的化学平衡常数K=
CuSe(s)+S2-(aq)的化学平衡常数K=
您最近半年使用:0次
名校
解题方法
5 . 乙烯是重要的工业原料,可用下列方法制备。
Ⅰ. 催化加氢法制乙烯:
催化加氢法制乙烯: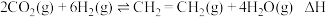
已知: 的燃烧热分别为:
的燃烧热分别为: ;
;

(1)该反应
___________  。
。
(2)将 和
和 按物质的量之比为2:3充入恒容密闭容器中,分别在不同催化剂条件下发生反应,测得相同时间
按物质的量之比为2:3充入恒容密闭容器中,分别在不同催化剂条件下发生反应,测得相同时间 的转化率与温度的关系如图所示:
的转化率与温度的关系如图所示:___________ 。
A.达平衡时,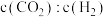 一定为2:3
一定为2:3
B.向反应体系中加入少量无水 固体,可提高
固体,可提高 的产率
的产率
C.b、d两状态下,化学反应速率一定相等
D.使用催化剂Ⅰ时反应的活化能比使用催化剂Ⅱ时低
E. 温度下,向容器中加入稀有气体,可提高
温度下,向容器中加入稀有气体,可提高 的转化率
的转化率
Ⅱ.工业上也可用甲烷催化法制取乙烯,只发生如下反应: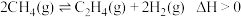 。
。
(3)温度T时,向2L的恒容反应器中充入 ,仅发生上述反应,反应过程中
,仅发生上述反应,反应过程中 的物质的量随时间变化如图所示:
的物质的量随时间变化如图所示: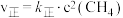 ,
,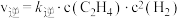 ,
, 为速率常数,只与温度有关,T温度时,
为速率常数,只与温度有关,T温度时,
___________ (用含有x的代数式表示);当温度升高时, 增大m倍,
增大m倍, 增大n倍,则m
增大n倍,则m___________ (填“>”“<”或“=”)n。
Ⅲ. 氧化
氧化 制乙烯:
制乙烯:
主反应为: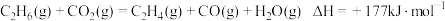
(4)某催化剂催化过程中,在催化剂表面发生了一系列反应:
①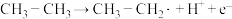 ,
,
②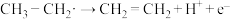 ,
,
③ ,
,
④___________。
则:④的反应式为___________ 。
(5)在 与
与 反应制
反应制 的过程中,
的过程中,
还会发生副反应:
①其他条件相同时,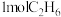 与
与 经相同反应时间测得如表实验数据:
经相同反应时间测得如表实验数据:
相同温度时,催化剂2催化下 产率更高的原因是
产率更高的原因是___________ 。
②在容器体积为1.0L,充入 和
和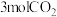 同时发生主、副反应,乙烷的平衡转化率、乙烯的选择性(
同时发生主、副反应,乙烷的平衡转化率、乙烯的选择性(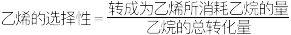 )与温度、压强的关系如图所示。M点主反应的平衡常数为
)与温度、压强的关系如图所示。M点主反应的平衡常数为___________ (结果保留2位有效数字)。
Ⅰ.
 催化加氢法制乙烯:
催化加氢法制乙烯: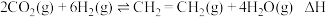
已知:
 的燃烧热分别为:
的燃烧热分别为: ;
;
(1)该反应

 。
。(2)将
 和
和 按物质的量之比为2:3充入恒容密闭容器中,分别在不同催化剂条件下发生反应,测得相同时间
按物质的量之比为2:3充入恒容密闭容器中,分别在不同催化剂条件下发生反应,测得相同时间 的转化率与温度的关系如图所示:
的转化率与温度的关系如图所示: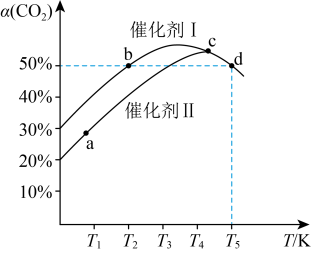
A.达平衡时,
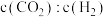 一定为2:3
一定为2:3B.向反应体系中加入少量无水
 固体,可提高
固体,可提高 的产率
的产率C.b、d两状态下,化学反应速率一定相等
D.使用催化剂Ⅰ时反应的活化能比使用催化剂Ⅱ时低
E.
 温度下,向容器中加入稀有气体,可提高
温度下,向容器中加入稀有气体,可提高 的转化率
的转化率Ⅱ.工业上也可用甲烷催化法制取乙烯,只发生如下反应:
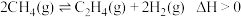 。
。(3)温度T时,向2L的恒容反应器中充入
 ,仅发生上述反应,反应过程中
,仅发生上述反应,反应过程中 的物质的量随时间变化如图所示:
的物质的量随时间变化如图所示:
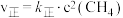 ,
,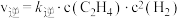 ,
, 为速率常数,只与温度有关,T温度时,
为速率常数,只与温度有关,T温度时,
 增大m倍,
增大m倍, 增大n倍,则m
增大n倍,则mⅢ.
 氧化
氧化 制乙烯:
制乙烯:主反应为:
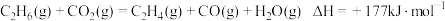
(4)某催化剂催化过程中,在催化剂表面发生了一系列反应:
①
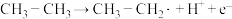 ,
,②
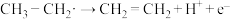 ,
,③
 ,
,④___________。
则:④的反应式为
(5)在
 与
与 反应制
反应制 的过程中,
的过程中,还会发生副反应:

①其他条件相同时,
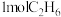 与
与 经相同反应时间测得如表实验数据:
经相同反应时间测得如表实验数据:| 实验 | 温度/K | 催化剂 |  的产率% 的产率% |
| 实验1 | 400 | 催化剂1 | 55.0 |
| 400 | 催化剂2 | 62.3 | |
| 实验2 | 500 | 催化剂1 | 68.5 |
| 500 | 催化剂2 | 80.1 |
 产率更高的原因是
产率更高的原因是②在容器体积为1.0L,充入
 和
和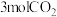 同时发生主、副反应,乙烷的平衡转化率、乙烯的选择性(
同时发生主、副反应,乙烷的平衡转化率、乙烯的选择性(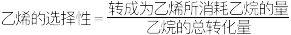 )与温度、压强的关系如图所示。M点主反应的平衡常数为
)与温度、压强的关系如图所示。M点主反应的平衡常数为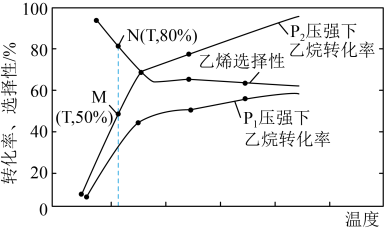
您最近半年使用:0次
6 . 二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。回答下列问题:
(1)已知: 、
、 和
和 键的键能分别为
键的键能分别为 、
、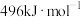 和
和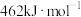 。
。

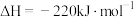

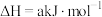
则
___________ 。
(2)已知: 在催化剂I和II的催化下的反应历程和能量变化如下图。
在催化剂I和II的催化下的反应历程和能量变化如下图。___________ (填I或II)时,反应过程中 所能达到的最高浓度更大。
所能达到的最高浓度更大。
②在相同条件下反应达到平衡状态,为提高 的平衡浓度和
的平衡浓度和 的平衡物质的量分数,可以采取的措施是
的平衡物质的量分数,可以采取的措施是___________ 。
(3)以 为原料合成
为原料合成 涉及的主要反应如下:
涉及的主要反应如下:
I.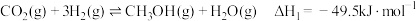
II.
在密闭容器中,压强恒为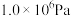 ,
,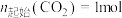 ,
,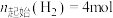 ,
, 平衡转化率、在催化剂作用下反应相同时间所测得的
平衡转化率、在催化剂作用下反应相同时间所测得的 实际转化率,随温度的变化如图所示。
实际转化率,随温度的变化如图所示。 的选择性可表示为
的选择性可表示为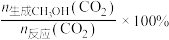 。
。
①反应的最佳温度___________ 。
②反应温度超过 时,
时, 平衡转化率逐渐增大的原因是
平衡转化率逐渐增大的原因是___________ 。
③反应温度超过 时,
时, 实际转化率逐渐减小的原因是
实际转化率逐渐减小的原因是___________ 。
④反应温度在 时,
时, 点
点 的选择性为
的选择性为 ,则平衡时
,则平衡时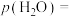
___________  (保留三位有效数字,后面相同),反应II的压强平衡常数
(保留三位有效数字,后面相同),反应II的压强平衡常数
___________ 。
(4)工业废气中含有的 和
和 可利用如下装置回收利用。
可利用如下装置回收利用。___________ 。
②装置b中,x和y为石墨电极,写出电极x的电极反应___________ 。
(1)已知:
 、
、 和
和 键的键能分别为
键的键能分别为 、
、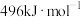 和
和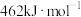 。
。
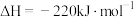

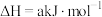
则

(2)已知:
 在催化剂I和II的催化下的反应历程和能量变化如下图。
在催化剂I和II的催化下的反应历程和能量变化如下图。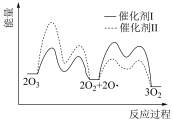
 所能达到的最高浓度更大。
所能达到的最高浓度更大。②在相同条件下反应达到平衡状态,为提高
 的平衡浓度和
的平衡浓度和 的平衡物质的量分数,可以采取的措施是
的平衡物质的量分数,可以采取的措施是(3)以
 为原料合成
为原料合成 涉及的主要反应如下:
涉及的主要反应如下:I.
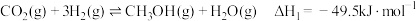
II.

在密闭容器中,压强恒为
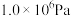 ,
,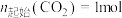 ,
,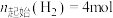 ,
, 平衡转化率、在催化剂作用下反应相同时间所测得的
平衡转化率、在催化剂作用下反应相同时间所测得的 实际转化率,随温度的变化如图所示。
实际转化率,随温度的变化如图所示。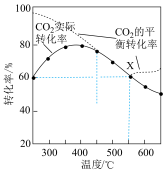
 的选择性可表示为
的选择性可表示为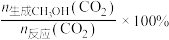 。
。①反应的最佳温度
②反应温度超过
 时,
时, 平衡转化率逐渐增大的原因是
平衡转化率逐渐增大的原因是③反应温度超过
 时,
时, 实际转化率逐渐减小的原因是
实际转化率逐渐减小的原因是④反应温度在
 时,
时, 点
点 的选择性为
的选择性为 ,则平衡时
,则平衡时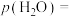
 (保留三位有效数字,后面相同),反应II的压强平衡常数
(保留三位有效数字,后面相同),反应II的压强平衡常数
(4)工业废气中含有的
 和
和 可利用如下装置回收利用。
可利用如下装置回收利用。
②装置b中,x和y为石墨电极,写出电极x的电极反应
您最近半年使用:0次
7 . 氙及其化合物在工业生产中有重要用途。
(1)1962年,化学家巴特利特合成了氙的第一个化合物 ,其在熔化时电离出
,其在熔化时电离出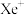 和
和 。Xe和
。Xe和 混合制得
混合制得 的反应可以表示如下:
的反应可以表示如下: )和1mol气态阴离子(
)和1mol气态阴离子( )所需要的能量叫做晶格能,
)所需要的能量叫做晶格能, 的晶格能为
的晶格能为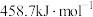 。
。
②Xe的第一电离能为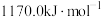 。
。
③
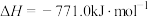 。
。
根据以上信息,计算反应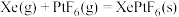

___________  。
。
(2)不久,在三个不同实验室里又分别合成了 、
、 、
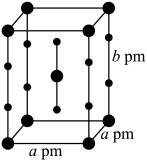
、 三种简单化合物。其中一种化合物的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,
三种简单化合物。其中一种化合物的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°, 表示阿伏伽德罗常数的值。则该化合物的化学式为
表示阿伏伽德罗常数的值。则该化合物的化学式为___________ ,中心原子的价层电子对数为___________ ,晶体密度为___________  。
。 混合气体,反应体系中存在的平衡及相应部分数据如下表所示。
混合气体,反应体系中存在的平衡及相应部分数据如下表所示。
已知:分压=总压×该组分物质的量分数;
对于反应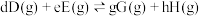
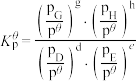
其中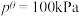 ,
,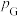 、
、 、
、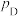 、
、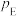 为各组分的平衡分压。
为各组分的平衡分压。
①
___________ 0(填“>”或“<”)。为提高平衡混合物中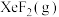 的含量,应
的含量,应___________ 投料比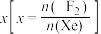 (填“增大”或“减小”)。
(填“增大”或“减小”)。
②673K时充入23.77molXe和 ,达平衡时容器内总压强
,达平衡时容器内总压强 ,各产物的物质的量如下表所示:
,各产物的物质的量如下表所示:
则 平衡转化率
平衡转化率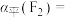
___________ (保留三位有效数字),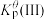
___________ 。
(1)1962年,化学家巴特利特合成了氙的第一个化合物
 ,其在熔化时电离出
,其在熔化时电离出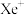 和
和 。Xe和
。Xe和 混合制得
混合制得 的反应可以表示如下:
的反应可以表示如下: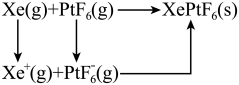
 )和1mol气态阴离子(
)和1mol气态阴离子( )所需要的能量叫做晶格能,
)所需要的能量叫做晶格能, 的晶格能为
的晶格能为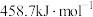 。
。②Xe的第一电离能为
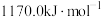 。
。③

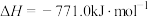 。
。根据以上信息,计算反应
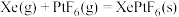

 。
。(2)不久,在三个不同实验室里又分别合成了
 、
、 、
、 三种简单化合物。其中一种化合物的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,
三种简单化合物。其中一种化合物的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°, 表示阿伏伽德罗常数的值。则该化合物的化学式为
表示阿伏伽德罗常数的值。则该化合物的化学式为 。
。
 混合气体,反应体系中存在的平衡及相应部分数据如下表所示。
混合气体,反应体系中存在的平衡及相应部分数据如下表所示。已知:分压=总压×该组分物质的量分数;
对于反应
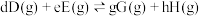
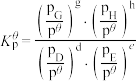
其中
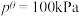 ,
,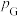 、
、 、
、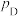 、
、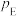 为各组分的平衡分压。
为各组分的平衡分压。标准压强平衡常数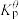 反应平衡 | 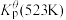 | 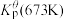 |
反应I: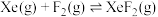  | 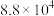 | 360 |
反应II: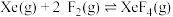  | ||
反应III: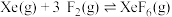  | 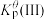 |

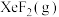 的含量,应
的含量,应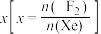 (填“增大”或“减小”)。
(填“增大”或“减小”)。②673K时充入23.77molXe和
 ,达平衡时容器内总压强
,达平衡时容器内总压强 ,各产物的物质的量如下表所示:
,各产物的物质的量如下表所示:| 化学式 |  |  |  |
| 物质的量/mol | 3.60 | 19.80 | 0.36 |
 平衡转化率
平衡转化率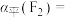
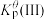
您最近半年使用:0次
8 . 含硫化合物在能源、材料及环境等工业领域均有广泛的应用。
Ⅰ.工业废气 分解可制取
分解可制取 。
。
(1)已知热化学方程式:
ⅰ.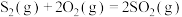

ⅱ.

ⅲ.

 热分解反应
热分解反应 的
的
___________ (用含 、
、 、
、 的式子表示)。
的式子表示)。
(2)一定温度下,2mol 在体积为VL的恒容密闭容器中发生上述分解反应,ts时
在体积为VL的恒容密闭容器中发生上述分解反应,ts时 的产率为40%,则0~ts内
的产率为40%,则0~ts内 的平均分解速率为
的平均分解速率为___________  ;
; 充分分解达到平衡时,容器中
充分分解达到平衡时,容器中 和
和 的分压相等,则该温度下的平衡常数
的分压相等,则该温度下的平衡常数
___________ 。
Ⅱ.KSCN可用于镀铬工业。常温下,用KSCN配制电镀液,溶液中 与
与 发生第一、二步络合的反应如下:
发生第一、二步络合的反应如下:
ⅳ.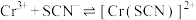
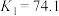
ⅴ.

(3)根据以上络合反应,下列说法正确的有___________(填字母)。
(4)常温下,某研究小组配制了起始浓度 、
、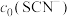 不同的系列溶液,测得平衡时
不同的系列溶液,测得平衡时 、
、 、
、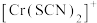 的浓度
的浓度 (含铬微粒)随
(含铬微粒)随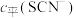 的变化曲线如图所示,平衡后其他含铬微粒
的变化曲线如图所示,平衡后其他含铬微粒 (3≤x≤6,图中未画出)总浓度为amol/L。
(3≤x≤6,图中未画出)总浓度为amol/L。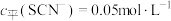 时,图中含铬微粒按浓度由大到小的顺序为
时,图中含铬微粒按浓度由大到小的顺序为___________ ;A点时,溶液中 的平衡浓度为
的平衡浓度为___________ (列出计算式即可)。
②在某电镀工艺中, 的浓度需要在
的浓度需要在 以上,结合计算判断C点所对应的溶液能否用于该电镀工艺
以上,结合计算判断C点所对应的溶液能否用于该电镀工艺________ (写出计算过程)。
Ⅰ.工业废气
 分解可制取
分解可制取 。
。(1)已知热化学方程式:
ⅰ.
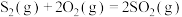

ⅱ.


ⅲ.


 热分解反应
热分解反应 的
的
 、
、 、
、 的式子表示)。
的式子表示)。(2)一定温度下,2mol
 在体积为VL的恒容密闭容器中发生上述分解反应,ts时
在体积为VL的恒容密闭容器中发生上述分解反应,ts时 的产率为40%,则0~ts内
的产率为40%,则0~ts内 的平均分解速率为
的平均分解速率为 ;
; 充分分解达到平衡时,容器中
充分分解达到平衡时,容器中 和
和 的分压相等,则该温度下的平衡常数
的分压相等,则该温度下的平衡常数
Ⅱ.KSCN可用于镀铬工业。常温下,用KSCN配制电镀液,溶液中
 与
与 发生第一、二步络合的反应如下:
发生第一、二步络合的反应如下:ⅳ.
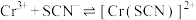
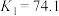
ⅴ.


(3)根据以上络合反应,下列说法正确的有___________(填字母)。
| A.加水稀释后,溶液中离子的总数减少 |
B.加入少量 固体,溶液中含铬微粒总数不变 固体,溶液中含铬微粒总数不变 |
C.反应 的平衡常数 的平衡常数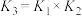 |
D.溶液中 减小, 减小, 与 与 浓度的比值减小 浓度的比值减小 |
(4)常温下,某研究小组配制了起始浓度
 、
、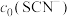 不同的系列溶液,测得平衡时
不同的系列溶液,测得平衡时 、
、 、
、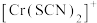 的浓度
的浓度 (含铬微粒)随
(含铬微粒)随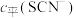 的变化曲线如图所示,平衡后其他含铬微粒
的变化曲线如图所示,平衡后其他含铬微粒 (3≤x≤6,图中未画出)总浓度为amol/L。
(3≤x≤6,图中未画出)总浓度为amol/L。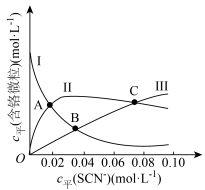
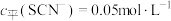 时,图中含铬微粒按浓度由大到小的顺序为
时,图中含铬微粒按浓度由大到小的顺序为 的平衡浓度为
的平衡浓度为②在某电镀工艺中,
 的浓度需要在
的浓度需要在 以上,结合计算判断C点所对应的溶液能否用于该电镀工艺
以上,结合计算判断C点所对应的溶液能否用于该电镀工艺
您最近半年使用:0次
9 . 二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。回答下列问题:
(1)二氧化碳加氢制甲醇的总反应可表示为:
该反应一般认为通过如下步骤来实现:
①
②
总反应的
___________  ;若反应①为慢反应,下列示意图中能体现上述反应能量变化的是
;若反应①为慢反应,下列示意图中能体现上述反应能量变化的是___________ (填标号)。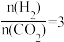 时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为
时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为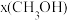 ,在
,在 ℃下的
℃下的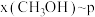 、在
、在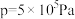 下的
下的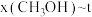 如图所示。
如图所示。
___________ ;
②图中对应等压过程的曲线是___________ ;
③当 时,
时, 的平衡转化率
的平衡转化率
___________ ,反应条件可能为___________ 或___________ 。
(1)二氧化碳加氢制甲醇的总反应可表示为:

该反应一般认为通过如下步骤来实现:
①

②

总反应的

 ;若反应①为慢反应,下列示意图中能体现上述反应能量变化的是
;若反应①为慢反应,下列示意图中能体现上述反应能量变化的是A. 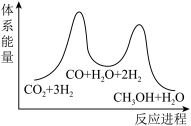 B.
B.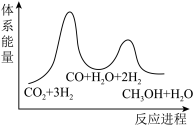
C. D.
D.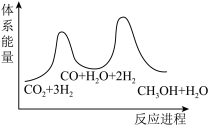
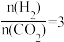 时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为
时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为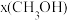 ,在
,在 ℃下的
℃下的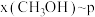 、在
、在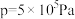 下的
下的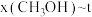 如图所示。
如图所示。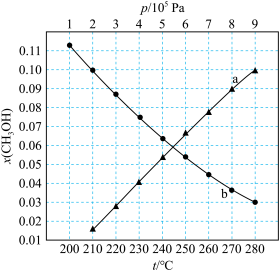

②图中对应等压过程的曲线是
③当
 时,
时, 的平衡转化率
的平衡转化率
您最近半年使用:0次
名校
解题方法
10 . 我国力争于2030年前做到“碳达峰”,2060年前实现“碳中和”, 制
制 是热点研究之一,中科院大连化物所研究团队直接利用
是热点研究之一,中科院大连化物所研究团队直接利用 与
与 合成甲醇,主要涉及以下反应:
合成甲醇,主要涉及以下反应:
①

②
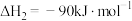
③
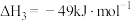
(1) =
=___________ 。
(2)反应①、②的平衡常数随温度变化曲线如图1所示,则表示反应②的 关系的曲线为
关系的曲线为___________ (填“ ”或“
”或“ ”)。
”)。 以后反应②在该体系中可以忽略,其依据是
以后反应②在该体系中可以忽略,其依据是___________ 。
②恒压下,向容器中充入 、
、 ,
, 的平衡转化率随温度变化曲线如图1中n线所示。若只发生反应①和③,在
的平衡转化率随温度变化曲线如图1中n线所示。若只发生反应①和③,在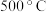 达到平衡时,体系中
达到平衡时,体系中 的物质的量为
的物质的量为 ,则此时
,则此时 的转化率为
的转化率为___________ 。此时反应①的平衡常数值为___________ 。
(4)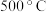 以后
以后 的平衡转化率随温度变化的可能原因是
的平衡转化率随温度变化的可能原因是___________ 。
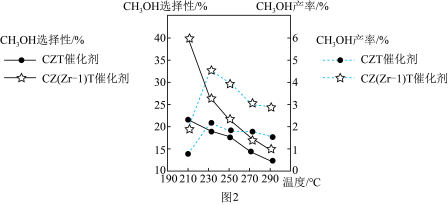
(5)恒压下将 和
和 按体积比1∶3混合,在不同催化剂作用下发生反应。在相同时间段内
按体积比1∶3混合,在不同催化剂作用下发生反应。在相同时间段内 的选择性和产率随温度的变化如图2所示。其中
的选择性和产率随温度的变化如图2所示。其中 的选择性=
的选择性= 。
。
 制
制 是热点研究之一,中科院大连化物所研究团队直接利用
是热点研究之一,中科院大连化物所研究团队直接利用 与
与 合成甲醇,主要涉及以下反应:
合成甲醇,主要涉及以下反应:①


②

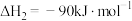
③

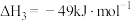
(1)
 =
=(2)反应①、②的平衡常数随温度变化曲线如图1所示,则表示反应②的
 关系的曲线为
关系的曲线为 ”或“
”或“ ”)。
”)。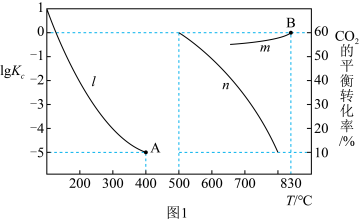
 以后反应②在该体系中可以忽略,其依据是
以后反应②在该体系中可以忽略,其依据是②恒压下,向容器中充入
 、
、 ,
, 的平衡转化率随温度变化曲线如图1中n线所示。若只发生反应①和③,在
的平衡转化率随温度变化曲线如图1中n线所示。若只发生反应①和③,在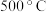 达到平衡时,体系中
达到平衡时,体系中 的物质的量为
的物质的量为 ,则此时
,则此时 的转化率为
的转化率为(4)
 以后
以后 的平衡转化率随温度变化的可能原因是
的平衡转化率随温度变化的可能原因是(5)恒压下将
 和
和 按体积比1∶3混合,在不同催化剂作用下发生反应。在相同时间段内
按体积比1∶3混合,在不同催化剂作用下发生反应。在相同时间段内 的选择性和产率随温度的变化如图2所示。其中
的选择性和产率随温度的变化如图2所示。其中 的选择性=
的选择性= 。
。
A. | B. | C. 催化 催化 | D. 催化剂 催化剂 |
您最近半年使用:0次



