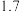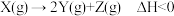 的影响,各物质浓度c随反应时间t的部分变化曲线如图。下列说法正确的是
的影响,各物质浓度c随反应时间t的部分变化曲线如图。下列说法正确的是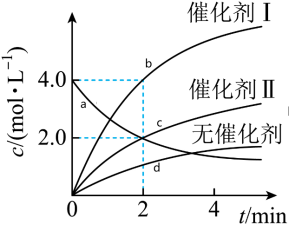
| A.无催化剂时,反应不能进行 |
| B.与催化剂Ⅰ相比,Ⅱ使反应活化能更低 |
C.使用催化剂Ⅰ, 时, 时,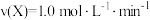 |
| D.c曲线可表示使用催化剂I时Z的浓度随t的变化 |
2 . “节能减排”和“低碳经济”的一项重要课题就是如何将 转化为可利用的资源。
转化为可利用的资源。
Ⅰ.目前工业上有一种方法是用 来生产燃料甲醇。
来生产燃料甲醇。
已知: 的燃烧热
的燃烧热 kJ⋅mol
kJ⋅mol 、
、 的燃烧热
的燃烧热 kJ⋅mol
kJ⋅mol
反应①:
 kJ⋅mol
kJ⋅mol
反应②:
 kJ⋅mol
kJ⋅mol
反应③:

(1)


(2)恒温条件下,在某恒容密闭容器中;按照
 投料发生反应③,测得
投料发生反应③,测得 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。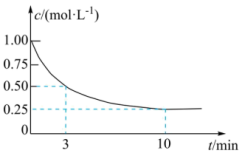
①从反应开始到3 min, 的平均反应速率
的平均反应速率
 ⋅min
⋅min ;试在图中绘制出
;试在图中绘制出 的浓度随时间变化的图像
的浓度随时间变化的图像
②该反应的平衡常数
(3)恒温条件下,在某恒压密闭容器中仅发生反应①,当反应达到平衡后,
Ⅰ.降低温度,CO的平衡转化率
Ⅱ.向平衡体系中通入惰性气体,平衡
(1)上述四种气体中直接排入空气时会引起酸雨的有
(2)回收大气污染物SO2的方法如下:
方法一:在复合组分催化剂作用下,CH4可使SO2转化为S,同时生成CO2和液态H2O。已知:
CH4(g)+2SO2(g)=CO2(g)+2S(s)+2H2O(1) △H=-295.9kJ·mol-1
S(s)+O2(g)=SO2(g) △H=-297.2kJ·mol-1
则CH4的燃烧热的热化学方程式为:
方法二:在恒容密闭容器中,用H2还原SO2生成S的反应分两步完成(如图1所示),该过程中部分物质的物质的量浓度随时间的变化关系如图2所示:

①由分析可知X为
②0~t1时间段H2的化学反应速率
方法三:利用反应:NO2(g)+SO2(g)
 SO3(g)+NO(g)。
SO3(g)+NO(g)。③一定条件下,将NO2与SO2以体积比1∶1置于恒温恒容的密闭容器中发生反应:NO2(g)+SO2(g)
 SO3(g)+NO(g),能说明反应达到平衡状态的是
SO3(g)+NO(g),能说明反应达到平衡状态的是a.混合气体的密度保持不变 b.SO2的物质的量保持不变
c.容器内混合气体原子总数不变 d.每生成1molSO3的同时消耗1molNO
e.容器内的混合气体平均相对分子质量保持不变
④已知该反应的平衡常数为
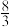 ,向某恒温恒容密闭容器中通入NO2、SO2、SO3、NO各1mol,此时v(正)
,向某恒温恒容密闭容器中通入NO2、SO2、SO3、NO各1mol,此时v(正)(3)在发动机的高温下,空气中的N2和CO2可能发生:N2(g)+CO2(g)
 C(s)+2NO(g),现向2L体积恒定的密闭容器中充入一定量N2和CO2来模拟此过程,其中N2、NO物质的量随时间变化的曲线如图所示。
C(s)+2NO(g),现向2L体积恒定的密闭容器中充入一定量N2和CO2来模拟此过程,其中N2、NO物质的量随时间变化的曲线如图所示。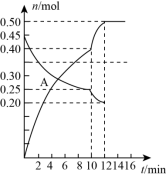
①图中A点v正
②第10min时,外界改变的条件可能是
A.加催化剂 B.增大C的物质的量 C.减小CO2的物质的量 D.升温 E.降温
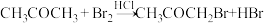 ,已知该反应的速率方程为
,已知该反应的速率方程为 ,其中k为与温度有关的常数。下列说法正确的是
,其中k为与温度有关的常数。下列说法正确的是| A.该反应为加成反应 | B.升高温度,k增大,化学反应速率加快 |
C.减小 ,化学反应速率减慢 ,化学反应速率减慢 | D.增大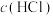 ,化学反应速率不变 ,化学反应速率不变 |
①CO(g)+2H2(g)
 CH3OH(g) ΔH1<0 K1
CH3OH(g) ΔH1<0 K1②2CH3OH(g)
 CH3OCH3(g)+H2O(g) ΔH2<0 K2
CH3OCH3(g)+H2O(g) ΔH2<0 K2③CO(g)+H2O(g)
 CO2(g)+H2(g) ΔH3<0 K3
CO2(g)+H2(g) ΔH3<0 K3(1)则反应3H2(g)+3CO(g)
 CH3OCH3(g)+CO2(g)的ΔH=
CH3OCH3(g)+CO2(g)的ΔH=(2)反应②达平衡后采取下列措施,能提高CH3OCH3产率的有
A.加入CH3OH B.升高温度 C.增大压强 D.移出H2O E.使用催化剂
(3)以下说法能说明反应3H2(g)+3CO(g)
 CH3OCH3(g)+CO2(g)达到平衡状态的
CH3OCH3(g)+CO2(g)达到平衡状态的A.H2和CO2的浓度之比为3∶1
B.单位时间内断裂3个H—H同时断裂1个C=O
C.恒温恒容条件下,气体的密度保持不变
D.恒温恒压条件下,气体的平均摩尔质量保持不变
E.绝热体系中,体系的温度保持不变
(4)200 ℃时,向恒容密闭容器中充入一定量的CH3OH(g)发生反应:
2CH3OH(g)
 CH3OCH3(g)+H2O(g),测得CH3OH(g)的浓度随时间(t)的变化如下表:
CH3OCH3(g)+H2O(g),测得CH3OH(g)的浓度随时间(t)的变化如下表:| t/min | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| c(CH3OH)/(mol·L-1) | 1.00 | 0.65 | 0.50 | 0.36 | 0.27 | 0.20 | 0.20 |
②反应达平衡时,容器内的压强为P0.该反应在200 ℃时的平衡常数Kp=
③200℃时,向该容器中投入三种成分的浓度如下:
| 物质 | CH3OH(g) | CH3OCH3(g) | H2O(g) |
| c/(mol·L-1) | 0.54 | 0.68 | 0.68 |
 4XO2(g) +O2(g)△H>0,T温度下的部分实验数据为:
4XO2(g) +O2(g)△H>0,T温度下的部分实验数据为:| t/s | 0 | 50 | 100 | 150 |
| c(X2O5) mol/L | 4.00 | 2.50 | 2.00 | 2.00 |
| A.50s内X2O5分解速率为 0.03 mol/ (L•s) |
| B.T温度下的平衡常数为K=64 (mol/L)3,100s时转化率为50% |
| C.T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若T1>T2,则Kl>K2 |
| D.若只将恒容改为恒压,其它条件都不变,则平衡时X2O5的转化率和平衡常数都增大 |
7 . 一定条件下,某容积为 的密闭容器中发生反应:
的密闭容器中发生反应: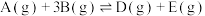
 ,反应过程中正、逆反应速率随着时间的变化如图所示,下列说法正确的是
,反应过程中正、逆反应速率随着时间的变化如图所示,下列说法正确的是
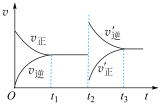
A. 时间段内, 时间段内, |
| B.若容器内气体的密度不再发生变化,则说明达到平衡状态 |
C. 时间段内平衡向正反应方向移动 时间段内平衡向正反应方向移动 |
D. 时刻改变的条件为向容器中加入生成物的同时分离出反应物 时刻改变的条件为向容器中加入生成物的同时分离出反应物 |
8 . Ⅰ.某探究小组用 与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用
与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用 浓度分别为
浓度分别为 、
、 ,大理石有细颗粒和粗颗粒两种规格,实验温度可选
,大理石有细颗粒和粗颗粒两种规格,实验温度可选 和
和 ,每次实验
,每次实验 的用量均为
的用量均为 ,大理石用量均为
,大理石用量均为 。
。
实验编号 | 温度( | 大理石规格 |
| 实验目的 |
① | 25 | 粗颗粒 |
| (Ⅰ)实验①和②探究浓度对反应速率的影响; (Ⅱ)实验①和③探究温度对反应速率的影响; (Ⅲ)实验①和④探究 |
② | 25 | 粗颗粒 |
| |
③ |
| 粗颗粒 |
| |
④ |
| 细颗粒 |
|
(1)请完成实验设计表:

 为
为(2)实验①中
 质量随时间变化的关系如图所示。在
质量随时间变化的关系如图所示。在 、
、 、
、 各时间段里,反应速率最大的时间段是
各时间段里,反应速率最大的时间段是 
Ⅱ.某小组利用 溶液和硫酸酸化的
溶液和硫酸酸化的 溶液反应来探究“外界条件对化学反应速率的影响”。实验室通过测定酸性
溶液反应来探究“外界条件对化学反应速率的影响”。实验室通过测定酸性 溶液褪色所需时间来判断反应的快慢,该小组进行实验并记录如下:
溶液褪色所需时间来判断反应的快慢,该小组进行实验并记录如下:
【实验原理】
【实验内容及记录】
实验编号 | 实验温度 | 试管中所加试剂及其用量 | 溶液褪至无色所需时间 | |||
|
|
|
| |||
① | 25 |
|
|
|
|
|
② | 25 |
|
|
|
|
|
③ | 50 |
|
|
|
|
|
(3)表中

(4)探究温度对化学反应速率的影响,应选择实验
(5)利用实验①中的数据,计算用
 表示的化学反应速率为
表示的化学反应速率为 。
。
(ⅰ)
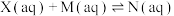
(ⅱ)
(ⅲ)

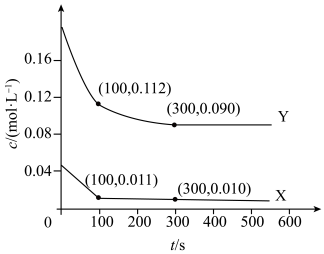
X、Y的物质的量浓度
 随反应时间
随反应时间 的变化关系如图所示,300 s后反应体系达到平衡状态。
的变化关系如图所示,300 s后反应体系达到平衡状态。下列说法正确的是
A.100~300 s内,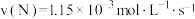 |
B. 时,反应(ⅲ)的逆反应速率大于正反应速率 时,反应(ⅲ)的逆反应速率大于正反应速率 |
C.若反应(ⅲ)的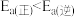 ,则X比Y更稳定 ,则X比Y更稳定 |
D.若再向容器中加入上述溶剂,则 、 、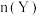 均不变 均不变 |
 ,B的浓度减少
,B的浓度减少 。对该反应速率的表示,下列说法正确的是
。对该反应速率的表示,下列说法正确的是A.用A表示的反应速率是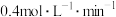 |
| B.用B、C 、D表示的反应速率之比为3∶2∶1 |
C.在 末,用B表示的反应速率是 末,用B表示的反应速率是 |
D.在 内用B表示的反应速率逐渐减小,用C表示的反应速率逐渐增大 内用B表示的反应速率逐渐减小,用C表示的反应速率逐渐增大 |

 )
) )
)








 溶液
溶液