名校
解题方法
1 . 现有四种元素的基态原子的核外电子排布式如下:
①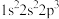 ;②
;② ;③
;③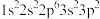 ;④
;④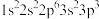 。下列说法错误的是
。下列说法错误的是
①
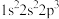 ;②
;② ;③
;③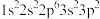 ;④
;④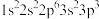 。下列说法错误的是
。下列说法错误的是| A.电负性:②>①>④>③ | B.原子半径:③>④>①>② |
| C.简单气态氢化物的稳定性:①>②>③>④ | D.第一电离能:②>①>④>③ |
您最近半年使用:0次
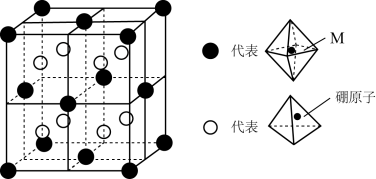
2 . 某种新型储氢材料的晶胞如图,八面体中心M为铁元素金属离子,顶点均为 配体;四面体中心为硼原子,顶点均为氢原子,下列说法正确的是
配体;四面体中心为硼原子,顶点均为氢原子,下列说法正确的是
 配体;四面体中心为硼原子,顶点均为氢原子,下列说法正确的是
配体;四面体中心为硼原子,顶点均为氢原子,下列说法正确的是
A.黑球微粒的化学式为 | B.白球微粒中存在配位键,硼原子提供空轨道 |
C.晶体中 分子间可能存在氢键作用 分子间可能存在氢键作用 | D.晶体中所含元素的电负性大小顺序为N>B>H>Fe |
您最近半年使用:0次
3 .  是一种新型光催化剂.下列说法错误的是
是一种新型光催化剂.下列说法错误的是
 是一种新型光催化剂.下列说法错误的是
是一种新型光催化剂.下列说法错误的是| A.Zn处于元素周期表中的ds区 |
B.基态Ge的价电子排布式为 |
| C.基态O原子的纺锤形轨道中电子具有的能量都相同 |
| D.三种元素电负性由大到小的顺序是O>Ge>Zn |
您最近半年使用:0次
4 . 锂电池中电解液的阻燃剂的结构式如图所示,其中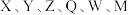 是原子序数依次增大的短周期主族元素。下列说法正确的是
是原子序数依次增大的短周期主族元素。下列说法正确的是
 是原子序数依次增大的短周期主族元素。下列说法正确的是
是原子序数依次增大的短周期主族元素。下列说法正确的是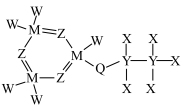
A.元素的第一电离能: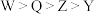 |
B.元素的电负性: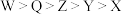 |
C.最高价氧化物对应的水化物的酸性: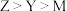 |
D.基态原子未成对电子数: |
您最近半年使用:0次
2024-03-03更新
|
216次组卷
|
2卷引用:山东省菏泽市东明县第一中学2023-2024学年高三下学期开学化学试题
5 . B、C、N、O、F是重要的非金属元素,在日常生活和化工生产中有广泛的应用。回答下列问题:
(1)C、N、O的第三电离能由大到小的顺序是_______ ,电负性由大到小的顺序是_______ 。
(2)三氟化硼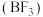 是一种无色气体,用于制造火箭的高能燃料。
是一种无色气体,用于制造火箭的高能燃料。 水解生成
水解生成 和另一种一元无氧酸(甲),甲中B的杂化方式是
和另一种一元无氧酸(甲),甲中B的杂化方式是 ,则甲的化学式是
,则甲的化学式是_______ 。
(3)已知: 中存在大π键:
中存在大π键: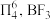 中
中 键的键能是
键的键能是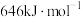 ,而
,而 中
中 键的键能仅
键的键能仅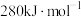 。
。 的分子构型是
的分子构型是_______ ; 中
中 键的键能大于
键的键能大于 中
中 键的键能的原因是
键的键能的原因是_______ 。
(4)亚肼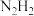 分子中四个原子在同一平面上,有两种结构:
分子中四个原子在同一平面上,有两种结构: 和
和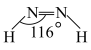 。试推测在水中的溶解度:
。试推测在水中的溶解度:
_______  (填“大于”或“小于”)。
(填“大于”或“小于”)。
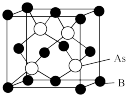
(5)超高热导率半导体材料一砷化硼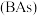 的晶胞结构如图所示,已知阿伏加德罗常数的值为
的晶胞结构如图所示,已知阿伏加德罗常数的值为 ,若该晶体的密度为
,若该晶体的密度为 ,则该晶胞中
,则该晶胞中 原子到B原子的最近距离为
原子到B原子的最近距离为_______  (列出含p、
(列出含p、 的计算式即可)。
的计算式即可)。
(1)C、N、O的第三电离能由大到小的顺序是
(2)三氟化硼
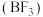 是一种无色气体,用于制造火箭的高能燃料。
是一种无色气体,用于制造火箭的高能燃料。 水解生成
水解生成 和另一种一元无氧酸(甲),甲中B的杂化方式是
和另一种一元无氧酸(甲),甲中B的杂化方式是 ,则甲的化学式是
,则甲的化学式是(3)已知:
 中存在大π键:
中存在大π键: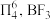 中
中 键的键能是
键的键能是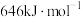 ,而
,而 中
中 键的键能仅
键的键能仅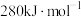 。
。 的分子构型是
的分子构型是 中
中 键的键能大于
键的键能大于 中
中 键的键能的原因是
键的键能的原因是(4)亚肼
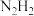 分子中四个原子在同一平面上,有两种结构:
分子中四个原子在同一平面上,有两种结构: 和
和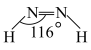 。试推测在水中的溶解度:
。试推测在水中的溶解度:
 (填“大于”或“小于”)。
(填“大于”或“小于”)。(5)超高热导率半导体材料一砷化硼
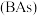 的晶胞结构如图所示,已知阿伏加德罗常数的值为
的晶胞结构如图所示,已知阿伏加德罗常数的值为 ,若该晶体的密度为
,若该晶体的密度为 ,则该晶胞中
,则该晶胞中 原子到B原子的最近距离为
原子到B原子的最近距离为 (列出含p、
(列出含p、 的计算式即可)。
的计算式即可)。
您最近半年使用:0次
6 . 高纯硅可以采用下列方法制备.下列说法正确的是

| A.晶体Si导电性介于导体和绝缘体之间,常用于制造光导纤维 |
B.可以通过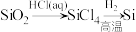 实现粗硅的制备 实现粗硅的制备 |
C.步骤①的反应为 ,不能说明碳的非金属性比硅强 ,不能说明碳的非金属性比硅强 |
D.已知电负性: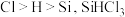 遇水会剧烈反应,化学方程式为 遇水会剧烈反应,化学方程式为 |
您最近半年使用:0次
名校
解题方法
7 . 硼单质及其化合物有重要的应用。阅读下列材料,回答问题:
硼晶体熔点为2076℃。BF3可与NH3反应生成NH3·BF3。乙硼烷(B2H6)具有还原性,易水解生成H3BO3 (一元弱酸);乙硼烷可与NH3反应生成氨硼烷(NH3·BH3),其在一定条件下可以脱氢,最终得到氮化硼;乙硼烷也可与NaH反应生成NaBH4。
(1)下列说法正确的是___________(填字母)。
(2)基态硼原子的最高能级电子排布式是___________ ;单质硼的晶体类型是___________ ;写出H3BO3的电离方程式:___________ ;F-B-F键角比较:BF3___________ (填写“>”“<”) NH3·BF3; 的空间结构是
的空间结构是___________ 。
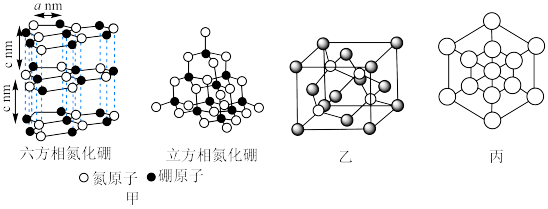
(3)氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂,但不能导电。立方相氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如图甲所示。
①六方氮化硼中,距离B原子最近的B原子个数为___________ 。若阿伏加德罗常数的数值为NA,晶体相关参数如图所示,晶体密度为___________ g/cm3(用含有a、c、NA的式子表示)。
②另一种立方BN晶体与金刚石结构相似,其晶胞结构如图乙。图丙中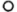 表示N原子的投影位置,在图中用
表示N原子的投影位置,在图中用 标出B原子的投影位置
标出B原子的投影位置___________ 。
硼晶体熔点为2076℃。BF3可与NH3反应生成NH3·BF3。乙硼烷(B2H6)具有还原性,易水解生成H3BO3 (一元弱酸);乙硼烷可与NH3反应生成氨硼烷(NH3·BH3),其在一定条件下可以脱氢,最终得到氮化硼;乙硼烷也可与NaH反应生成NaBH4。
(1)下列说法正确的是___________(填字母)。
| A.元素的电负性大小顺序是O>N>B>H |
| B.乙硼烷水解方程式为B2H6+6H2O=2H3BO3+6H2↑ |
| C.氨硼烷分子中N提供孤电子对,B提供空轨道形成配位键 |
| D.NaBH4晶体中存在的相互作用有离子键、共价键、氢键 |
(2)基态硼原子的最高能级电子排布式是
 的空间结构是
的空间结构是(3)氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂,但不能导电。立方相氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如图甲所示。
①六方氮化硼中,距离B原子最近的B原子个数为
②另一种立方BN晶体与金刚石结构相似,其晶胞结构如图乙。图丙中
 表示N原子的投影位置,在图中用
表示N原子的投影位置,在图中用 标出B原子的投影位置
标出B原子的投影位置
您最近半年使用:0次
解题方法
8 . X、Y、Z、W的原子序数依次增大的前四周期元素,X的基态原子核外电子位于四个原子轨道上,Y与X位于同一周期, 与
与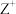 具有相同的电子构型,W为过渡元素,其基态原子最外层电子数与基态Cu原子最外层电子数相同。下列说法正确的是
具有相同的电子构型,W为过渡元素,其基态原子最外层电子数与基态Cu原子最外层电子数相同。下列说法正确的是
 与
与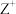 具有相同的电子构型,W为过渡元素,其基态原子最外层电子数与基态Cu原子最外层电子数相同。下列说法正确的是
具有相同的电子构型,W为过渡元素,其基态原子最外层电子数与基态Cu原子最外层电子数相同。下列说法正确的是A. 分子是一种弱电解质 分子是一种弱电解质 |
| B.电负性:Y>X>Z>W |
C.Y、W形成的 的结构式可表示为 的结构式可表示为 |
| D.工业上用相同的方法制备Z单质和W单质 |
您最近半年使用:0次
9 . 氮氧化物会导致光化学烟雾和酸雨,在 的催化作用下,
的催化作用下, 可将NO还原为无污染的气体,反应历程如图,下列说法正确的是
可将NO还原为无污染的气体,反应历程如图,下列说法正确的是
 的催化作用下,
的催化作用下, 可将NO还原为无污染的气体,反应历程如图,下列说法正确的是
可将NO还原为无污染的气体,反应历程如图,下列说法正确的是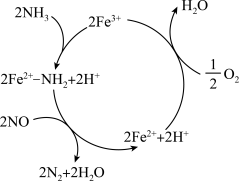
A.基态 的价层电子排布式为 的价层电子排布式为 |
| B.电负性:N>O>H>Fe |
| C.该过程中存在极性键和非极性键的断裂和形成 |
D.图中的总反应可表示为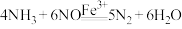 |
您最近半年使用:0次
2024-02-25更新
|
260次组卷
|
5卷引用:山东省青岛市莱西市2023-2024学年高二上学期1月期末考试化学试题
10 . 结构决定性质,下列性质差异与结构因素匹配错误的是
| 选项 | 性质差异 | 结构因素 |
| A | 键能:F-F键<Cl-Cl键 | 电负性 |
| B | 稳定性:H2O>H2S | 半径:O<S |
| C | 酸性:HClO3<HClO4 | 羟基极性 |
| D | 沸点:正戊烷>新戊烷 | 分子间作用力 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次



