名校
1 . 环戊二烯可用于制备二茂铁 [Fe(C5H5)2];二茂铁分子是一种金属有机配合物,结构如图所示,是燃料油的添加剂,用以提高燃烧的效率和去烟,可作为导弹和卫星的涂料等。下列说法正确的是
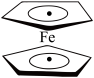

A.1 mol环戊二烯(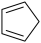 )中含有5 mol σ键 )中含有5 mol σ键 |
| B.环戊二烯分子中所有原子共平面 |
| C.二茂铁分子中存在配位键 |
| D.Fe2+的价电子排布式为3d44s2 |
您最近一年使用:0次
2020-05-26更新
|
131次组卷
|
3卷引用:重庆市万州第二高级中学2021-2022学年高二下学期期中考试化学试题
名校
解题方法
2 . 下列物质中,分子的立体结构与水分子相似的是 ( )
| A.CO2 | B.H2S | C.PCl3 | D.SiCl4 |
您最近一年使用:0次
2020-05-23更新
|
753次组卷
|
11卷引用:重庆市荣昌永荣中学校2021-2022学年高二下学期期末考试化学试题
重庆市荣昌永荣中学校2021-2022学年高二下学期期末考试化学试题2016-2017学年河北省张家口一中高二12月月考化学卷广西靖西市第二中学2019-2020学年高二下学期开学考试化学试题山东省淄博市般阳中学2020-2021学年高二上学期期中考试化学试题(人教版2019)选择性必修2 第二章 分子结构与性质 第二节 分子的空间结构(人教版2019)选择性必修2 第二章 分子结构与性质 章末综合检测卷(鲁科版2019)选择性必修2 第2章 微粒间相互作用与物质性质 第2节 共价键与分子的空间结构(已下线)2.2.1 分子空间结构的理论分析-2020-2021学年高二化学课时同步练(鲁科2019选择性必修2)宁夏海原第一中学2020-2021学年高二下学期期末考试化学试题吉林地区普通高中友好学校联合体2021-2022学年高二下学期期末考试化学试题第二节 分子的空间结构 第1课时 分子结构的测定 多样的分子空间结构 价层电子对互斥模型
名校
3 . X、Y、Z、W是四种原子序数依次增大的短周期元素,W的最外层电子数比X的最外层电子数少1个,X、Y、Z为同一周期元素,X、Y、Z组成一种化合物(ZXY)2的结构式如图所示。下列叙述不正确的是( )
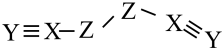
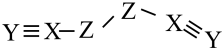
| A.化合物(ZXY)2中Z元素的化合价为-2价 |
| B.Y的氧化物对应的水化物可能是弱酸 |
| C.(ZXY)2分子中X原子的杂化方式为sp杂化 |
| D.X、Y、Z、W四种元素电负性的大小顺序为:Z>Y>X>W |
您最近一年使用:0次
2020-05-20更新
|
134次组卷
|
3卷引用:重庆市第八中学2020-2021学年高二下学期期中考试化学试题
4 . 铁及其化合物在生产生活中有着广泛的应用。回答下列问题:
(1)基态Fe原子的外围电子排布图为____ ,基态Fe2+中,核外电子占据最高能层的符号是____ ,Fe2+和Fe3+是铁的两种常见离子,Fe3+的稳定性强于Fe2+,原因是____ 。
(2)Fe3+可以与SCN—形成一系列不同配位数的红色配合物,所以常用KSCN溶液检验Fe3+的存在,KSCN中四种元素的电负性由小到大的顺序为_______ ,SCN—的几何构型为______ ,中心原子的杂化类型为_______ 。
(3)实验中常用K3[Fe(CN)6]检验Fe2+, K3[Fe(CN)6]晶体中的化学键有_________ (填写选项字母)
a.离子键. b.共价键 c,氢键 d .配位键 e.金属键
1mol K3[Fe(CN)6]中含有σ键与π键的数目比为_____________ 。
(4)FexO为氯化钠型结构,在实际晶体中,由于存在缺陷,x<1。 测得Fe0.92O晶体的晶胞参数a=428.0pm,则该晶体的密度ρ=__________ g/cm3 (列出计算式),晶体中最近的两个铁离子间的距离为_______ pm。
(1)基态Fe原子的外围电子排布图为
(2)Fe3+可以与SCN—形成一系列不同配位数的红色配合物,所以常用KSCN溶液检验Fe3+的存在,KSCN中四种元素的电负性由小到大的顺序为
(3)实验中常用K3[Fe(CN)6]检验Fe2+, K3[Fe(CN)6]晶体中的化学键有
a.离子键. b.共价键 c,氢键 d .配位键 e.金属键
1mol K3[Fe(CN)6]中含有σ键与π键的数目比为
(4)FexO为氯化钠型结构,在实际晶体中,由于存在缺陷,x<1。 测得Fe0.92O晶体的晶胞参数a=428.0pm,则该晶体的密度ρ=
您最近一年使用:0次
2020-05-20更新
|
386次组卷
|
3卷引用:重庆市第八中学2020届高三高考模拟试卷化学试题(三)
解题方法
5 . 铜是人类知道最早的金属之一,也是广泛使用的第一种金属。回答下列问题:
(1)镍白铜(铜镍合金)可用于制作仿银饰品。第二电离能I2(Cu)______________ Ⅰ2(Ni)(填“>"或 “<”),其原因为______________ 。
(2)向[Cu(NH3)2]Cl溶液中通入乙炔(C2H2)气体,可生成红棕色沉淀Cu2C2。
①C2H2分子中 键与
键与 键的数目之比为
键的数目之比为______________ ;碳原子的杂化方式为______________ 。
②写出与Cu2C2中阴离子C22-互为等电子体的一种分子和一种离子______________ 。
(3)乙二胺(H2N-CH2CH2-NH2)易与Cu2+形成络合物用于Cu2+的定量测定。
①形成的络合物中提供孤对电子的原子为______________ (填元素符号)。
②乙二胺中所含元素的电负性由大到小的顺序为______________ ;乙二胺在水中溶解度较大的原因为______________ 。
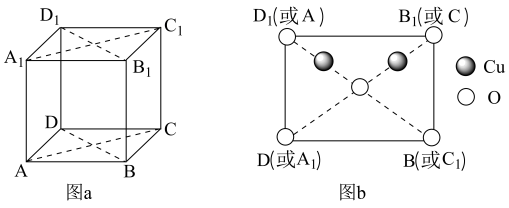
(4)铜与氧构成的某种化合物的立方晶胞如图a所示,图b是沿晶胞对角面取得的截图,晶胞中所有原子均在对角面上。氧原子的配位数为______________ ,若Cu原子之间最短距离为dpm,阿伏加 德罗常数的值为NA,该晶体的密度为______________ g·cm-3(列出计算式即可)。
(1)镍白铜(铜镍合金)可用于制作仿银饰品。第二电离能I2(Cu)
(2)向[Cu(NH3)2]Cl溶液中通入乙炔(C2H2)气体,可生成红棕色沉淀Cu2C2。
①C2H2分子中
 键与
键与 键的数目之比为
键的数目之比为②写出与Cu2C2中阴离子C22-互为等电子体的一种分子和一种离子
(3)乙二胺(H2N-CH2CH2-NH2)易与Cu2+形成络合物用于Cu2+的定量测定。
①形成的络合物中提供孤对电子的原子为
②乙二胺中所含元素的电负性由大到小的顺序为
(4)铜与氧构成的某种化合物的立方晶胞如图a所示,图b是沿晶胞对角面取得的截图,晶胞中所有原子均在对角面上。氧原子的配位数为

您最近一年使用:0次
2020-05-17更新
|
137次组卷
|
2卷引用:重庆市重点中学2021届高三下学期开学考试(新高考)化学试题
解题方法
6 . 铜及其化合物在生产生活中有着广泛的应用。请回答下列问题:
(1)铜元素位于元素周期表中第四周期________ 族,属于元素周期表中________ 区元素,基态Cu原子有___________ 种不同能级的电子。
(2)元素铜与镍的第二电离能分别为:ICu=1958 kJ·mol-1、INi=1753 kJ·mol-1, ICu>INi的原因是________________________________________________________ 。
(3)硫化亚铜和氧化亚铜均为离子晶体,二者比较,熔点较高的是氧化亚铜,原因为_________________________________________ 。
(4)某含铜化合物的离子结构如图1所示。

①该离子中存在的作用力有______________ (填标号)。
A.离子键 B.共价键 C.配位键 D.氢键 E.范德华力
②该离子中碳原子的杂化类型有____________ 。
(5)CuCl2和CuCl是铜的两种氯化物。
①图2中表示的是________ (填“CuCl2”或“CuCl”)的晶胞。
②原子坐标参数可用来表示晶胞内部各原子的相对位置。图2中各原子坐标参数A为(0,0,0);B为(0,1,1);C为(1,1,0);则D原子的坐标参数为____________ 。
③已知图2所示晶胞中C、D两原子核间距为298pm,阿伏加 德罗常数的值为NA,则该晶体密度为___________________ g·cm-3(列出计算式即可)。
(1)铜元素位于元素周期表中第四周期
(2)元素铜与镍的第二电离能分别为:ICu=1958 kJ·mol-1、INi=1753 kJ·mol-1, ICu>INi的原因是
(3)硫化亚铜和氧化亚铜均为离子晶体,二者比较,熔点较高的是氧化亚铜,原因为
(4)某含铜化合物的离子结构如图1所示。

①该离子中存在的作用力有
A.离子键 B.共价键 C.配位键 D.氢键 E.范德华力
②该离子中碳原子的杂化类型有
(5)CuCl2和CuCl是铜的两种氯化物。
①图2中表示的是
②原子坐标参数可用来表示晶胞内部各原子的相对位置。图2中各原子坐标参数A为(0,0,0);B为(0,1,1);C为(1,1,0);则D原子的坐标参数为
③已知图2所示晶胞中C、D两原子核间距为298pm,阿伏加 德罗常数的值为NA,则该晶体密度为
您最近一年使用:0次
名校
解题方法
7 . 钢化玻璃因其优良的性能广泛应用于日常生活,但由于制作玻璃时里面含有极少量硫化镍,使得钢化玻璃在极限条件下的使用受到限制。
(1)基态硫原子价层电子的轨道表达式 电子排布图
电子排布图 为
为__ ,基态镍原子中核外电子占据最高能层的符号为__ 。
(2)Ni(CO)4常用于制备纯镍,溶于乙醇、CCl4、苯等有机溶剂,为__ 晶体,Ni(CO)4空间构型与甲烷相同,中心原子的杂化轨道类型为__ ,写出与配体互为等电子体的阴离子__  任写一种
任写一种 。
。
(3)与硫同族的硒元素有两种常见的二元含氧酸,请比较它们酸性强弱__ >__  填化学式
填化学式 ,理由是
,理由是__ 。
(4)H2S的键角__ 填“大于”“小于”“等于”)H2O的键角,请从电负性的角度说明理由__ 。
(5)NiO与NaCl的晶胞结构相似,如图所示,阴离子采取面心立方堆积,阳离子填充在位于阴离子构成的__ 空隙中,已知Ni2+半径为69nm,O2-半径为140nm,阿伏加 德罗常数为NA,NiO晶体的密度为__ g/cm3(只列出计算式 。
。

(1)基态硫原子价层电子的轨道表达式
 电子排布图
电子排布图 为
为(2)Ni(CO)4常用于制备纯镍,溶于乙醇、CCl4、苯等有机溶剂,为
 任写一种
任写一种 。
。(3)与硫同族的硒元素有两种常见的二元含氧酸,请比较它们酸性强弱
 填化学式
填化学式 ,理由是
,理由是(4)H2S的键角
(5)NiO与NaCl的晶胞结构相似,如图所示,阴离子采取面心立方堆积,阳离子填充在位于阴离子构成的
 。
。
您最近一年使用:0次
名校
解题方法
8 . 元素A、B、C、D、E的原子序数依次增大,且均小于36。A的基态原子2p能级有3个单电子;C的基态原子2p能级有1个单电子;D的价电子数为2且与E同周期;E的基态原子的内部各能层均排满,且4s能级有1个单电子。回答下列问题:
(1)基态E原子的价电子排布式为____________________
(2)A、B、C三种元素第一电离能由大到小的顺序为___________ (用元素符号表示)。
(3)与A的单质分子互为等电子体的分子和离子分别是________ (用分子和离子符号表示)。AB2的空间构型为___________ ,其中A原子的杂化类型是_______________
(4)B元素简单氢化物的沸点是同族元素中最高的,原因是_____________
(5)向含E元素的硫酸盐溶液中加入过量氨水,可得到深蓝色透明溶液。向溶液中加入乙醇,将析出深蓝色晶体。该晶体的化学式为[Cu(NH3)4]SO4∙H2O晶体中阳离子的结构式为____________
(6)C和D形成化合物的晶胞结构如图所示,已知晶体的密度为ρg/cm,阿伏加 德罗常数为NA,则晶胞边长a=______________ cm(用含ρ、NA的计算式表示)。

(1)基态E原子的价电子排布式为
(2)A、B、C三种元素第一电离能由大到小的顺序为
(3)与A的单质分子互为等电子体的分子和离子分别是
(4)B元素简单氢化物的沸点是同族元素中最高的,原因是
(5)向含E元素的硫酸盐溶液中加入过量氨水,可得到深蓝色透明溶液。向溶液中加入乙醇,将析出深蓝色晶体。该晶体的化学式为[Cu(NH3)4]SO4∙H2O晶体中阳离子的结构式为
(6)C和D形成化合物的晶胞结构如图所示,已知晶体的密度为ρg/cm,阿伏加 德罗常数为NA,则晶胞边长a=

您最近一年使用:0次
2020-05-09更新
|
105次组卷
|
2卷引用:重庆市凤鸣山中学2020届高三6月月考理综化学试题
名校
解题方法
9 . 据世界权威刊物《自然》最近报道,我国科学家选择碲化锆(ZrTe2)和砷化镉(Cd3As2)为材料验证了三维量子霍尔效应,并发现了金属-绝缘体的转换。回答下列问题:
(1)锌和镉位于同副族,而锌与铜相邻。现有 4 种铜、锌元素的相应状态,①锌:[Ar]3d104s2、②锌:[Ar]3d104s1、③铜:[Ar]3d104s1、④铜:[Ar]3d10。失去1个电子需要的能量由大到小排序是______ (填字母)。
A.④②①③ B.④②③① C.①②④③ D.①④③②
(2)硫和碲位于同主族,H2S的分解温度高于H2Te,其主要原因是_______ 。在硫的化合物中,H2S、CS2都是三原子分子,但它们的键角(立体构型)差别很大,用价层电子对互斥理论解释:_________ ;用杂化轨道理论解释:_________ 。
(3)Cd2+与NH3等配体形成配离子。[Cd(NH3)4]2+中2个NH3被2个Cl-替代只得到1种结构,它的立体构型是___________ 。1 mol [Cd(NH3)4]2+含___________ mol σ键。
(4)砷与卤素形成多种卤化物。AsCl3、AsF3、AsBr3的熔点由高到低的排序为__________ 。
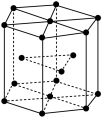
(5)锆晶胞如图所示,1个晶胞含_______ 个Zr原子;这种堆积方式称为__________ 。
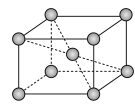
(6)镉晶胞如图所示。已知:NA是阿伏加 德罗常数的值,晶体密度为 d g·cm-3。在该晶胞中两个镉原子最近核间距为______ nm(用含NA、d的代数式表示),镉晶胞中原子空间利用率为________ (用含π的代数式表示)。
(1)锌和镉位于同副族,而锌与铜相邻。现有 4 种铜、锌元素的相应状态,①锌:[Ar]3d104s2、②锌:[Ar]3d104s1、③铜:[Ar]3d104s1、④铜:[Ar]3d10。失去1个电子需要的能量由大到小排序是
A.④②①③ B.④②③① C.①②④③ D.①④③②
(2)硫和碲位于同主族,H2S的分解温度高于H2Te,其主要原因是
(3)Cd2+与NH3等配体形成配离子。[Cd(NH3)4]2+中2个NH3被2个Cl-替代只得到1种结构,它的立体构型是
(4)砷与卤素形成多种卤化物。AsCl3、AsF3、AsBr3的熔点由高到低的排序为
(5)锆晶胞如图所示,1个晶胞含

(6)镉晶胞如图所示。已知:NA是阿伏加 德罗常数的值,晶体密度为 d g·cm-3。在该晶胞中两个镉原子最近核间距为

您最近一年使用:0次
2020-04-23更新
|
371次组卷
|
3卷引用:重庆市第一中学2019-2020学年高二下学期期末考试化学试题
名校
解题方法
10 . 储氢材料是一类能可逆地吸收和释放氢气的材料。LaNi5合金、NaBH4、H3B-NH3、Mg2NiH4等都是潜在储氢材料。回答下列问题:
(1)基态Ni原子的核外电子排布式为____ ,有___________ 个未成对的电子;
(2)NaBH4中H为-1价,Na、B、H电负性由大到小的顺序是_________ 。BH4-离子的立体构型为________ ,其中B的杂化轨道类型为_____ 。
(3)B2H6和NH3化合可以生成H3B-NH3,H3B-NH3加热时发生反应:H3B-NH3=BN+3H2,缓慢释放出H2。BN有类似于石墨的结构,B2H6、NH3和BN的沸点由高到低的顺序为_________ , 原因是___ 。
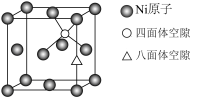
(4)X-射线衍射分析表明,Mg2NiH4 的立方晶胞的面心和顶点均被Ni原子占据,所有Mg原子的Ni配位数都相等。则Mg原子填入由Ni原子形成的_____ 空隙中(填“四面体”或“八面体”),其空隙占有百分率为_____ 。
(5)已知Mg2NiH4 晶体的晶胞参数为646.5 pm,液氢的密度为0.0708 g·cm-3。若以材料中氢的密度与液态氢密度之比定义储氢材料的储氢能力,则Mg2NiH4 的储氢能力是液氢的___ 倍(列出计算式即可)。
(1)基态Ni原子的核外电子排布式为
(2)NaBH4中H为-1价,Na、B、H电负性由大到小的顺序是
(3)B2H6和NH3化合可以生成H3B-NH3,H3B-NH3加热时发生反应:H3B-NH3=BN+3H2,缓慢释放出H2。BN有类似于石墨的结构,B2H6、NH3和BN的沸点由高到低的顺序为
(4)X-射线衍射分析表明,Mg2NiH4 的立方晶胞的面心和顶点均被Ni原子占据,所有Mg原子的Ni配位数都相等。则Mg原子填入由Ni原子形成的
(5)已知Mg2NiH4 晶体的晶胞参数为646.5 pm,液氢的密度为0.0708 g·cm-3。若以材料中氢的密度与液态氢密度之比定义储氢材料的储氢能力,则Mg2NiH4 的储氢能力是液氢的

您最近一年使用:0次



