名校
解题方法
1 . 标准状况下,V L某气体(此气体不与水反应)溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为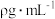 ,溶质的摩尔质量为
,溶质的摩尔质量为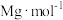 ,溶质的质量分数为w,溶质的物质的量浓度为
,溶质的质量分数为w,溶质的物质的量浓度为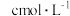 ,溶液的体积为
,溶液的体积为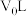 ,下列关系中正确的是
,下列关系中正确的是
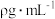 ,溶质的摩尔质量为
,溶质的摩尔质量为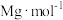 ,溶质的质量分数为w,溶质的物质的量浓度为
,溶质的质量分数为w,溶质的物质的量浓度为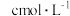 ,溶液的体积为
,溶液的体积为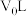 ,下列关系中正确的是
,下列关系中正确的是A.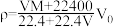 | B. |
C.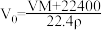 | D.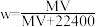 |
您最近一年使用:0次
2021-01-11更新
|
2127次组卷
|
3卷引用:四川省攀枝花市成都外国语学校2021-2022学年高一上学期期中考试化学试题
2 . 一定温度下,在3个体积均为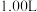 的恒容密闭容器中发生反应
的恒容密闭容器中发生反应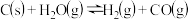
 ,相关数据如下表(已知:炭粉足量)。
,相关数据如下表(已知:炭粉足量)。
下列说法错误的是
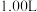 的恒容密闭容器中发生反应
的恒容密闭容器中发生反应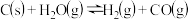
 ,相关数据如下表(已知:炭粉足量)。
,相关数据如下表(已知:炭粉足量)。| 容器 | T/℃ | 物质的起始浓度/( ) ) | 物质的平衡浓度
| ||
 |  | 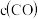 | |||
| Ⅰ |  | 1.00 | 0 | 0 | 0.85 |
| Ⅱ |  | 0 | 1.00 | 1.00 | x |
| Ⅲ |  | 2.00 | 0 | 0 | 1.60 |
A. | B.达到平衡所需时间: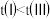 |
C.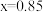 | D. ℃,该反应的化学平衡常数 ℃,该反应的化学平衡常数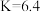 |
您最近一年使用:0次
2021-01-10更新
|
2126次组卷
|
5卷引用:四川省成都市蒲江县蒲江中学2021-2022学年高二下学期5月月考化学试题
解题方法
3 . 氮化物应用广泛,如叠氮化钠(NaN3)是典型的高能量密度含能材料,氮化硼是特殊的耐磨和切削材料,氮化铬、氮化钼等过渡金属氮化物常用作高强度材料。回答下列问题:
(1)Na、N、B中,原子半径由大到小的顺序是___________ 。
(2)基态N原子价层电子的电子排布图为___________ 。基态铬原子核外未成对电子数为___________ 。
(3)NaN3中阴离子N 是直线型离子。1个N
是直线型离子。1个N 中的σ键数目为
中的σ键数目为___________ 。分子或离子中的大π键可用符号Π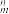 表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如CO2分子中存在两个大π键Π
表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如CO2分子中存在两个大π键Π ),则N
),则N 中的大π键应表示为
中的大π键应表示为___________ 。
(4)石墨型(BN)x转变为金刚石型(BN)x时,B原子的杂化轨道类型由___________ 变为___________ 。金刚石型(BN)x的硬度比金刚石大,推测其原因是___________ 。
(5)氮化钼作为锂离子电池负极材料具有很好的发展前景。它属于填隙式氮化物,N原子部分填充在Mo原子立方晶格的八面体空隙中,晶胞结构如图所示。
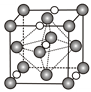
氮化钼的化学式为___________ ,如果让Li+填入氮化钼晶体的八面体空隙,一个晶胞最多可以填入___________ 个Li+。氮化钼晶胞边长为a nm,晶体的密度ρ=___________ g·cm-3(列出计算式,设NA为阿伏加德罗常数的值)。
(1)Na、N、B中,原子半径由大到小的顺序是
(2)基态N原子价层电子的电子排布图为
(3)NaN3中阴离子N
 是直线型离子。1个N
是直线型离子。1个N 中的σ键数目为
中的σ键数目为 表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如CO2分子中存在两个大π键Π
表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如CO2分子中存在两个大π键Π ),则N
),则N 中的大π键应表示为
中的大π键应表示为(4)石墨型(BN)x转变为金刚石型(BN)x时,B原子的杂化轨道类型由
(5)氮化钼作为锂离子电池负极材料具有很好的发展前景。它属于填隙式氮化物,N原子部分填充在Mo原子立方晶格的八面体空隙中,晶胞结构如图所示。

氮化钼的化学式为
您最近一年使用:0次
名校
4 . 钪是地壳中含量极少的稀土元素,但在照明、合金和陶瓷材料、催化化学等领域具有重要应用价值。钛铁矿主要成分为TiO2、FeO、Fe2O3,还含有Mg、Si、Sc等元素,从钛铁矿中提取Sc2O3的流程如下:

回答下列问题:
(1)“酸浸”时,为提高浸取效率,可以采取的措施有___________ (答两个)。滤渣1的主要成分是___________ 。
(2)“酸浸”后Ti元素转化为TiOSO4,其水解反应的化学方程式是___________ 。
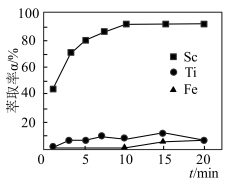
(3)“萃取”时,使用10%P2O4+5%TBP+煤油作为萃取剂,一定条件下萃取率α受振荡时间的影响如图,萃取时适宜的振荡时间为___________ min。“洗钛”所得[TiO(H2O2)]2+为橘黄色的稳定离子,其中氧的化合价有-2、-1两种,则Ti的化合价为___________ 。
(4)“酸溶”后滤液中存在的金属阳离子Sc3+、TiO2+、Fe3+浓度均小于0.01 mol/L,再用氨水调节溶液pH使TiO2+、Fe3+沉淀完全而Sc3+不沉淀,则调pH应控制的pH范围是___________ 。
已知:当离子浓度减小至10-5 mol/L时可认为沉淀完全。lg2=0.3;室温下TiO2+完全沉淀的pH为1.05,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Sc(OH)3]=1.25×10-33。
(5)加草酸“沉钪”的离子方程式为___________ 。
(6)“沉钪”后获得Sc2O3的方法是___________ ,该反应产生的气体必须回收利用,其意义是___________ 。

回答下列问题:
(1)“酸浸”时,为提高浸取效率,可以采取的措施有
(2)“酸浸”后Ti元素转化为TiOSO4,其水解反应的化学方程式是
(3)“萃取”时,使用10%P2O4+5%TBP+煤油作为萃取剂,一定条件下萃取率α受振荡时间的影响如图,萃取时适宜的振荡时间为

(4)“酸溶”后滤液中存在的金属阳离子Sc3+、TiO2+、Fe3+浓度均小于0.01 mol/L,再用氨水调节溶液pH使TiO2+、Fe3+沉淀完全而Sc3+不沉淀,则调pH应控制的pH范围是
已知:当离子浓度减小至10-5 mol/L时可认为沉淀完全。lg2=0.3;室温下TiO2+完全沉淀的pH为1.05,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Sc(OH)3]=1.25×10-33。
(5)加草酸“沉钪”的离子方程式为
(6)“沉钪”后获得Sc2O3的方法是
您最近一年使用:0次
2021-01-07更新
|
1949次组卷
|
7卷引用:四川省自贡市田家炳中学2021届高三12月月考化学试题
四川省自贡市田家炳中学2021届高三12月月考化学试题四川省绵阳南山中学2021-2022学年高三上学期入学考试理综化学试题四川省泸州市泸县第四中学2022届高三三诊模拟考试理科综合化学试题四川省绵阳市梓潼中学校2023-2024学年高三上学期入学考试理科综合化学试题(已下线)解密06 金属及其化合物(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密06 金属及其化合物(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)工业流程题
名校
解题方法
5 . 常温下,向1L 1.0mol/L的NaClO溶液中缓慢通入SO2气体,使其充分吸收,溶液pH与通入SO2物质的量关系如图所示(忽略溶液体积的变化和NaClO、HClO的分解)。下列说法错误的是
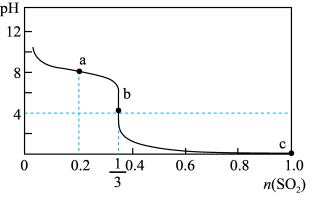

| A.常温下,HClO电离平衡常数的数量级为10﹣8 |
| B.a点溶液中存在 4c(Cl-)=c(HClO)+c(ClO-) |
C.b点溶液中存在c(Na+)>c(SO )>c(Cl-)>c(H+)>c(OH-) )>c(Cl-)>c(H+)>c(OH-) |
| D.c点溶液中c(H+)=2mol/L |
您最近一年使用:0次
2020-11-12更新
|
1729次组卷
|
5卷引用:四川省阆中中学2021届高三上学期开学考试化学试题
10-11高二上·吉林·期中
名校
解题方法
6 . 在容积恒定的密闭容器中充入2molA和1molB发生反应:2A(g)+B(g) xC(g),达到平衡后,C的体积分数为w;若维持容器的容积和温度不变,按起始物质的量:0.6molA(g)、0.3molB(g)和1.4molC(g)充入容器,达到平衡后,C的体积分数仍为w,则x的值为( )
xC(g),达到平衡后,C的体积分数为w;若维持容器的容积和温度不变,按起始物质的量:0.6molA(g)、0.3molB(g)和1.4molC(g)充入容器,达到平衡后,C的体积分数仍为w,则x的值为( )
 xC(g),达到平衡后,C的体积分数为w;若维持容器的容积和温度不变,按起始物质的量:0.6molA(g)、0.3molB(g)和1.4molC(g)充入容器,达到平衡后,C的体积分数仍为w,则x的值为( )
xC(g),达到平衡后,C的体积分数为w;若维持容器的容积和温度不变,按起始物质的量:0.6molA(g)、0.3molB(g)和1.4molC(g)充入容器,达到平衡后,C的体积分数仍为w,则x的值为( )| A.只能为2 | B.只能为3 |
| C.可能为2,也可能为3 | D.无法确定 |
您最近一年使用:0次
2020-10-31更新
|
1298次组卷
|
19卷引用:四川省成都市实验外国语学校(西区)2019-2020 学年高二上学期期中考试化学试题
四川省成都市实验外国语学校(西区)2019-2020 学年高二上学期期中考试化学试题(已下线)2010年吉林省吉林一中高二上学期期中考试化学试题(已下线)2015届甘肃省肃南县第一中学高三10月月考理综化学试卷2015-2016学年广东省宝安第一外国语学校高二上期中考试化学试卷山西省太原市山西大学附属中学2015-2016学年高二下2月模块诊断化学卷2016-2017学年河南省漯河中学高二上第一次月考化学卷河北省张家口市第一中学2016-2017学年高一(衔接班)下学期期末考试(理)化学试题2018版化学(苏教版)高考总复习专题七增分补课7--化学平衡分析中的虚拟过程--化学反应的方向和限度辽宁省辽阳2017-2018学年高二化学上学期期末考试题河南省安阳县第一高级中学2017-2018学年高二上学期第三次月考化学试卷河北省安平中学2019届高三上学期第五次月考化学试题【市级联考】福建省三明市2019届高三上学期期末质量检测化学试题甘肃省白银市会宁县第一中学2019-2020学年高二上学期期中考试化学(理)试题黑龙江省绥化市明水县第一中学2020-2021学年高二上学期第一次月考化学试题北京二中2020-2021学年高二上学期10月月考化学试题河北省邢台市第二中学2021届高三上学期第四次月考化学试题河南省延津第一高级中学2021-2022学年高二上学期第五次考试化学试题陕西省宝鸡市长岭中学2021-2022学年高二上学期期中考试化学试题江西省临川一中暨临川一中实验学校2021-2022学年高二上学期期末考试化学试题
名校
解题方法
7 . 25℃时, 用0.10mol/L的氨水滴定10.00mL 0.05mol/L的二元酸H2A的溶液,滴定过程中加入氨水的体积(V)与溶液中 的关系如图所示。下列说法错误的是( )
的关系如图所示。下列说法错误的是( )
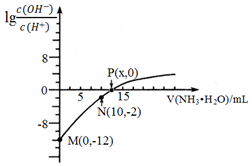
 的关系如图所示。下列说法错误的是( )
的关系如图所示。下列说法错误的是( )
| A.H2A为强电解质,是一种强酸 |
| B.M、N、P三点的溶液中,水电离程度最大的是N点 |
C.P点溶液中,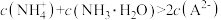 |
| D.25℃时,氨水的电离平衡常数:K=10-7/(0.2x-1) |
您最近一年使用:0次
2020-09-07更新
|
1701次组卷
|
2卷引用:四川省内江市第六中学2021届高三上学期10月月考化学试题
名校
8 . 常温下,向10.00mL浓度均为0.100mol•L-1的NaOH溶液和二甲胺[(CH3)2NH•H2O]的混合溶液中逐滴加入盐酸。利用传感器测得该过程溶液中的阳离子总浓度变化曲线如图;已知二甲胺在水中电离与氨相似,常温下Kb[(CH3)2NH•H2O]=l.60×l0-4。下列说法正确的是( )


| A.a点溶液中,c[(CH3)2NH2+]约为l.60×l0-4mol/L |
| B.从a到c的过程中,水的电离程度最大的是b点 |
| C.c点溶液中:3c(Na+)+c[(CH3)2NH2+]=2c(Cl-) |
| D.V(HCl)=15.00mL时,c[(CH3)2NH2+]<c[(CH3)2NH•H2O] |
您最近一年使用:0次
2020-06-05更新
|
1419次组卷
|
3卷引用:四川省广汉中学2021届高三上学期第一次阶段考试化学试题
名校
解题方法
9 . 下列关于同分异构体的说法正确的是 ( )
| A.分子式为C3H6BrC1的有机物不考虑立体异构共4种 |
| B.C8H11N的同分异构体中含苯环且苯环上有两个取代基的种数为9 |
C.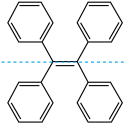 的一氯代物有5种 的一氯代物有5种 |
D.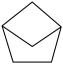 的一氯代物有4种 的一氯代物有4种 |
您最近一年使用:0次
2020-05-17更新
|
1879次组卷
|
3卷引用:四川省成都市成都外国语学校2022届高三下学期第二次诊断性考试理科综合化学试题
10 . 向1.00L浓度均为0.0100mol/L的Na2SO3、NaOH 混合溶液中通入HCl气体调节溶液pH(忽略溶液体积变化)。其中比H2SO3、HSO3-、SO32-平衡时的分布系数(各含硫物种的浓度与含硫物种总浓度的比)随HCl气体体积(标况下)的变化关系如图所示(忽略SO2气体的逸出);已知Ka1代表H2SO3在该实验条件下的一级电离常数。下列说法正确的是


| A.Z点处的pH=-lgKa1(H2SO3) |
| B.从X点到Y点发生的主要反应为SO32- +H2O⇌HSO3- +OH- |
| C.当V(HCl)≥672mL时,c(HSO3-) = c(SO32-)=0mol/L |
| D.若将HCl改为NO2,Y点对应位置不变 |
您最近一年使用:0次



