1 . 2023年化学诺贝尔奖授予三位科学家以表彰他们发现和合成量子点方面做出的贡献.我国化学家研究的一种新型复合光催化剂[碳量子点(CQDS)氮化碳( )纳米复合物]可利用太阳光实现高效分解水,原理如图所示.现以每生成2mol
)纳米复合物]可利用太阳光实现高效分解水,原理如图所示.现以每生成2mol 或1mol
或1mol 计,水分解、反应Ⅰ及反应Ⅱ的焓变依次为
计,水分解、反应Ⅰ及反应Ⅱ的焓变依次为 、
、 、
、 .下列说法错误的是
.下列说法错误的是
 )纳米复合物]可利用太阳光实现高效分解水,原理如图所示.现以每生成2mol
)纳米复合物]可利用太阳光实现高效分解水,原理如图所示.现以每生成2mol 或1mol
或1mol 计,水分解、反应Ⅰ及反应Ⅱ的焓变依次为
计,水分解、反应Ⅰ及反应Ⅱ的焓变依次为 、
、 、
、 .下列说法错误的是
.下列说法错误的是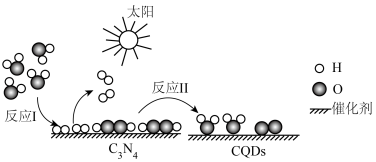
A.反应Ⅰ的化学方程式为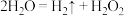 |
| B.该过程涉及太阳能、热能及化学能之间的转化 |
C.该过程实现高效分解水的同时也产生副产物 |
D.若 ,则 ,则 与 与 的大小关系为 的大小关系为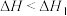 |
您最近一年使用:0次
2024-02-22更新
|
128次组卷
|
2卷引用:山东省青岛市2023-2024学年高二上学期1月期末化学试题
2 . 某离子反应涉及 六种微粒,其中
六种微粒,其中 随反应进行逐渐减小,下列说法正确的是
随反应进行逐渐减小,下列说法正确的是
 六种微粒,其中
六种微粒,其中 随反应进行逐渐减小,下列说法正确的是
随反应进行逐渐减小,下列说法正确的是A.反应中每减少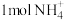 ,转移 ,转移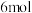 电子 电子 |
B.反应中 被还原 被还原 |
| C.反应前后溶液的酸碱性无明显变化 |
D.参加反应的氧化剂与还原剂的物质的量之比为 |
您最近一年使用:0次
解题方法
3 . 硝酸铈(Ⅳ)铵的化学式为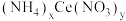 ,是一种橙红色结晶性粉末,易溶于水和乙醇,几乎不溶于浓硝酸,主要用作分析试剂和氧化剂。实验室设计如下实验进行制备并测定其化学式。
,是一种橙红色结晶性粉末,易溶于水和乙醇,几乎不溶于浓硝酸,主要用作分析试剂和氧化剂。实验室设计如下实验进行制备并测定其化学式。
步骤一:NH4HCO3溶液与CeCl3溶液反应制备Ce2(CO3)3。
已知:①氮化钙遇水可迅速产生NH3;②Ce(Ⅲ)易被空气氧化成Ce(Ⅳ)。___________ ,装置C的作用是___________ 。该实验以氮化钙和水制备NH3应选择装置___________ (填“A”或“D”)。
(2)实验时,“a”、“b”、“c”三个旋塞的打开顺序为___________ 。装置B中发生反应的离子方程式为___________ 。
(3)该实验装置存在的一处缺陷为___________ 。
步骤二:制备硝酸铈(Ⅳ)铵___________ 。
(5)“烘干”采取自然干燥的原因为___________ 。
步骤三:测定化学式
①称取一定质量的硝酸铈(Ⅳ)铵,充分灼烧得CeO2mg。
②另称取相同质量的硝酸铈(Ⅳ)铵,加入足量NaOH溶液微热,将产生的气体全部用V1mL水吸收。将吸收液滴入甲基橙,用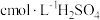 标准溶液滴定,重复2~3次,平均消耗H2SO4标准溶液V2mL。
标准溶液滴定,重复2~3次,平均消耗H2SO4标准溶液V2mL。
(6)计算y=___________ (用上述字母表示)。
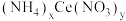 ,是一种橙红色结晶性粉末,易溶于水和乙醇,几乎不溶于浓硝酸,主要用作分析试剂和氧化剂。实验室设计如下实验进行制备并测定其化学式。
,是一种橙红色结晶性粉末,易溶于水和乙醇,几乎不溶于浓硝酸,主要用作分析试剂和氧化剂。实验室设计如下实验进行制备并测定其化学式。步骤一:NH4HCO3溶液与CeCl3溶液反应制备Ce2(CO3)3。
已知:①氮化钙遇水可迅速产生NH3;②Ce(Ⅲ)易被空气氧化成Ce(Ⅳ)。
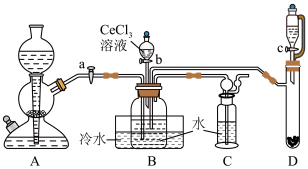
(2)实验时,“a”、“b”、“c”三个旋塞的打开顺序为
(3)该实验装置存在的一处缺陷为
步骤二:制备硝酸铈(Ⅳ)铵

(5)“烘干”采取自然干燥的原因为
步骤三:测定化学式
①称取一定质量的硝酸铈(Ⅳ)铵,充分灼烧得CeO2mg。
②另称取相同质量的硝酸铈(Ⅳ)铵,加入足量NaOH溶液微热,将产生的气体全部用V1mL水吸收。将吸收液滴入甲基橙,用
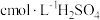 标准溶液滴定,重复2~3次,平均消耗H2SO4标准溶液V2mL。
标准溶液滴定,重复2~3次,平均消耗H2SO4标准溶液V2mL。(6)计算y=
您最近一年使用:0次
2024-02-02更新
|
256次组卷
|
3卷引用:山东省青岛市黄岛区2023-2024学年高三上学期期末考试化学试题
4 . 综合处理含SO2的尾气工艺流程如图。下列说法正确的是

A.“吸收”过程发生的反应为 |
B.可用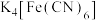 溶液检验“氧化”是否完全 溶液检验“氧化”是否完全 |
C.综合处理的总反应为 |
| D.向煤中加入石灰石可实现脱硫减排,该过程存在氧化还原反应 |
您最近一年使用:0次
2024-02-02更新
|
359次组卷
|
3卷引用:山东省青岛市黄岛区2023-2024学年高三上学期期末考试化学试题
名校
解题方法
5 . 下列离子方程式书写正确的是
A.向NaAl(OH)4溶液中通入过量 |
B.CuO溶于NaHSO4溶液: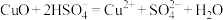 |
C.向0.1mol/LNaNO3溶液中通入 |
D.Fe与稀硝酸反应,当 时: 时: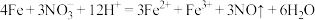 |
您最近一年使用:0次
名校
解题方法
6 . 某矿石的主要成分为MgCO3,还含有CaO、SiO2、Fe3O4、Al2O3及少量其它杂质。某工厂采用该矿石为主要原料生产碱式碳酸镁,流程如下(已知:温度低于700℃时,SiO2不会与CaO等反应)。下列有关说法不正确的是
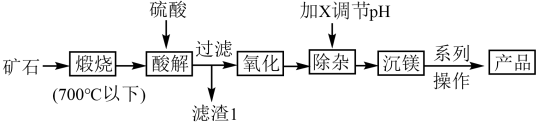

A.煅烧过程所发生的主要化学反应方程式为: |
| B.滤渣1的成分是SiO2 |
C.氧化步骤发生反应的离子方程式可以是: |
| D.加X调pH的X是氢氧化钠 |
您最近一年使用:0次
名校
解题方法
7 . 硫酸镁可用于印染、造纸、医药工业。利用某水泥厂的废料(含50%MgO,还有少量CaO、MnO2、Fe2O3、FeO、Al2O3、SiO2等杂质),制取 的流程如图:
的流程如图:

回答下列问题
(1)“酸浸”时,pH控制为1,若提高浸取速率,可采取的措施是___________ (任写一条)。
(2)“氧化”时,NaClO与Mn2+按物质的量1:1反应生成MnO2,其离子方程式为___________ ;调节pH时可加入试剂X为___________ 。
A.NaOH B.MgCO3 C.MgO D.CuO
(3)滤渣除Al(OH)3、Fe(OH)3外还有氧化物___________ 。
(4)“除钙”时,控温在60℃时除去MgSO4和CaSO4混合溶液中的CaSO4。参照表格,简要说明除钙的操作方法___________ 。
部分物质的溶解度(g/100gH2O)如表:
(5)为了提高原料中镁的利用率,操作a后滤液的处理方法是___________ 。
 的流程如图:
的流程如图:
回答下列问题
(1)“酸浸”时,pH控制为1,若提高浸取速率,可采取的措施是
(2)“氧化”时,NaClO与Mn2+按物质的量1:1反应生成MnO2,其离子方程式为
A.NaOH B.MgCO3 C.MgO D.CuO
(3)滤渣除Al(OH)3、Fe(OH)3外还有氧化物
(4)“除钙”时,控温在60℃时除去MgSO4和CaSO4混合溶液中的CaSO4。参照表格,简要说明除钙的操作方法
部分物质的溶解度(g/100gH2O)如表:
| 温度/℃ 物质 | 20 | 40 | 60 | 80 |
| MgSO4 | 28.6 | 30.9 | 36 | 40.8 |
| CaSO4 | 0.272 | 0.23 | 0.204 | 0.184 |
(5)为了提高原料中镁的利用率,操作a后滤液的处理方法是
您最近一年使用:0次
23-24高三上·河南南阳·阶段练习
8 . 镍酸锂(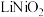 )被认为是一种具有较好发展前景的锂离子电池材料。一种以铁镍铜合金废料为原料生产
)被认为是一种具有较好发展前景的锂离子电池材料。一种以铁镍铜合金废料为原料生产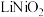 的工艺流程如图。
的工艺流程如图。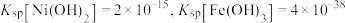 ,
,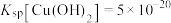 ,
, ,
,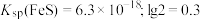 。
。
②常温下,有关金属阳离子开始沉淀和沉淀完全的pH如表。
回答下列问题:
(1)“酸溶”后,废料中的铁、镍和铜完全溶于混酸中,所得溶液中的溶质为 及过量的
及过量的 ,则尾气的主要成分为
,则尾气的主要成分为_____ 。
(2)“氧化”是将“酸溶”后溶液中的少量 氧化,适当升高温度会加快“氧化”速率,但温度高于60℃时,“氧化”速率会降低,其原因为
氧化,适当升高温度会加快“氧化”速率,但温度高于60℃时,“氧化”速率会降低,其原因为_____ 。
(3)“除铁”后滤渣的主要成分为_____ (写化学式),表格中的
_____ 。
(4)“沉铜”时,加入的试剂X可能为_____ (填字母)。
a.NaOH溶液 b. 气体 c.
气体 c. 溶液 d.FeS
溶液 d.FeS
(5)“沉镍”析出 沉淀,则滤液中的溶质主要为
沉淀,则滤液中的溶质主要为_____ (填化学式);在空气中“煅烧”的化学方程式为_____ 。
(6)若1.0t铁镍铜合金废料(含镍质量分数为59.0%)经过上述流程制得 ,则
,则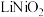 的产率为
的产率为_____ %(结果保留3位有效数字)。
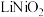 )被认为是一种具有较好发展前景的锂离子电池材料。一种以铁镍铜合金废料为原料生产
)被认为是一种具有较好发展前景的锂离子电池材料。一种以铁镍铜合金废料为原料生产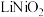 的工艺流程如图。
的工艺流程如图。
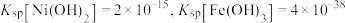 ,
,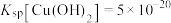 ,
, ,
,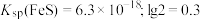 。
。②常温下,有关金属阳离子开始沉淀和沉淀完全的pH如表。
| 金属阳离子 |  |  |  |  |
| 开始沉淀的pH | 2.2 | 5.8 | 4.2 | 6.7 |
沉淀完全( )的pH )的pH | x | 8.8 | 7.7 | 9.3 |
(1)“酸溶”后,废料中的铁、镍和铜完全溶于混酸中,所得溶液中的溶质为
 及过量的
及过量的 ,则尾气的主要成分为
,则尾气的主要成分为(2)“氧化”是将“酸溶”后溶液中的少量
 氧化,适当升高温度会加快“氧化”速率,但温度高于60℃时,“氧化”速率会降低,其原因为
氧化,适当升高温度会加快“氧化”速率,但温度高于60℃时,“氧化”速率会降低,其原因为(3)“除铁”后滤渣的主要成分为

(4)“沉铜”时,加入的试剂X可能为
a.NaOH溶液 b.
 气体 c.
气体 c. 溶液 d.FeS
溶液 d.FeS(5)“沉镍”析出
 沉淀,则滤液中的溶质主要为
沉淀,则滤液中的溶质主要为(6)若1.0t铁镍铜合金废料(含镍质量分数为59.0%)经过上述流程制得
 ,则
,则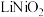 的产率为
的产率为
您最近一年使用:0次
名校
解题方法
9 . 某班同学用如下实验探究 、
、 的性质。请回答下列问题:
的性质。请回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol/L的溶液。在 溶液中需加入少量铁屑,结合化学方程式说明其目的是
溶液中需加入少量铁屑,结合化学方程式说明其目的是________ 。
(2)甲组同学取 溶液,加入几滴
溶液,加入几滴 ,再加入1滴KSCN溶液,溶液变红,说明
,再加入1滴KSCN溶液,溶液变红,说明 可将
可将 氧化。
氧化。 溶液与
溶液与 反应的离子方程式为:
反应的离子方程式为:________ 。
(3)乙组同学认为甲组的实验不够严谨,该组同学在 溶液中先加入0.5mL煤油,再于液面下依次加入几滴
溶液中先加入0.5mL煤油,再于液面下依次加入几滴 和1滴KSCN溶液,溶液变红,煤油的作用是
和1滴KSCN溶液,溶液变红,煤油的作用是_______ 。
(4)丙组同学向 溶液滴加氢氧化钠溶液并在空气中放置一段时间,沉淀转化的化学方程式为:
溶液滴加氢氧化钠溶液并在空气中放置一段时间,沉淀转化的化学方程式为:_______ 。
(5)丁组同学模拟电子工业用 溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出
溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出 溶液与铜反应的离子方程式:
溶液与铜反应的离子方程式:_________ 。
(6)戊组同学模拟工业上用 氧化酸性
氧化酸性 废液制备
废液制备 。
。
①若酸性 废液中:
废液中: ,
,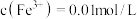 ,
,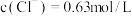 ,则该溶液的
,则该溶液的
_______ 。
②完成 氧化酸性
氧化酸性 的离子方程式:
的离子方程式:______ 。__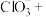 __
__ ____=___
____=___ ___
___ ____
____
 、
、 的性质。请回答下列问题:
的性质。请回答下列问题:(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol/L的溶液。在
 溶液中需加入少量铁屑,结合化学方程式说明其目的是
溶液中需加入少量铁屑,结合化学方程式说明其目的是(2)甲组同学取
 溶液,加入几滴
溶液,加入几滴 ,再加入1滴KSCN溶液,溶液变红,说明
,再加入1滴KSCN溶液,溶液变红,说明 可将
可将 氧化。
氧化。 溶液与
溶液与 反应的离子方程式为:
反应的离子方程式为:(3)乙组同学认为甲组的实验不够严谨,该组同学在
 溶液中先加入0.5mL煤油,再于液面下依次加入几滴
溶液中先加入0.5mL煤油,再于液面下依次加入几滴 和1滴KSCN溶液,溶液变红,煤油的作用是
和1滴KSCN溶液,溶液变红,煤油的作用是(4)丙组同学向
 溶液滴加氢氧化钠溶液并在空气中放置一段时间,沉淀转化的化学方程式为:
溶液滴加氢氧化钠溶液并在空气中放置一段时间,沉淀转化的化学方程式为:(5)丁组同学模拟电子工业用
 溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出
溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出 溶液与铜反应的离子方程式:
溶液与铜反应的离子方程式:(6)戊组同学模拟工业上用
 氧化酸性
氧化酸性 废液制备
废液制备 。
。①若酸性
 废液中:
废液中: ,
,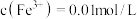 ,
,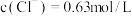 ,则该溶液的
,则该溶液的
②完成
 氧化酸性
氧化酸性 的离子方程式:
的离子方程式: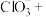 __
__ ____=___
____=___ ___
___ ____
____
您最近一年使用:0次
名校
10 . 高效灭菌消毒剂 气态时不稳定,受热或光照易分解,浓度过高时甚至会发生爆炸。工业上通常以氯酸盐(
气态时不稳定,受热或光照易分解,浓度过高时甚至会发生爆炸。工业上通常以氯酸盐( )、过氧化氢和碳酸盐为主要原料制备稳定性
)、过氧化氢和碳酸盐为主要原料制备稳定性 溶液的流程如图:
溶液的流程如图:
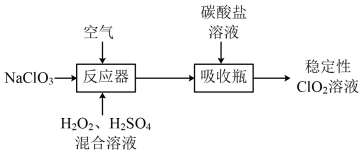
(1)①反应器中发生的主要反应为_________ (离子方程式)。
②制备时向反应器中通入空气的作用是_________ 。
(2)反应器中的反应温度控制在80℃左右为宜。
①工业上采用的加热方式为_________ 。
②当温度超过80℃, 的收率
的收率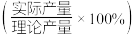 随温度升高而减小,其原因可能是
随温度升高而减小,其原因可能是_________ (写出两条即可)。
(3)吸收瓶中发生反应 获得稳定性
获得稳定性 溶液。当有
溶液。当有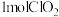 参加反应,转移的电子数为
参加反应,转移的电子数为_________  。
。
(4)亚氯酸钠( )也是一种高效的消毒剂和漂白剂。
)也是一种高效的消毒剂和漂白剂。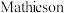 法制备亚氯酸钠的流程如下:
法制备亚氯酸钠的流程如下:
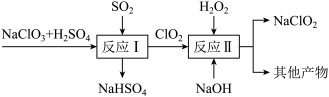
请写出反应 的化学方程式
的化学方程式_________ ;反应 中的其他产物包含
中的其他产物包含_________ 。
 气态时不稳定,受热或光照易分解,浓度过高时甚至会发生爆炸。工业上通常以氯酸盐(
气态时不稳定,受热或光照易分解,浓度过高时甚至会发生爆炸。工业上通常以氯酸盐( )、过氧化氢和碳酸盐为主要原料制备稳定性
)、过氧化氢和碳酸盐为主要原料制备稳定性 溶液的流程如图:
溶液的流程如图:
(1)①反应器中发生的主要反应为
②制备时向反应器中通入空气的作用是
(2)反应器中的反应温度控制在80℃左右为宜。
①工业上采用的加热方式为
②当温度超过80℃,
 的收率
的收率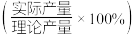 随温度升高而减小,其原因可能是
随温度升高而减小,其原因可能是(3)吸收瓶中发生反应
 获得稳定性
获得稳定性 溶液。当有
溶液。当有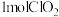 参加反应,转移的电子数为
参加反应,转移的电子数为 。
。(4)亚氯酸钠(
 )也是一种高效的消毒剂和漂白剂。
)也是一种高效的消毒剂和漂白剂。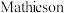 法制备亚氯酸钠的流程如下:
法制备亚氯酸钠的流程如下:
请写出反应
 的化学方程式
的化学方程式 中的其他产物包含
中的其他产物包含
您最近一年使用:0次



