1 . 向酸性 溶液中滴加KI溶液,发生的离子反应为:□
溶液中滴加KI溶液,发生的离子反应为:□ □
□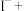 □
□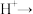 □
□ □
□ □
□ (未配平)。下列说法正确的是
(未配平)。下列说法正确的是
 溶液中滴加KI溶液,发生的离子反应为:□
溶液中滴加KI溶液,发生的离子反应为:□ □
□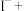 □
□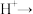 □
□ □
□ □
□ (未配平)。下列说法正确的是
(未配平)。下列说法正确的是| A.溶液由紫红色变成无色 | B. 是氧化产物 是氧化产物 |
C. 的系数为8 的系数为8 | D.生成1mol  时转移5mol电子 时转移5mol电子 |
您最近一年使用:0次
2023高三·全国·专题练习
2 . 废旧锂离子电池经处理得到的正极活性粉体中含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 等,采用以下工艺流程可从废旧锂离子电池中分离回收钻、镍、锰,制备正极材料的前驱体(
等,采用以下工艺流程可从废旧锂离子电池中分离回收钻、镍、锰,制备正极材料的前驱体( )。
)。

回答下列问题:
(1)“酸浸”温度为85℃,“酸浸”过程中温度不能过高的原因可能是_______ ;粉体中的钴(以 形式存在)发生反应的化学方程式为
形式存在)发生反应的化学方程式为_______ ;浸渣为_______ (填化学式)。
(2)“除铁”时需将溶液的pH调至3左右,加入的化合物X是_______ (填化学式)。
(3)“除铜”时获得萃余液的操作名称是_______ 。
(4)“除铝”时反应的离子方程式为_______ 。萃余液中 为
为 ,通过计算说明,常温下“除铝”控制溶液pH为4.5,是否造成
,通过计算说明,常温下“除铝”控制溶液pH为4.5,是否造成 的损失?
的损失?_______ (列出算式并给出结论)。已知: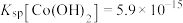 。
。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 等,采用以下工艺流程可从废旧锂离子电池中分离回收钻、镍、锰,制备正极材料的前驱体(
等,采用以下工艺流程可从废旧锂离子电池中分离回收钻、镍、锰,制备正极材料的前驱体( )。
)。
回答下列问题:
(1)“酸浸”温度为85℃,“酸浸”过程中温度不能过高的原因可能是
 形式存在)发生反应的化学方程式为
形式存在)发生反应的化学方程式为(2)“除铁”时需将溶液的pH调至3左右,加入的化合物X是
(3)“除铜”时获得萃余液的操作名称是
(4)“除铝”时反应的离子方程式为
 为
为 ,通过计算说明,常温下“除铝”控制溶液pH为4.5,是否造成
,通过计算说明,常温下“除铝”控制溶液pH为4.5,是否造成 的损失?
的损失?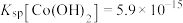 。
。
您最近一年使用:0次
3 . Ⅰ. 某磁铁矿石A的主要成分是磁性氧化铁( ),还含少量的
),还含少量的 、
、 。某工厂利用此矿石进行有关物质的回收利用,工艺流程如下:(已知
。某工厂利用此矿石进行有关物质的回收利用,工艺流程如下:(已知 不溶于水和碱,但溶于酸:
不溶于水和碱,但溶于酸: )。根据流程回答下列问题:
)。根据流程回答下列问题:
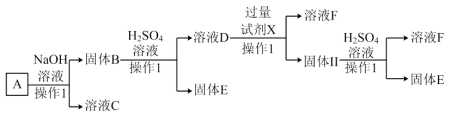
(1)操作Ⅰ涉及的化学反应方程式是_______ 。
(2)在溶液F中加稀硝酸酸化时产生了无色气体,该反应的离子方程式为_______ 。
Ⅱ. 化合物A由四种常见元素组成,是一种重要的化工原料。某实验小组按如图所示流程进行相关实验:
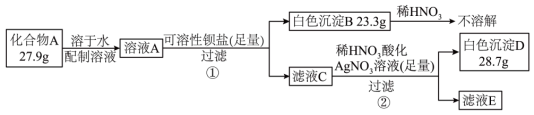
已知化合物A含有两种阴离子和一种阳离子,向溶液A滴加 溶液产生蓝色沉淀。
溶液产生蓝色沉淀。
(3)A的化学式为_______ 。
(4)溶液A中加入稍过量的 溶液,生成沉淀(
溶液,生成沉淀( )的同时有一种气体产生,写出反应的化学方程式:
)的同时有一种气体产生,写出反应的化学方程式:_______ 。
(5)设计实验检验化合物A是否变质,写出检验出化合物A没有变质的方案。_______
 ),还含少量的
),还含少量的 、
、 。某工厂利用此矿石进行有关物质的回收利用,工艺流程如下:(已知
。某工厂利用此矿石进行有关物质的回收利用,工艺流程如下:(已知 不溶于水和碱,但溶于酸:
不溶于水和碱,但溶于酸: )。根据流程回答下列问题:
)。根据流程回答下列问题:
(1)操作Ⅰ涉及的化学反应方程式是
(2)在溶液F中加稀硝酸酸化时产生了无色气体,该反应的离子方程式为
Ⅱ. 化合物A由四种常见元素组成,是一种重要的化工原料。某实验小组按如图所示流程进行相关实验:

已知化合物A含有两种阴离子和一种阳离子,向溶液A滴加
 溶液产生蓝色沉淀。
溶液产生蓝色沉淀。(3)A的化学式为
(4)溶液A中加入稍过量的
 溶液,生成沉淀(
溶液,生成沉淀( )的同时有一种气体产生,写出反应的化学方程式:
)的同时有一种气体产生,写出反应的化学方程式:(5)设计实验检验化合物A是否变质,写出检验出化合物A没有变质的方案。
您最近一年使用:0次
名校
解题方法
4 . Ⅰ.掌握电解质和非电解质的概念,能熟练判断一种物质是否是电解质,是认识电解质的性质的前提:以下有①~⑩种物质:①石墨②液氯③氨水④ ⑤
⑤ ⑥
⑥ ⑦红褐色的氢氧化铁胶体⑧稀硫酸⑨熔融
⑦红褐色的氢氧化铁胶体⑧稀硫酸⑨熔融 ⑩蔗糖⑪银
⑩蔗糖⑪银
(1)上述物质导电的是_______ ;(填序号,多写不给分,下同),属于非电解质的是_______ 。
(2)下列制备⑦的操作方法正确的是_______。(填字母)
(3)向盛有⑦的烧杯中还滴加入盐酸至过量,会出现一系列变化,现象为:_______ 。
(4)写出⑥溶液中加入⑨溶液至溶液呈中性的离子反应方程式_______ 。
Ⅱ.请配平以下化学方程式: (未配平)
(未配平)
(5)配平上述方程式________
(6)若反应过程中转移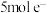 ,则生成标准状况下
,则生成标准状况下 的体积为
的体积为_______  。
。
 ⑤
⑤ ⑥
⑥ ⑦红褐色的氢氧化铁胶体⑧稀硫酸⑨熔融
⑦红褐色的氢氧化铁胶体⑧稀硫酸⑨熔融 ⑩蔗糖⑪银
⑩蔗糖⑪银(1)上述物质导电的是
(2)下列制备⑦的操作方法正确的是_______。(填字母)
| A.向饱和氯化铁溶液中滴加适量的氢氧化钠稀溶液 |
| B.加热煮沸氯化铁饱和溶液 |
| C.在氨水中滴加氯化铁浓溶液 |
| D.在沸水中滴加饱和氯化铁溶液,煮沸至出现红褐色液体 |
(4)写出⑥溶液中加入⑨溶液至溶液呈中性的离子反应方程式
Ⅱ.请配平以下化学方程式:
 (未配平)
(未配平)(5)配平上述方程式
(6)若反应过程中转移
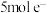 ,则生成标准状况下
,则生成标准状况下 的体积为
的体积为 。
。
您最近一年使用:0次
5 . 汽车剧烈碰撞时,安全气囊中发生的反应为 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是A. 、 、 |
| B.上述反应中涉及的物质均是电解质 |
C. 的电离方程式为 的电离方程式为 |
D.还原产物与氧化产物的质量之比为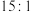 |
您最近一年使用:0次
解题方法
6 . Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。工业以锂辉矿(主要成分为Li2O•Al2O3•4SiO2,含少量铁、钙、镁)为原料制备LiFePO4的工艺流程如图:

已知:①Li2O•Al2O3•4SiO2+H2SO4(浓) Li2SO4+Al2O3•4SiO2•H2O↓
Li2SO4+Al2O3•4SiO2•H2O↓
②常温下,相关金属离子(浓度为0.1mol•L-1)形成氢氧化物沉淀的pH范围如表:
③Li2CO3的溶解度随温度变化如表:
回答下列问题:
(1)滤渣1的主要成分为_____ 。
(2)向滤液1中加入适量的CaCO3细粉除去Fe3+,若n(CaCO3):n(Fe3+)=3:1时反应的离子方程式为_____ ;加入石灰乳调pH,其目的是_____ 。
(3)“操作1”为_____ 。
(4)Li2CO3煅烧制备LiFePO4的化学方程式为_____ 。
(5)LiFePO4充放电过程结构变化如图所示:

(b)→(a)的电极反应式为_____ ;用该电池电解精炼铜,电池正极质量增加2.8g时,电解精炼得到9.6g铜,则电流利用率为_____ (已知:电流利用率= ×100%)。
×100%)。

已知:①Li2O•Al2O3•4SiO2+H2SO4(浓)
 Li2SO4+Al2O3•4SiO2•H2O↓
Li2SO4+Al2O3•4SiO2•H2O↓②常温下,相关金属离子(浓度为0.1mol•L-1)形成氢氧化物沉淀的pH范围如表:
| 金属离子 | Fe2+ | Fe3+ | Mg2+ | Ca2+ |
| 开始沉淀的pH | 6.3 | 1.8 | 9.5 | 12.4 |
| 完全沉淀的pH | 8.3 | 3.2 | 11.1 | 13.8 |
③Li2CO3的溶解度随温度变化如表:
| 温度 | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度(g) | 1.63 | 1.33 | 1.05 | 0.90 | 0.75 | 0.70 |
回答下列问题:
(1)滤渣1的主要成分为
(2)向滤液1中加入适量的CaCO3细粉除去Fe3+,若n(CaCO3):n(Fe3+)=3:1时反应的离子方程式为
(3)“操作1”为
(4)Li2CO3煅烧制备LiFePO4的化学方程式为
(5)LiFePO4充放电过程结构变化如图所示:

(b)→(a)的电极反应式为
 ×100%)。
×100%)。
您最近一年使用:0次
名校
解题方法
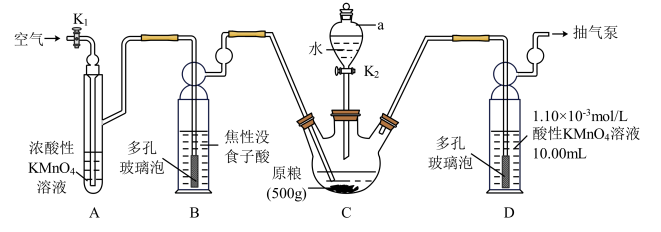
7 . 磷化铝是一种广谱性熏蒸杀虫剂,与水反应产生高毒的 气体,可用于粮食熏蒸杀虫。实验室可采用以下装置测定粮食中残留的磷化物含量:
气体,可用于粮食熏蒸杀虫。实验室可采用以下装置测定粮食中残留的磷化物含量:
已知:① 易自然,具有强还原性;
易自然,具有强还原性;
②焦性没食子酸学名连苯三酚,白色固体,溶于水,易被氧化,在空气中易变色;
③食品安全标准规定:粮食中磷化物(以 计)的含量低于
计)的含量低于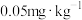 时合格。
时合格。
回答下列问题:
(1)仪器a的名称是_______ ;打开 前,需先打开
前,需先打开 ,用抽气泵抽一段时间空气,主要目的是
,用抽气泵抽一段时间空气,主要目的是_______ 。
(2)装置C中反应的化学方程式为_______ 。
(3)装置B的作用是_______ ;多孔玻璃泡的作用是_______ 。
(4)装置D中 被氧化为磷酸,发生反应的离子方程式为
被氧化为磷酸,发生反应的离子方程式为_______ 。
(5)实验结束,将D中溶液及D的洗涤液转移至锥形瓶中,用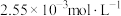
 标准溶液进行滴定,滴定达终点时,共消耗
标准溶液进行滴定,滴定达终点时,共消耗 标准溶液10.00 mL。
标准溶液10.00 mL。
①该滴定达终点的判断方法是_______ ;
②该原粮中磷化物的含量是_______ 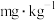 。
。
 气体,可用于粮食熏蒸杀虫。实验室可采用以下装置测定粮食中残留的磷化物含量:
气体,可用于粮食熏蒸杀虫。实验室可采用以下装置测定粮食中残留的磷化物含量:
已知:①
 易自然,具有强还原性;
易自然,具有强还原性;②焦性没食子酸学名连苯三酚,白色固体,溶于水,易被氧化,在空气中易变色;
③食品安全标准规定:粮食中磷化物(以
 计)的含量低于
计)的含量低于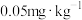 时合格。
时合格。回答下列问题:
(1)仪器a的名称是
 前,需先打开
前,需先打开 ,用抽气泵抽一段时间空气,主要目的是
,用抽气泵抽一段时间空气,主要目的是(2)装置C中反应的化学方程式为
(3)装置B的作用是
(4)装置D中
 被氧化为磷酸,发生反应的离子方程式为
被氧化为磷酸,发生反应的离子方程式为(5)实验结束,将D中溶液及D的洗涤液转移至锥形瓶中,用
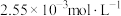
 标准溶液进行滴定,滴定达终点时,共消耗
标准溶液进行滴定,滴定达终点时,共消耗 标准溶液10.00 mL。
标准溶液10.00 mL。①该滴定达终点的判断方法是
②该原粮中磷化物的含量是
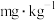 。
。
您最近一年使用:0次
2023-01-12更新
|
385次组卷
|
3卷引用:山东省青岛市胶州市2022-2023学年高三上学期期末学业水平检测化学试题
8 . 应对新冠肺炎疫情时所采取的措施是对环境进行彻底消毒,二氧化氯( ,黄绿色易溶于水的气体)是一种安全稳定、高效低毒的消毒剂。工业上通过惰性电极电解氯化铵和盐酸的方法制备
,黄绿色易溶于水的气体)是一种安全稳定、高效低毒的消毒剂。工业上通过惰性电极电解氯化铵和盐酸的方法制备 的原理如图所示,下列说法错误的是
的原理如图所示,下列说法错误的是
 ,黄绿色易溶于水的气体)是一种安全稳定、高效低毒的消毒剂。工业上通过惰性电极电解氯化铵和盐酸的方法制备
,黄绿色易溶于水的气体)是一种安全稳定、高效低毒的消毒剂。工业上通过惰性电极电解氯化铵和盐酸的方法制备 的原理如图所示,下列说法错误的是
的原理如图所示,下列说法错误的是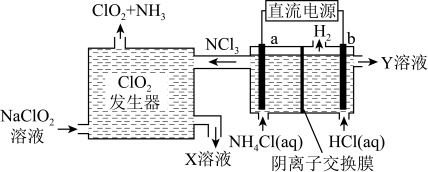
| A.装置工作时,a与电源的正极连接,b极附近溶液pH逐渐减小 |
B.a极上发生的电极反应为 |
C. 发生器内发生反应 发生器内发生反应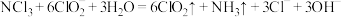 |
D.当有0.3 mol阴离子通过离子交换膜时,理论上产生2.24 L(STP) |
您最近一年使用:0次
2023-01-12更新
|
333次组卷
|
3卷引用:山东省青岛市胶州市2022-2023学年高三上学期期末学业水平检测化学试题
名校
解题方法
9 . 工业上以软锰矿(主要成分为 )为主要原料制备高锰酸钾(
)为主要原料制备高锰酸钾( )的方法如下:
)的方法如下:

已知:①熔烧时有 和KCl生成。
和KCl生成。
② 歧化法:调溶液pH至弱碱性,歧化生成
歧化法:调溶液pH至弱碱性,歧化生成 和
和
下列说法正确的是
 )为主要原料制备高锰酸钾(
)为主要原料制备高锰酸钾( )的方法如下:
)的方法如下:
已知:①熔烧时有
 和KCl生成。
和KCl生成。②
 歧化法:调溶液pH至弱碱性,歧化生成
歧化法:调溶液pH至弱碱性,歧化生成 和
和
下列说法正确的是
A.熔烧时所用坩埚的材质可以选用 |
B.熔烧时理论上每生成1 mol  转移 转移 个电子 个电子 |
C.电解法与 歧化法的理论产率之比为3:2 歧化法的理论产率之比为3:2 |
D.采用 歧化法时,可将滤液蒸发结晶得到 歧化法时,可将滤液蒸发结晶得到 固体 固体 |
您最近一年使用:0次
2023-01-12更新
|
404次组卷
|
4卷引用:山东省青岛市胶州市2022-2023学年高三上学期期末学业水平检测化学试题
10 .  是一种可溶性盐,它能被常见的强氧化剂氧化。回答下列问题:
是一种可溶性盐,它能被常见的强氧化剂氧化。回答下列问题:
(1)金属加工后的废液中含有2%~5%的 ,它是一种环境污染物。人们用
,它是一种环境污染物。人们用 溶液来处理此废液,使亚硝酸钠转化为无毒物质。该反应分两步进行:
溶液来处理此废液,使亚硝酸钠转化为无毒物质。该反应分两步进行:
第一步: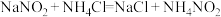
第二步: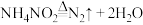
下列对上述反应的叙述中正确的是_______(填字母)。
①两步均为氧化还原反应 ②第二步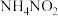 仅发生氧化反应 ③第二步
仅发生氧化反应 ③第二步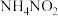 发生了分解反应 ④第二步中
发生了分解反应 ④第二步中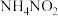 既被氧化又被还原 ⑤第一步为复分解反应
既被氧化又被还原 ⑤第一步为复分解反应
(2)实验室中,亚硝酸钠可用来处理过量的叠氮化钠,有关反应的化学方程式如下:
a.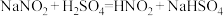
b.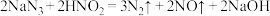
用单线桥法标出b反应中电子转移情况:_______ 。
(3) 、
、 、
、 、
、 、
、 、
、 组成的一个氧化还原反应体系中,发生
组成的一个氧化还原反应体系中,发生 的反应过程。
的反应过程。
①该反应中,被氧化的元素是_______ (填元素符号),氧化剂是_______ (填离子符号)。
②将以上物质分别填入下面对应的横线上,并配平该反应:_______ 。
_______+_______+_______=_______+_______+_______ 。
。
 是一种可溶性盐,它能被常见的强氧化剂氧化。回答下列问题:
是一种可溶性盐,它能被常见的强氧化剂氧化。回答下列问题:(1)金属加工后的废液中含有2%~5%的
 ,它是一种环境污染物。人们用
,它是一种环境污染物。人们用 溶液来处理此废液,使亚硝酸钠转化为无毒物质。该反应分两步进行:
溶液来处理此废液,使亚硝酸钠转化为无毒物质。该反应分两步进行:第一步:
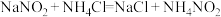
第二步:
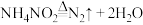
下列对上述反应的叙述中正确的是_______(填字母)。
①两步均为氧化还原反应 ②第二步
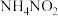 仅发生氧化反应 ③第二步
仅发生氧化反应 ③第二步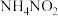 发生了分解反应 ④第二步中
发生了分解反应 ④第二步中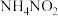 既被氧化又被还原 ⑤第一步为复分解反应
既被氧化又被还原 ⑤第一步为复分解反应| A.①③ | B.①④ | C.②③④ | D.③④⑤ |
a.
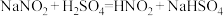
b.
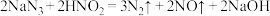
用单线桥法标出b反应中电子转移情况:
(3)
 、
、 、
、 、
、 、
、 、
、 组成的一个氧化还原反应体系中,发生
组成的一个氧化还原反应体系中,发生 的反应过程。
的反应过程。①该反应中,被氧化的元素是
②将以上物质分别填入下面对应的横线上,并配平该反应:
_______+_______+_______=_______+_______+_______
 。
。
您最近一年使用:0次



