解题方法
1 . 硫脲( )是一种白色而有光泽的晶体,味苦,可用于制造树脂,也用作橡胶的硫化促进剂以及金属矿物的浮选剂等。回答下列问题:
)是一种白色而有光泽的晶体,味苦,可用于制造树脂,也用作橡胶的硫化促进剂以及金属矿物的浮选剂等。回答下列问题:
(1)①硫脲中硫的化合价为___________ ;与硫脲互为同分异构且能与FeCl3溶液发生显色反应的化合物的化学式为_____ 。
②向盛有少量硫脲的试管中加入NaOH溶液,有NH3放出,检验该气体的方法为_____ 。
③可用酸性KMnO4溶液滴定硫脲,已知MnO 被还原为Mn2+,CS(NH2)2被氧化为CO2、N2及SO
被还原为Mn2+,CS(NH2)2被氧化为CO2、N2及SO ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
(2)某化学实验小组同学用Ca(HS)2与CaCN2(石灰氮)合成硫脲并测定硫脲含量。
①制备Ca(HS)2溶液,所用装置如图(已知酸性:H2CO3 > H2S):

装置b中盛放的试剂是___________ ,装置c中的长直导管的作用是___________ 。
②制备硫脲:将CaCN2与Ca(HS)2溶液混合,加热至80℃时,可合成硫脲,同时生成一种常见的碱。合适的加热方式是___________ ;该反应的化学方程式为___________ 。
③测定硫脲含量的方法如下:
步骤1:准确称取a g产品,经溶解等步骤最后在500 mL容量瓶中定容。
步骤2:准确量取20.00 mL配制好的溶液注入碘量瓶中,加入V1 mL c1 mol·L-1 I2的标准溶液及适量的NaOH溶液,于暗处放置10 min。 (2NaOH+I2=NaIO+NaI+H2O,4NaIO+(NH2)2CS+H2O =(NH2)2CO+4NaI+H2SO4)
步骤3:加水及适量的盐酸,摇匀。
步骤4:用c2 mol·L-1标准Na2S2O3溶液滴定剩余的I2 ( I2+2Na2S2O3=2NaI+Na2S4O6) ,加入淀粉溶液,滴定至终点时消耗Na2S2O3溶液V2mL。“步骤4”滴定至终点时的颜色变化是___________ ,产品中(NH2)2CS的质量分数为_______ (列出计算式)。
 )是一种白色而有光泽的晶体,味苦,可用于制造树脂,也用作橡胶的硫化促进剂以及金属矿物的浮选剂等。回答下列问题:
)是一种白色而有光泽的晶体,味苦,可用于制造树脂,也用作橡胶的硫化促进剂以及金属矿物的浮选剂等。回答下列问题:(1)①硫脲中硫的化合价为
②向盛有少量硫脲的试管中加入NaOH溶液,有NH3放出,检验该气体的方法为
③可用酸性KMnO4溶液滴定硫脲,已知MnO
 被还原为Mn2+,CS(NH2)2被氧化为CO2、N2及SO
被还原为Mn2+,CS(NH2)2被氧化为CO2、N2及SO ,该反应的离子方程式为
,该反应的离子方程式为(2)某化学实验小组同学用Ca(HS)2与CaCN2(石灰氮)合成硫脲并测定硫脲含量。
①制备Ca(HS)2溶液,所用装置如图(已知酸性:H2CO3 > H2S):

装置b中盛放的试剂是
②制备硫脲:将CaCN2与Ca(HS)2溶液混合,加热至80℃时,可合成硫脲,同时生成一种常见的碱。合适的加热方式是
③测定硫脲含量的方法如下:
步骤1:准确称取a g产品,经溶解等步骤最后在500 mL容量瓶中定容。
步骤2:准确量取20.00 mL配制好的溶液注入碘量瓶中,加入V1 mL c1 mol·L-1 I2的标准溶液及适量的NaOH溶液,于暗处放置10 min。 (2NaOH+I2=NaIO+NaI+H2O,4NaIO+(NH2)2CS+H2O =(NH2)2CO+4NaI+H2SO4)
步骤3:加水及适量的盐酸,摇匀。
步骤4:用c2 mol·L-1标准Na2S2O3溶液滴定剩余的I2 ( I2+2Na2S2O3=2NaI+Na2S4O6) ,加入淀粉溶液,滴定至终点时消耗Na2S2O3溶液V2mL。“步骤4”滴定至终点时的颜色变化是
您最近一年使用:0次
解题方法
2 . 铬元素是一种重金属元素,工业上处理含铬废水并将其资源化的工艺有多种,其中两种工艺如图所示:
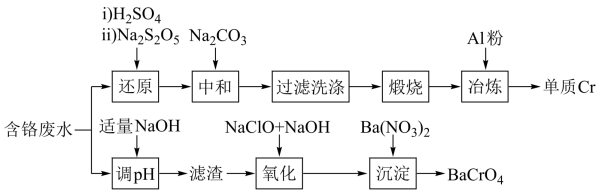
已知含铬废水中铬元素主要存在微粒为Cr3+、CrO 、Cr2O
、Cr2O 。“中和”过程中,产生Cr(OH)3。回答下列问题:
。“中和”过程中,产生Cr(OH)3。回答下列问题:
(1)“还原”时,先加入H2SO4酸化的目的是___________ ,用硫酸而不用盐酸,原因是___________ ,再加入Na2S2O5固体,其发生反应的离子方程式为___________ 。
(2)“中和”时加入Na2CO3的作用是___________ ,“过滤洗涤”时,洗涤沉淀的操作为___________ 。
(3)写出“氧化”时,发生反应的化学方程式___________ 。
(4)已知Ksp(BaCrO4) = 2.4×10-10,利用氧化法除铬时,欲使废液中铬元素的含量不高于0.26 mg·L-1,则此滤液中c(Ba2+)的范围为___________ 。

已知含铬废水中铬元素主要存在微粒为Cr3+、CrO
 、Cr2O
、Cr2O 。“中和”过程中,产生Cr(OH)3。回答下列问题:
。“中和”过程中,产生Cr(OH)3。回答下列问题:(1)“还原”时,先加入H2SO4酸化的目的是
(2)“中和”时加入Na2CO3的作用是
(3)写出“氧化”时,发生反应的化学方程式
(4)已知Ksp(BaCrO4) = 2.4×10-10,利用氧化法除铬时,欲使废液中铬元素的含量不高于0.26 mg·L-1,则此滤液中c(Ba2+)的范围为
您最近一年使用:0次
3 . Ⅰ.中学化学中几种常见物质的转化关系如图(部分产物未列出)。A是一种金属单质,D是一种非金属固体单质。
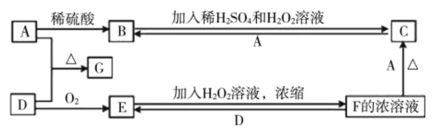
请回答下列问题:
(1)写出反应E+H2O2→F的化学方程式:___________ 。
(2)若反应F+D→E转移的电子数为3.01×1023,则消耗D的质量为___________ g。
Ⅱ.氮气是一种常见的气体,其在一定条件下可以转化为氮氧化物NO、NO2等。
(3)NO、NO2均为有毒气体,可以把NO、NO2一起通入氢氧化钠溶液中进行尾气处理,得到一种常见的食品添加剂。写出该过程发生的离子方程式:___________ 。
(4)把a g的Mg、Cu固体混合物加到足量的硝酸溶液中得到蓝色溶液和气体。所产生的气体与b L(标准状况)的O2一起通入水中得到只含硝酸的水溶液。往蓝色溶液中滴加氢氧化钠溶液至恰好完全沉淀,所得沉淀的质量为___________ g.(用a、b的代数式表示)
(5)金属Mg可以在NO2燃烧,产物可能为MgO、Mg3N2和N2,现有13.2g的Mg粉,在足量的NO2中充分燃烧,得到21.0g的固体和1120mL(标准状况)的气体。写出燃烧过程发生的化学方程式:___________ 。

请回答下列问题:
(1)写出反应E+H2O2→F的化学方程式:
(2)若反应F+D→E转移的电子数为3.01×1023,则消耗D的质量为
Ⅱ.氮气是一种常见的气体,其在一定条件下可以转化为氮氧化物NO、NO2等。
(3)NO、NO2均为有毒气体,可以把NO、NO2一起通入氢氧化钠溶液中进行尾气处理,得到一种常见的食品添加剂。写出该过程发生的离子方程式:
(4)把a g的Mg、Cu固体混合物加到足量的硝酸溶液中得到蓝色溶液和气体。所产生的气体与b L(标准状况)的O2一起通入水中得到只含硝酸的水溶液。往蓝色溶液中滴加氢氧化钠溶液至恰好完全沉淀,所得沉淀的质量为
(5)金属Mg可以在NO2燃烧,产物可能为MgO、Mg3N2和N2,现有13.2g的Mg粉,在足量的NO2中充分燃烧,得到21.0g的固体和1120mL(标准状况)的气体。写出燃烧过程发生的化学方程式:
您最近一年使用:0次
名校
解题方法
4 . 含氮化合物过多蓄积会导致水体富营养化,需将其从水体中除去,该过程称为脱氮。常用的脱氮方法有吹脱法和折点氯化法。
吹脱法:调节水体 至8左右,然后持续向水中吹入空气。
至8左右,然后持续向水中吹入空气。
折点氯化法:调节水体 至6左右,向水中加入适量
至6左右,向水中加入适量 。
。
下列分析不正确的是
吹脱法:调节水体
 至8左右,然后持续向水中吹入空气。
至8左右,然后持续向水中吹入空气。折点氯化法:调节水体
 至6左右,向水中加入适量
至6左右,向水中加入适量 。
。下列分析不正确的是
A.含氨和铵盐的水体中存在平衡: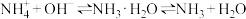 |
B.吹脱法的原理是通过鼓气降低 浓度,从而降低水中 浓度,从而降低水中 与 与 的含量 的含量 |
C.折点氯化法除 的原理为: 的原理为: |
D.吹脱法无法对含 的水体脱氮,但折点氯化法可以对含 的水体脱氮,但折点氯化法可以对含 的水体脱氮 的水体脱氮 |
您最近一年使用:0次
2021-10-19更新
|
1049次组卷
|
17卷引用:山东省济宁市泗水县2021届高三上学期期中考试化学试题
山东省济宁市泗水县2021届高三上学期期中考试化学试题2020届高三化学海淀区高三第一学期期中练习北京市海淀区2019-2020学年高三期中考试化学试题(已下线)考点24 元素与理论综合——《备战2020年高考精选考点专项突破题集》湖北省龙泉中学、潜江中学2020届高三12月联考理综化学试题(已下线)课时24 环境污染与保护-2022年高考化学一轮复习小题多维练(全国通用)北京市北京中国人民大学附属中学2022届高三10月检测化学试卷(已下线)2022年新高考化学时事热点情境化考题---化学与文化生活(已下线)备战2022年高考化学精准检测卷【全国卷】11(已下线)二轮拔高卷2-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(北京专用)天津市五校2022-2023学年高三上学期期中联考化学试题天津市咸水沽第一中学2022-2023学年高三上学期线上期末考试化学试题(已下线)章末综合评价(四)THUSSAT新高考地区2022年12月诊断性测试化学试题北京市交通大学附属中学2023-2024学年高一上学期12月月考化学试题 重庆市2023-2024学年高三下学期2月月度质量检测化学试题(已下线)通关练02 重要无机化合物的性质及应用-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)
名校
5 . 二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或浓H2SO4反应生成SeO2以回收Se。
已知:①Se+2H2SO4(浓)=2SO2↑+SeO2+2H2O;
②2SO2+SeO2+2H2O=Se+2SO +4H+。
+4H+。
(1)依据Se与浓H2SO4反应写出Se和浓HNO3(还原产物为NO2)反应的化学方程式:_______ 。
(2)Se与浓HNO3的反应中还原剂是_______ ,反应中被还原的元素是_______ 。当有标准状况下22.4 L NO2气体生成时,转移电子的物质的量是_______ mol。
(3)用双线桥法标出反应②电子转移的方向和数目:_______ 。
(4)SeO2、KI和HNO3发生如下反应:SeO2+KI+HNO3→Se+I2+KNO3+H2O配平上述反应的化学方程式_______ 。
已知:①Se+2H2SO4(浓)=2SO2↑+SeO2+2H2O;
②2SO2+SeO2+2H2O=Se+2SO
 +4H+。
+4H+。(1)依据Se与浓H2SO4反应写出Se和浓HNO3(还原产物为NO2)反应的化学方程式:
(2)Se与浓HNO3的反应中还原剂是
(3)用双线桥法标出反应②电子转移的方向和数目:
(4)SeO2、KI和HNO3发生如下反应:SeO2+KI+HNO3→Se+I2+KNO3+H2O配平上述反应的化学方程式
您最近一年使用:0次
解题方法
6 . 雾霾微颗粒中硫酸盐的生成可能存在三个阶段的转化,其主要过程的示意图如下。下列说法正确的是
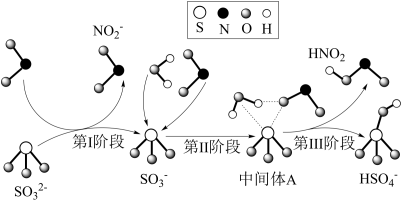

A.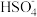 的摩尔质量为97 的摩尔质量为97 |
| B.第I阶段的反应中NO2被氧化 |
| C.HNO2、NO2、H2O均为电解质 |
D.第II、III阶段总反应的化学方程式为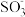 +H2O+NO2=HNO2+ +H2O+NO2=HNO2+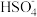 |
您最近一年使用:0次
2021-10-13更新
|
452次组卷
|
7卷引用:山东省济宁市兖州区2021-2022学年高一上学期期中考试化学试题
解题方法
7 . 回答下列问题:
(1)我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成的,即“一硫二硝三炭”,其爆炸时的反应为:S+2KNO3+3C=K2S+N2↑+3CO2↑,根据方程式,该反应中被还原的物质是_______ (填化学式)。
(2)NaH可在野外作生氢剂,反应原理为NaH + H2O = NaOH + H2↑,H2O中氢元素_______ (填“被氧化”或“被还原”)。
(3)实验室常用浓盐酸与高锰酸钾发生反应快速制备少量氯气,配平该反应:______
_______KMnO4 + _______HCl(浓) =_______ MnCl2 + _______KCl + _______Cl2↑ + _______H2O
该反应中氧化剂为_______ (填化学式)。氧化剂与起还原作用的HCl之比是_______ 。
(4)已知在碱性溶液中可发生如下反应2R(OH)3+3ClO-+4OH-=2RO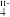 +3Cl-+5H2O,则RO
+3Cl-+5H2O,则RO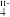 中R的化合价是_______(填字母) 。
中R的化合价是_______(填字母) 。
(5)针对以下四个涉及H2O2的反应(未配平)填空:
A.Na2O2+HCl→H2O2+NaCl
B.Ag2O+H2O2→Ag+O2+H2O
C.H2O2→H2O+O2
D.H2O2+Cr2(SO4)3+KOH→K2CrO4+K2SO4+H2O
H2O2仅体现氧化性的反应是_______ (填字母,下同),H2O2既体现氧化性又体现还原性的反应是_______ 。
(1)我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成的,即“一硫二硝三炭”,其爆炸时的反应为:S+2KNO3+3C=K2S+N2↑+3CO2↑,根据方程式,该反应中被还原的物质是
(2)NaH可在野外作生氢剂,反应原理为NaH + H2O = NaOH + H2↑,H2O中氢元素
(3)实验室常用浓盐酸与高锰酸钾发生反应快速制备少量氯气,配平该反应:
_______KMnO4 + _______HCl(浓) =_______ MnCl2 + _______KCl + _______Cl2↑ + _______H2O
该反应中氧化剂为
(4)已知在碱性溶液中可发生如下反应2R(OH)3+3ClO-+4OH-=2RO
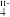 +3Cl-+5H2O,则RO
+3Cl-+5H2O,则RO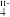 中R的化合价是_______(填字母) 。
中R的化合价是_______(填字母) 。| A.+3 | B.+4 | C.+5 | D.+6 |
A.Na2O2+HCl→H2O2+NaCl
B.Ag2O+H2O2→Ag+O2+H2O
C.H2O2→H2O+O2
D.H2O2+Cr2(SO4)3+KOH→K2CrO4+K2SO4+H2O
H2O2仅体现氧化性的反应是
您最近一年使用:0次
8 . NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,一种生产NaClO2的工艺如图:

已知:①ClO2是一种强氧化性气体,浓度大时易分解爆炸。在生产使用时要用稀有气体或空气等进行稀释,同时避免光照、震动等。②NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2·3H2O,高于38℃时析出的晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。③I2+2S2O =2I-+S4O
=2I-+S4O
回答下列问题:
(1)最近科学家又在“反应”步骤的基础上研究出用H2C2O4代替SO2制备ClO2的新方法,该方法的化学方程式为____ ,该新方法最突出的优点是____ 。
(2)获得产品NaClO2的“操作”包括以下步骤:
①减压,55℃蒸发结晶;②趁热过滤;③____ ;④低于60℃干燥,得到产品。
(3)为了测定产品NaClO2的纯度,取上述所得产品12.5g溶于水配成1L溶液,取出10.00mL溶液于锥形瓶中,再加入足量酸化的KI溶液,充分反应后(ClO 被还原为Cl-,杂质不参加反应),加入2~3滴淀粉溶液,用0.25mol·L-1Na2S2O3标准液滴定,达到滴定终点时用去标准液20.00mL,试计算产品NaClO2的纯度
被还原为Cl-,杂质不参加反应),加入2~3滴淀粉溶液,用0.25mol·L-1Na2S2O3标准液滴定,达到滴定终点时用去标准液20.00mL,试计算产品NaClO2的纯度___ 。
(4)NaClO2变质可分解为NaClO3和NaCl。取等质量变质前后的NaClO2试样均配成溶液,分别与足量FeSO4溶液反应时,消耗Fe2+的物质的量____ (填“相同”“不同”或“无法判断”)。

已知:①ClO2是一种强氧化性气体,浓度大时易分解爆炸。在生产使用时要用稀有气体或空气等进行稀释,同时避免光照、震动等。②NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2·3H2O,高于38℃时析出的晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。③I2+2S2O
 =2I-+S4O
=2I-+S4O
回答下列问题:
(1)最近科学家又在“反应”步骤的基础上研究出用H2C2O4代替SO2制备ClO2的新方法,该方法的化学方程式为
(2)获得产品NaClO2的“操作”包括以下步骤:
①减压,55℃蒸发结晶;②趁热过滤;③
(3)为了测定产品NaClO2的纯度,取上述所得产品12.5g溶于水配成1L溶液,取出10.00mL溶液于锥形瓶中,再加入足量酸化的KI溶液,充分反应后(ClO
 被还原为Cl-,杂质不参加反应),加入2~3滴淀粉溶液,用0.25mol·L-1Na2S2O3标准液滴定,达到滴定终点时用去标准液20.00mL,试计算产品NaClO2的纯度
被还原为Cl-,杂质不参加反应),加入2~3滴淀粉溶液,用0.25mol·L-1Na2S2O3标准液滴定,达到滴定终点时用去标准液20.00mL,试计算产品NaClO2的纯度(4)NaClO2变质可分解为NaClO3和NaCl。取等质量变质前后的NaClO2试样均配成溶液,分别与足量FeSO4溶液反应时,消耗Fe2+的物质的量
您最近一年使用:0次
2010·江西·二模
名校
解题方法
9 . 已知NH4CuSO3与足量的10mol·L-1硫酸混合微热,产生下列现象:①有红色金属生成②产生刺激性气味的气体③溶液呈现蓝色。据此判断下列说法正确的是
| A.反应中硫酸作氧化剂 |
| B.NH4CuSO3中硫元素被氧化 |
| C.刺激性气味的气体是氨气 |
| D.1molNH4CuSO3完全反应转移0.5mol电子 |
您最近一年使用:0次
2021-09-14更新
|
408次组卷
|
93卷引用:2012届山东省济宁市邹城二中高三第二次质量检测化学试卷
(已下线)2012届山东省济宁市邹城二中高三第二次质量检测化学试卷山东省济宁市微山县亚马逊中学2019届高三上学期11月月考化学试题山东省济宁市2020届高三10月月考化学试卷山东省济宁市邹城第一中学2020届高三10月月考化学试题山东省济宁市汶上圣泽中学2019-2020学年高二下学期第二次检测化学试题(已下线)江西省重点中学协作体2010届高三第二次联考(化学)(已下线)2011届河南省豫南九校高三上学期第二次联考化学试卷(已下线)2012届黑龙江省牡丹江一中高三上学期期中考试化学试卷2014届河北衡水中学高三上学期期中考试化学试卷(已下线)2014届黑龙江省佳木斯市第一中学高三第三次调研化学试卷(已下线)2014届河北冀州中学高三上学期期中考试往届化学试卷(已下线)2014高考名师推荐化学氧化还原反应的概念2015届辽宁省抚顺市二中高三上学期期中考试化学试卷2016届河北省衡水中学高三上学期二调化学试卷2016届重庆市万州二中高三上学期9月月考化学试卷2016届山东省潍坊第一中学高三上学期10月月考化学试卷2016届甘肃省天水市第一中学高三上学期期中测试化学试卷2016届山东省青岛市高三上学期期中测试化学试卷2016届江苏省淮安市四星级高中高三上学期10月阶段测化学试卷2016届黑龙江省双鸭山一中高三上学期12月月考化学试卷2015-2016学年湖北省枣阳市第七中学高一上学期期中考试化学试卷2015-2016学年浙江省杭州市五校联盟高三12月月考化学试卷2016届吉林省东北师大附属中学高三上四次模拟化学卷2015-2016学年河南省信阳高级中学高一下开学测化学试卷2016届内蒙古赤峰市宁城县高三下学期第三次统一模拟考试化学试卷2016届内蒙古赤峰二中高三第四次模拟理综化学试卷2016-2017学年河北正定中学高二上开学考试化学卷2017届吉林省松原油田高中高三上第一次阶段测化学卷2017届福建省仙游一中高三上第一次月考化学试卷2017届江西省南昌二中高三上第二次考试化学试卷2017届河北省石家庄辛集中学高三上期中化学试卷2017届河南省周口市淮阳中学高三上10月月考化学试卷2017届内蒙古赤峰市宁城县高三上统一考试化学试卷2017届江西省兴国中学、兴国三中等四校高三上第一次联考化学卷2016-2017学年河北省冀州中学高一上11月月考化学卷2017届辽宁省沈阳东北育才学校高三上期中模拟化学卷2017届江西省兴国中学等四校高三上联考一化学试卷2017届吉林省长春实验中学高三第五次模拟化学卷2016-2017学年湖北省鄂东南省级示范高中高一下学期期中联考化学试卷陕西省西藏民族学院附属中学2017届高三考前冲刺(一)理科综合化学试题辽宁省瓦房店市高级中学2016-2017学年高二下学期期末考试化学试题黑龙江省大庆实验中学2017-2018学年高二上学期开学考试化学试题2018届高三一轮复习化学:微考点11-氧化还原反应的概念江西省临川区第二中学2018届高三上学期第三次月考化学试题湖南省永州市祁阳县第一中学2018届高三10月月考化学试题陕西省西安市长安区第一中学2017-2018学年高一下学期第一次教学质量检测化学试题广西陆川县中学2017-2018学年高一下学期3月月考化学试题【全国百强校】山东师范大学附属中学2017-2018学年高二下学期第八次学分认定(期末)考试化学试题【全国百强校】黑龙江省哈尔滨市第六中学2019届高三上学期开学阶段性考试(8月)化学试题湖南省湖南师范大学附属中学2019届高三上学期月考(一)化学试题【全国百强校】陕西省陕西师大附属中学2019届高三上学期月考化学试题【全国百强校】湖南省师范大学附属中学2019届高三上学期月考化学试题江西省赣州市会昌中学2019届高三上学期第一次月考(10月)化学试题河北省承德市第一中学2019届高三上学期第三次月考理科综合化学试题山东省商河市第一中学2019届高三上学期11月月考理科综合化学试题山东省滨州市北镇中学2019届高三上学期12月份质量检测化学试题江西省九江市同文中学2019届高三上学期期中考试化学试题江西省上饶市横峰中学2018-2019学年高一下学期开学考试化学试题吉林省东辽五中2020届高三上学期9月月考化学试题江西省临川第二中学2020届高三10月月考化学试题吉林省白城市通榆县第一中学2020届高三上学期第二次月考化学试题甘肃省兰州市第一中学2020届高三上学期9月月考化学试题山东省莱阳市第一中学2020届高三10月月考化学试题吉林省长春市东北师范大学附中2020届高三上学期第一次摸底考试化学试题山东省肥城市泰西中学2019-2020学年高三上学期第一次月考化学试题新疆乌鲁木齐县柴窝堡林场中学2019届高三第三次模拟考试理科综合化学试题陕西省汉中市龙岗学校2019-2020学年高一上学期期中考试化学试题福建省厦门市湖滨中学2020届高三上学期期中考试化学试题四川省宜宾市叙州区第二中学校2019-2020学年高一下学期第一次在线月考化学试题(已下线)【南昌新东方】2018-2019莲塘一中 高三12月 014(已下线)专题3.4 金属材料及金属矿物的开发利用(练)——2020年高考化学一轮复习讲练测安徽省安庆市2019-2020学年高一下学期期末测试化学试卷吉林省长春外国语学校2020-2021学年高三上学期期初考试化学试题河南省郑州市第一中学2021届高三上学期开学测试化学试题福建省永安市第三中学2021届高三9月月考化学试题吉林省大安市第一中学校2021届高三上学期第二次月考化学试题(已下线)第二章 元素与物质世界(能力提升)-2020-2021学年高一化学必修第一册单元测试定心卷 (鲁科版2019)四川省乐山沫若中学2021届高三上学期第二次理综化学试题江西省高安中学2020-2021学年高一上学期期中考试化学试题四川省射洪中学2019-2020学年高一上期期末英才班能力素质监测化学试题广东省中山纪念中学2021届高三上学期第一次月考化学试题湖南省/(常德市芷兰实验中学2020-2021学年高一上学期第二次月考化学试题河南省信阳高级中学2020-2021学年高一上学期1月月考化学试题福建省莆田第十五中学2020届高三9月月考化学试题(已下线)解密07 非金属及其化合物(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密07 非金属及其化合物(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练云南省昭通市昭阳区第一中学2020-2021学年高一上学期第三次月考化学试题(已下线)【一飞冲天】名家原创卷1河北省廊坊市河北省三河市第一中学2020-2021学年高一下学期第二次阶段考化学试题吉林省大安市第一中学校2021-2022学年高二上学期期初考试化学试题吉林省辉南县第六中学2022届高三上学期第一次月考化学试题 山东省济南市章丘区第四中2022-2023学年高一上学期1月期末线上测试化学试题内蒙古自治区科尔沁左翼中旗实验高级中学2023-2024学年高三上学期11月月考化学试题
解题方法
10 . Ⅰ.硫元素是动植物生长不可缺少的元素,下图是硫元素的常见化合价与部分物质类别的对应关系,回答下列问题。
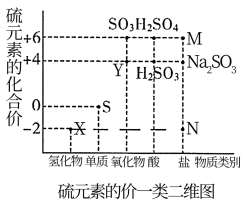
(1)图中X对应的物质是___________ ,将X气体通入 溶液中会出现淡黄色沉淀,反应物
溶液中会出现淡黄色沉淀,反应物 作
作___________ 剂(填“氧化”或“还原”)。
(2)空气中易造成硫酸酸雨的主要气体是___________ (填化学式);
(3)请写出铜和浓硫酸反应的化学方程式___________ 。
Ⅱ.氨和硝酸是重要的工业产品,如图是工业合成氨及制备硝酸的流程示意图:
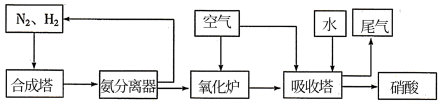
(1)氧化炉中, 转化为NO的化学方程式为
转化为NO的化学方程式为___________ 。
(2)氨分离器中压强约为15MPa,温度约为-20℃,分离氨应用了氨的___________ 性质。
(3)写出硝酸的电离方程式___________ 。
(4)吸收塔中出来的尾气可用 溶液吸收,主要反应为:
溶液吸收,主要反应为:
a.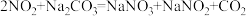
b.
根据反应b,每产生11.2L(标准状况下) ,吸收液质量将增加
,吸收液质量将增加___________ g。

(1)图中X对应的物质是
 溶液中会出现淡黄色沉淀,反应物
溶液中会出现淡黄色沉淀,反应物 作
作(2)空气中易造成硫酸酸雨的主要气体是
(3)请写出铜和浓硫酸反应的化学方程式
Ⅱ.氨和硝酸是重要的工业产品,如图是工业合成氨及制备硝酸的流程示意图:

(1)氧化炉中,
 转化为NO的化学方程式为
转化为NO的化学方程式为(2)氨分离器中压强约为15MPa,温度约为-20℃,分离氨应用了氨的
(3)写出硝酸的电离方程式
(4)吸收塔中出来的尾气可用
 溶液吸收,主要反应为:
溶液吸收,主要反应为:a.
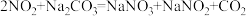
b.

根据反应b,每产生11.2L(标准状况下)
 ,吸收液质量将增加
,吸收液质量将增加
您最近一年使用:0次



