解题方法
1 . 向铜屑、稀盐酸和铁盐的混合溶液中持续通入空气可制备氯化铜,其反应过程如图所示。下列说法不正确 的是
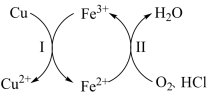

A.制备 的总反应为 的总反应为 |
B.反应Ⅰ中 作氧化剂 作氧化剂 |
C.反应Ⅱ中 作还原剂 作还原剂 |
D.还原性: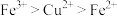 |
您最近半年使用:0次
名校
解题方法
2 . 焦亚硫酸钠( )在化学工业中用途广泛。其一种制备流程如下:
)在化学工业中用途广泛。其一种制备流程如下:
(1) 分子中,中心原子价层电子对数为
分子中,中心原子价层电子对数为__________ 。
(2)“ 制备”所用实验装置(夹持仪器已省略)如下图:
制备”所用实验装置(夹持仪器已省略)如下图:__________ 。
②饱和碳酸氢钠溶液的作用是__________ 。
③三颈烧瓶中生成 反应的化学方程式为
反应的化学方程式为__________ ( 为沉淀物)。
为沉淀物)。
(3)“ 制备”反应过程分四步:
制备”反应过程分四步:
步骤Ⅰ.在碳酸钠溶液中通入 至pH为4.1,生成
至pH为4.1,生成 溶液;
溶液;
步骤Ⅱ.停止通 ,向
,向 溶液中再加入
溶液中再加入 溶液调至pH为7~8,转化为
溶液调至pH为7~8,转化为 ;
;
步骤Ⅲ.继续通入 ,至pH达4.1,又生成
,至pH达4.1,又生成 溶液;
溶液;
步骤Ⅳ.当溶液中 含量达到过饱和浓度时析出
含量达到过饱和浓度时析出 。
。
①步骤Ⅰ测量溶液的pH=4.1所用仪器是__________ 。
②写出步骤Ⅱ中反应的离子方程式:__________ 。
③写出Ⅰ~Ⅳ步骤中总反应的化学方程式:__________ 。
 )在化学工业中用途广泛。其一种制备流程如下:
)在化学工业中用途广泛。其一种制备流程如下:
(1)
 分子中,中心原子价层电子对数为
分子中,中心原子价层电子对数为(2)“
 制备”所用实验装置(夹持仪器已省略)如下图:
制备”所用实验装置(夹持仪器已省略)如下图: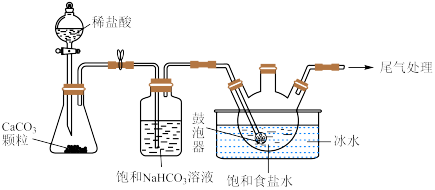
②饱和碳酸氢钠溶液的作用是
③三颈烧瓶中生成
 反应的化学方程式为
反应的化学方程式为 为沉淀物)。
为沉淀物)。(3)“
 制备”反应过程分四步:
制备”反应过程分四步:步骤Ⅰ.在碳酸钠溶液中通入
 至pH为4.1,生成
至pH为4.1,生成 溶液;
溶液;步骤Ⅱ.停止通
 ,向
,向 溶液中再加入
溶液中再加入 溶液调至pH为7~8,转化为
溶液调至pH为7~8,转化为 ;
;步骤Ⅲ.继续通入
 ,至pH达4.1,又生成
,至pH达4.1,又生成 溶液;
溶液;步骤Ⅳ.当溶液中
 含量达到过饱和浓度时析出
含量达到过饱和浓度时析出 。
。①步骤Ⅰ测量溶液的pH=4.1所用仪器是
②写出步骤Ⅱ中反应的离子方程式:
③写出Ⅰ~Ⅳ步骤中总反应的化学方程式:
您最近半年使用:0次
2024-03-30更新
|
262次组卷
|
5卷引用:甘肃省酒泉市九师联盟2023-2024学年高三下学期3月月考化学试题
名校
3 . 钒电池的安全性能优良,中国科学技术大学研制出锌离子和水分子共插层的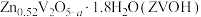 理想的水系锌离子电池材料,制备过程如下:
理想的水系锌离子电池材料,制备过程如下:
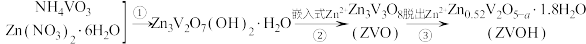
该电极放电时变化为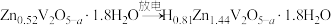 已知制备过程中V的化合价未发生改变,所涉及物质中除ZVO外均为电中性物质,过程②可视为转化成电中性材料后,再嵌入Zn2+。下列说法中正确的是
已知制备过程中V的化合价未发生改变,所涉及物质中除ZVO外均为电中性物质,过程②可视为转化成电中性材料后,再嵌入Zn2+。下列说法中正确的是
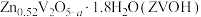 理想的水系锌离子电池材料,制备过程如下:
理想的水系锌离子电池材料,制备过程如下: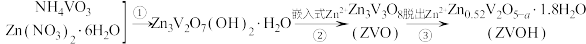
该电极放电时变化为
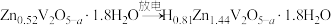 已知制备过程中V的化合价未发生改变,所涉及物质中除ZVO外均为电中性物质,过程②可视为转化成电中性材料后,再嵌入Zn2+。下列说法中正确的是
已知制备过程中V的化合价未发生改变,所涉及物质中除ZVO外均为电中性物质,过程②可视为转化成电中性材料后,再嵌入Zn2+。下列说法中正确的是| A.ZVOH作为新型电池的负极材料 |
| B.反应①属于复分解反应 |
| C.获得Zn(NO3)2·6H2O时,当溶液出现大量晶体时应停止加热,余热蒸干 |
D.ZVO中嵌入进来的Zn2+占总锌量的 |
您最近半年使用:0次
4 . 下列反应的离子方程式正确的是
| A.用三氯化铁溶液蚀刻线路板:Fe3++Cu=Cu2++Fe2+ |
B.用铜做电极电解硫酸铜溶液: |
C.用氢氧化钠溶液吸收二氧化氮: 2OH-+2NO2=2 +H2O +H2O |
| D.用过氧化氢从酸化的海带灰浸取液中提取碘:H2O2+2I-+2H+=I2+2H2O |
您最近半年使用:0次
解题方法
5 . 过氧化氢(H2O2,俗名为双氧水)、过氧化银(Ag2O2)广泛应用于抗菌消毒和化学能源等领域。


(1)根据下列三个反应回答问题:
反应Ⅰ.Ag2O+H2O2=2Ag+O2↑+H2O
反应Ⅱ.2H2O2=2H2O+O2↑
反应Ⅲ.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
①从氧化还原反应角度分析,反应Ⅰ中H2O2表现的性质为_____ 。
②上述反应说明H2O2、Ag2O、K2CrO4的氧化性由强到弱的顺序为_____ 。
③某强酸反应体系中发生一个氧化还原的离子反应,反应物和生成物共六种微粒:O2、Mn 、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→O2.写出该反应的离子方程式:
、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→O2.写出该反应的离子方程式:_____ 。
(2)过氧化银(Ag2O2)为活性物质,可用作新型电池材料。用NaClO-NaOH溶液氧化AgNO3,能制得高纯度的纳米级Ag2O2.
①NaClO中Cl的化合价为_____ ,Ag2O2中O的化合价为_____ 。
②写出上述反应的化学方程式:_____ 。


(1)根据下列三个反应回答问题:
反应Ⅰ.Ag2O+H2O2=2Ag+O2↑+H2O
反应Ⅱ.2H2O2=2H2O+O2↑
反应Ⅲ.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
①从氧化还原反应角度分析,反应Ⅰ中H2O2表现的性质为
②上述反应说明H2O2、Ag2O、K2CrO4的氧化性由强到弱的顺序为
③某强酸反应体系中发生一个氧化还原的离子反应,反应物和生成物共六种微粒:O2、Mn
 、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→O2.写出该反应的离子方程式:
、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→O2.写出该反应的离子方程式:(2)过氧化银(Ag2O2)为活性物质,可用作新型电池材料。用NaClO-NaOH溶液氧化AgNO3,能制得高纯度的纳米级Ag2O2.
①NaClO中Cl的化合价为
②写出上述反应的化学方程式:
您最近半年使用:0次
2024-03-23更新
|
49次组卷
|
2卷引用:甘肃省白银市靖远县第二中学2023-2024学年高一上学期12月期末化学试题
6 . 对于反应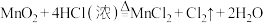
(1)MnO2在反应中电子____________ (填“得到”或“失去”),所含元素化合价____________ (填“升高”或“降低”),发生____________ 反应(填“氧化”或“还原”)。
(2)HCl在反应中____________ 电子(填“得到”或“失去”),所含元素化合价____________ (填“升高”或“降低”),发生____________ 反应(填“氧化”或“还原”)。
(3)配平下列化学方程式:
________ 
________ 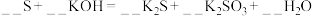
(4)用双线桥表示下列氧化还原反应。
①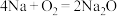
____________
②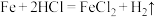
____________
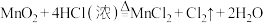
(1)MnO2在反应中电子
(2)HCl在反应中
(3)配平下列化学方程式:

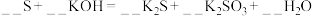
(4)用双线桥表示下列氧化还原反应。
①
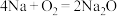
②
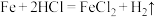
您最近半年使用:0次
解题方法
7 . 甘肃矿产资源丰富,镍、钴、铂等金属储量全国领先,有色金属冶炼在国民经济发展有着重要作用。利用紫硫镍铁矿石提取粗镍并回收铁、铜、钴等元素的工艺流程如下:
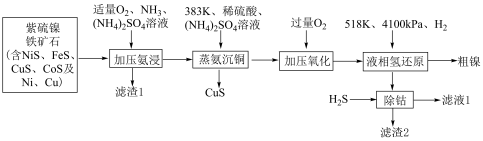
已知:①“加压氨浸”过程中镍硫化物发生反应的方程式为: ;在此过程中,钴硫化物的反应与镍硫化物相似。
;在此过程中,钴硫化物的反应与镍硫化物相似。
②以上流程中均无SO2产生。
请回答:
(1)滤渣1的主要成分为___________ 。
(2)结合下列图表选择“加压氨浸”的最佳条件___________ 。

(3)“加压氨浸”过程中“加压”的目的是___________ 、___________ ;Cu发生反应的化学方程式为___________ 。
(4)“加压氧化”的目的是氧化残留的___________ (填离子符号)。
(5)“除钴”过程中发生反应的离子方程式为___________ 。
(6)流程中可以循环利用的物质有___________ (填化学式)。

已知:①“加压氨浸”过程中镍硫化物发生反应的方程式为:
 ;在此过程中,钴硫化物的反应与镍硫化物相似。
;在此过程中,钴硫化物的反应与镍硫化物相似。②以上流程中均无SO2产生。
请回答:
(1)滤渣1的主要成分为
(2)结合下列图表选择“加压氨浸”的最佳条件

(3)“加压氨浸”过程中“加压”的目的是
(4)“加压氧化”的目的是氧化残留的
(5)“除钴”过程中发生反应的离子方程式为
(6)流程中可以循环利用的物质有
您最近半年使用:0次
2024·广西柳州·一模
名校
解题方法
8 . 我国的歼-20战机使用了大量的钛金属,四氯化钛是生产海绵钛的重要中间原料,某小组同学利用如下装置在实验室制备 (夹持装置略去)。
(夹持装置略去)。
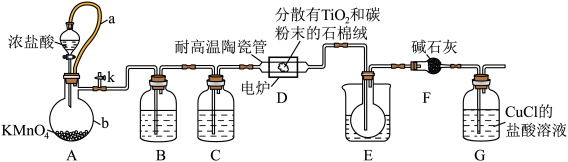
已知:① 的盐酸溶液可以与CO反应;
的盐酸溶液可以与CO反应;
②有关物质的性质。
请回答下列问题:
(1)仪器b的名称为_______ 。
(2)装置C中的药品为_______ ,装置G的作用为_______ 。
(3)组装好仪器后,部分实验步骤如下:①装入药品 ②打开分液漏斗活塞 ③检查装置气密性 ④关闭分液漏斗活塞 ⑤停止加热,充分冷却 ⑥加热装置D中陶瓷管。从上述选项选择合适操作(不重复使用)并排序:③①_______ (填序号)。
(4)装置D中发生两个反应,其中副反应为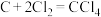 ,主反应中氧化剂与还原剂的物质的量相等且只有两种产物,写出主反应化学方程式
,主反应中氧化剂与还原剂的物质的量相等且只有两种产物,写出主反应化学方程式_______ 。
(5)进一步提纯E中产物的方法是_______ 。
(6)测定 的含量:取
的含量:取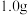 产品于烧瓶中,通过安全漏斗加入足量蒸馏水,充分反应后将安全漏斗及烧瓶中的液体转移到容量瓶中配成
产品于烧瓶中,通过安全漏斗加入足量蒸馏水,充分反应后将安全漏斗及烧瓶中的液体转移到容量瓶中配成 溶液。取
溶液。取 于锥形瓶中,滴加2~3滴
于锥形瓶中,滴加2~3滴 溶液为指示剂,用
溶液为指示剂,用 的
的 标准溶液滴定至终点,消耗溶液
标准溶液滴定至终点,消耗溶液 。该产品纯度为
。该产品纯度为_______ 。下列实验操作会导致产品纯度测定结果偏低的有_______ 。
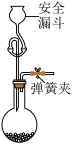
A.未用标准液润洗滴定管 B.未将安全漏斗中的液体转移到容量瓶中
C.滴定终点时仰视读数 D.滴加过多的 溶液
溶液
 (夹持装置略去)。
(夹持装置略去)。
已知:①
 的盐酸溶液可以与CO反应;
的盐酸溶液可以与CO反应;②有关物质的性质。
| 熔点/℃ | 沸点/℃ | 密度/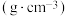 | 水溶性 | |
 |  | 136.4 | 1.7 | 易水解生成白色沉淀,能溶于有机溶剂 |
 | 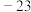 | 76.8 | 1.6 | 难溶于水 |
(1)仪器b的名称为
(2)装置C中的药品为
(3)组装好仪器后,部分实验步骤如下:①装入药品 ②打开分液漏斗活塞 ③检查装置气密性 ④关闭分液漏斗活塞 ⑤停止加热,充分冷却 ⑥加热装置D中陶瓷管。从上述选项选择合适操作(不重复使用)并排序:③①
(4)装置D中发生两个反应,其中副反应为
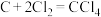 ,主反应中氧化剂与还原剂的物质的量相等且只有两种产物,写出主反应化学方程式
,主反应中氧化剂与还原剂的物质的量相等且只有两种产物,写出主反应化学方程式(5)进一步提纯E中产物的方法是
(6)测定
 的含量:取
的含量:取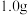 产品于烧瓶中,通过安全漏斗加入足量蒸馏水,充分反应后将安全漏斗及烧瓶中的液体转移到容量瓶中配成
产品于烧瓶中,通过安全漏斗加入足量蒸馏水,充分反应后将安全漏斗及烧瓶中的液体转移到容量瓶中配成 溶液。取
溶液。取 于锥形瓶中,滴加2~3滴
于锥形瓶中,滴加2~3滴 溶液为指示剂,用
溶液为指示剂,用 的
的 标准溶液滴定至终点,消耗溶液
标准溶液滴定至终点,消耗溶液 。该产品纯度为
。该产品纯度为
A.未用标准液润洗滴定管 B.未将安全漏斗中的液体转移到容量瓶中
C.滴定终点时仰视读数 D.滴加过多的
 溶液
溶液
您最近半年使用:0次
9 . 黄铁矿(主要成分为FeS2)是工业制取硫酸的重要原料,矿区中的黄铁矿暴露在空气中会被缓慢氧化,氧化过程如图所示。下列说法正确的是
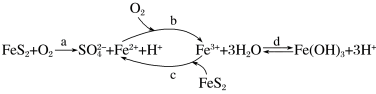

| A.d步生成的Fe(OH)3可作净水剂、消毒剂 |
B.a步发生反应的离子方程式为2FeS2+7O2+2H2O=2Fe2++4SO +4H+ +4H+ |
| C.空气中O2约占五分之一,0.1 mol FeS2完全被氧化时消耗标准状况下空气的体积约为8.4 L |
| D.缓慢氧化过程中对矿区的生态环境没有影响 |
您最近半年使用:0次
名校
解题方法
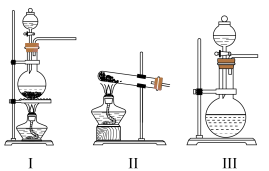
10 . 某学习小组根据氨气还原氧化铜的反应,设计实验测定铜元素相对原子质量Ar(Cu)(近似值)。甲同学模拟合成氨工业制备氨气,反应前先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量m(H2O),由此计算Ar(Cu)。装置图如下: 。请回答下列问题:
。请回答下列问题:
(1)C装置应选用______ (填“Ⅰ”“Ⅱ”或“Ⅲ”)。
(2)装置B的作用是:①使气体混合均匀;②______ ;③______ 。
(3)氨气还原炽热氧化铜(产物之一为空气中含量最多的气体)化学方程式为____________________ 。
(4)干燥管F中盛放的干燥剂为______(填字母代号)。
(5)G装置的作用是①______ ;②______ 。
若没有G装置,测得结果Ar(Cu)______ (填“偏大”“偏小”或“无影响”)。
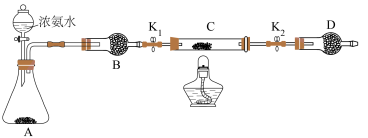
(6)乙同学认为上述装置操作麻烦,对原装置改进,新装置如图所示。实验前将石英玻璃管(带两端开关K1和K2)(设为装置C)称重,记为m1 g。将氧化铜装入石英玻璃管中,再次将装置C称重,记为m2 g。按下图连接好装置进行实验,通入NH3,充分反应直至C恒重,记为m3 g。______ (填化学式)
②根据实验记录,计算铜元素相对原子质量Ar(Cu)=______ (用含有m1、m2、m3的式子表示)。
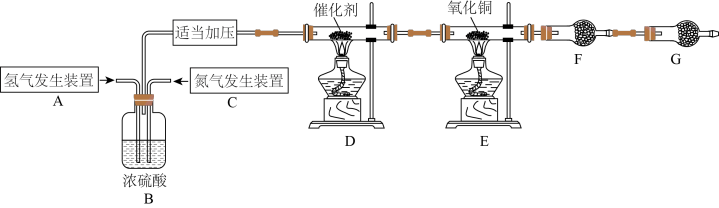
 。请回答下列问题:
。请回答下列问题:(1)C装置应选用
(2)装置B的作用是:①使气体混合均匀;②
(3)氨气还原炽热氧化铜(产物之一为空气中含量最多的气体)化学方程式为
(4)干燥管F中盛放的干燥剂为______(填字母代号)。
| A.五氧化二磷 | B.无水CuSO4 | C.碱石灰 | D.无水CaCl2 |
(5)G装置的作用是①
若没有G装置,测得结果Ar(Cu)
(6)乙同学认为上述装置操作麻烦,对原装置改进,新装置如图所示。实验前将石英玻璃管(带两端开关K1和K2)(设为装置C)称重,记为m1 g。将氧化铜装入石英玻璃管中,再次将装置C称重,记为m2 g。按下图连接好装置进行实验,通入NH3,充分反应直至C恒重,记为m3 g。
②根据实验记录,计算铜元素相对原子质量Ar(Cu)=
您最近半年使用:0次
2024-03-12更新
|
570次组卷
|
5卷引用:甘肃省兰州第一中学2023-2024学年高一下学期3月月考化学试题



