名校
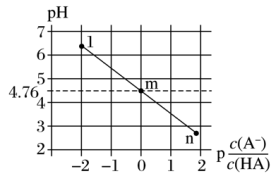
1 . 常温下,将NaOH溶液滴加到20mL等浓度的某一元酸(HA)溶液中,测得混合溶液的pH与离子浓度变化关系如图所示[已知:p =-lg
=-lg ]。下列叙述不正确的是
]。下列叙述不正确的是
 =-lg
=-lg ]。下列叙述不正确的是
]。下列叙述不正确的是
| A.m点对应的NaOH溶液体积大于10mL |
| B.Ka(HA)的数量级为10-5 |
| C.1点所示溶液中:c(Na+)<c(A-)+c(HA) |
| D.各点的水溶液中水的电离程度大小关系:n>m>1 |
您最近一年使用:0次
2021-05-01更新
|
562次组卷
|
3卷引用:山东省泰安市2021届高考第二次模拟化学试题
名校
解题方法
2 . 在不同温度下的水溶液中离子浓度曲线如图所示,下列说法不正确的是
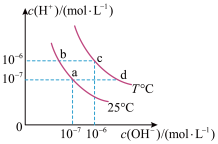

| A.向b点对应的醋酸溶液中滴加NaOH溶液至a点,此时c(Na+)=c(CH3COO-) |
| B.25℃时,加入CH3COONa可能引起由b向a的变化,升温可能引起由a向c的变化 |
| C.T℃时,将pH=2的硫酸与pH=10的KOH等体积混合后,溶液显酸性 |
D.b点对应的溶液中大量存在:K+、Ba2+、 、I- 、I- |
您最近一年使用:0次
3 . 某温度下,向10 mL 0.1 mol·L-1 CuCl2溶液中滴入0.1 mol·L-1的Na2S溶液,溶液中-lgc(Cu2+)随滴入的Na2S溶液体积的变化如图所示。下列叙述不正确的是
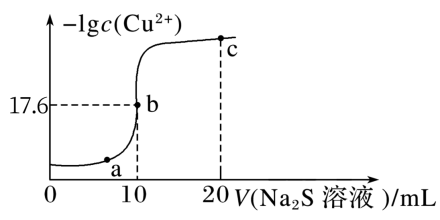

| A.Ksp(CuS)的数量级为10-36 |
| B.c点对应溶液中:c(S2-)+c(Cl-)=c(Na+) |
| C.a、b、c三点对应溶液中,b点水的电离程度最小 |
| D.Na2S溶液中:2c(S2-)+c(HS-)+c(OH-)=c(Na+)+c(H+) |
您最近一年使用:0次
名校
解题方法
4 . 室温下,体积均为20mL、浓度均为0.1mol·L-1的HX溶液、HY溶液中分别滴加同浓度的NaOH溶液,反应后溶液中水电离的c(H+)水的负对数[–lgc(H+)水]与滴加氢氧化钠溶液体积的关系如图所示。下列说法正确的是
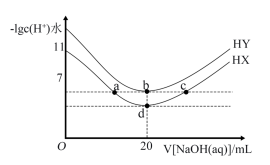

| A.室温时,Ka(HX)=10-6 |
| B.a、b、c三点溶液均显中性 |
| C.b、d两点溶液的离子总浓度不同 |
| D.c点溶液中c(X-)+c(HX)=0.1mol·L-1 |
您最近一年使用:0次
2021-03-12更新
|
1004次组卷
|
5卷引用:安徽省马鞍山市2021届高三第一次模拟理综化学试题
安徽省马鞍山市2021届高三第一次模拟理综化学试题(已下线)押全国卷理综第12题 水溶液中的离子平衡-备战2021年高考化学临考题号押题(课标全国卷)(已下线)小题20 弱电解质的电离,水的电离,溶液pH——备战2021年高考化学经典小题考前必刷(全国通用)广东省华附、省实、广雅、深中四校2020-2021学年高二下学期期末联考化学试题甘肃省张掖市高台县第一中学2022-2023学年高三上学期第四次检测化学试题
20-21高二·浙江·期中
解题方法
5 . 在某温度时,将n mol/L氨水滴入10 mL 1.0 mol/L盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示。下列有关说法错误的是
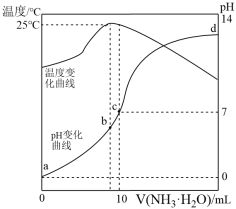

| A.a点的Kw≠1.0×10-14 |
B.b点:c(Cl-)>c( )>c(H+)>c(OH-) )>c(H+)>c(OH-) |
| C.水的电离程度:b>c>a>d |
D.c点:25℃时c(Cl-)=c( )>c(H+)=c(OH-) )>c(H+)=c(OH-) |
您最近一年使用:0次
20-21高二·浙江·期中
解题方法
6 . 下列各组离子在指定溶液中一定能大量共存的是
A.由水电离出来的氢离子浓度为10-13mol/L的溶液中:CH3COO-、K+、 、Cl- 、Cl- |
B.能使甲基橙变红的溶液中:K+、Mg2+、 、 、 |
C.c(H+)/c(OH-)=107的溶液:Fe2+、Al3+、 、C1- 、C1- |
D.含有大量Fe3+的溶液: Na+、 Cl-、 、 、 |
您最近一年使用:0次
解题方法
7 . 下列说法正确的是
| A.室温下,将pH=5的醋酸加水稀释至原体积的100倍,稀释后pH=7 |
| B.某温度下,水的离子积常数为1×10-13,则该温度下pH=6.5的溶液呈酸性 |
| C.室温下,pH相同的NH4Cl溶液和CH3COOH溶液中,由水电离产生的c(H+)相同 |
| D.室温下,pH=3的盐酸和pH=11的Ba(OH)2溶液等体积混合后溶液呈中性 |
您最近一年使用:0次
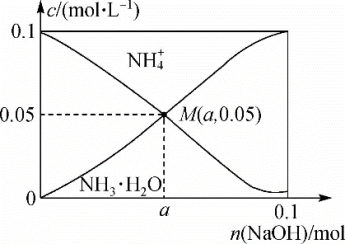
8 . 常温下,向1L0.1mol·L-1NH4Cl溶液中不断加入固体NaOH后,NH 与NH3·H2O 的变化趋势如图所示(不考虑溶液体积的变化和氨的挥发),下列说法正确的是
与NH3·H2O 的变化趋势如图所示(不考虑溶液体积的变化和氨的挥发),下列说法正确的是
 与NH3·H2O 的变化趋势如图所示(不考虑溶液体积的变化和氨的挥发),下列说法正确的是
与NH3·H2O 的变化趋势如图所示(不考虑溶液体积的变化和氨的挥发),下列说法正确的是
| A.M点溶液中水的电离程度比原溶液大 |
| B.在M点时,n(OH-)-n(H+)=(a +0.05)mol |
C.当n(NaOH)=0.05mol时,溶液中有:c(Cl-)>c(Na+)>c(NH )>c(OH-)>c(H+ ) )>c(OH-)>c(H+ ) |
| D.随着NaOH的加入,一定存在c(Cl-)+c(OH-)+c(NH3·H2O)>0.1 mol·L-1 |
您最近一年使用:0次
2021-02-13更新
|
204次组卷
|
2卷引用:广西河池市2021届高三上学期期末教学质量检测理科综合化学试题
名校
解题方法
9 . 盐在化学工业中有重要的应用,请回答下列问题。
(1)用离子方程式表示明矾可作净水剂的原因:_______ 。
(2)常温下,在pH=3的硫酸与pH=11的Na2S溶液中,水电离出来的c(OH-)之比为_______ 。
(3)物质的量浓度相等的下列溶液①NH4Cl;②NH4HSO4;③(NH4)2SO4;④CH3COONH4;⑤NH3·H2O,溶液中的pH由大到小的顺序是_______ (用序号表示)
(4)25℃,两种酸的电离平衡常数如下表:
①0.10mol/L NaHSO3溶液中离子浓度由大到小的顺序为_______ ;
②向Na2S溶液中通入足量二氧化硫时反应的离子方程式_______ 。
③向NaHS溶液中通入少量CO2时反应的离子方程式_______ 。
(1)用离子方程式表示明矾可作净水剂的原因:
(2)常温下,在pH=3的硫酸与pH=11的Na2S溶液中,水电离出来的c(OH-)之比为
(3)物质的量浓度相等的下列溶液①NH4Cl;②NH4HSO4;③(NH4)2SO4;④CH3COONH4;⑤NH3·H2O,溶液中的pH由大到小的顺序是
(4)25℃,两种酸的电离平衡常数如下表:
| H2SO3 | H2CO3 | H2S | |
| Ka1 | 1.3×10-2 | 4.2×10-7 | 1.9×10-8 |
| Ka2 | 6.3×10-8 | 5.6×10-11 | 1.0×10-12 |
①0.10mol/L NaHSO3溶液中离子浓度由大到小的顺序为
②向Na2S溶液中通入足量二氧化硫时反应的离子方程式
③向NaHS溶液中通入少量CO2时反应的离子方程式
您最近一年使用:0次
名校
解题方法
10 . 常温下,磷酸钠溶液中含磷微粒的分布随pH的变化如图所示,M、N、P三点对应的pH分别为a、b、c,其中δ表示含磷微粒的物质的量分数。下列说法错误的是
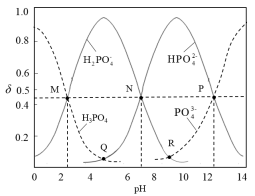

A.常温下, 的一级电离平衡常数Ka1=10-a 的一级电离平衡常数Ka1=10-a |
B.常温下,溶液中水电离出的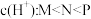 |
C.Q点与R点对应溶液的pH差: |
D.用磷酸标准溶液滴定NaOH溶液,选择酚酞作指示剂,终点时溶质主要为 |
您最近一年使用:0次
2021-02-03更新
|
1091次组卷
|
7卷引用:河南省新乡市2020-2021学年高二上学期期末考试化学试题
河南省新乡市2020-2021学年高二上学期期末考试化学试题湖北省仙桃中学、天门中学(B班)2021-2022学年高二上学期期中考试化学试题(已下线)专题18 酸碱混合图像为载体考查离子平衡-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)江西省宜春市铜鼓中学2021-2022学年高二下学期第一次月考(实验班)化学试卷(已下线)专题11 水溶液中的离子平衡图像(选择题)-2023年高考化学毕业班二轮热点题型归纳与变式演练(已下线)专题四 电解质溶液图象(练)湖南省衡阳市第八中学2022-2023学年高二下学期5月月考化学试题



