名校
1 . 在 和
和 的混合溶液中,逐滴加入NaOH溶液直至过量。经测定,加入的NaOH的物质的量(mol)和所得沉淀的物质的量(mol)的关系如下图所示。
的混合溶液中,逐滴加入NaOH溶液直至过量。经测定,加入的NaOH的物质的量(mol)和所得沉淀的物质的量(mol)的关系如下图所示。
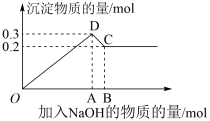
(1)原溶液中 、
、 的物质的量浓度之比为
的物质的量浓度之比为_______ 。
(2)图中线段
_______ 。
 和
和 的混合溶液中,逐滴加入NaOH溶液直至过量。经测定,加入的NaOH的物质的量(mol)和所得沉淀的物质的量(mol)的关系如下图所示。
的混合溶液中,逐滴加入NaOH溶液直至过量。经测定,加入的NaOH的物质的量(mol)和所得沉淀的物质的量(mol)的关系如下图所示。
(1)原溶液中
 、
、 的物质的量浓度之比为
的物质的量浓度之比为(2)图中线段

您最近一年使用:0次
名校
2 . 现有14.4 g CO和CO2的混合气体,在标准状况下其体积为8.96 L。回答问题:
(1)该混合气体的平均摩尔质量为___________ 。
(2)混合气体中碳原子的个数为___________ (用NA表示阿伏加德罗常数的值)。
(3)将混合气体依次通过如图所示装置,最后收集在气球中。
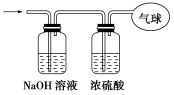
①气球中收集到的气体的摩尔质量为___________ 。
②气球中收集到的气体中,电子总数为___________ (用NA表示阿伏加德罗常数的值)。
③标准状况下,气球中收集到的气体的体积为___________ L。
(1)该混合气体的平均摩尔质量为
(2)混合气体中碳原子的个数为
(3)将混合气体依次通过如图所示装置,最后收集在气球中。

①气球中收集到的气体的摩尔质量为
②气球中收集到的气体中,电子总数为
③标准状况下,气球中收集到的气体的体积为
您最近一年使用:0次
3 . 将0.1 mol的镁、铝混合物溶于100 mL 2 mol/LH2SO4溶液中,然后再滴加1 mol/L NaOH溶液。若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如图所示。当V1=160 mL时:
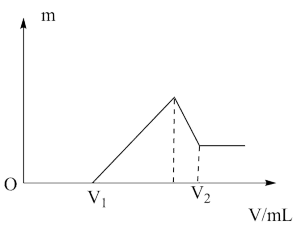
(1)镁的物质的量______
(2)V2=_____ mL

(1)镁的物质的量
(2)V2=
您最近一年使用:0次
名校
4 . 水的电离平衡曲线如图所示。
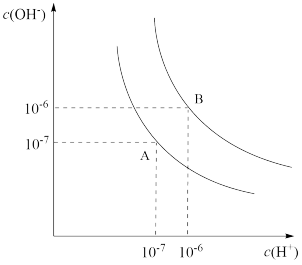
(1)若以A点表示25℃时水在电离平衡时的离子浓度,当温度升到100℃时,水的电离平衡状态到B点,则此时水的离子积从___________ 增加到___________ 。
(2)将常温下的pH=8的Ba(OH)2溶液与常温下的pH=5的稀盐酸混合,并保持100℃的恒温,欲使混合溶液pH=6,则Ba(OH)2与盐酸的体积比为___________ 。

(1)若以A点表示25℃时水在电离平衡时的离子浓度,当温度升到100℃时,水的电离平衡状态到B点,则此时水的离子积从
(2)将常温下的pH=8的Ba(OH)2溶液与常温下的pH=5的稀盐酸混合,并保持100℃的恒温,欲使混合溶液pH=6,则Ba(OH)2与盐酸的体积比为
您最近一年使用:0次
名校
解题方法
5 . 已知MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,用MnO2与100mL物质的量浓度为10mol/L的浓盐酸反应,制得氯气3.36L(标准状况)。
MnCl2+Cl2↑+2H2O,用MnO2与100mL物质的量浓度为10mol/L的浓盐酸反应,制得氯气3.36L(标准状况)。
(1)需要消耗MnO2的质量是多少?___________
(2)被氧化的HCl的物质的量是多少?___________
(3)若反应后溶液的体积不变,则反应后溶液中Cl-的物质的量浓度是多少?___________
 MnCl2+Cl2↑+2H2O,用MnO2与100mL物质的量浓度为10mol/L的浓盐酸反应,制得氯气3.36L(标准状况)。
MnCl2+Cl2↑+2H2O,用MnO2与100mL物质的量浓度为10mol/L的浓盐酸反应,制得氯气3.36L(标准状况)。(1)需要消耗MnO2的质量是多少?
(2)被氧化的HCl的物质的量是多少?
(3)若反应后溶液的体积不变,则反应后溶液中Cl-的物质的量浓度是多少?
您最近一年使用:0次
名校
6 . 计算
(1)0.5 mol CH4的质量为__________ ,在标准状况下的体积为________ 。
(2)15.6 g NaR含0.4 mol Na+,则NaR的摩尔质量为______ ,含R质量为3.2 g的NaR,其物质的量为_____ 。
(3)将标准状况下___ LNH3溶于水得到500 mL 0.5 mol/L的氨水;配制100 mL0.1mol/LFeSO4溶液,需要用托盘天平称FeSO4·7H2O_______ g。
(4)标准状况下,CH4和CO的混合气体6.72 L,质量为6 g,此混合物中CH4的质量为______ ,CO的物质的量为________ 。
(1)0.5 mol CH4的质量为
(2)15.6 g NaR含0.4 mol Na+,则NaR的摩尔质量为
(3)将标准状况下
(4)标准状况下,CH4和CO的混合气体6.72 L,质量为6 g,此混合物中CH4的质量为
您最近一年使用:0次
7 . 相同条件下,若X2与氮气比1:4混合,该混合气体相对氢气的密度为14.4,则X2的相对分子质量为。___________ 。
您最近一年使用:0次
名校
8 . 物质的量是高中化学中常用的物理量,请完成以下内容。(注意:用NA表示阿伏加德罗常数)
(1)3.01×1023个NH3分子中含有氢原子的个数为_______ 。
(2)常温常压下,92gNO2气体含有的原子数为_______ 。
(3)200mLAl2(SO4)3溶液中含Al3+5.4g,则溶液中c(SO )=
)=_______ 。
(4)32gSO2标况下的体积为_______ L
(5)实验室有密度为1.84g/cm3、溶质的质量分数为98%的浓硫酸,其物质的量浓度为_______ 某同学需要0.10mol/L的硫酸500mL,需量取98%浓硫酸的体积为_______ mL
(1)3.01×1023个NH3分子中含有氢原子的个数为
(2)常温常压下,92gNO2气体含有的原子数为
(3)200mLAl2(SO4)3溶液中含Al3+5.4g,则溶液中c(SO
 )=
)=(4)32gSO2标况下的体积为
(5)实验室有密度为1.84g/cm3、溶质的质量分数为98%的浓硫酸,其物质的量浓度为
您最近一年使用:0次
名校
9 . 将质量为5.4g的铝箔(有小孔)包裹4.6g金属钠,投入到盛有足量水的烧杯中,可生成标况下气体_______ 升(写出发生反应的方程式并计算)。
您最近一年使用:0次
名校
10 . 将70克由Na2O2和Na2O组成的混合物跟98克H2O充分反应后,所得NaOH溶液中溶质的质量分数为50%。(注意:无计算过程不给分)
(1)求原混合物中过氧化钠和氧化钠的质量___________ ;
(2)产生的气体标况下体积___________ 。
(1)求原混合物中过氧化钠和氧化钠的质量
(2)产生的气体标况下体积
您最近一年使用:0次



